铁氰化钾比色法检测黄瓜中谷胱甘肽
吴锁柱,王妍,郭红媛
(1.山西农业大学 食品科学与工程学院,山西 太谷030801;2.山西农业大学 农学院,山西太谷030801)
谷胱甘肽是一种由谷氨酸、半胱氨酸和甘氨酸通过肽键缩合形成的二肽化合物,以还原型和氧化型两种形态广泛存在于动植物体中[1]。还原型谷胱甘肽具有重要的生理功能,如清除自由基、解毒、维持蛋白质结构和功能、参与氨基酸的吸收和转运等,在生物医学领域具有广泛的用途,也可用于食品工业食品品质的改善,如防止果蔬类食品褐变、强化肉制品风味、改善面制品面团的流变特性等[1,2]。因此,探索建立一种简单、灵敏、准确的还原型谷胱甘肽检测方法具有重要的现实意义。
目前,谷胱甘肽的检测方法主要有酶循环法[1]、荧光法[3~6]、高效液相色谱法[7,8]、高效液相色谱−质谱联用法[9,10]等,这些检测方法虽然灵敏度较高,但存在试剂成本高、仪器设备昂贵、检测步骤繁琐、对操作人员专业素养要求较高等缺陷。与上述检测方法相比,比色法是一种实验成本低、操作简单、快速、仪器设备简单的谷胱甘肽测定方法[11~17]。
黄瓜是一种深受大众喜爱的蔬菜,其营养成分丰富。黄瓜中的还原型谷胱甘肽是一种天然的抗氧化成分,可以清除人体内的自由基,也可以保护体内含巯基的蛋白质和酶分子发挥正常的生理功能,有益于人体健康。黄瓜中还原型谷胱甘肽含量的多少与其营养价值及功效密切相关,因此,对其含量的检测具有重要意义。
本研究拟以铁氰化钾与还原型谷胱甘肽的显色反应为基础,建立一种简单、有效的比色检测黄瓜中还原型谷胱甘肽的新方法,以期为食品质量控制、功能食品开发、临床检测等过程中谷胱甘肽成分的准确、可靠分析提供技术支撑。
1 材料和方法
1.1 试验材料
铁氰化钾、还原型谷胱甘肽、磷酸二氢钠、磷酸氢二钠和氢氧化钠均购自上海阿拉丁生化科技股份有限公司。磷酸购自中国医药公司北京采购供应站。市售黄瓜购自山西农业大学家属院菜市场。
1.2 试验方法
溶液配制:0.1 mol·L-1磷酸缓冲溶液(pH 为5.0~9.0)由磷酸二氢钠、磷酸氢二钠、磷酸和氢氧化钠调节配制;采用0.1 mol·L-1磷酸缓冲溶液(pH 为5.0~9.0)分别配制5.0 mmol·L-1铁氰化钾溶液和1.0 mg·mL-1的谷胱甘肽溶液。
黄瓜样品预处理:首先,对市售黄瓜样品进行去皮、榨汁和过滤处理;然后,将过滤后的黄瓜样品汁液在5 000 r·min-1条件下离心10 min,取上清液供显色反应使用。
显色反应:将一定体积的5.0 mmol·L-1铁氰化钾溶液、1.0 mg·mL-1的谷胱甘肽溶液及0.1 mol·L-1磷酸缓冲溶液充分混合,待显色反应一段时间后,采用智能手机(型号:红米4X)对反应后的溶液进行拍照,并用SP-754 型紫外可见分光光度计对同一条件下反应后稀释2 倍的溶液进行多次光谱扫描平行测定。
本试验首先对铁氰化钾比色法检测谷胱甘肽方法进行了验证。然后,考察了铁氰化钾浓度、缓冲液pH、反应时间等因素对显色反应的影响,获得最佳的谷胱甘肽检测条件。接着,在最佳的检测条件下,对不同标准浓度的谷胱甘肽溶液进行测定,获得该方法检测谷胱甘肽的线性范围、检出限等响应性能。最后,将建立的方法用于市售黄瓜样品中谷胱甘肽含量的测定。采用标准加入法测定黄瓜样品中谷胱甘肽的含量;将一定体积的5.0 mmol·L-1铁氰化钾溶液、9.0 mg·mL-1的谷胱甘肽溶液、0.1 mol·L-1磷酸缓冲溶液及离心后的黄瓜样品上清液充分混合,待显色反应一段时间后,采用智能手机对反应后的溶液进行拍照,并用分光光度计对含不同标准浓度谷胱甘肽的黄瓜样品溶液进行测定,绘制标准曲线。
1.3 统计分析
采用Excel 软件对获得的数据进行平均值和标准偏差计算,并用Origin 软件作图。
2 结果与分析
2.1 铁氰化钾与谷胱甘肽的显色反应
图1 为2.0 mmol·L-1铁氰化钾与0.50 mg·mL-1谷胱甘肽反应前后溶液的颜色变化图和溶液稀释2 倍后的吸收光谱图。由图1A 可见,反应前铁氰化钾溶液的颜色为黄绿色,而谷胱甘肽溶液的颜色为无色;反应后铁氰化钾溶液的颜色明显变浅。光谱测定结果表明可在419 nm 波长处观察到铁氰化钾溶液的最大吸收峰,而在相应波长范围内未观察到谷胱甘肽溶液的吸收峰;当铁氰化钾溶液与谷胱甘肽发生反应后,反应后的溶液仍在419 nm 波长处有最大吸收峰,但与单独的铁氰化钾溶液的吸光度相比,其吸光度明显降低(图1B)。这些结果表明具有还原性的谷胱甘肽可以将具有氧化性的铁氰化钾还原,同时引起铁氰化钾溶液颜色和吸光度的变化。因此,有望借助铁氰化钾溶液颜色和吸光度的变化实现对谷胱甘肽含量的测定。
2.2 铁氰化钾浓度对显色反应的影响
由于反应前与反应后铁氰化钾溶液的颜色均呈现不断加深的趋势,这使得通过溶液颜色变化难以获得最佳的铁氰化钾浓度。因此,进一步通过考察反应前后溶液的吸光度差值变化来优化铁氰化钾浓度对显色反应的影响。由图2 可见,随着铁氰化钾浓度的不断增大,反应前后溶液的吸光度差值首先逐渐升高,然后趋于稳定。由于铁氰化钾浓度为2.4 mmol·L-1时反应前后溶液的吸光度差值变化最为明显,因此,后续选择该浓度的铁氰化钾进行谷胱甘肽的测定。
2.3 缓冲液pH 对显色反应的影响
由图3 可见,随着缓冲液pH 的不断增大,反应前铁氰化钾溶液的颜色变化较难分辨,与谷胱甘肽反应后溶液的颜色变化较为明显,而且缓冲液pH 为8.0 时溶液的颜色较其它条件下更淡并趋于无色。由于缓冲液pH 为8.0 时反应前后溶液的颜色变化最为明显,因此,选择该缓冲液pH 进行谷胱甘肽的后续测定。
2.4 反应时间对显色反应的影响
由图4 可见,随着反应时间的不断延长,溶液的颜色逐渐变浅,在反应27 min 后溶液的颜色达到稳定状态并趋于无色。因此,选择27 min 为最佳反应时间进行谷胱甘肽的后续测定。

图1 2.0 mmol·L-1铁氰化钾与0.50 mg·mL-1谷胱甘肽反应前后溶液的颜色变化图(A)和溶液稀释两倍后的吸收光谱图(B)Fig.1 Diagrams of solution color change(A)and absorption spectrum(B)of the two-fold diluted solution before and after reacting between 2.0 mmol·L-1 potassium ferricyanide and 0.50 mg·mL-1 glutathione

图2 不同浓度铁氰化钾与0.50 mg·mL-1谷胱甘肽反应前后溶液的吸光度差变化图Fig.2 Diagram of the variation of absorbance difference at different concentration of potassium ferricyanide before and after reacting with 0.50 mg·mL-1 glutathione
2.5 不同浓度谷胱甘肽的测定
由图5 可见,随着谷胱甘肽浓度的不断增大,反应后溶液的颜色逐渐变浅(图5A)。同时,吸光度也随着谷胱甘肽浓度的增加在不断降低;当谷胱甘肽浓度高于0.36 mg·mL-1时,溶液吸光度趋于稳定(图5B)。而且,在0~0.36 mg·mL-1浓度范围内,吸光度与谷胱甘肽浓度呈现良好的线性关系(R=−0.992,图5C)。据空白溶液吸光度信号的3 倍标准偏差除以拟合曲线斜率获得该方法的检出限为3.0 μg·mL-1。
2.6 样品检测

图3 2.4 mmol·L-1 铁氰化钾与0.50 mg·mL-1 谷胱甘肽在不同缓冲液pH 条件下反应前(A)后(B)溶液的颜色变化图Fig.3 Diagram of solution color change of 2.4 mmol·L-1 potassium ferricyanide before(A)and after(B)reacting with 0.50 mg·mL-1 glutathione under different buffer solution pH
通过光谱测定获得的标准曲线方程计算黄瓜样品中谷胱甘肽的浓度为0.31 mg·mL-1,回收率为89.8%~103.9%。这些结果表明可以将建立的比色检测方法成功用于黄瓜样品中谷胱甘肽含量的准确测定。
3 讨论与结论

图4 2.4 mmol·L-1 铁氰化钾与0.50 mg·mL-1 谷胱甘 肽 反应不同时间时溶液的颜色变化图Fig.4 Diagram of solution color change of 2.4 mmol·L-1 potassium ferricyanide reacting with 0.50 mg·mL-1 glutathione for different time
目前,已报道的酶循环法、荧光法、高效液相色谱法、高效液相色谱−质谱联用法等谷胱甘肽检测方法虽然灵敏度或准确度较高,但也存在一些不足之处,如试剂成本高、仪器设备昂贵、对操作人员专业素养要求较高等。本研究建立的铁氰化钾比色检测谷胱甘肽方法有望弥补上述检测方法的不足之处。例如,与酶循环法相比,本研究建立的方法在试剂成本和稳定性方面存在明显优势。本试验所用的铁氰化钾试剂的价格远较酶试剂的低,而且受环境温度、pH 等因素的影响较小。又如,与荧光法、高效液相色谱法、高效液相色谱-质谱联用法相比,本研究建立的方法在仪器设备成本、对操作人员专业素养要求方面存在显著优势。本试验所用的智能手机和紫外可见分光光度计设备的价格较荧光分光光度计、高效液相色谱、质谱设备低得多,而且对操作人员专业素养要求较低,易推广。
铁氰化钾溶液颜色为黄绿色,谷胱甘肽溶液颜色为无色,将二者混合后一段时间,溶液颜色明显变浅且吸光度降低。该现象说明具有还原性的谷胱甘肽可以与具有氧化性的铁氰化钾发生氧化还原反应,并伴随铁氰化钾溶液颜色和吸光度的变化。这为利用铁氰化钾溶液颜色和吸光度的变化实现对谷胱甘肽的比色测定提供了一种可能。
本研究基于还原型谷胱甘肽可以引起铁氰化钾溶液褪色和吸光度降低的现象,实现对黄瓜样品中谷胱甘肽含量的比色检测。在最佳的检测条件下,随着谷胱甘肽浓度的不断升高,反应后铁氰化钾溶液的颜色逐渐变浅,而且溶液的吸光度与谷胱甘肽浓度在0~0.36 mg·mL-1浓度范围内呈现良好的线性关系,检出限为3.0 μg·mL-1,黄瓜样品中谷胱甘肽的回收率为89.8%~103.9%。
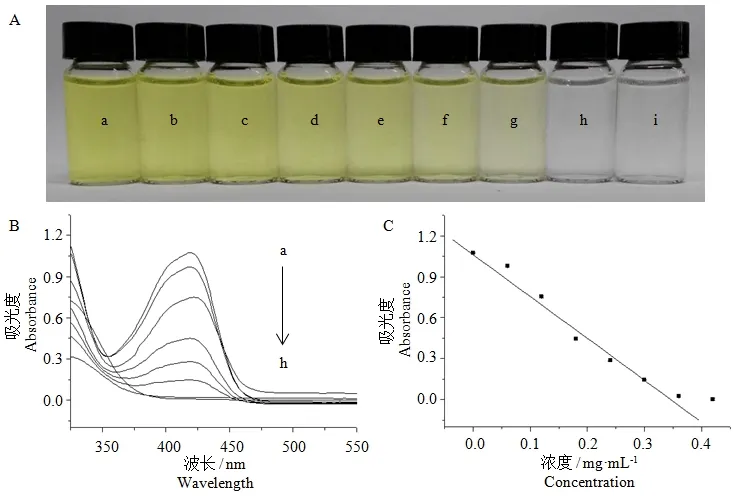
图5 2.4 mmol·L-1铁氰化钾与不同浓度谷胱甘肽反应后溶液的颜色变化图(A)、溶液稀释两倍后的吸收光谱图(B)及吸光度随谷胱甘肽浓度的变化关系图(C)Fig.5 Diagrams of solution color change(A),absorption spectrum of the two-fold diluted solution(B)and relationships of absorbance with glutathione concentration(C)after reacting between 2.4 mmol·L-1 potassium ferricyanide and different concentration of glutathione
综上所述,本研究建立了一种比色检测还原型谷胱甘肽的方法,该方法具有操作简单、成本低、灵敏、准确度高等优点,为食品样品中谷胱甘肽含量的测定提供了一种新途径。

