亚甲蓝光病毒灭活血浆的研究进展*
黄佳丽 刘正婷 陈尚良 周义文
在过去的几十年里,由于采用了献血者筛选、敏感的传染病检测等方法,血液安全得到了显著改善。然而,供应临床的血液仍面临着新发传染病病原体和未知病原体的威胁。输血安全是基于预防与异体输血有关的两大主要风险,即感染风险和免疫风险。免疫介导的反应是输注血浆最常见的不良反应,严重者可出现过敏性休克导致死亡。亚甲蓝光病毒灭活血浆已应用于临床输注20余年,在奥地利、比利时、希腊、波兰、俄罗斯、西班牙、英国等国家被批准使用[1,2]。《血站技术操作规程(2019版)》规定,我国应用于血浆病毒灭活的方法可选用亚甲蓝光化学法、核黄素光化学法以及补骨脂素光化学法[3]。亚甲蓝光化学法作为我国获准用于血浆病毒灭活的一种方法,能有效灭活人类免疫缺陷病毒、乙型肝炎病毒、丙型肝炎病毒等大多数脂质包膜病毒,减少经血液传播病毒的风险[1]。可是,在亚甲蓝光化学法灭活血浆病毒的过程中,不可避免造成血浆凝血因子的损失以及亚甲蓝的残余。亚甲蓝光化学法灭活血浆病毒,经过滤后,血浆中仍残余少量亚甲蓝,仅≤0.30 μmol/L,即≤0.096 mg/L,远低于临床常用的剂量(1~2)mg/kg[4,5]。为探讨亚甲蓝光病毒灭活血浆的安全性,现对亚甲蓝光化学法灭活病毒的有效性、对凝血因子的影响、输注的不良反应及血浆残余亚甲蓝的安全性综述如下。
1 亚甲蓝光化学法灭活血浆病毒的有效性 亚甲蓝与病毒核酸链嵌合,通过可见光激发,使能量转移产生高活性的单线态氧,后者氧化鸟苷,从而破坏核酸链,阻止病原体复制,实现对病毒的灭活[1]。亚甲蓝光化学法灭活病毒的能力依赖于亚甲蓝与核酸的结合,其对双链核酸病毒的灭活效果优于单链核酸病毒,尽管包含这两种类型核酸的病毒都可以被有效地灭活[6]。亚甲蓝光化学法可灭活血浆中大多数脂质包膜病毒,对无脂质包膜病毒的灭活效果表现不均一,且大多数无效。亚甲蓝光化学法对脂质包膜病毒人类免疫缺陷病毒、乙型肝炎病毒、丙型肝炎病毒、西尼罗病毒、单纯疱疹病毒的灭活效果良好,至少为4logs,甚至在5logs以上[1,6]。近年来,亚甲蓝光化学法不断地被用于研究对可通过血液传播的病毒或对血液造成潜在威胁的病毒的灭活效果,尤其对脂质包膜病毒的灭活。亚甲蓝光化学法对严重急性呼吸系统综合症冠状病毒、克里米亚-刚果出血热病毒、尼帕病毒、寨卡病毒、黄热病病毒、埃博拉病毒、中东呼吸综合征冠状病毒、登革热病毒、基孔肯雅病毒等近年来引起关注的脂质包膜病毒同样有良好的灭活作用[7-11]。此外,亚甲蓝光化学法对无包膜病毒的灭活效果不均一,例如对甲型肝炎病毒、猪细小病毒、脊髓灰质炎病毒无效,但能有效灭活猴空泡病毒40、杯状病毒、细小病毒B19[1,6]。亚甲蓝光化学法的灭活效果见表1。
2 亚甲蓝光化学法对血浆凝血因子的影响 亚甲蓝光化学法减少了经血传播病毒的感染风险,但在一定程度上导致凝血因子的损失。先前文献报道,亚甲蓝光病毒灭活血浆中凝血因子的回收率约为83%,且大部分凝血因子的回收率>80%,但以纤维蛋白原(FIB)、凝血因子Ⅷ(FⅧ)、凝血因子Ⅺ(FⅪ)降低明显[12]。虽然不同实验室对血浆进行亚甲蓝光化学法处理,造成凝血因子的损失有所差异,但GB18469-2012《全血及成分血质量要求》对亚甲蓝光病毒灭活血浆的质量规定:FIB含量≥2 g/L;总蛋白(TP)含量≥50 g/L;FⅧ≥0.5 IU/mL,保证了血浆输注的有效性[4, 13]。
GRAVEMANN U等研究发现,亚甲蓝光化学法对病毒的灭活效果和凝血因子活性的影响与灭活病毒期间的温度有关[14]。FⅧ和FIB在(22±2)℃时的活性降幅最大且随着血浆温度升高,凝血时间变化及凝血因子活性损失越大。此外,在(5±2)℃时,病毒的灭活效果明显低于高温条件下的灭活效果。因此,亚甲蓝光病毒灭活血浆制备的温度应严格控制。在灭活病毒期间,尽量不要打开医用病毒灭活箱门或者在里面加放血浆,以保证血浆病毒的灭活效果及凝血因子活性。此外,钟锐等研究发现,亚甲蓝光病毒灭活血浆的光照强度及滤器的使用对血浆凝血因子活性有不同程度的影响[15]。采用不同强度的荧光和红光照射对血浆外源性凝血途径无明显影响,但对内源性凝血途径有一定的影响,且随着光照强度的增加,导致活化部分凝血活酶时间(APTT)延长及FⅧ活性降低更明显。这可能是由于亚甲蓝光化学法的光化学效应对一些蛋白质产生损伤[6]。总之,亚甲蓝光化学法对凝血因子有影响,但严格控制温度、选择合适的光强度及滤器,可以在达到灭活病毒效果的同时,尽可能保留凝血因子的活性。
3 亚甲蓝用于血浆的安全性
3.1 亚甲蓝光病毒灭活血浆的安全性
3.1.1 过敏反应:亚甲蓝光化学法减少了经血传播病毒的感染风险,提高了血浆输注的安全性。免疫介导的反应是输注血浆最常见的不良反应。2011年,NUBRET K等报道了两例因输注亚甲蓝光病毒灭活血浆出现过敏性休克的病例,这使得对亚甲蓝光病毒灭活血浆的使用安全性提出质疑[16]。同年,法国国家药品监管机构决定逐步停止临床使用亚甲蓝光病毒灭活血浆。做出这一决定的一个原因是,相关研究报道,输注亚甲蓝光病毒灭活血浆的患者发生严重过敏反应的风险增加[1]。然而,这一更高的风险与法国一项单中心回顾性血液警戒报告及其他国家的研究并不一致。在法国一个地区为期10年的回顾性输血不良反应研究中发现,亚甲蓝光病毒灭活血浆输注的不良反应发生率为3/10 283,其中严重不良反应发生率为1/10 283,且过敏反应的发生率与未经病毒灭活的新鲜冰冻血浆和其他类型血浆无显著差异[17]。在希腊为期11年的研究中发现,过敏反应是新鲜冰冻血浆最常见的不良反应,输注亚甲蓝光病毒灭活血浆出现不良反应的发生率为1/24 593,比未灭活病毒的新鲜冰冻血浆低[18]。在西班牙加泰罗尼亚地区为期5年的研究中发现,输注亚甲蓝光病毒灭活血浆的严重过敏反应发生率有减少的趋势,从2008年的0.021%下降到2013年的0.010%[19]。在一项国际性多中心、前瞻性的研究中,输注亚甲蓝光病毒灭活血浆共19 315个单位,有8例出现不良反应,仅1例出现严重不良反应[2]。总之,与未灭活病毒的新鲜冰冻血浆相比,亚甲蓝光病毒灭活血浆的过敏反应及严重过敏反应发生率未见增加,表明其应用的安全性是可被接受的。
NUBRET K等报道的两例因输注亚甲蓝光病毒灭活血浆出现过敏性休克的病例中,两名患者均出现亚甲蓝皮内注射试验阳性,其中一名患者流式细胞术检测亚甲蓝激活嗜碱性细胞的活化试验阳性,表明了亚甲蓝光病毒灭活血浆中残余亚甲蓝的致敏性。DEWACHTER P等报道了一例输注亚甲蓝光病毒灭活血浆出现过敏性反应的病例,该患者对亚甲蓝的皮内实验及嗜碱性粒细胞活化试验呈阳性,同样证实了亚甲蓝光病毒灭活血浆中残余亚甲蓝的致敏性[20]。临床使用亚甲蓝导致的过敏反应也偶有报道[21]。由此可见,部分亚甲蓝光病毒灭活血浆引起的过敏反应可能与亚甲蓝相关。
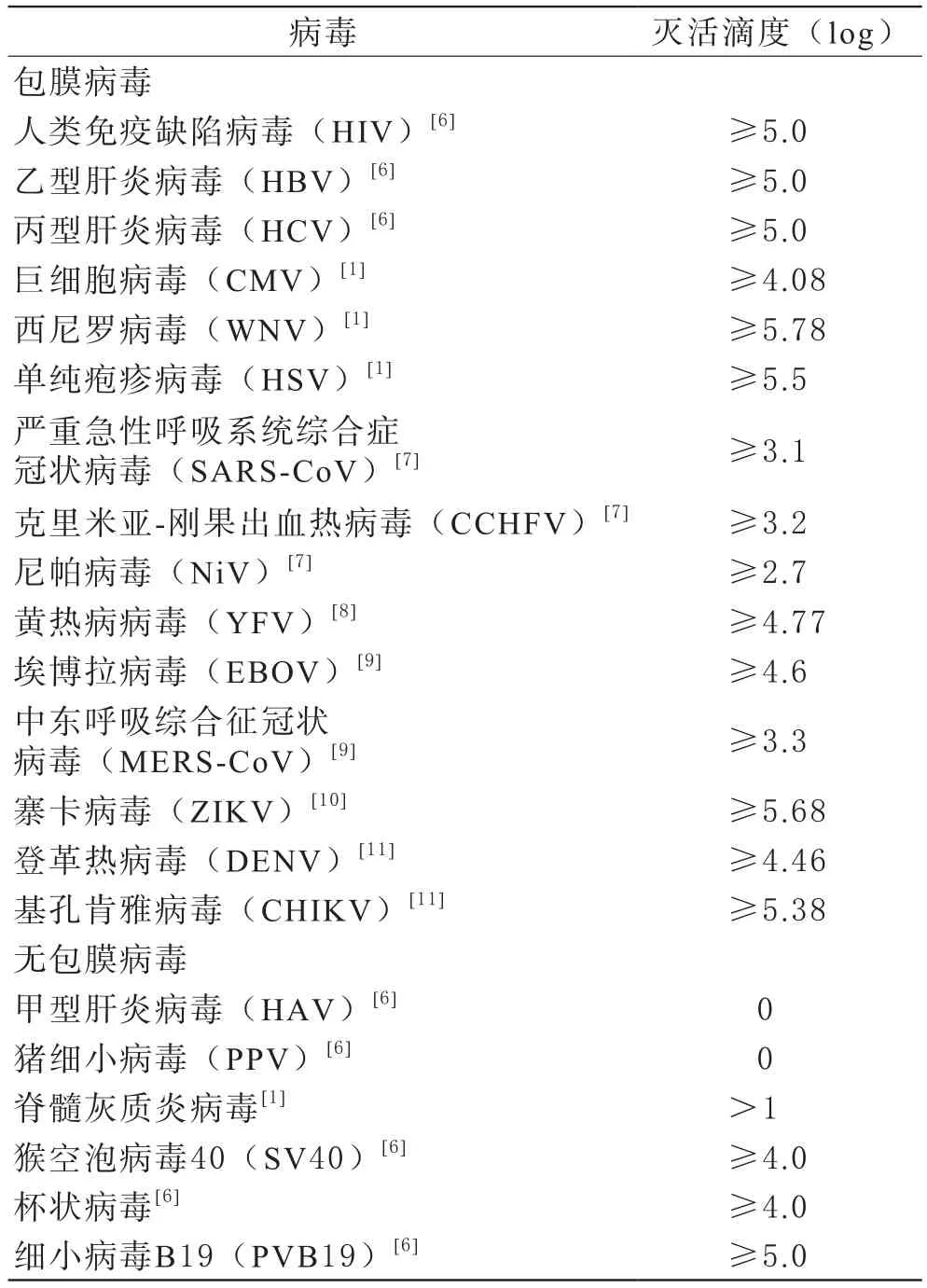
表1 亚甲蓝光化学法对病毒的灭活滴度
3.1.2 对免疫功能的影响:临床病人大多数存在免疫功能异常。亚甲蓝对免疫细胞有一定的调节能力。在百草枯中毒模型的实验中,亚甲蓝不仅改善胸腺细胞的氧化损伤,而且能够调节胸腺T淋巴细胞亚群在皮质和髓质区的分布,使机体持续性氧化损伤得到缓解[22]。在实验性自身免疫性脑脊髓炎动物模型中,亚甲蓝通过下调Th17/Treg细胞的比例和减少炎性细胞因子的产生来减轻炎症症状[23]。WERNER I等发现,亚甲蓝呈时间和剂量性影响人外周血单个核细胞(PBMC)的跨内皮细胞迁移能力[24]。姚仁南等发现,新鲜冰冻血浆与亚甲蓝光病毒灭活血浆对人细胞因子诱导的杀伤细胞的增殖及杀伤功能的影响无显著差异[25]。现有的研究来看,亚甲蓝对免疫细胞有一定的调节能力,但病毒灭活血浆残余亚甲蓝对免疫细胞的功能是否有影响有待进一步研究。临床病人大多数存在免疫功能异常,且大量输注血浆的患者多为免疫功能紊乱的危重病人,因此,血浆中残余亚甲蓝对需要大量输注血浆或反复输注血浆患者的免疫功能是否造成影响值得探讨。
此外,亚甲蓝的光化学效应对免疫细胞有一定的影响。在体外及牙周炎动物模型中,亚甲蓝介导的光动力疗法通过活性氧诱导巨噬细胞凋亡,缓解牙周炎症状[26]。TREVISAN E等发现,亚甲蓝介导的光动力疗法影响人中性粒细胞粘附性、产生活性氧及杀菌功能[27]。蓝光能激发亚甲蓝的光化学效应。相关的研究报道,进行蓝光治疗的新生儿在应用亚甲蓝后出现溶血反应[28]。因此,对于进行蓝光治疗的新生儿,亚甲蓝光病毒灭活血浆中残余亚甲蓝是否会对其免疫系统及其他身体机能造成影响值得探讨。
3.2 亚甲蓝作为临床治疗的安全性:亚甲蓝在临床常用的剂量为1~2 mg/kg,一般耐受性良好,但临床上使用亚甲蓝可出现潮红、头晕、恶心、四肢疼痛等不良反应[5]。亚甲蓝作为蓝色染料,临床使用可出现皮肤、尿液颜色改变,但这种影响一般可自行消退[5]。亚甲蓝是一种单胺氧化酶抑制剂(MAOI),剂量低至0.75 mg/kg可达到抑制中枢神经系统单胺氧化酶A(MAO-A)的水平[29]。MAOI与5-羟色胺能药物联合使用易导致中枢神经系统中5-羟色胺浓度增加,出现5-羟色胺综合征,严重者可能死亡[30]。在亚甲蓝诱导的5-羟色胺综合征的病例中发现,几乎所有患者均同时服用5-羟色胺能抗抑郁药[31]。因此,在使用亚甲蓝之前应慎重考虑5-羟色胺综合征的使用。AUERBACH SS等在为期2年的动物实验中发现,亚甲蓝对肿瘤的发生有影响,但仅在较高剂量下使肿瘤的发生率有所增加[32]。这在一定程度上反应了低剂量亚甲蓝使用的安全性。亚甲蓝过量使用,特别是在G6PD缺乏症患者中,易导致氧化溶血效应及高铁血红蛋白血症。近年来,亚甲蓝引起的溶血反应鲜有报道。ARUNACHALAM SN等报道了一例使用1 mg/kg亚甲蓝出现溶血反应的病例,虽然期间检查无G6PD缺乏,但仍高度怀疑为亚甲蓝所致[33]。早产新生儿使用亚甲蓝出现溶血反应已有病例报道[34,35]。它证明了新生儿使用亚甲蓝的风险,特别是在易感的新生儿中。虽然,有病例报道亚甲蓝在低剂量使用于无G6PD缺乏的患者出现高铁血红蛋白血症,但亚甲蓝引起的高铁蛋白血症更倾向于发生在其剂量超过4 mg/kg及G6PD缺乏症患者中[5,36]。正如AKAZAWA M等报道的,利用PUBMED、Web of Science、Scopus数据库统计了到2018年6月为止,有6例病例报道在腹腔镜手术中用亚甲蓝染色后出现高铁血红蛋白血症,其中5例为G6PD缺乏症患者[21]。因此,有必要在大剂量或持续输注亚甲蓝的情况下监测高铁血红蛋白水平及强调G6PD缺乏症患者禁止使用亚甲蓝。
亚甲蓝光病毒灭活血浆中残余亚甲蓝仅≤0.30 μmol/L,即≤0.096 mg/L,远低于临床引起不良反应的剂量,提示病毒灭活血浆中残余亚甲蓝对输注血浆患者具有较高安全性[4,37]。虽然病毒灭活血浆残余亚甲蓝浓度低下,但为达到血浆输注更高的安全性,可能需要在输注亚甲蓝光病毒灭活血浆前,了解病人有无相关过敏史、有无同时服用5-羟色胺能抗抑郁药、有无G6PD缺乏、肝肾功能状态等病史,以尽可能减少不良反应的发生。
4 总结 亚甲蓝光化学法对大多数脂质包膜病毒有良好的灭活效果,减少经血液传播病毒的风险。亚甲蓝光化学法灭活病毒的同时,造成血浆凝血因子的损失,但《全血及成分血质量要求》[4]对血浆质量的规定,保证了血浆输注的有效性。亚甲蓝光病毒灭活血浆不良反应的发生率与未灭活病毒的新鲜冰冻血浆相比无显著差异,提示其具有较高的安全性。虽然病毒灭活血浆中残余亚甲蓝浓度低下,但需要输血的患者大多数存在免疫功能异常,因此,血浆中残余亚甲蓝对需要大量输注血浆或反复输注血浆患者的免疫功能是否造成影响值得探讨。此外,由于蓝光能激发亚甲蓝的光化学效应以及新生儿免疫功能发育不完全,对于进行蓝光治疗的新生儿,亚甲蓝光病毒灭活血浆中残余亚甲蓝是否会对其免疫系统及其他身体机能造成影响值得探讨。亚甲蓝光病毒灭活血浆中残余亚甲蓝远低于其临床应用引起不良反应的剂量,提示病毒灭活血浆中残余亚甲蓝对输注血浆患者具有较高安全性,但针对亚甲蓝的临床不良反应,可能需要在输注亚甲蓝光病毒灭活血浆前,了解患者有无相关过敏史、有无同时服用5-羟色胺能抗抑郁药、有无G6PD缺乏、肝肾功能状态等病史,以达到亚甲蓝光病毒灭活血浆输注更高的安全性。
利益冲突所有作者均声明不存在利益冲突。

