青霉胺结晶热力学及拆分工艺研究
王东博,张蕾蕾,翟晶焕,张丽娟,刘锡建,朱雪焱,陆杰
(1 上海工程技术大学化学化工学院,上海201620; 2 中国医药工业研究总院化学制药部,上海201203)
引 言
目前,超过50%的药物活性成分具有手性[1],由于生物体内的受体或酶是手性的,往往只有一种对映体药物能够与其选择性地作用,进而提供所需的生理效应[2],而另一种对映体则没有这种相互作用,甚至是有害的[3]。例如,20 世纪60 年代的“反应停”事件——沙利度胺的悲剧,其沙利度胺R 构型对孕妇具有镇静作用,而S 构型具有强烈的胎儿致畸作用,但市面上销售的是沙利度胺的外消旋体,导致全世界数万畸形儿的诞生,这起事件引起了科学家对药物手性纯度的重视[4]。本实验研究的青霉胺(penicillamine,Pen)虽然构型相似,但药理作用完全相反。其中,D-青霉胺是一种重要的硫醇类化合物,临床上可用于治疗Wilson 氏病,亦可用作铜、汞等重金属解毒药[5]。近年来,研究还发现它能够用于治疗类风湿性关节炎和肝炎,以及预防婴幼儿视网膜等疾病[6]。然而,L-青霉胺却有相当大的毒性,对人体有毒害作用[7]。
结晶拆分法即通过结晶的方式,使得外消旋溶液中某一种对映异构体结晶析出,而另一种对映异构体仍留在溶液中,从而达到手性拆分的目的,一般包括非对映体成盐拆分[8-9]、优先结晶[10-12]、优先富集[13-14]、Viedma 熟化[15-17]等。其中,优先结晶法又称直接结晶法,具有简单、高效及便捷等特点,是一种重要的拆分手性异构体的方法,即向外消旋体的过饱和溶液中加入某一纯的对映体作为晶种,仅使该对映体的晶体从溶液中析出的方法[18-20]。
近年来,一些学者对青霉胺的手性分离进行了研究。Nakashima 等[21]、He 等[5]分别采用高效液相色谱和毛细管电泳法拆分其外消旋体。虽然其拆分方法能够获得较高纯度的单一对映体,但方法烦琐不能用于实际的工业生产。另外,国家对工业生产过程中的环境保护工作高度重视[22-23],因此开发环保、高效、便捷及能够实现工业化生产的结晶拆分技术,对D-青霉胺的实际生产与临床应用具有重要意义。
本项研究首先测定了DL-及D-青霉胺在273.15~333.15 K、不同质量比的乙醇-水混合溶剂中的溶解度,以此选定质量分数为34.47%乙醇-水作为降温结晶溶剂,并绘制不同温度下青霉胺溶解度曲线。结果表明其二元共饱和点的对映体过量值(ee值)为85%。随后,以313.15 K下、ee值为87%的饱和溶液为模型体系,研究了其在0.3 K/min、不同晶种量下的介稳区宽度(metastable zone width,MSZW),以及不同初始过冷度下的等温结晶过程和不同降温速率、不同晶种量的降温结晶过程,为青霉胺结晶拆分过程的理解、优化、工艺设计提供基础。
1 实验材料和方法
1.1 实验材料
D-青霉胺、L-青霉胺与DL-青霉胺(纯度>98%),北京百灵威科技有限公司;乙醇(纯度>99.7%),麦克林试剂;超纯水,上海乐枫生物科技有限公司Direct-Pure系统。
1.2 实验设备
低温恒温槽,F12-ME 型,德国优莱博公司;高效液相色谱仪(配有四元泵及自动进样器,DAD 检测器),1260 型,美国安捷伦公司;电子天平,XP 205型,梅特勒托利多集团;真空干燥箱,DZF-6050 型,上海慧泰仪器制造有限公司;热重分析仪,TGA PT-1000型,林赛斯(上海)科学仪器有限公司;X射线衍射仪,D2 PHASER 型,德国布鲁克公司;激光发射器、接收器等相关组件由西安赛普林激光技术研究所制造。
1.3 实验方法
1.3.1 固液平衡 室温下准确称量一定量的乙醇和超纯水置于某恒定温度的结晶器中,加入过量DL-青霉胺、D-青霉胺或不同初始ee 值青霉胺,恒温搅拌12 h,并静置6 h(在此项工作中利用激光检测系统在线监测溶液浊度变化情况。当搅拌6 h 后激光强度变化缓慢,当静置3 h 时后激光强度达到极大值并趋于稳定),注射器抽取上清液,用0.22 μm 的膜过滤器过滤后注入小瓶中,烘干,称重,用式(1)计算摩尔分数溶解度x[24-27]。残留固体分析其ee值、溶剂化以及晶型改变与否。
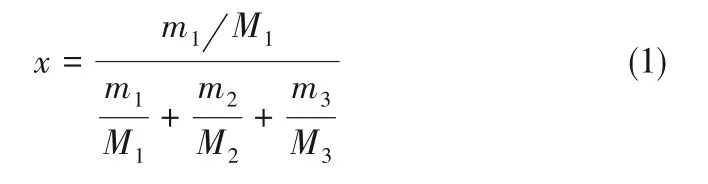
式中,m1、m2、m3分别表示青霉胺、去离子水、乙醇在饱和溶液中的质量,M1、M2、M3分别表示各自的摩尔质量。
1.3.2 介稳区宽度 D-青霉胺、DL-青霉胺以及ee值为87%溶液的介稳区宽度用激光检测法测定:根据溶解度曲线准确称取溶质与溶剂,放入结晶器后,将恒温水浴温度设置比饱和温度高5 K,搅拌2 h,待溶液稳定后,以0.3 K/min 恒定降温速率降温,待激光强度开始变弱,溶液变浑浊时记录溶液温度,此温度与饱和温度之差就是所测的介稳区宽度。
1.3.3 成核实验 配制ee 值为80%、87%、90%和95%在313.15 K 下的饱和溶液,分别快速移入温度已恒定在303.15、298.15、293.15、288.15 和283.15 K的结晶器中,当激光强度开始变弱,溶液浑浊时分析固体ee值。
1.3.4 恒温结晶 配制ee 值为87%在313.15 K 下的饱和溶液,移入温度已恒定在307.15、303.15、298.15 或293.15 K 的结晶器中,晶种量为无、1%、2%、4%或8%(相对于起始饱和溶液中D-青霉胺的量),以结晶时间间隔30 min 分析产品ee 值,并确定产品ee 值始低于99%的时间点及在该时间点下结晶收率(产品质量减去晶种加入量后与原料液中D-对映体的质量之比)。
1.3.5 降温结晶 配制ee 值为87%在313.15 K 下的饱和溶液,降温速率分别为0.05、0.1、0.2 和0.4 K/min,晶种量为1%、2%、4%或8%,以结晶时间间隔20 min 分析产品ee 值,并确定产品ee 值始低于99%的时间点及在该时间点下结晶收率。
1.3.6 高效液相色谱分析 采用高效液相色谱(HPLC)测量ee 值。色谱条件:大赛璐CR(+)手性色谱柱(4.0 mm×150 mm,5 μm),流动相为pH=1 的高氯酸-水溶液,流速为0.1 ml/min,柱温15℃,检测波长λ=202 nm,进样量5 μl。
2 实验结果与讨论
2.1 DL-和D-青霉胺在不同质量比乙醇-水混合溶剂中的溶解度
乙醇质量分数分别为0、16.21%、34.47% 和52.09%的乙醇-水混合溶剂中DL-及D-青霉胺在273.15~333.15 K 温度范围内的溶解度如图1所示。
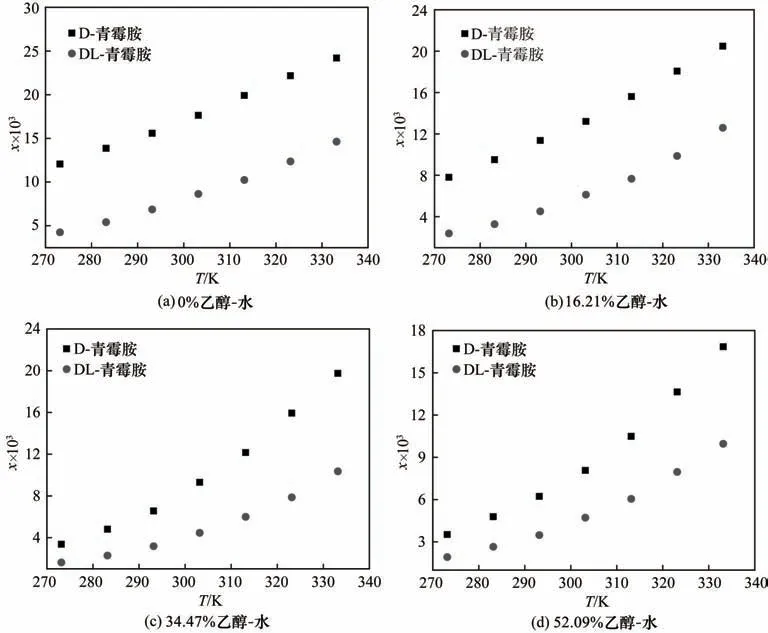
图1 DL-和D-青霉胺在不同质量比乙醇-水混合溶剂中的溶解度Fig.1 Solubility of DL-and D-penicillamine in ethanol-water mixed solvents with different mass ratios
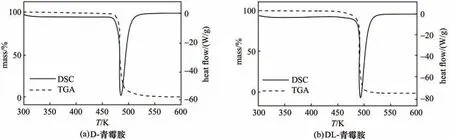
图2 D-和DL-青霉胺残余固体的热分析谱图Fig.2 DSC and TGA thermograms of the residual solids of D-and DL-penicillamine
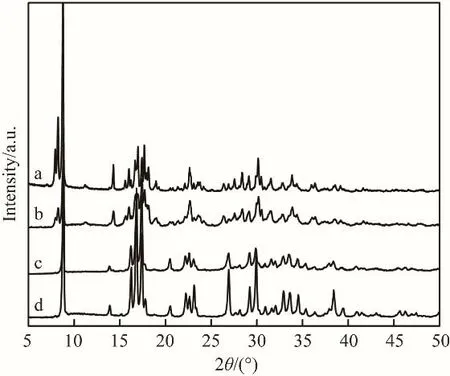
图3 D-和DL-青霉胺原料与固液平衡后残余固体的X射线衍射谱图Fig.3 XRD patterns of the raw materials and the residual solids after solid-liquid equilibrium of D-and DL-penicillamine
研究发现,在实验的温度范围下,D-及DL-青霉胺残余固体的热分析谱图如图2 所示,其原料与残余固体的X 射线衍射光谱如图3 所示,从图中可发现残余的固体无溶剂化及晶型改变现象。溶解度单调地随温度的升高而增大,且DL-青霉胺溶解度小于D-青霉胺溶解度,说明青霉胺外消旋体类型可能是外消旋化合物。此外,在纯水中,DL-及D-青霉胺溶解度非常大(293.15 K时,DL-和D-青霉胺摩尔溶解度分别为6.863×10-3和15.589×10-3),且随着混合溶剂中乙醇含量的增加,溶解度降低。
2.2 不同ee值青霉胺的溶解度
在乙醇质量分数为34.47%的乙醇-水混合溶剂中,273.15、283.15、293.15、303.15、313.15 和323.15 K六个固液平衡温度下不同ee值青霉胺的溶解度如图4所示。结果显示,在六个温度下,二元共饱和点ee 值不发生变化,始终为85%。六个温度下的溶解度曲线形状类似,可进一步证明青霉胺外消旋体为外消旋化合物[28]。
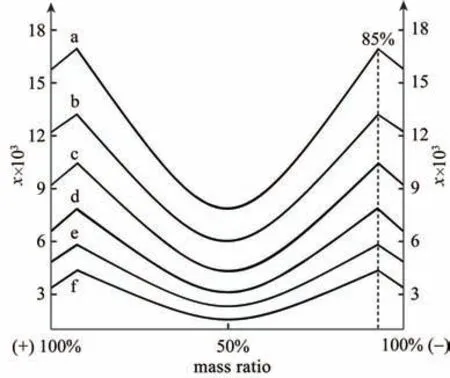
图4 不同ee值青霉胺的溶解度Fig.4 The solubility of penicillamine with various ee values
2.3 D-青霉胺、DL-青霉胺以及ee 值为87%溶液的介稳区宽度
在乙醇质量分数为34.47%的乙醇-水混合溶剂中不同温度下的D-青霉胺、DL-青霉胺及ee 值为87%饱和溶液的介稳区宽度如图5 所示。介稳区宽度随温度升高而减小,主要是因为在高温下溶液黏度降低,溶质扩散系数增大,分子热运动加剧,成核较低温时更容易,在实验温度范围内,相同饱和温度下的D-青霉胺溶液的介稳区宽度比外消旋体溶液的介稳区宽度宽[29]。ee 值为87%、温度为313.15 K 的饱和溶液在不加晶种时,其介稳区宽度为17.6 K;加入1%、2%、4%和8%晶种时,其介稳区宽度分别为16.4、15.3、13.0 和8.3 K。介稳区宽度随晶种加入量的增加而减小,这可能是由于加入的晶种降低了初级成核势垒,成核更容易,介稳区宽度减小。
2.4 成核实验
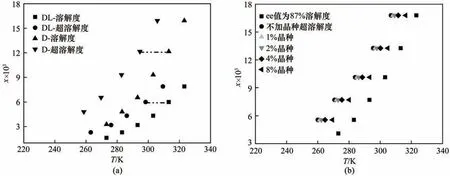
图5 D-青霉胺、DL-青霉胺和ee=87%饱和溶液的介稳区宽度Fig.5 The MSZW of D-penicillamine,DL-penicillamine and saturation solution with ee=87%
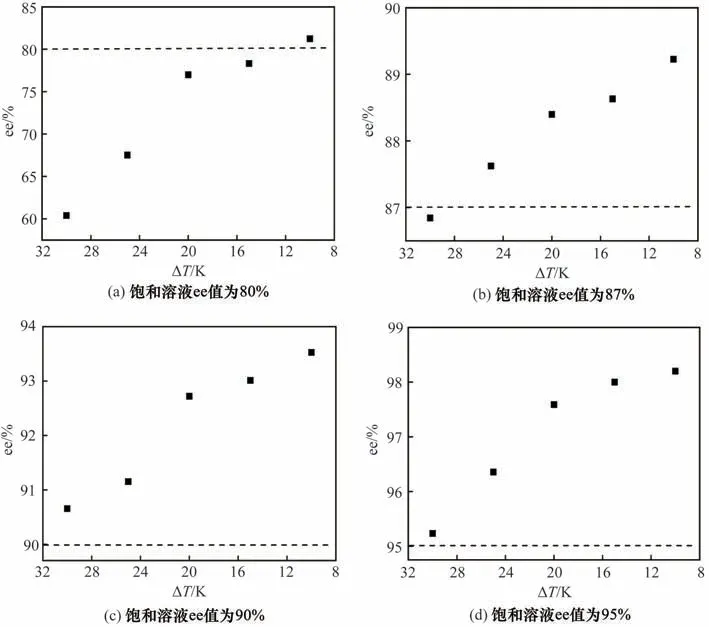
图6 过冷度对初始成核的影响Fig.6 Effect of subcooling on initial nucleation
313.15 K下不同ee值的饱和溶液在不同成核温度下的初始晶核的ee 值如图6 所示。成核温度越低、初始过冷度越大,晶核量越多,ee 值越小。反之,成核温度越高,初始过冷度越小,晶核量越少,ee值越大。如ee 值为87%、饱和温度为313.15 K 的饱和溶液[图6(b)],在283.15 K 成核时,晶核的ee 值为86.84%;在303.15 K成核时,晶核的ee值为89.23%。也就是说,对于青霉胺手性体系可通过优先结晶法提高产品ee值。
2.5 恒温结晶
2.5.1 不加晶种 ee 值为87%、313.15 K 下的饱和溶液在初始过冷度为6、10、15 和20 K 时固体ee 值随结晶时间的变化情况如图7所示。在四个恒定温度下,初始晶核的ee 值均大于87%,产品ee 值随时间先增大后减小,但增大过程的时间随结晶温度变化较大,例如ee 值增加趋势在293.15 K 下仅维持约2 min,而在307.15 K 下能维持约40 min。也就是说,初始晶核中D-对映体晶核比外消旋体晶核多,在其生长过程中,随着过饱和度的消耗,外消旋体晶体逐渐增多。
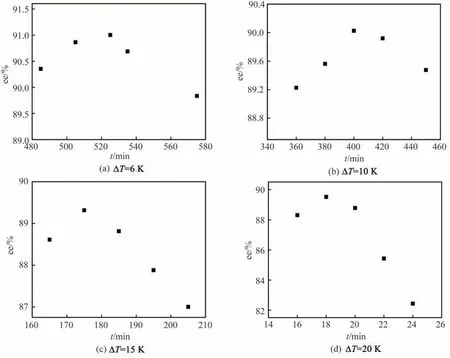
图7 固体ee值随结晶时间的变化Fig.7 Change of the ee value of solids with crystallization time
2.5.2 加晶种 ee 值为87%、313.15 K 下的饱和溶液在初始过冷度为6、10、15 和20 K 以及晶种量为1%、2%、4%和8%时固体ee值随结晶时间变化情况如图8 所示。与2.5.1 节不加晶种实验相比,加入晶种后,固体产品的ee 值随结晶时间单调地降低。在同样晶种加入量下,固体ee 值下降速度随初始过冷度的增加而增大。正如前文所述,晶种为1%、2%、4%和8%时,该饱和溶液介稳区宽度分别为16.4、15.3、13.0 和8.3 K。当采用过大的初始过冷度(如10、15 和20 K),加入的晶种量越多,诱导成核的速率和晶核量越高,产品ee 值越小且快速下降。当初始过冷度为6 K时,晶种量为2%的结晶产品ee值随时间变化最为缓慢。这是因为在该初始过冷度下,晶种量较大时,成核发生加快,晶核量增多,产品ee值较快下降;而晶种量较小如1%时,不足以诱导二次成核,且晶种提供的生长面较少,诱导期后的初级成核速率较大,产品ee 值相应下降较快。因此,结晶拆分应选择适宜的过饱和度及与其相应的晶种量。
2.5.3 结晶收率 按照2.5.2 节的实验结果重复实验并分析固体ee值始低于99%时间点时产品收率,结果如表1所示。产品收率随晶种加入量和初始过冷度的增大而增大。在实验采用的初始过冷度中,随初始过冷度的增加,收率增加逐渐变缓,这主要是因为初始过冷度较大时,产生的晶核较多,产品粒度较小。
2.5.4 过程分析 以初始过冷度为10 K、晶种量为2%为例,固体和母液ee值随时间变化情况如图9所示。固体ee 值在前300 min 缓慢减小,超过300 min后迅速下降。母液ee 值在前300 min 一直减小,说明D-对映体晶体和外消旋体晶体从母液中以不同速率析出,并逐渐变缓,超过300 min 后外消旋体晶体大比例析出,产品ee 值快速下降,母液ee 值快速上升,最终趋向于二元共饱和点ee 值。根据母液ee值变化绘制的结晶过程路线“trajectory”如图10 所示[30],溶液ee值先快后慢减小,到达拐点后逐渐增大至二元共饱和点ee值。
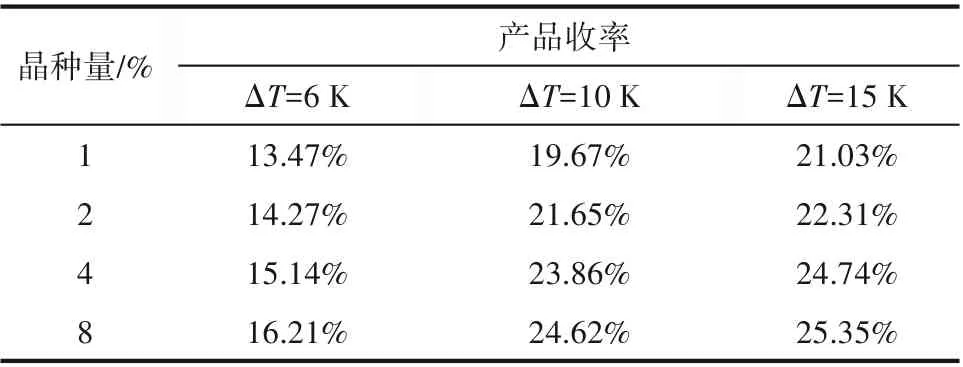
表1 青霉胺恒温结晶收率Table 1 Yield of penicillamine of thermostatic crystallization
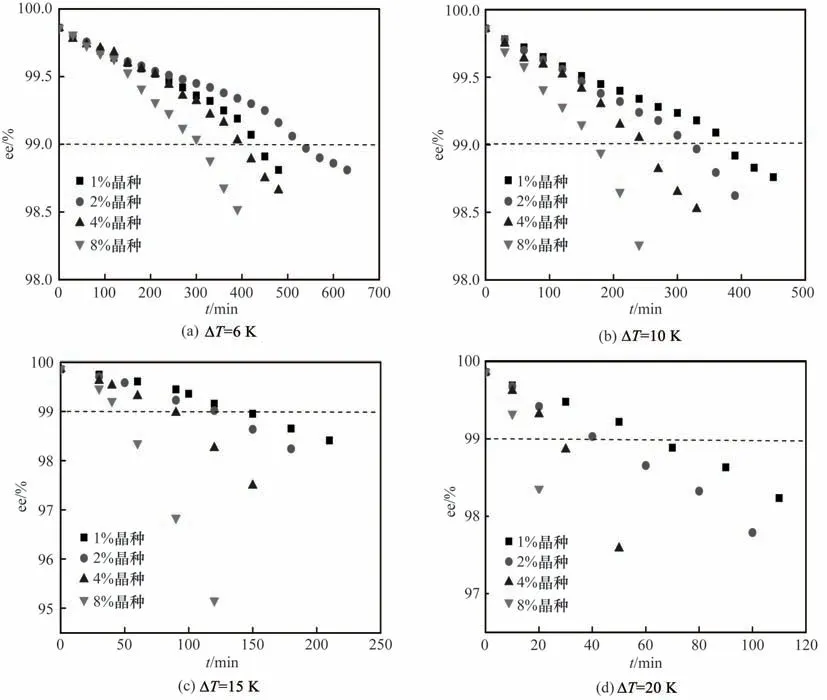
图8 固体ee值随时间变化曲线Fig.8 Curve of solid ee values over time
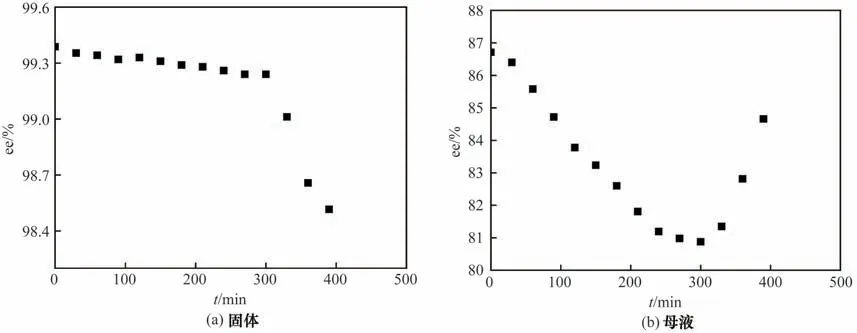
图9 结晶过程中固体和母液ee值变化Fig.9 Change in ee value of the solid and mother liquor during crystallization process
2.6 降温结晶
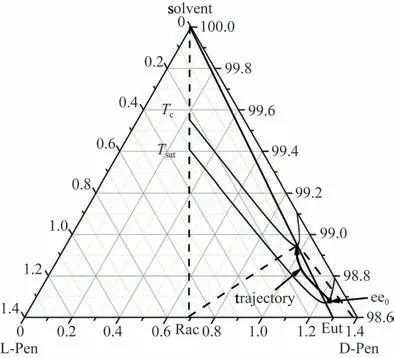
图10 青霉胺恒温结晶过程Fig.10 The thermostatic crystallization process of penicillamine
2.6.1 过程分析 ee 值为87%、313.15 K 下的饱和溶液在晶种量为1%、2%、4%和8%以及降温速率为0.05、0.1、0.2 和0.4 K/min 时固体ee 值随结晶时间变化情况如图11所示。在同一晶种加入量下,固体ee值下降趋势随降温速率的加快而增加,这是因为降温速率越快,成核推动力越大,成核速度快,产品光学纯度降低越快;在同一降温速率下,固体ee 值变化趋势随晶种加入量的增加而变缓,这是因为纯D-对映体晶种加入量越多,越高比例的过饱和度消耗于生长而不是成核,由于D-晶种具有一定的光学选择性,晶种越多,ee值降低越慢。
2.6.2 结晶收率 按照2.6.1 节的实验结果重复实验并分析固体ee值始低于99%时间点时产品收率,结果如表2 所示。在相同的起始料液和降温速率下,晶种加入量增加,收率增加,这与2.6.1节中结晶产品始低于99%的时间点越长是一致的。在相同的起始料液和晶种加入量下,降温速率减小,收率增加,这是由于:一方面,虽然到达固体ee 值始低于99%的时间点较长,但降低的温度较小,这会导致产品收率下降;但另一方面,降温速率的降低,产品粒度增大,过滤后产品也会增多。
3 结 论
(1)通过静态法测量溶解度数据,绘制不同温度下青霉胺溶解度曲线。同时测量了D-青霉胺、DL-青霉胺以及ee值为87%溶液的介稳区宽度。
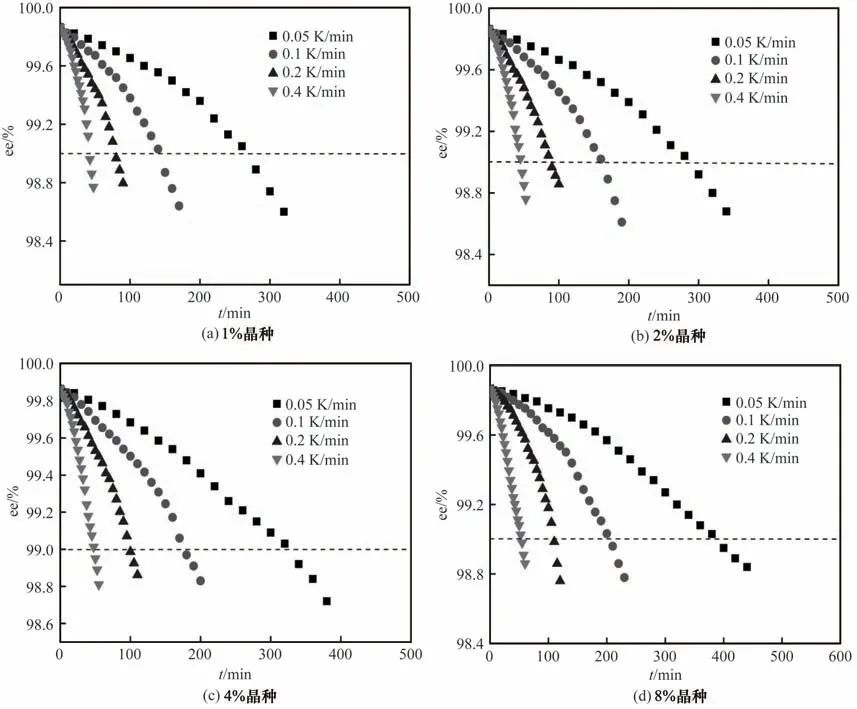
图11 固体ee值在不同降温速率中随时间变化曲线Fig.11 Curve of solid ee values over time at different cooling rates
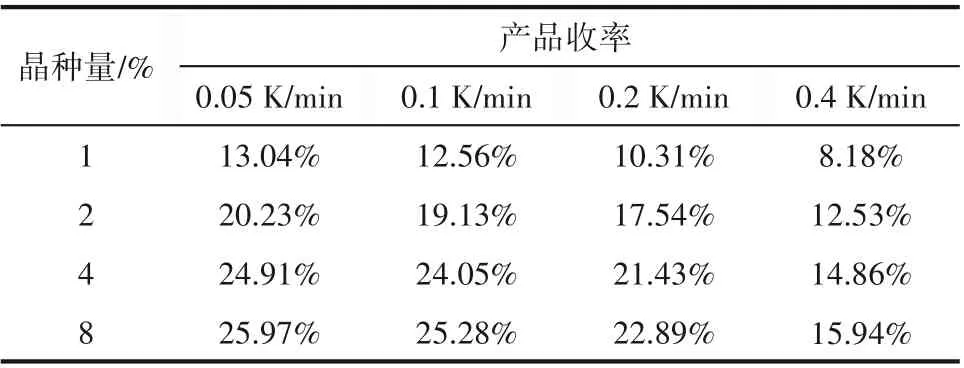
表2 青霉胺降温结晶收率Table 2 Yield of penicillamine of cooling crystallization
(2)通过成核实验发现,对于ee 值大于二元共饱和点的起始溶液,其初始晶核的ee 值总是高于起始溶液的ee 值,但随着成核温度的降低,初始过冷度的增加,晶核量越多,ee值越小。
(3)考察了降温速率、晶种量对降温结晶过程中产品ee 值和收率随时间的变化情况,对于相同的起始溶液,ee 值大于99%的产品收率随着晶种的加入量和降温速率的减小而增加。
(4)研究表明,对于青霉胺这一手性体系,优先结晶法可在一定程度上提高固体的光学纯度,但收率较低,需要开发更为高效的手性结晶拆分技术与工艺。
符 号 说 明
M——摩尔质量,g/mol
m——质量,g
T——热力学温度,K
ΔT——过冷度,K
t——时间,min
x——摩尔分数溶解度

