注射用青蒿琥酯含量测定能力验证结果评价
丁建东 朱荣 卢日刚 常艳 陈华 项新华
【摘 要】 [HTH]目的:[HTSS]通过组织化学药品注射用青蒿琥酯含量测定高效液相色谱法的能力验证,评价各参加实验室化学药品含量测定的能力。[HTH]方法:[HTSS] 采用单因子方差分析法对能力验证样品进行了均匀性实验 ,采用t检验对样品进行稳定性考察,均符合要求。采用经典统计Z比分数法,评价各参加实验室的结果。[HTH]结果:[HTSS] 报名参加本次能力验证计划的实验室共57家。94.6%的实验室结果为“满意”。[HTH]结论:[HTSS]国内实验室青蒿琥酯含量测定检测能力总体较好, 个别实验室的检测能力有待改进提高。
【关键词】 能力验证; 含量测定;高效液相色谱法;注射用青蒿琥酯
【中图分类号】R285.5 【文獻标志码】 A【文章编号】1007-8517(2021)01-0054-04
Data Assessment and Technical Interpretation of Proficiency Testing for Assays of Artesunate for Injection
DING Jiangdong1 ZHU Rong1 LU Rigang1 CHANG Yang2 CHENG Hua2 XIANG Xinghuang2*
1.Guangxi Institute for food and drug control, Nanning 530021,China;
2. National Institute for Food and Drug Control,Beijing 100050,China
Abstract:[WTHZ]Objective[WTBZ] The proficiency testing for assays of artesunate for injection by HPLC was organized to assess the competences of chemical content determination assays conducted by participants. [WTHZ]Method[WTBZ] The testing was implemented in conformity to CNAS schemes. Uniformity test was applied through One-Way ANOVA to samples, whose stabilities were studied by T test. The z-score was introduced for the assessment. [WTHZ]Results[WTBZ] 1 laboratory quitted among the 57 participants. 53 results were reported satisfactory. 2 performances were unsatisfactory and 1 result was susceptible.94.6% of the laboratory results were satisfactory. [WTHZ]Conclusion[WTBZ] The capacity of national laboratories for assays of artesunate for injection has been ranked as satisfactory according to statistical analysis of the proficiency testing program results. Only a small portion of the participants require further improvement in their capacities.
Keywords:Proficiency Testing; Assay; HPLC; Artesunate for Injection
能力验证是评价实验室技术能力的有效手段,是实验室通过外部措施对其内部质量控制方法的一种重要补充手段,是确保实验室质量管理体系持续改进的有效措施之一[1] 。实验室应该积极参与并认真对待每次能力验证,做到为我所用,不断提升自身管理能力和技术水平[2]。
注射用青蒿琥酯是我国拥有完全自主知识产权的创新药,也是首个获世界卫生组织推荐的重症疟疾一线治疗药物,目前研究发现青蒿琥酯在其他疾病的治疗上也有一定功效[3-5] 。高效液相色谱法是药品检验常用的检测方法[6],在药品检测领域有着广泛的应用,已为各国药典广泛收载。本次含量测定能力验证的主要目的是,考察药品生产企业QC实验室和药品检验实验室的检验技术水平及检测数据的准确性,确定实验室进行化学药品高效液相色谱法进行成分含量测定的能力,识别实验室中的问题以及实验室间的差异,增加实验室客户对实验室能力的信任。文章将就能力验证的实施过程和统计技术进行讨论。
1 仪器与试药
1.1 仪器 高效液相色谱仪,十万分之一电子天平。
1.2 试药 双氢青蒿素对照品(批号100184-201202)、青蒿素对照品(批号100202-200402)、青蒿琥酯对照品(批号100200-201003)均购自中国食品药品检定研究院;甲醇、乙腈为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法
2.1 样品制备 样品来源于桂林南药股份有限公司生产的原料药,为白色粉末,装于西林瓶,轧盖包装,每瓶装量约120 mg,随机数字编号,编号为QA0099-**** 。
2.2 样品均匀性、稳定性检验和运输实验
2.2.1 样品均匀性、常温稳定性、加速稳定性检验 随机抽取,随机抽取20瓶,在重复条件下测定2次。检验方法按《中国药典》2015年版二部“注射用青蒿琥酯”项下含量测定方法测定[7]。考察样品拟定包装,在常温放置0个月、1个月、2个月和在加速(温度40℃±2℃、相对湿度75%±5%)下放置的第5、10、15天分别随机抽取样品3份,进行重复测定2次,所得结果为稳定性的数据。
2.2.2 运输过程稳定性试验 根据地域分布,考虑距离和环境因素,选择距离较远、气温较高的3家实验室,海南、湖北、西藏各选一个邮寄试验点,各寄1份样品,嘱其原件邮回,收回后进行青蒿琥酯的含量测定,观察其稳定性情况。
2.2.3 引湿性检验 取样品约0.2 g,平铺于称量瓶中,精密称定,实验室环境下敞口放置,分别在10 min、30 min、60 min后称定,计算引湿增重。
2.3 检测要求 本次能力验证对每个参加实验室赋予了一个唯一代码。各参加实验室会收到 2 支标注为:“QA0099-实验室代码”的样品。作业指导书、结果报告单、被测物品接收状态确认表。要求实验室按照作业指导书的要求在规定的期限内进行检验并反馈检验结果。
2.4 参加实验室的具体情况 本次能力验证共有57家实验室报名参加,最后反馈检验结果的为56家。提交结果。参加实验室分布于22个省(自治区)、直辖市,其中,食品药品检验机构42家,药品生产企业QC实验室4家,其他检验机构10家。
2.5 能力验证数据统计分析的设计及评价原则
2.5.1 统计分析的设计 本次能力验证采用经典统计[8]技术方法对结果进行统计分析,即采用经典统计计算各实验室结果的 Z 比分数统计的算术平均值作为指定值,传统标准差作为能力评定标准差。能力验证样品为单一浓度样品,按下式分别计算本次能力验证计划参加者的检测结果,按公式计算Z值:Z=(x-X)/σ,式中x为参加者测试结果;X为算术平均值;σ为能力评定标准差。
本次能力验证以Z比分数评价实验室的结果,即:若|Z|≤2,检测结果为满意;若 2<|Z|<3,检测结果为有问题;若|Z|≥3,检测结果为不满意或离群值。
2.5.2 评价原则 本次能力验证以每个实验室报告的样品的检测结果为基础,采用经典统计技术进行处理,用算术平均值作为指定值,传统标准差作为能力评定标准差。主要统计量包括:样本数、算术平均值、传统标准差等。
3 统计处理及统计分析评价
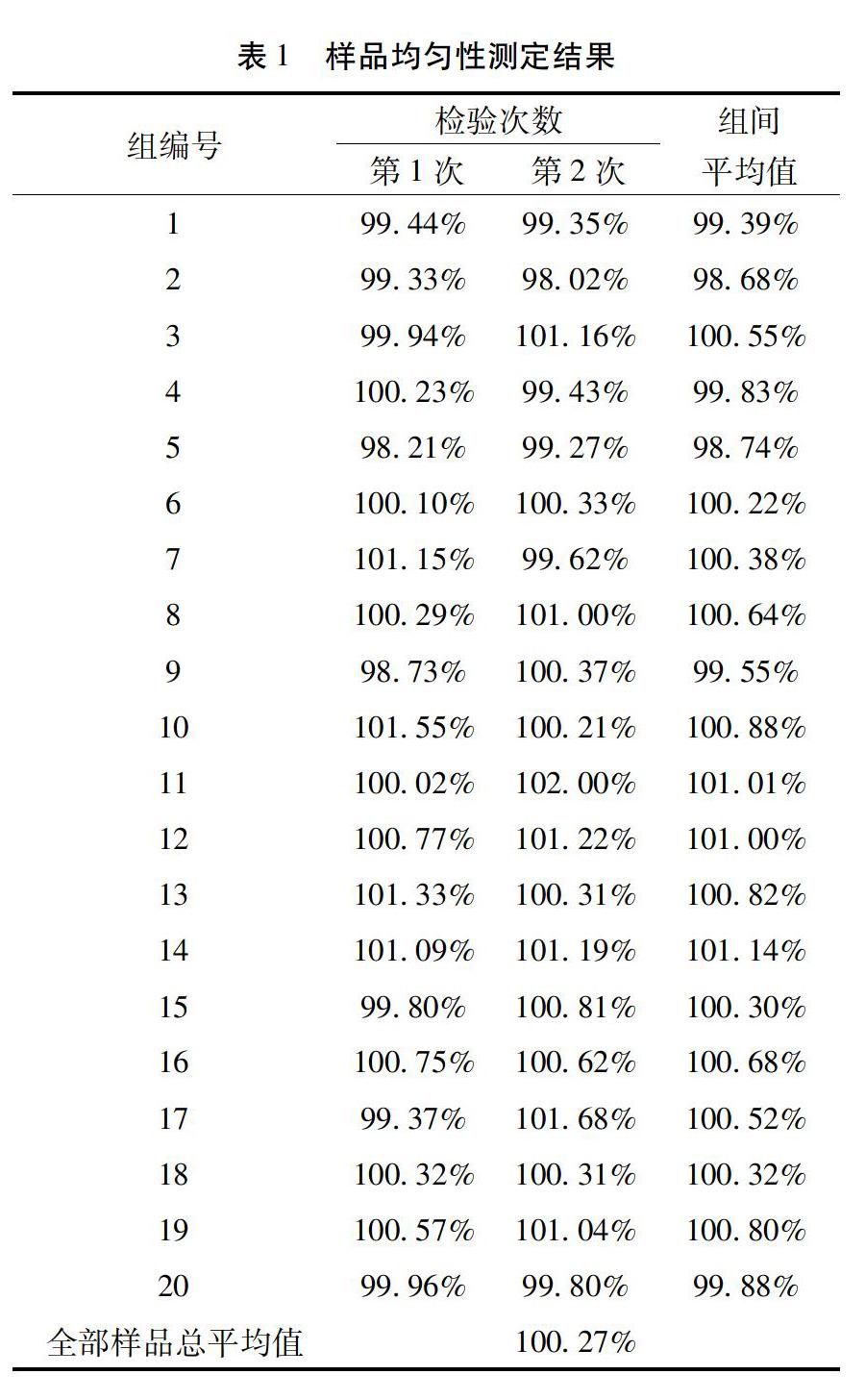
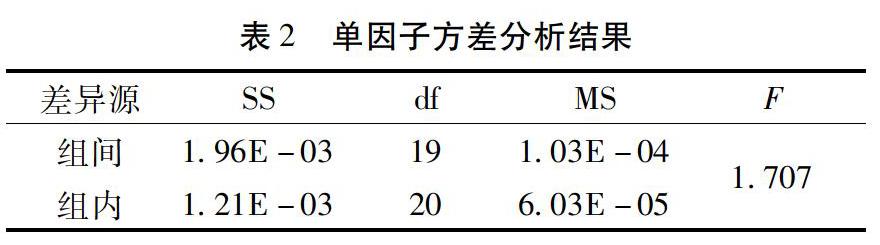
3.1 样品均匀性检验结果 采用单因子方差分析法[9]对检验结果进行统计处理,均匀性的试验测定结果和方差分析见表1和表2。样品检测值的 F 值为 1.707,均小于 F 临界值 F0.05(19,20) (2.137),组间无显著差异:F
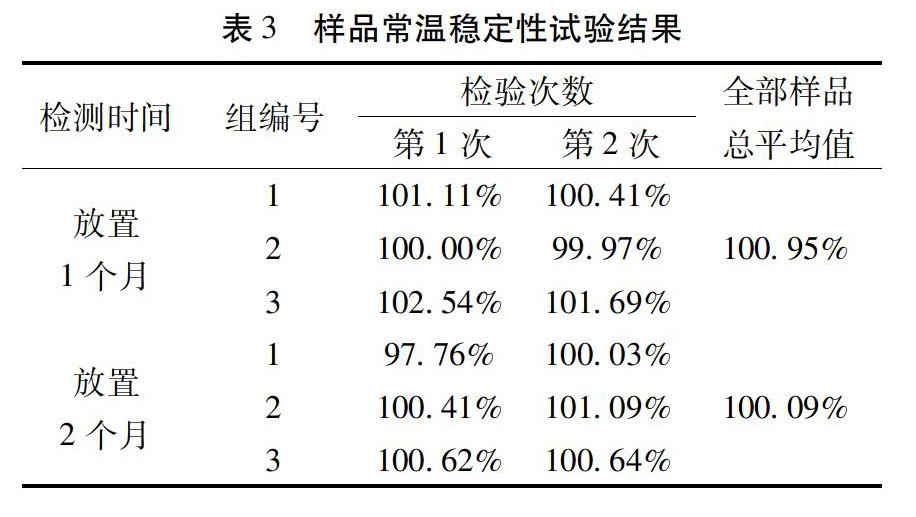
3.2 样品稳定性检验结果 根据样品均匀性试样,样品的初始含量100.27%。样品进行常温稳定性试验的结果和统计分析结果分别见表3。
采用 t 检验法[9],分别对常温稳定性检验(F 值1.016,小于Fcrit 3.982)、加速稳定性实验(F 值1.356小于Fcrit 3.239)、运输实验的样品(F 值4.559小于Fcrit 5.192)结果进行统计处理, F 值均小于F 临界值,且P-value>0.05,表明无显著性差异,样品的稳定性符合要求。
3.3 引湿性检验结果 取样品约0.2 g,平铺于称量瓶中,精密称定,实验室环境下敞口放置,分别在10 min、30 min、60 min后称定,计算引湿增重,均小于0.1%,表明试验取样时,水分对结果的影响可以忽略。
3.4 能力验证结果 报名参加本次能力验证计划的实验室共57家。1家中途退出,56家报告了结果。使用SPSS(13.0版本)数理统计软件对56家实验室测得的青蒿琥酯含量数据进行Kolmogorov-Smirnov法正态性检验 ,结果显示:Kolmogorov-Smirnov Z值为0.863,P值大于0.05(P=0.446),接受正态分布的假设。同时采用格拉布斯准则[11]判断无异常值,基于这种分布,适合采用经典统计办法评价各参加实验室的检测结果。经典统计参数汇总见表4。结果满意的、不满意的、可疑的实验室分别为53家、2家和1家,占反馈结果实验室总数(56家)比例分别为94.6%、3.6%和1.8%。为了清晰表示各实验室参加能力验证计划的结果,能力验证的结果使用Z比分数柱状图表示(见图 1),使每个实验室能够很容易地与其它实验室的结果进行比较。[FL)]
4 技术分析及技术建议
4.1 不满意和可疑结果原因分析 色谱分离及色谱行为欠佳从本次能力验证提供的原始记录系统适用性色谱图看,2家离群的实验室中,1家分离度1.4,未達要求,主峰明显变形,导致其含量测定结果与其他实验室之间有较大的差异;有一家色谱峰主峰略有变形。1家实验室的主峰与双氢青蒿素之间还有未知峰积分,存在色谱行为相关参数相对较差的现象。
4.2 记录问题 记录存在以下问题:①液相色谱分析图谱缺系统适用性试验图;②对照品的配置中未见称量记录;③缺对照品的称量记录及对照品批号等关键信息记录;④有手动积分的情况。以上数据反映部分参加实验室在数据的可靠性、完整性方面的管理有待提高。
4.3 电子数据存储问题 原始记录有2家实验室的色谱图没有存盘路径,建议为利于检验的溯源,图谱的存盘路径应包含操作者姓名,一目了然,便于检索,建议为://姓名/检品编号+检品名称;有2家色谱数据采集方法、分析方法和结果图,保存于系统盘(C盘),建议实验室加强数据的安全性管理,以免系统崩溃时,数据无法恢复,给溯源带来问题。
4.4 技术建议 此次能力验证94.6%的实验室结果为“满意”,说明多数实验室在执行中国药典标准时能够保证测定结果的重现性和准确性。但也有少部分实验室由于色谱条件不够理想、实验操作不规范,导致测定结果为“可疑”甚至“不满意”,建议加强人员色谱技术分析的培训。
5 讨论
5.1 设备和色谱柱情况 根据各实验室提交原始记录,使用的仪器设备和色谱柱均不同,在本次计划中有17种不同品牌和10种规格的色谱柱被使用,涉及6种进口品牌7种不同型号的高效液相色谱仪。提示,设备型号和色谱柱对该检测结果影响不大,表明标准的适用性良好。
5.2 科学选择统计方法 本次能力验证曾采用稳健统计(四分位距)Z比分数法对实验结果进行统计,结果有5家离群,3家可疑,满意率为83%,但由于实验室上报数据相对较集中,稳健统计四分位法计算得到的标准偏差过严,导致满意率明显下降,易出现统计学“弃真”错误。改用经典统计,可有效避免这类错误。所以,为确保能力验证计划的科学性,使所有参加能力验证活动的实验室都能获得公平公正的评价,选择合适的统计方法十分重要[11]。
5.3 记录的重要性 本次能力验证采用经典统计Z比分数法,对实验结果进行统计,绝大多数实验室获得了满意的结果,真实的反映了实验室的能力水平。但从各实验室提交的原始记录看,还存在一定的问题,实验室需引起重视并加以改进。详实的记录是质量体系成熟的标志,是支持检验结果和保护实验人员的最佳物证[12],同时也是实验能够溯源和复现的依据。
6 结论
通过本次注射用青蒿琥酯含量测定能力验证活动,结果表明,实验室高效液相色谱法的检测能力总体较好, 个别不满意实验室应进一步查证原因,采取措施及时纠正。今后不仅要加强药品检测人员的业务综合技能的培训,还要重视实验记录的重要性,确保检测数据的溯源性及准确可靠性。
参考文献
[1]
席静,张思群,刘静宇,等.论能力验证活动对实验室能力建设的作用和意义[J].中国卫生检验杂志,2011,21(6):1576-1578.
[2]丁秀琼,林锏锐,郑俏慧,等.化妆品中微生物检测能力验证结果分析[J].中国卫生检验杂志,2017,20(10):2935-2952.
[3]岑彦艳,赵祎博,李攀,等.青蒿琥酯的药代动力学以及相关药理作用研究进展[J].中国中药杂志,2018,43(19):3970-3978.
[4]程瑶,孟岩,郑岩,等. 青蒿琥酯白蛋白纳米粒的制备及抗肿瘤活性初步研究[J].中国民族民间医药,2016,25(24):33-36.
[5]ZHANG Y,HE W,DU Y W,et al. Dimeric artesunate phospholipid-conjugated liposomes as promising anti-inflammatory therapy for rheumatoid arthritis[J]. International Journal of Pharmaceutics, 2020(579):119178.
[6]國家药典委员会编.中国药典[S].四部.北京:中国医药科技出版社,2015:59-61.
[7]国家药典委员会编.中国药典[S].二部.北京:中国医药科技出版社,2015:539.
[8]CNAS-GL002:2018,能力验证结果的统计处理和能力验证评价指南[S].北京:中国标准出版社,2018.
[9]CNAS-GL003:2018,能力验证样品均匀性和稳定性评价指南[S]. 北京:中国标准出版社,2018.[ZK)]
[10][ZK(#]GB/T 63.79.2-2004,测量方法与结果的准确度(正确度与精密度)第2部分:确定标准测量方法的重现性与再现性的基本方法[S]. 北京:中国标准出版社,2018.
[11]赵新玥,陈华.药品检验能力验证统计方法研究[J].中国药学杂志,2017,52(2):319-322.
[12]石岩,肖新月,熊婧,等.加强药品检验机构理化实验室参与能力验证工作[J].中国药事,2012,26(6):582-584.
(收稿日期:2020-07-17 编辑:刘斌)

