Al对Cu-20Ni-19Fe合金微观组织和 高温抗氧化性能的影响
刘英 梁志敏 王立伟 彭珍珍 汪殿龙


摘 要:為了解决Cu-Ni-Fe惰性阳极在铝电解过程中高温抗氧化性能差的问题,采用真空熔炼法制备不同Al含量的Cu-20Ni-19Fe-xAl(x=0%,6%,8%,10%,质量分数,下同)合金,于850 ℃和1.013×105 Pa氧分压下进行高温氧化实验,氧化时间为100 h,研究Al添加量对合金微观组织结构及高温氧化性能的影响。结果表明:铸造Cu-20Ni-19Fe合金由富Ni/Fe的枝晶相(γ1)和富Cu,Ni的基体相(γ2)组成;添加6% Al的Cu-20Ni-19Fe合金,Al固溶在合金基体中;添加8%和10%Al的Cu-20Ni-19Fe合金,微观组织中形成了针状或块状NiAl相,且NiAl相随Al含量的增加而增多;Cu-20Ni-19Fe合金在850 ℃和1.013×105 Pa氧分压下氧化动力学呈直线规律;添加Al元素后,合金的高温氧化动力学曲线由直线转变为指数规律,Al含量越高,合金氧化速率指数越小。Al元素的加入提高了Cu-20Ni-19Fe合金的高温抗氧化性能,使其有望成为惰性阳极铝电解中的备选阳极材料。
关键词:有色金属及其合金;Cu-Ni-Fe合金;微观组织;高温氧化;铝电解
中图分类号:TG171 文献标识码:A
doi:10.7535/hbkd.2021yx03012
Effect of Al on the microstructure and high temperature oxidation performance of Cu-20Ni-19Fe alloy
LIU Ying1,2, LIANG Zhimin1,2, WANG Liwei1,2, PENG Zhenzhen1,2, WANG Dianlong1,2
(1.School of Materials Science and Engineering,Hebei University of Science and Technology,Shijiazhuang,Hebei 050018,China;
2.Hebei Key Laboratory of Material Near-net Forming Technology,Shijiazhuang,Hebei 050018,China)
Abstract:In order to solve the problem of poor oxidation resistance of Cu-Ni-Fe inert anode at high temperature during aluminum electrolysis,Cu-20Ni-19Fe-xAl alloys (x=0%,6%,8%,10%) with different Al contents were prepared by vacuum melting method,and the alloys were used for the high temperature oxidation experiments which were carried out at 850 ℃ with oxygen partial pressure of 1.013×105 Pa and oxidation time of 100 h,and the effects of Al addition on the microstructure and high temperature oxidation properties of the alloy were investigated.The results show that the as-cast Cu-20Ni-19Fe alloy is composed of Ni/Fe-rich dendritic phase (γ1) and Cu/Ni-rich matrix phase (γ2);Al was dissolved in the Cu-20Ni-19Fe alloy matrix with 6% content of Al added;The needle-like or blocky NiAl phase was formed in the microstructure of Cu-20Ni-19Fe alloy with 8% and 10% Al added;The content of NiAl phase increases with the increasing addition of Al;The oxidation kinetics of Cu-20Ni-19Fe alloy follow the straight line under 850 ℃ and oxygen partial pressure of 1.013×105 Pa;After the addition of Al,the oxidation kinetic curve of Cu-20Ni-19Fe-xAl alloy follow an exponential law,and the oxidation rate index of the Cu-20Ni-19Fe-xAl alloy was much smaller with more content of Al.The high-temperature oxidation resistance of Cu-20Ni-19Fe alloy was greatly improved by the addition of Al,which proves the Cu-20Ni-19Fe alloy may be used as an alternative anode material for aluminum electrolysis.
Keywords:
nonferrous metals and their alloys;Cu-Ni-Fe alloy;microstructure;high temperature oxidation;aluminium electrolysis
Cu-Ni合金由于具有优良的力学性能和耐腐蚀性而得到了广泛应用[1-2]。在Cu-Ni合金中加入Fe元素,可以提高合金的高温力学性能;加入Al元素,可以形成NiAl相,提高合金的强度和耐腐蚀性能[3],用作新型无碳铝冶炼中的阳极材料[4-7]。然而,在无碳铝冶炼用阳极材料的工程应用中,电解析氧高温熔盐环境会使Cu-Ni合金因铜的快速扩散氧化而表现出较差的抗氧化性能。电解原铝中Cu杂质含量过高[8-9],会限制Cu-Ni基阳极材料的工程化应用。
在合金中添加活性元素,是一种常见的提高合金力学性能和抗氧化性能的方法。在高温合金[10]和铝电解惰性阳极材料[11-13]中,一般添加Al和Cr等选择性氧化元素或稀土元素[14],合金氧化过程中能在其表面形成具有保护功能的Al2O3 ,Cr2O3或其他复合氧化物膜层,保护合金基体,避免其被进一步氧化。由于铜的氧化物不具有自保护性,因而通常情况下通过向铜中添加适当的合金元素来改善铜的抗氧化性能[15]。为了拓展铜合金的应用领域,尤其是Cu-Ni合金在无碳铝冶炼工艺所处高温、氧化性冰晶石熔盐环境中的应用,笔者以Cu-Ni合金为基体,通过添加Fe提高合金的熔点及其在高温环境下的力学性能,制备Cu-20Ni-19Fe三元合金,研究Al添加量对Cu-20Ni-19Fe合金铸态组织和高温抗氧化性能的影响,为Cu-Ni合金在铝电解高温冰晶石熔盐中的应用提供数据支撑。
1 实验过程
合金采用高纯电解镍板、高纯铜板、高纯铁棒和高纯电解铝锭作为原材料,分别配制4种不同Al含量的Cu-20Ni-19Fe-xAl(x=0%,6%,8%,10%,质量分数,下同)合金材料。采用熔模铸造法制备合金,将其在真空感应炉中熔炼后浇注成尺寸为300 mm×150 mm×60 mm的铸件。采用线切割方法,将Cu-20Ni-19Fe-xAl合金铸件加工成Φ10 mm×4 mm的圆柱试样,将样品表面经机械抛光和砂纸打磨,去除表面油污和氧化物层,用乙醇超声清洗,烘干冷却后,用游标卡尺测量试样的表面积,再用精密天平测量试样的原始质量,待用。合金经腐蚀后(腐蚀溶液为2 g Fe(NO3)3+2 mL HCl+40 mL酒精+40 mL蒸馏水),采用LaiCa DM4000M光学显微镜观察金相组织。合金高温氧化性能的测试在Setsys Evo 1750型同步热分析仪(法国赛特拉姆公司提供)上进行,氧化温度为850 ℃,氧分压为1.013×105 Pa,氧化进行时间为100 h。实验过程中,用仪器自动记录样品氧化增重随氧化时间的变化,得到不同Al含量下的Cu-20Ni-19Fe-xAl合金在850 ℃时的高温氧化动力学曲线。采用JSM-6360LV型扫描电子显微镜观察合金氧化后膜层表面及截面的微观组织形貌。
2 结果与分析
2.1 合金微观组织
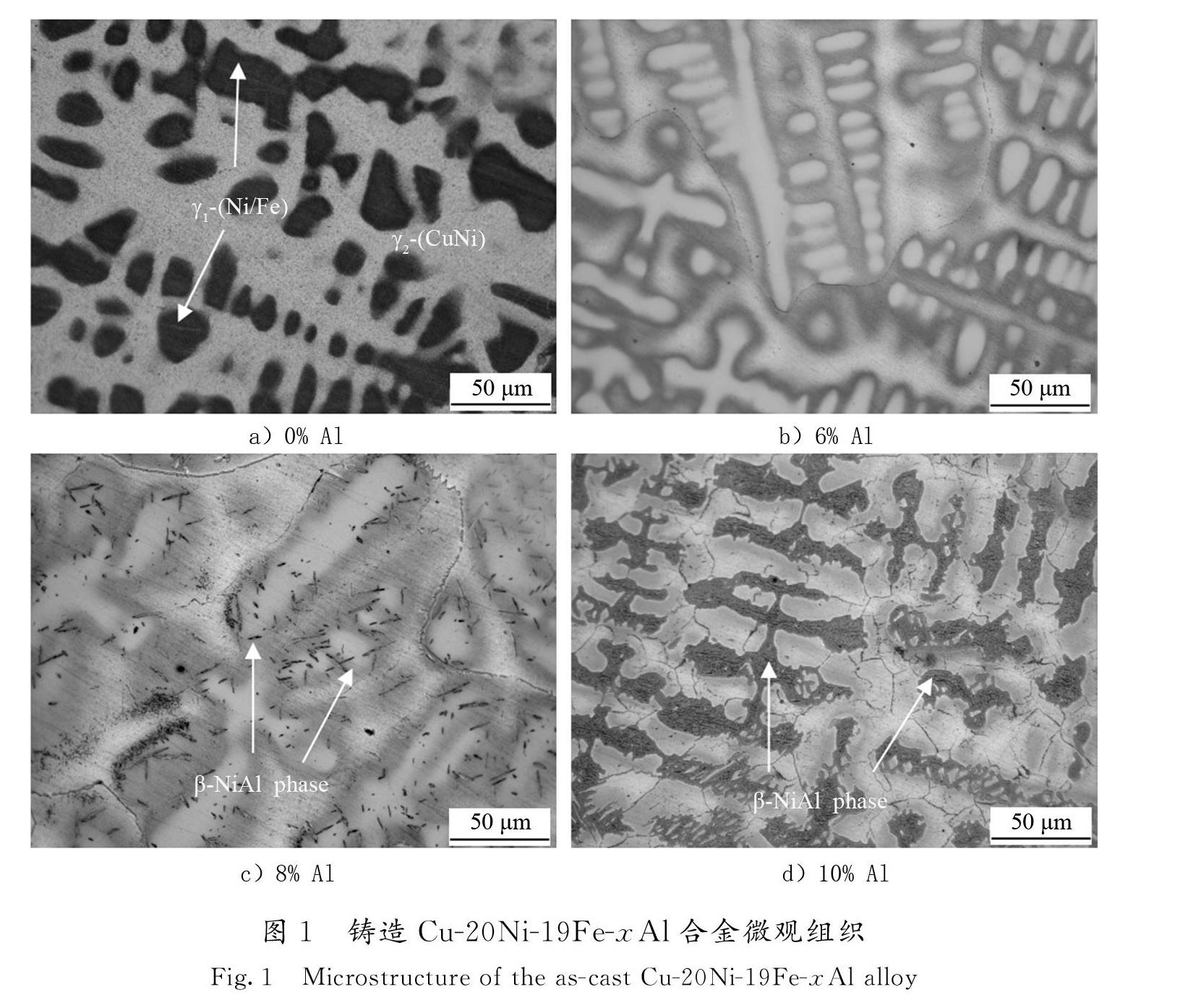
图1为Cu-20Ni-19Fe-xAl合金铸造后金相微观组织,图2为Cu-Ni-Fe三元合金在20 ℃下的等温相图[16]。从图1 a)和图2可以看出,不添加Al的Cu-20Ni-19Fe三元合金铸态微观组织中存在两相,实验用成 分为Cu-20Ni-19Fe的三元合金处于γ1和γ2两相区,对应铸态组织中的两相,深色的为富Ni/Fe枝晶相(γ1),浅色的为CuNi基体相(γ2),树枝状γ1枝晶均匀分布于γ2相基体中,枝晶大小为20~200 mm。图1 b)—图1 d)为添加不同Al后Cu-20Ni-19Fe-xAl合金的微观组织。从图1 b)可以看出,添加6%Al的Cu-20Ni-19Fe-6Al合金基体组织与不添加Al的Cu-20Ni-19Fe合金类似,组织中只有富Cu相以及富Ni和Fe的枝晶相。图1 c)所示为添加8%Al的Cu-20Ni-19Fe-8Al合金微观组织,可以看出,合金组织中除富Cu相、Ni和Fe枝晶相以外,还有针状NiAl相生成,针状NiAl相主要沿原始的Ni/Fe枝晶相分布。图1 d)所示为添加10%Al的Cu-20Ni-19Fe-10Al合金微观组织,相比于图1 c),图1 d)中生成了大量的块状NiAl相,覆盖了原来的Ni/Fe枝晶相(见图1 b)),分布于合金基体中。通过对微观组织进行分析對比可以看出,Cu-20Ni-19Fe合金中添加的Al元素含量高于8%时会形成NiAl相,随着Al含量的增加,NiAl相由针状变成大面积的块状相,且含量增加。
2.2 合金高温氧化动力学曲线
图3所示为Cu-20Ni-19Fe合金在850 ℃下氧化100 h的高温氧化动力学曲线。
从图3中可以看出,Cu-20Ni-19Fe合金在850 ℃高温下氧化动力学曲线呈直线规律,在氧化初期前5 h,合金的氧化增重急剧增加,随着氧化时间的延长,氧化增重呈直线规律,当氧化至100 h时,Cu-20Ni-19Fe合金的氧化增重为65 mg/cm2。对Cu-20Ni-19Fe合金在850 ℃下的氧化动力学曲线进行直线拟合,拟合方程如下:
Δm=a+k0t。(1)
式中:Δm为合金单位面积的氧化增重,mg/cm2;k0为氧化速率常数,mg/(cm2·h);t为氧化时间,h。拟合后k0为0.60 mg/(cm2·h),拟合参数见表1。
图4为添加不同Al的Cu-20Ni-19Fe-xAl合金在850 ℃及1.013×105 Pa氧分压下氧化100 h后的氧化动力学曲线。从图4可以看出,在氧化初期的前10 h内,合金氧化增重随氧化时间的延长迅速增加;之后,随着氧化时间的延长,合金氧化增重逐渐减缓,整个氧化过程呈指数规律。另外,从图4中的氧化增重数据还可以看出,添加6%,8%和10% Al的3种合金在850 ℃氧化100 h后,单位面积氧化增重分别为0.72,0.53和0.47 mg/cm2,远低于不添加Al的Cu-20Ni-19Fe合金氧化100 h后的增重(65 mg/cm2),添加的Al含量越高,合金氧化增重越小,说明合金高温抗氧化性能越好。对合金氧化增重曲线应用幂函数方程进行拟合,拟合式如下:
Δm=ktn。(2)
式中:Δm为合金单位面积氧化增重,mg/cm2;k为氧化速率常数;t为氧化时间,h; n为氧化速率指数。
表2列出了按照幂函数方程进行拟合后的氧化速率指数n和氧化速率常数k以及曲线拟合相关度R的值,添加6%和8% Al的Cu-20Ni-19Fe-xAl合金在850 ℃高温下氧化时动力学曲线拟合分别符合6次方(1/n=5.76)和4次方(1/n=4.22)关系,添加10% Al的Cu-20Ni-19Fe-10Al合金氧化850 ℃动力学曲线符合立方抛物线规律(1/n=2.95)。也就是说,Cu-20Ni-19Fe合金中添加的Al含量越高,合金氧化速率指数越小,合金抗氧化性能越好。
2.3 氧化膜层表面微观组织
图5为Cu-20Ni-19Fe合金850 ℃氧化100 h后的膜层XRD结果。从图5可以看出,Cu-20Ni-19Fe合金850 ℃氧化100 h后膜层以CuO,Cu2O,NiO和Fe2O3为主。图6为Cu-20Ni-19Fe合金850 ℃氧化50 h和100 h后膜层表面的微观组织形貌,图6中不同区域EDS能谱结果如表3所示。结合膜层XRD结果和表面EDS能谱结果,可以判断膜层表面氧化物主要为CuO。另外,从图6 a)Cu-20Ni-19Fe合金氧化50 h的膜层表面形貌可以看出,膜层表面有裂纹形成;从图6 b)合金继续氧化至100 h时氧化膜层的表面形貌中可以看出,部分氧化膜层出现剥落,未剥落的最表层膜层为
CuO(见图6 b)中区域2及能谱结果所示),剥落后的次表层膜层仍然为CuO,只是膜层成分中的O含量明显减少。O/Cu原子比远小于1,说明最外层的CuO是由内层的Cu2O与氧气氛接触后进一步氧化形成的。如果氧化时间继续延长,则合金将进一步氧化,膜层反复剥落,剥落的氧化膜的下面位置会继续形成新的氧化膜。如此循环,Cu-20Ni-19Fe合金表现出较差的高温抗氧化性能,合金氧化曲线呈直线规律。
图7所示为添加不同Al的Cu-20Ni-19Fe-xAl合金氧化100 h后膜层表面的组织形貌。图7 a)为添加6%Al的Cu-20Ni-19Fe-6Al合金氧化100 h后的膜层表面组织,结合EDS能谱分析结果可知,合金表面所生成的氧化膜主要有2种,一种为结晶颗粒粗大的CuO氧化物(见图7 a)中箭头所示,EDS能谱结果显示为44.56% O-55.44% Cu),另一种为结晶细小的Al2O3(见图7 a)中箭头所示),EDS能谱结果显示为67.32% O-32.68% Al。可以看出,所生成的Al2O3膜层未能完全覆盖CuO膜层,使得在合金表面2种氧化物共存,所生成的Al2O3膜层对基体合金不能完全起到保护作用。图7 b)—图7 d)所示分别为含8%和10% Al的Cu-20Ni-19Fe-xAl合金氧化100 h后的膜层表面组织。可以看到,氧化100 h后2个合金表面均生成了大面积的Al2O3膜层,将Cu及其他合金元素所生成的氧化物完全覆盖于Al2O3膜层下面,Al2O3膜层隔绝了氧气氛与其他金属氧化物,对合金基体起到了完全保护作用,阻止了合金的进一步氧化,合金氧化动力学曲线呈指数规律。另外,从图7 d)中还可以看到,当添加Al含量为10%时,合金长期氧化(100 h)后膜层出现剥落,说明当Al含量过高时所生成的氧化膜层易开裂,开裂后膜层与基体的黏附性能变差,Al2O3膜层一旦脱落,其对合金基体的保护作用失效,合金会进一步氧化。
2.4 氧化膜层截面微观组织
图8所示为Cu-20Ni-19Fe和Cu-20Ni-19Fe-8Al合金氧化100 h后膜層截面SEM组织照片。从图8 a)可以看出,不添加Al的Cu-20Ni-19Fe合金氧化100 h后,膜层较厚,为200~300 μm。EDS分析结果显示,外侧膜层为Cu的氧化物(49.56% O-50.44% Cu),内部为Ni和Fe的混合氧化物膜层。整个膜层厚薄不均匀,膜层内部有大量孔洞,与基体结合处出现裂纹,说明氧化膜层不致密,与基体结合率较差。外侧CuO膜层是Cu的快速外扩散氧化形成的,Cu外扩散后残留在膜层和基体界面的空位逐渐聚合,形成孔洞。从图8 b)可以看出,添加8% Al的Cu-20Ni-19Fe-8Al合金氧化100 h后,合金表面形成一层Al2O3保护膜,膜层较薄,约20 μm,说明合金氧化程度较小,Al2O3膜层的形成,可有效保护合金基体,避免合金进一步氧化。同时,结合添加Al后的合金氧化膜层表面及截面微观组织可以发现,添加Al后合金膜层较脆,易剥落。通过对比可以看出,Cu-20Ni-19Fe合金中添加Al元素之后,能大幅度降低合金氧化时生成氧化膜的厚度,添加8% Al元素所形成的氧化膜的厚度为不添加Al元素时形成氧化膜厚度的1/10,说明Al的添加大大提高了Cu-20Ni-19Fe合金材料的高温抗氧化性能。
3 讨 论
结合Cu-Ni-Fe三元合金在20 ℃下的等温相图(见图2)和Cu-20Ni-19Fe合金微观组织(见图1 a)),可以判断Cu-20Ni-19Fe合金铸态组织中存在明显的两相:γ1-(NiFe)枝晶相和固溶有Ni的γ2-(CuNi)基体相。当Cu-20Ni-19Fe合金中添加Al后,若Al元素含量较少(≤6%),Al固溶在合金基体中,形成固溶体;当加入的Al含量较高、超过Al在合金基体中的固溶度时,合金中的Ni与Al会形成金属间化合物NiAl相,Al含量为8%时形成的NiAl相为针状,Al含量为10%时形成的NiAl相变为块状。
Cu-20Ni-19Fe合金在850 ℃和1.013×105 Pa氧气氛中氧化时,气氛中的氧分压大于各金属的平衡氧分压。氧化初期,氧气氛与金属基体接触,从热力学角度来看合金表面形成各金属的氧化物,因此,在氧化初期为反应控制型,氧化速率较快。随着氧化的进一步进行,氧化物横向生长,覆盖整个合金表面,使内部金属基体与氧气氛隔绝,氧化变为扩散控制型,氧化速率有所降低。由于NiO,FeO和Cu2O均是p-type金属氧化物[17](阳离子空位引起的金属缺失),在这种氧化物中,金属阳离子的扩散占主导,且Cu氧化物的空位浓度大于Ni和Fe氧化物的空位浓度,也就是说从动力学来讲,Cu在Cu氧化物中的扩散速率远远大于Ni和Fe在其各自氧化物中的扩散速率[18],随着氧化的逐渐进行,最外层形成了连续的Cu的氧化物层。结合Cu-O二元系稳定相图[19],Cu2O在850 ℃的平衡氧分压为101.3 Pa。因此,Cu2O在实验氧化条件下不稳定,继续被氧化时,外侧膜层全部转化成CuO,合金在最外层形成稳定的CuO膜层[20]。
添加8% Al的Cu-20Ni-19Fe-8Al合金在850 ℃和1.013×105 Pa氧分壓下氧化,初期形成各自的金属氧化物。随着氧化的进行,由于合金中添加了Al元素,所以在氧化膜层最外侧形成了Al2O3,Al2O3膜层的形成阻碍了气氛中的氧向合金内部的进一步扩散,氧化膜/合金界面氧分压逐渐降低,基体内部的Cu,Ni和Fe氧化程度逐渐减小。同时,Al2O3膜层的形成阻碍了Cu的外扩散,且随着氧化的进行Al2O3膜横向生长,形成连续完全覆盖的Al2O3氧化膜。当合金表面形成完全覆盖的Al2O3膜层后,合金基体与反应气氛完全隔开,阻碍了Cu,Ni和Fe等基体元素的外扩散和氧的内扩散,进一步抑制了合金的氧化。当Al的含量足以使合金从发生内氧化向外氧化转变时,Al能赋予Cu基合金良好的抗氧化性能。随着Al含量的添加,Cu-20Ni-19Fe-Al合金高温抗氧化性能提高,有望成为铝电解用惰性阳极材料的备选材料。
4 结 语
1)Cu-20Ni-19Fe合金铸态组织为两相:γ1 -(NiFe)枝晶相和γ2-(CuNi)基体相。合金中添加少量Al后,Al固溶在合金基体中形成固溶体;当Al含量大于8%时,合金中形成针状NiAl相;当Al含量继续增大时,针状NiAl相转变为块状,且NiAl相含量随Al含量的增加而增多。
2)不添加Al的Cu-20Ni-19Fe三元合金在850 ℃和1.013×105 Pa氧分压下,高温氧化动力学曲线呈直线规律,合金抗氧化性能较差。添加Al元素后,合金的氧化动力学曲线转变为指数规律,添加6%,8%和10% Al的Cu-20Ni-19Fe-Al合金,氧化速率指数分别为5.76,4.22和2.95,Al含量越高,合金氧化增重越小,抗氧化性能越好。
3)针对Cu-Ni-Fe合金高温抗氧化性能差的问题,本研究提出通过添加Al来提高合金的高温抗氧化性能。然而,添加Al后合金氧化膜层会变脆,易从基体上剥落。因此,未来需对提高合金氧化膜层与基体的黏附性,以及合金在电解环境下的腐蚀性能开展研究,为合金在铝电解阳极材料中的应用提供实验支撑。
参考文献/References:
[1] 管卫华,林用满,谢再晋.工程机械用Cu-Ni合金的腐蚀行为研究[J].热加工工艺,2021,50(4):71-76.
GUAN Weihua,LIN Yongman,XIE Zaijin.Study on corrosion behavior of Cu-Ni alloy for construction machinery[J].Hot Working Technology,2021,50(4):71-76.
[2] 罗富鑫.Cu-Ni-Mn合金的组织演变与强化机制研究[D].赣州:江西理工大学,2020.
LUO Fuxin.Study on Microstructure Evolution and Strengthening Mechanism of Cu-Ni-Mn Alloy[D].Ganzhou:Jiangxi University of Science and Technology,2020.
[3] 刘平,任凤章,贾淑果.铜合金及其应用[M].北京:化学工业出版社,2007.
[4] GOUPIL G,BONNEFONT G,IDRISSI H,et al.Consolidation of mechanically alloyed Cu-Ni-Fe material by spark plasma sintering and evaluation as inert anode for aluminum electrolysis[J].Journal of Alloys and Compounds,2013,580:256-261.
[5] HELLE S,PEDRON M,ASSOULI B,et al.Structure and high-temperature oxidation behaviour of Cu-Ni-Fe alloys prepared by high-energy ball milling for application as inert anodes in aluminium electrolysis[J].Corrosion Science,2010,52:3348-3355.
[6] GALLINO I,KASSNER M E,BUSCH R.Oxidation and corrosion of highly alloyed Cu-Fe-Ni as inert anode material for aluminum electrowinning in as-cast and homogenized conditions[J].Corrosion Science,2012,63:293-303.
[7] GAVRILOVA E,GOUPIL G,DAVIS B,et al.On the key role of Cu on the oxidation behavior of Cu-Ni-Fe based anodes for Al electrolysis[J].Corrosion Science,2015,101:105-113.
[8] LIU Ying,CHAI Dengpeng,WANG Wei,et al.Influences of heat treatment on the oxidation and corrosion behavior of Cu-Ni-Fe inert anodes for aluminium electrolysis[J].Journal of Alloys and Compounds,2020,832:154848.
[9] PENG Weiping,LIU Ying,GUO Jie,et al.Effect of La on the electrolysis performance of 46Cu-25Ni-19Fe-10Al metal anonde[J].Light Metals,2014,99:1301-1304.
[10]郭建亭.幾种微量元素在高温合金中的作用与机理[J].中国有色金属学报,2011,21(3):465-475.
GUO Jianting.Effects of several minor elements on superalloys and their mechanism[J].The Chinese Journal of Nonferrous Metals,2011,21(3):465-475.
[11]朱宇平,何业东,王德仁.Fe-40Cr-5Al合金阳极在800 ℃和900 ℃的电解腐蚀行为[J].北京科技大学学报,2011,33(12):1485-1491.
ZHU Yuping,HE Yedong,WANG Deren.Electrolysis corrosion behaviors of Fe-40Cr-5Al alloy anodes at 800 ℃ and 900 ℃[J].Journal of University of Science and Technology Beijing,2011,33(12):1485-1491.
[12]XUE Jilai,FENG Luxing,GERMAIN N K,et al.High-temperature oxidation and corrosion behaviors of Ni-Fe-Cr alloy for inert anode materials in aluminum electrolysis[C]//4th International Symposium on High-temperature Metallurgical Processing.[S.l.]:[s.n.],2013:177-184.
[13]WEI Wei,GENG Shujiang,XIE Dongbai,et al.High temperature oxidation and corrosion behaviours of Ni-Fe-Cr alloys as inert anode for aluminum electrolysis[J].Corrosion Science,2019,157:382-391.
[14]刘英,张永安,王卫,等.稀土Y对Ni-Fe-Co-Cu合金微观组织和高温氧化性能的影响[J].稀有金属,2020,44(1):9-17.
LIU Ying,ZHANG Yong′an,WANG Wei,et al.The influence of rare earth Y on the microstructure and high temperature oxidation behaviour of Ni-Fe-Co-Cu alloy[J].Rare Metals,2020,44(1):9-17.
[15]刘国军.铜合金高温抗氧化性能的研究[D].长春:吉林大学,2008.
LIU Guojun.Oxidation Resistance of Copper Alloys at High Temperature[D].Jilin:Changchun University,2008.
[16]KOTTCAMP E H,LANGER E L.ASM Metals HandBook Volume 03:Alloy Phase Diagrams[M].[S.l.]:ASM International,1992:1645-1647.
[17]辛丽,王文.金属高温氧化导论[M].北京:高等教育出版社,1989.
[18]LIU Ying,ZHANG Yong′an,WANG Wei,et al.The effect of La on the oxidation and corrosion resistance of Cu52Ni30Fe18 alloy inert anode for aluminum electrolysis[J].Arabian Journal for Science and Engineering,2018,43(11):6285-6295.
[19]NEUMANN J P,ZHONG T,CHANG Y A,ASM Metals HandBook Volume 03:Alloy Phase Diagrams[M].[S.l.]:ASM International,1992.
[20]HAUGSRUD R.High-temperature oxidation of Cu-10% Ni and Cu-15% Ni at 900~1 050 ℃[J].Corrosion Science,2000,42:383-399.

