球状纳米CaO2的制备及其协同电渗透污泥深度脱水
李亚林,刘蕾,李坤鹏,林康,窦雪,毕雅洁
(1 河南工程学院资源与环境学院,河南郑州 451191;2 长江大学资源与环境学院,湖北武汉 430100)
过氧化钙(CaO2)氧化是一类新型的高级氧化技术,主要被应用于受有机污染土壤和地下水的原位修复[1-2]。它可以被认为是固体形式的H2O2,在自然状态下溶解在水中可以在可控速率下产生H2O2而具有强氧化性[3]。近年来,部分学者对CaO2用于污泥有机物破解释放的可行性进行了初步探索,证实了CaO2可以在一定程度上改善污泥的脱水性能[4-6]。但传统市售的CaO2粒径普遍偏大,使得在实际污泥调理过程中其不容易在介质中分散而出现团聚的现象,降低了CaO2与污泥絮体的接触机会和反应速度,限制了CaO2对污泥中有机物质的破坏,从而导致药剂使用量增加或反应效果变差。
电渗透是土壤原位修复中常用的一类技术,其对有机污染物和重金属去除有良好的效果[7]。近年来,一些研究者利用其对不同种类的污泥进行处理,以期实现污泥的深度脱水,但由于在电渗透脱水的过程中往往发生包括电化学反应和电迁移等电动力学现象[8],污泥脱水的效果并不稳定,处理过程中电渗流量会逐渐降低[9],脱水后污泥的剩余含水率由阳极至阴极不断增加、脱水效果递减。
目前,已有学者将高级氧化技术与电渗透组合用于废水中有机物的处理,证明了两种技术联用对有机物有明显的破坏和降解作用[10]。在此基础上,一些学者将该联合技术用于污泥脱水的研究中,初步证实了高级氧化与电渗透技术联用可以改善污泥的脱水性能[11-12]。本文作者在前期研究中同样验证了高级氧化与电渗透技术协同进行污泥脱水的可行性[13-14],但存在高级氧化反应剧烈、与电化学反应的叠加作用会造成污泥脱水过程中反应热量增加、能耗升高等问题。寻找合适的氧化剂,在确保污泥脱水效果的同时减缓脱水体系的反应程度具有一定的意义。
基于此,本研究以CaCl2和H2O2为原料,加入分散剂制备纳米CaO2,对制备条件进行了优化,并对其形貌进行了表征。在此基础上利用自制纳米CaO2可控的反应性、高效的氧化性以及良好的分散性和迁移性,协同电渗透对市政污泥进行深度脱水,考察不同操作参数对污泥脱水效果的影响,探讨纳米CaO2协同电渗透污泥深度脱水技术的可行性。
1 材料和方法
1.1 材料
实验中制备CaO2的原料包括无水CaCl2、NH3·H2O、30%的H2O2、聚乙二醇(PEG200),以上均为分析纯,由上海麦克林生化科技有限公司生产。污泥取自新郑市某市政污水处理厂的浓缩池,该厂采用CASS处理工艺,污泥的含水率为98.66%~99.14%,有机质含量为47.96%,pH 为7.59。污泥取回后放置在4℃的冰箱中保存,实验前将污泥取出,放至室温后使用。
1.2 纳米CaO2的制备流程
取定量无水CaCl2于烧杯中,按照固液比1∶10 添加去离子水搅拌使其溶解制得反应母液,将定量分散剂加入反应母液,并用NH3·H2O溶液将反应母液pH调节为9.5~11.0,磁力搅拌30min使其完全混合。然后通过恒压滴液漏斗将定量H2O2溶液(质量分数为30%)以一定速率加入到维持500r/min转速搅拌的反应液中,滴加完成后静置2h,使钙盐与H2O2充分反应。以NaOH溶液作为沉淀剂加入至反应液中,使得CaO2沉淀形成混合液,再用布氏漏斗抽滤得到固体,用无水乙醇反复洗涤后,真空干燥,即得到纳米CaO2粉末,制备的反应如式(1)和式(2)所示。
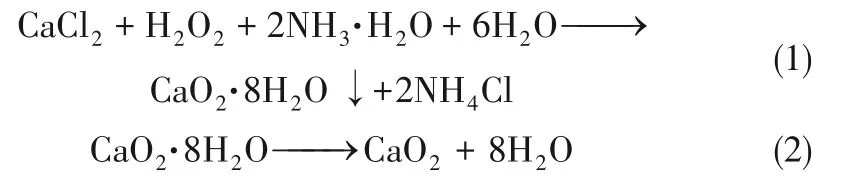
1.3 纳米CaO2纯度、产率测定及形貌表征
以纯度和产率作为纳米CaO2制备的评价指标,计算如式(3)和式(4)所示,制备的CaO2纯度采用高锰酸钾法进行测定[15],样品平行测定3次,结果取平均值。
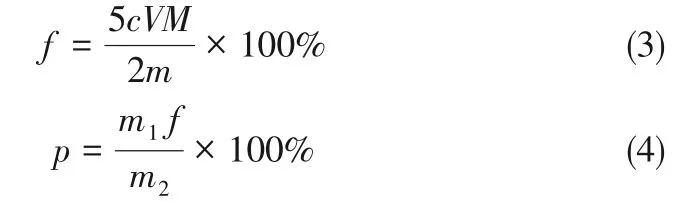
式中,f为纳米CaO2的纯度,%;c为KMnO4溶液的浓度,mol/L;V为KMnO4滴定的体积,L;M为CaO2的摩尔质量,g/mol;m为所取样品纳米CaO2的质量,g;p为纳米CaO2的产率,%;m1为实际制得纳米CaO2的质量,g;m2为理论制得纳米CaO2的质量,g。
制得的纳米CaO2样品粉末涂片,使用X射线衍射仪(XRD,德国布鲁克公司,型号D8 ADVANCE)对其物相组成进行鉴别,样品的物相组成采用Highscore 软件进行分析;纳米CaO2样品粉末置于装有乙醇溶液的试管中,充分混合后置于超声清洗机(深圳云奕科技股份有限公司生产,型号YD0203)分散1h,之后在滴加在喷有碳膜的铜网和单晶抛光硅片上,使用透射电子显微镜(TEM,日本电子株式会社,型号JEM2100)和聚焦离子束扫描电子显微镜(FIB-SEM,德国卡尔·蔡司股份公司,型号Auriga)对其进行形貌分析。
1.4 污泥电渗透脱水装置
如图1所示,装置包括水平放置的圆柱形反应器(自制,有机玻璃,φ100mm,长190mm)、稳压直流电源(无锡安耐斯电子科技有限公司生产,型号JP150200)、电子天平(上海衡际科学仪器有限公司生产,型号YP10001P)、智能温控表(上海誉赫电子科技有限公司生产,型号CHB902)和电动液压推杆(常州龙翔气弹簧有限公司生产,型号XTL)组成[16]。其中阳极为碳电极(φ90mm,纯度90%),嵌入活塞左端,接正电;阴极为铜电极(φ100mm),具有的排水孔(16 个φ3mm,21 个φ6mm),嵌入反应器左端,接负电,反应器左端放置48μm(300 目)的玻璃纤维滤布,用来拦截污泥颗粒以便及时排出脱除的水分;下方放置称重设备,用来记录实时脱除水分的质量,此过程中蒸发水分与脱除水分质量相比可以忽略不计。
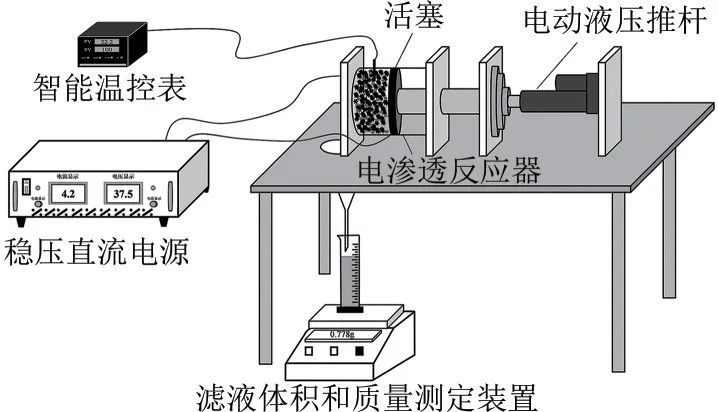
图1 污泥电渗透脱水装置
1.5 污泥脱水指标及测定方法
以实时脱水比例和脱水泥饼含水率作为污泥脱水的评价指标,其中脱水比例计算如式(5)所示,脱水泥饼的含水率采用烘干称重法进行测定[17],实验中每组样品作3个平行样,数据测定3次后取平均值。
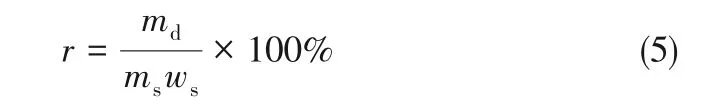
式中,r为实时脱水比例,%;md为实时脱出水分的质量,g;ms为原污泥的质量,g;ws为原污泥的含水率,%。
2 结果与讨论
2.1 纳米CaO2的制备及其条件优化
2.1.1 搅拌速率及分散剂用量对CaO2纯度和产率的影响
取3.0000g无水CaCl2,加入去离子水制备反应母液,控制分散剂(PEG200)的加入量为60mL,以0.25mL/min 的速率向母液中滴加15mL 的H2O2溶液,设定不同转速进行搅拌,反应完成后静置,加入沉淀剂,得到含CaO2混合液,抽滤,滤饼真空干燥,测定产率和纯度,考察搅拌速率对CaO2制备的影响;获得最佳搅拌速率后,改变分散剂(PEG200)的加入量,其他条件不变,考察分散剂用量对CaO2制备的影响,结果如图2所示。
由图2(a)分析,随着搅拌速率的增加,CaO2的纯度和产率均呈现出先增加后降低的趋势,在搅拌速率为500r/min 时产率和纯度达到最高,分别为72.09%、75.11%。对不同搅拌速率条件下制得CaO2进行SEM 表征,结果如图3 所示,从图3(a)可以看出当转速较小时,CaCl2和H2O2可以充分反应,在此过程中生成的CaO2颗粒不会被搅拌形成的机械力打碎,但会有一定的团聚现象;随着转速的增加,反应物之间接触机会也随之增加,反应更加充分,产物纯度和产率随之提高;由图3(b)和图3(c)的对比可以发现当搅拌速度大于500r/min时,CaO2的颗粒再次发生聚集,推测是H2O2在剧烈搅拌中加速分解,同时搅拌器外缘与反应器壁间的流体线性流速过大,出现的湍流区不利于中间产物与H2O2的混合,故造成反应物的浓度和反应程度的下降。
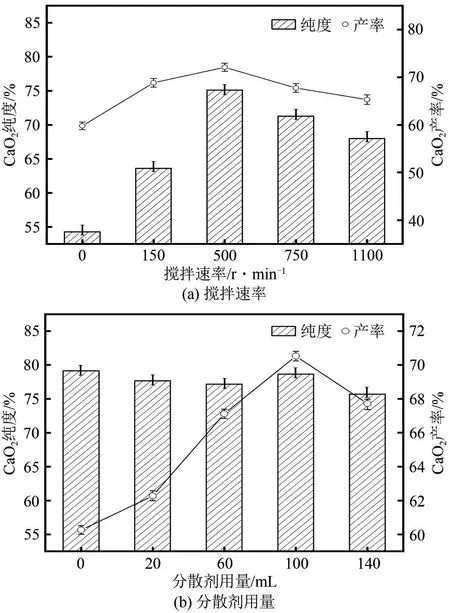
图2 搅拌速率及分散剂用量对CaO2纯度和产率的影响

图3 不同搅拌速率条件下制得CaO2的SEM图像
由图2(b)分析,随着分散剂用量的增加CaO2的纯度稳定在75.71%~79.13%之间,而产率则随着分散剂的增加呈现出先增加后降低的趋势。对在不同分散剂用量条件下制得的CaO2进行SEM 表征,结果如图4所示。结合图4(a)可以发现CaCl2浆液会随着分散剂的增加与H2O2充分接触反应,在分散剂用量较少时,反应生成颗粒的分散性较差,相互形成机械力无法打散的硬团聚体[18],其较小的比表面积使反应速率降低,纯度及产率偏低。当分散剂的用量在100mL时,CaO2的产率达到70.52%。
此时可以从图4(b)中看出制得的CaO2趋近于规则的球状颗粒,且具有较好的分散度;而图4(c)中发现进一步增加分散剂用量时,分散剂在浆液中的分散性降低,黏性增加,分散剂的高分子长链会发生相互缠绕,促进微小晶粒相互团聚成一次颗粒[19],大颗粒的CaCl2形成局部堆积,与H2O2的反应效率下降,产率下降。
2.1.2 H2O2滴加速率及用量对CaO2纯度和产率的影响
取3.0000g无水CaCl2,加入去离子水制备反应母液,投加100mL 的分散剂PEG200,以不同滴加速率向母液中滴加15mL 的H2O2溶液,500r/min 转速搅拌反应完成后静置,加入沉淀剂,得到含CaO2混合液,抽滤,滤饼真空干燥,得到产品,称量,测定产率和纯度,考察H2O2滴加速率对CaO2制备的影响;获得最佳滴加速率后,改变H2O2加入量,其他条件不变,考察H2O2用量对CaO2制备的影响,结果如图5所示。
由图5(a)分析,随着滴加速率的提高,CaO2的纯度和产率大致呈现上升趋势,后趋于平缓,最终分别稳定在75.64%和75.52%。对在不同H2O2滴加速率条件下制得的CaO2进行SEM表征,结果如图6所示,结合图6(c)分析可以发现,当H2O2滴加速率较大时,CaO2的颗粒粒径较大,推测快速滴加H2O2使得反应过程迅速放热,反应液温度上升,部分CaCl2未参与反应即被包裹,同时H2O2自身发生快速分解,利用率降低,从而影响反应纯度和产率;由图6(b)分析当滴加速率降低后,促使滴加时间显著增加,为一次颗粒的生成提供了更长的反应时间,CaO2颗粒变小且具有更好的均匀性;但当滴加速率过低时,使颗粒间的相互碰撞概率增加,二次颗粒也因长时间的反应,参与在不规则的团聚运动中[20],CaO2颗粒聚集,图6(a)中的形貌变化印证了该推测。

图4 不同分散剂用量条件下制得CaO2的SEM图像
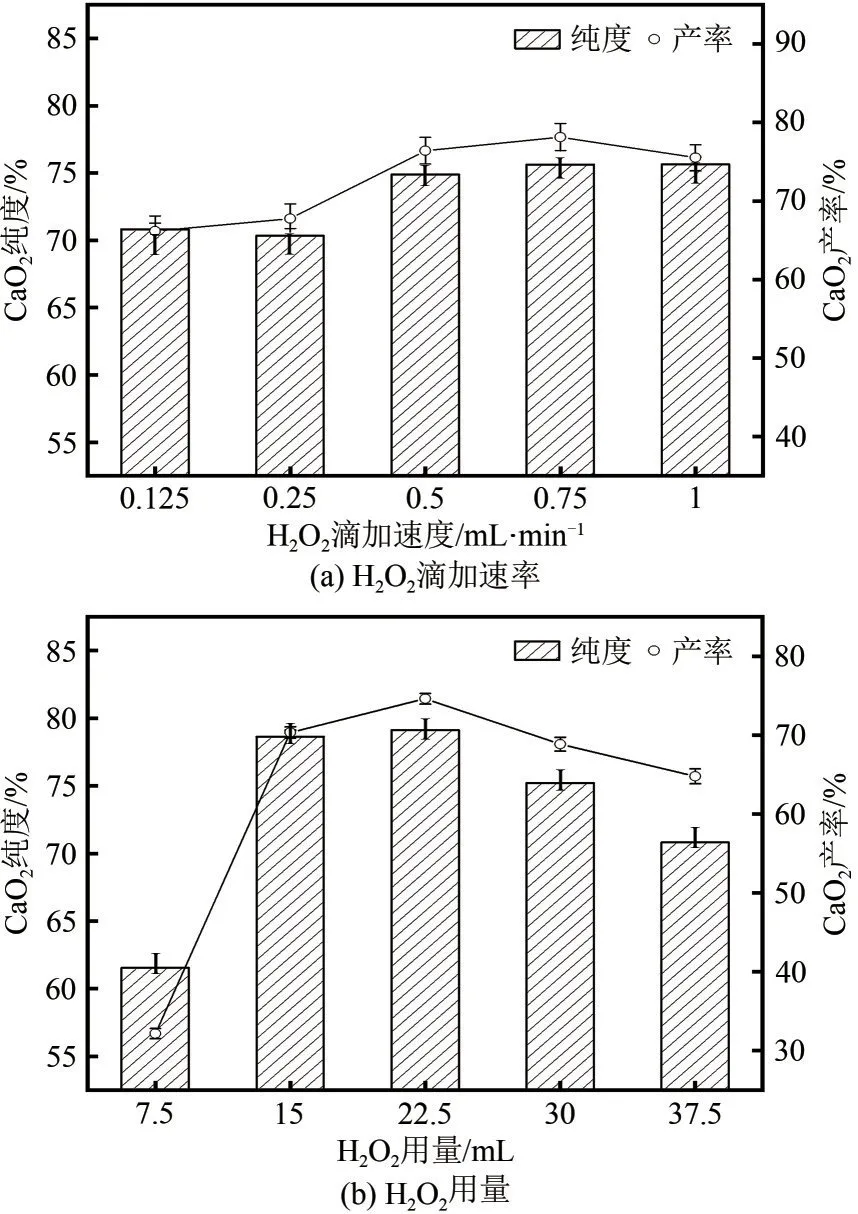
图5 H2O2滴加速率及用量对CaO2纯度和产率的影响
由图5(b)分析,随着H2O2用量的增加,CaO2的纯度和产率均呈现出先增加后降低的趋势,在用量为22.5mL 时,CaO2的产率达到74.62%,纯度达到79.13%。因为当H2O2用量不足时,CaCl2无法充分反应,而H2O2用量过多时,体系反应速率加快,此时体系中的反应为放热反应,温度上升使H2O2受热分解,CaO2的纯度和产率下降。对在不同H2O2用量条件下制得的CaO2进行SEM 表征,结果如图7 所示。结合图7 分析,H2O2用量改变对于CaO2的整体形貌影响不明显,但值得注意的是在图7(b)中的CaO2相较于图7(a)和图7(c)中颗粒分散性更好,成球现象明显,这一形貌在自制纳米CaO2与市售CaO2表征对比中得到了进一步印证。
2.1.3 自制纳米CaO2与市售CaO2表征对比
控制分散剂用量为100mL,搅拌速率为500r/min,H2O2用量为22.5mL,滴加速率为0.75min/mL 制备得到CaO2样品,与市售CaO2进行表征对比,结果如图8所示。
通过图8(a)中市售CaO2与自制CaO2的XRD 图谱对比分析可以看出,在2θ为30.273°、35.598°、47.306°、51.594°、53.210°和60.897°时均出现衍射峰,这与CaO2的图谱特征峰一致,证明制得的物质为CaO2,同时在市售CaO2图谱中还有一定量的Ca(OH)2,而在自制CaO2图谱中未发现对应峰的存在。对比图8(b)和图8(c)可以看出市售CaO2与自制CaO2在形貌方面有较明显区别,市售CaO2形貌除了规则的六边体外还存在不规则的团聚态,而自制CaO2大多为球状或椭球状,粒度在45~300nm 之间,这一点与图8(d)自制CaO2的TEM 图中观察到的形貌相吻合。

图6 不同H2O2滴加速率条件下制得CaO2的SEM图像

图7 不同H2O2用量条件下制得CaO2的SEM图像

图8 市售CaO2与自制CaO2表征结果
2.2 纳米CaO2协同电渗透对污泥脱水的影响
控制初始污泥量为352.5g(根据电渗透反应器的横截面积计算出污泥等效装填厚度为3cm)与不同投加量的自制纳米CaO2搅拌混匀后置于电渗透脱水装置中,脱水过程中每脱除100g水电动液压推杆推进一次,控制电压为30V,考察纳米CaO2投加量对污泥脱水的影响;获得最佳CaO2投加量后,改变通电电压,其他条件不变,考察电压梯度对污泥脱水的影响;在此基础上,最后改变初始污泥量,考察初始污泥量对污泥脱水的影响,脱水实验中当脱除水量为0.01g/s时终止实验[21],结果如图9所示。
由图9(a)分析,随着CaO2投加量的增加,r逐渐升高。因为CaO2在水中可发生式(6)中的反应;电极板电解产生的Cu2+可以催化H2O2产生高活性的氧化自由基,如式(7)和式(8)所示[22],而Cu2+/Cu+体系能够继续与H2O2发生式(9)中的反应生成·OH[23],反应生成的·HO2和·OH会对污泥絮体造成持续的破坏,促进污泥中的水分脱出。而当CaO2投加量大于100mg/g DS时,r随着CaO2投加量的增加而降低,这是因为CaO2的过量投加会在体系中释放更多的H2O2,而部分·OH会与过量的H2O2发生反应被猝灭,如式(10)所示[24]。同时,体系中Ca(OH)2的生成会造成体系的碱度升高,不利于类Fenton反应的持续。
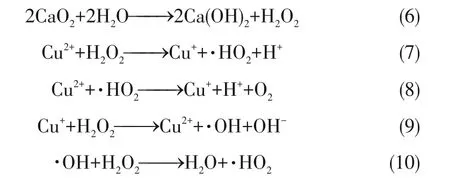
由图9(b)可知,r随着电压梯度的升高呈现出先升后降的趋势,在电压为50V时,r达到最高值,此时脱水污泥的含水率为81.74%。因为在电压较低时,反应体系的温度维持在较低的水平,随着电压的增加,体系温度增高,污泥黏度降低,有助于水分从阳极至阴极的迁移;但过高的电压容易造成阳极附近污泥中的水分迅速流失,电阻变大,所获得分压增大,此时阴极附近所分电压减小,电场对水分的驱动力变弱,脱水速率减缓[25]。
由图9(c)可知,当初始污泥量少于705g(等效污泥填充厚度为6cm)时,r随着泥量的增加而增大,当初始污泥量多于705g时,r随泥量的增加先减后增。当初始泥量较少时,靠近阳极的污泥含水率快速下降,污泥颗粒间孔隙的水分减少导致电阻增大,电流迅速减小,污泥迅速达到脱水极限,如初始污泥为352.5g 时,脱水时间仅持续了50min。而初始污泥量过多时,阴阳极的间距增加,电阻随之增加,电流减小,脱水时间延长,脱水效果变差。
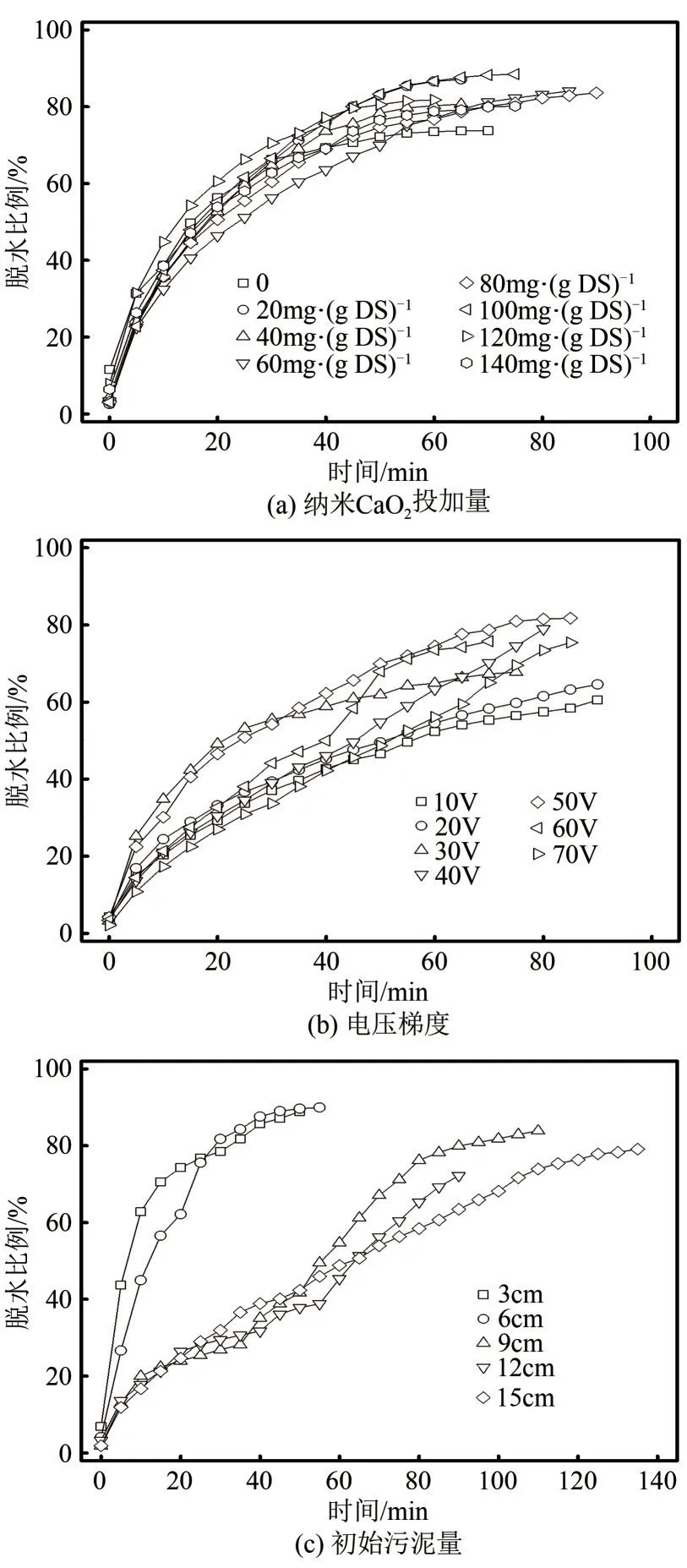
图9 不同操作参数对污泥脱水的影响
针对获得的脱水最佳条件,控制初始污泥量为705g,电压为50V,分别投加100mg/g DS的自制和市售CaO2进行污泥脱水,结果见表1。

表1 自制和市售CaO2协同电渗透污泥脱水效果对比
由表1 可知,与单纯电渗透脱水相比,投加CaO2协同电渗透可以显著降低污泥的含水率,采用自制纳米CaO2与市售CaO2相比,污泥脱水效果提升明显。
为了探究上述关于CaO2作用于污泥机理的推断,使用SEM 分别对原污泥和脱水污泥进行形貌表征,结果如图10所示。
由图10(a)可以看出,原污泥呈现清晰的絮状结构,表面多为板片状,这种结构决定了污泥会对水产生大面积的包裹作用而其难以脱除;图10(b)中的CaO2脱水污泥表面较原污泥最大的变化是板片状结构消失,絮体表面呈现不规则的凹凸;同时,局部放大的图10(c)中可以发现CaO2的颗粒,这些颗粒一定程度上也可以充当骨架作用,强化污泥的脱水效果。

图10 原污泥和CaO2脱水污泥的SEM图像
3 结论
(1)在纳米CaO2的制备过程中,分散剂用量、搅拌速率、H2O2滴加速率及H2O2用量均会对CaO2的纯度、产率和形貌造成影响,在分散剂用量为100mL、搅拌速率为500r/min、H2O2用量为22.5mL、H2O2滴加速率为0.75mL/min 时,制备得到CaO2的纯度和产率分别可以达到79.13%和74.62%。
(2)自制纳米CaO2粒度在45~300nm 之间,颗粒大多为球状或椭球状,与市售CaO2规则的六边体及不规则的团聚态形貌有显著差别,在污泥脱水时与市售CaO2相比具有更好的分散度。
(3)自制CaO2与电渗透协同可以实现污泥的深度脱水,当CaO2投加量为100mg/gDS、电压为50V、初始污泥量为705g时,可以将污泥含水率降至67.52%,与未投加CaO2相比,污泥含水率降低了17.78%,与同等条件下使用市售CaO2相比,污泥脱术效果也得到了明显提升。

