基于网络药理学探讨黄芪治疗支气管哮喘的作用机制
李竹英 陈 璐 袁星星 王 婷 张 玉 连梦尧 李 星
1.黑龙江中医药大学附属第一医院呼吸科,黑龙江哈尔滨 150040;2.黑龙江中医药大学研究生院,黑龙江哈尔滨 150040;3.齐齐哈尔医学院病理学院,黑龙江齐齐哈尔 161000
支气管哮喘(以下简称“哮喘”)是一种慢性气道炎症性疾病,因其不断增长的发病率和死亡率而备受世界关注。中国肺健康研究显示,目前我国哮喘患病人数约4570 万,总体发病率达4.2%[1]。西医治疗哮喘最有效的药物为糖皮质激素,虽然其具有较强的抗炎作用,但是长期服用会造成口咽念珠菌感染、声音嘶哑等副作用,给患者带来较大的心理负担。近年来,中药治疗哮喘越来越受到重视,具有药性温和、药效持久、副作用小、成本低廉等优势。
黄芪颗粒、黄芪注射液及黄芪类复方对哮喘的治疗有积极的作用,可以提高患者的临床控制率,减轻气道炎症反应,增强机体免疫功能,改善肺功能[2-4]。黄芪味甘性微温,归脾、肺经,有补气健脾、益卫固表之效。现代药理研究证实,黄芪具有兴奋呼吸中枢、免疫调节、抗炎、抗缺氧、提高机体的抗病力等作用。已有数据表明,黄芪的化学成分可通过调控相关的炎症因子及基因蛋白等途径发挥治疗哮喘的作用[5-6]。但目前的研究多从单一成分或单一靶点对黄芪治疗哮喘的机制进行探讨,很难阐明中药治疗疾病的整体性与系统性。因此,本研究基于网络药理学的方法,从多维度探究黄芪治疗哮喘的活性成分、作用靶点和相关通路,为黄芪治疗哮喘机制的系统研究提供新的思路。
1 材料与方法
1.1 黄芪活性成分及靶点获取
通过中药系统药理学数据库与分析平台(TCMSP)输入“黄芪”检索其化学成分,再根据口服生物利用度(OB)≥30%、类药性(DL)≥0.18 的标准筛选出符合条件的活性化学成分[7]。然后在TCMSP 中,利用蛋白质数据库(Uniprot)筛选出黄芪中的活性化学成分所对应的靶点蛋白基因名,重复靶点仅保留1 个,所得靶点即为黄芪活性化学成分的预测靶点。
1.2 哮喘相关靶点的获取
以“asthma”为检索词从Genecards 网络平台库中检索哮喘的相关靶点。同时将黄芪活性化学成分的预测靶点与哮喘的相关靶点在Venny 2.1.0 中映射筛选出共同靶点,即为黄芪作用于哮喘的潜在靶点。
1.3 黄芪-化合物-靶点-哮喘网络构建
将黄芪活性化合物及“1.2”中获取的潜在靶点导入Cytoscape 3.7.0 中,构建黄芪-化合物-靶点-哮喘网络,通过计算节点的度值(degree)来筛选关键化合物。
1.4 蛋白质-蛋白质相互作用(PPI)网络的构建
将“1.2”中获取的潜在靶点导入STRING 数据库,获取PPI 数据,将PPI 数据导入Cytoscape 3.7.0 中构建网络图。
1.5 基因本体论(GO)功能富集分析及日本京都基因和基因组百科全书(KEGG)通路富集分析
基于R 语言软件,利用Bioconductor 生物信息软件包对黄芪作用于哮喘的潜在靶点进行GO 功能富集分析和KEGG 通路富集分析,通过R 语言中“Cluster profiler”进行可视化处理,设定阈值P <0.05 为指标进行筛选,选取P 值由小到大前20 条目制图。
2 结果
2.1 黄芪活性成分及靶点筛选结果
从TCMSP 平台中搜索符合标准的黄芪活性化合物19 个。见表1。将所获得的活性化合物对应的靶点蛋白名导入Uniprot 数据库进行基因标准化,删除重复项,共得到黄芪活性化合物的预测靶点97 个。

表1 黄芪活性化合物信息
2.2 哮喘相关靶点的获取结果
在Genecards 数据库中搜索到哮喘相关靶点5973 个,将97 个黄芪活性化合物的预测靶与哮喘相关靶点进行映射,取二者交集得到共同靶点81 个。见图1。
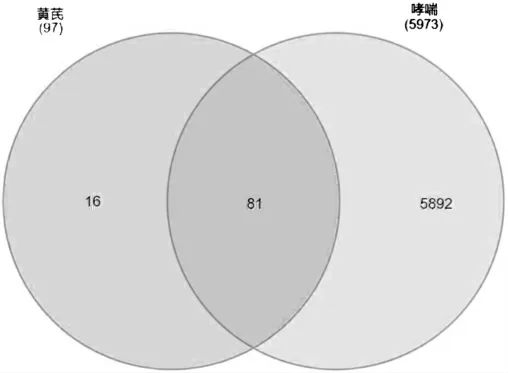
图1 哮喘相关靶点与黄芪活性化合物的预测靶点韦恩图
2.3 黄芪-化合物-靶点-哮喘网络构建结果
网络中共有96 个节点和272 条边,见图2。靶点数较多的前5 位化合物依次为槲皮素(65 个)、山奈酚(29 个)、异鼠李素(15 个)、刺芒柄花素(13 个)、毛蕊异黄酮(10 个),其可能是黄芪发挥治疗哮喘作用的关键化合物。
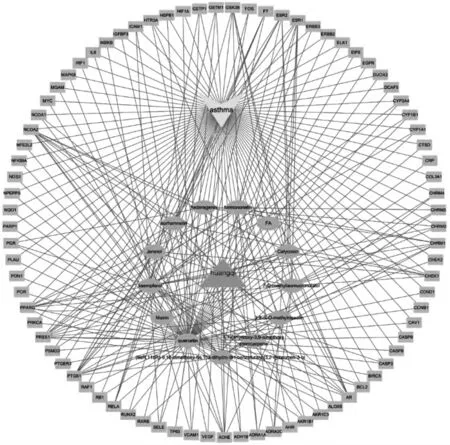
图2 黄芪-化合物-靶点-哮喘网络
2.4 PPI 网络构建结果
为进一步研究黄芪治疗哮喘的作用机制,将映射所得81 个共同靶点进行PPI 网络分析并进行可视化处理,网络图中包括18 个节点,89 条边,图中节点的大小表示靶点的degree 值,颜色由黄色到紫色,表示靶点的度值由小到大,见图3(封三)。丝裂原激活蛋白激酶8(MAPK8)、表皮生长因子受体(EGFR)、白细胞介素(IL)-6、细胞周期蛋白D1(Cyclin D1)、血管内皮生长因子(VEGF)、MYC 的degree 值排名靠前,可能是黄芪发挥中医临床功效及与哮喘产生关联的关键作用靶点。
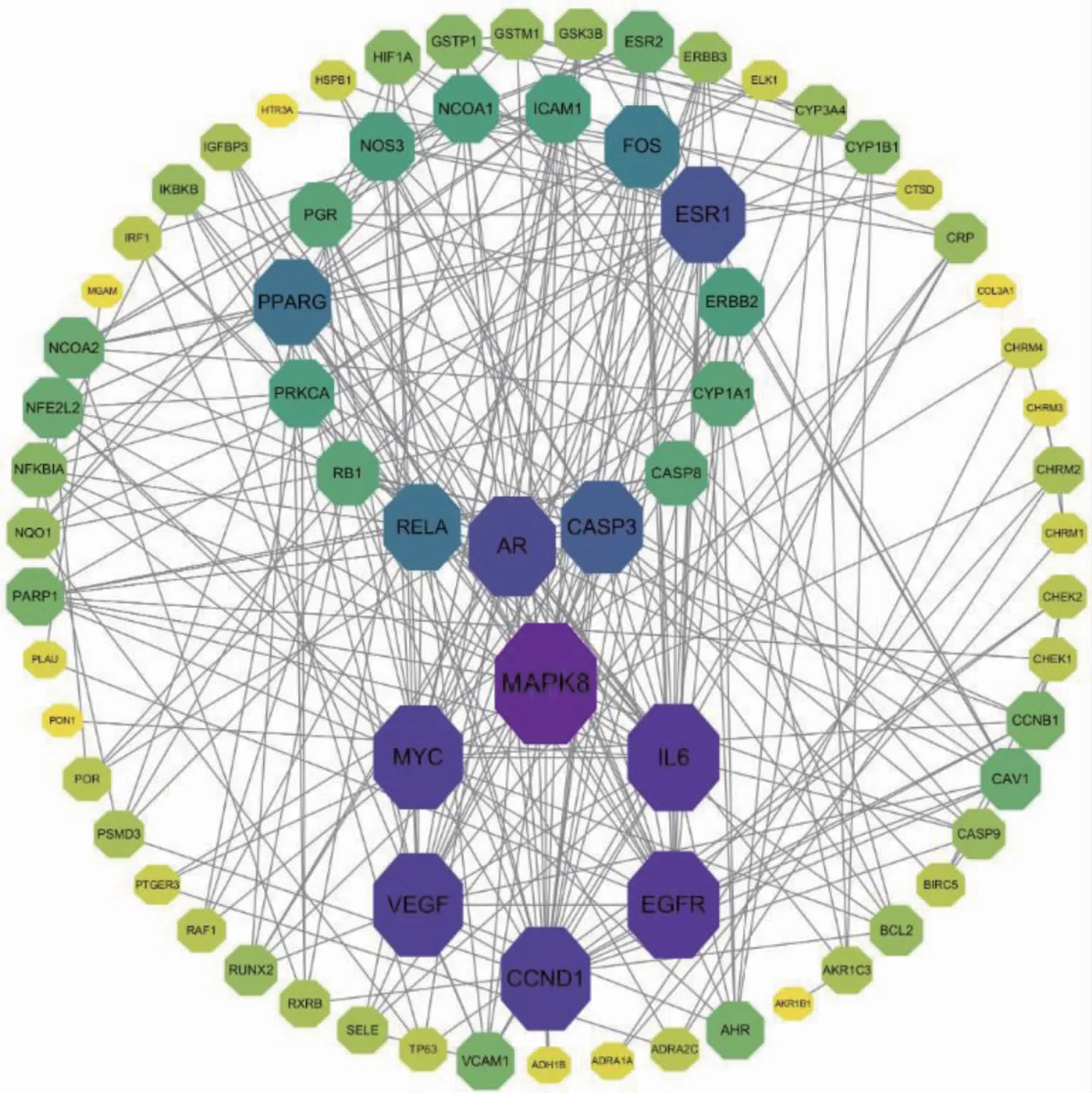
图3 黄芪和哮喘共同靶点蛋白质-蛋白质相互作用网络图
2.5 GO 功能富集分析和KEGG 通路富集分析结果
将上述81 个潜在靶点经R 语言运行后可得到GO 功能富集分析110 个条目(P <0.05),按照P 值从小到大顺序排列,排名前20 的GO 条目绘制成气泡图,气泡节点越大则富集基因数目越多,颜色越红则富集越显著,见图4(封三),其中在DNA 结合转录因子结合、DNA 结合转录激活因子活性、RNA 聚合酶Ⅱ特异性、泛素样蛋白连接酶结合、氧化还原酶活性、激活转录因子结合等方面靶点富集较集中。
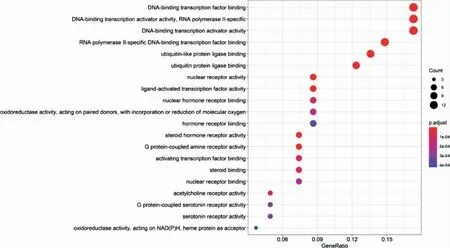
图4 基因本体论功能富集分析
KEGG 通路富集分析筛选得到119 条通路(P <0.05),按照P 值从小到大顺序排列,排名前20 的通路绘制成柱状图,柱状图长度越长则富集基因数目越多,颜色越红则富集越显著,见图5(封四),其中黄芪治疗哮喘的主要信号通路为AGE-RAGE 信号通路、TNF 信号通路、PI3K-Akt 信号通路和p53 信号通路。
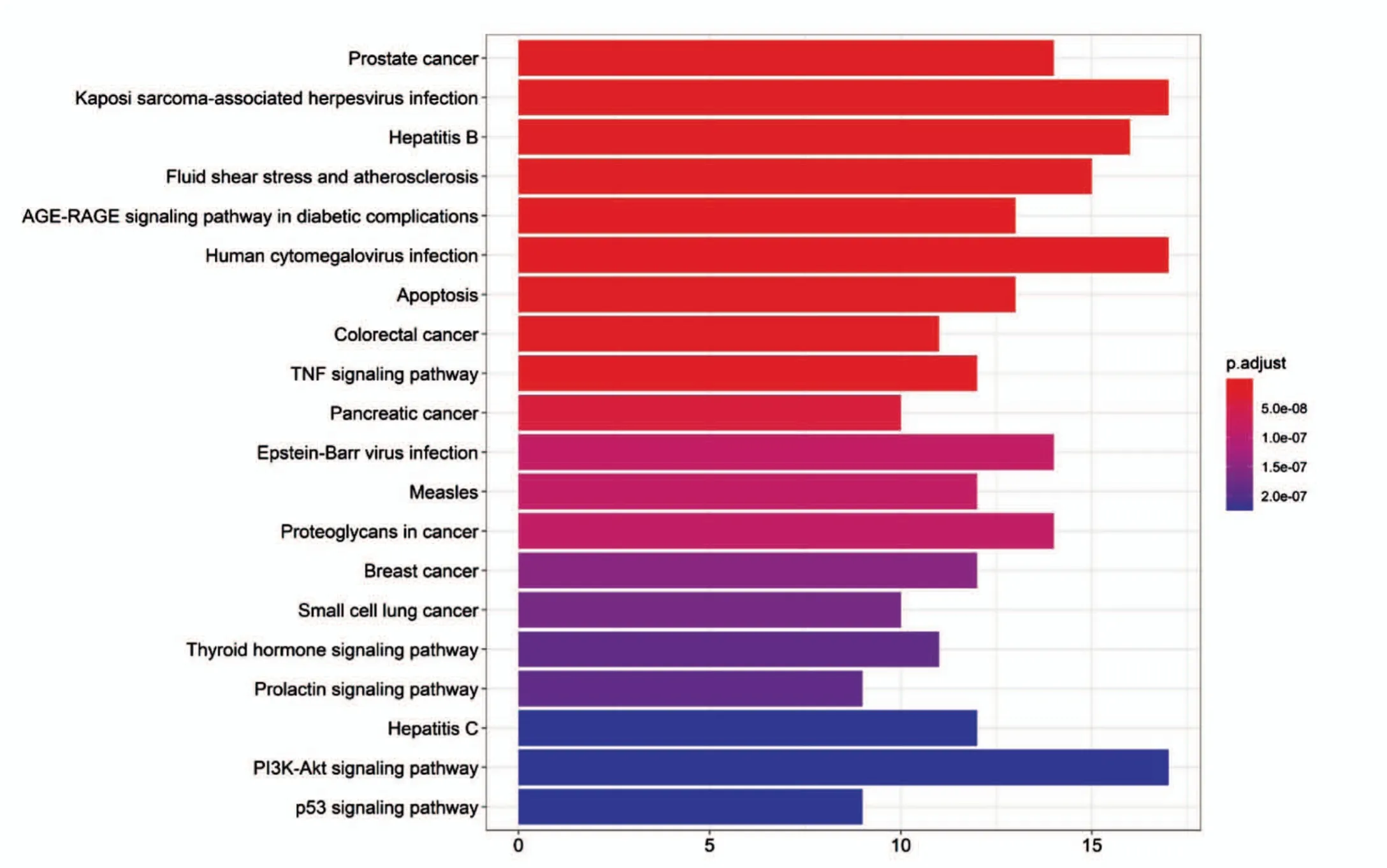
图5 日本京都基因和基因组百科全书通路富集分析
3 讨论
本研究筛选出黄芪治疗哮喘的主要活性成分为槲皮素、山柰酚、异鼠李素、刺芒柄花素、毛蕊异黄酮。其中槲皮素可以通过抑制气道炎症、降低气道高反应性和免疫调节等多种途径对哮喘起到明显的治疗作用。Luo 等[8]研究发现槲皮素可以通过抑制IL-6、IL-1β和TNF-α 等炎症因子的表达减轻气道炎症反应,缓解哮喘小鼠的症状。山柰酚可以抑制哮喘气道重塑重要靶点转化生长因子-β1(TGF-β1)mRNA 的表达[9]。异鼠李素能够通过抑制树突细胞(DCs)表面共刺激分子的表达调节机体免疫能力和减轻炎症反应[10]。刺芒柄花素可以减轻炎症反应、抗氧化及调节免疫机制,能够通过促进相关免疫器官免疫活性细胞的增殖和成熟来增强机体的免疫功能[11]。毛蕊异黄酮可以抑制过敏性炎症的早期反应,其机制可能与降低核因子κB(NF-κB)转录活性,进而减少胸腺基质淋巴细胞生成素的生成有关[12]。由此可见黄芪中的主要活性成分具有抗炎、抗氧化、免疫调节等功能,对哮喘引发的炎症反应及气道重塑具有潜在的治疗作用。
通过PPI 网络分析筛选degree 值前6 位的靶点依次为:MAPK8、EGFR、IL-6、Cyclin D1、VEGF、MYC,可能为黄芪发挥中医临床功效及与哮喘产生关联的关键作用靶点。MAPK8 是MAPK 家族成员之一,MAPK 信号通路可以通过介导炎症、免疫应答、气道结构细胞反应等途径参与哮喘的发生和发展[13]。EGFR 能够与表皮生长因子、转化生长因子等配体结合,促进上皮细胞和成纤维细胞的增殖、分化,从而致使气道上皮组织损伤和气道重塑,加重哮喘的病情[14]。IL-6 是哮喘的重要促炎性细胞因子,能够刺激Th2 细胞、嗜酸性粒细胞等释放多种炎症介质,诱发哮喘患者气道炎症,加重哮喘症状[15]。VEGF 能够刺激血管内皮细胞增殖,促进气道血管扩张和通透性增强,促使支气管周围纤维化,加重哮喘气道重塑[16]。研究证实,Cyclin D1 和MYC 基因均能够促进气道平滑肌细胞的增殖力,两者在哮喘大鼠肺组织中的表达水平与气道重塑程度呈正相关[17-18]。
GO 功能富集分析发现,黄芪治疗哮喘的潜在靶点主要涉及DNA 和RNA 的转录调控、细胞因子与转录因子的活性及受体结合、抗氧化应激、激素调节、蛋白质结合和酶活性等生物学功能。通过KEGG 富集分析并查阅文献发现黄芪可以通过调控多条信号通路达到治疗哮喘的目的。其中AGE-RAGE 信号通路能够磷酸化NF-κB,促进大量黏附分子、生长因子、炎症细胞因子的表达和释放,引发气道炎症反应[19]。AGE-RAGE 信号通路可以通过激活蛋白激酶C 增强TGF-β1 的表达,致细胞外基质的沉积及气道上皮间质化,最终导致气道重塑[20-21]。TNF 信号通路是哮喘发病过程中的重要通路,能够促使中性粒细胞、嗜酸性粒细胞等多种炎症细胞聚集于气道产生炎症反应,调控支气管平滑肌细胞增殖分化和增加血管通透性参与气道重塑,并刺激G 蛋白偶联受体、内皮素受体的表达引发气道高反应性[22]。PI3K/Akt 信号通路与哮喘气道重塑关系密切,可促进气道平滑肌细胞增殖,造成气道壁增厚和管腔狭窄[23]。研究发现,PI3K/Akt 信号通路可调控Th1/Th2,促进Th2 细胞炎症因子的分泌,引发哮喘的气道炎症反应及气道高反应性[24]。嗜酸性粒细胞的凋亡过程主要由细胞抗凋亡基因(Bcl 基因家族)调控,p53 信号通路可以激活线粒体上的Bax 基因,使其与Bcl-2 结合而解除Bcl-2 抑制细胞凋亡的作用,从而诱导嗜酸性粒细胞凋亡,控制哮喘的炎症反应[25]。以上的研究结果与本研究的网络药理学预测结果较为一致,进一步印证了黄芪治疗哮喘的作用机制。
综上所述,黄芪的主要活性成分可通过多靶点、多通路发挥对哮喘的治疗作用。黄芪中槲皮素、山柰酚、异鼠李素、刺芒柄花素、毛蕊异黄酮通过调控AGERAGE 信号通路、TNF 信号通路、PI3K-Akt 信号通路和p53 信号通路作用于MAPK8、EGFR、IL-6、Cyclin D1、VEGF、MYC 等靶点,发挥抗炎、抗氧化、免疫调节等作用,对哮喘所引发的炎症反应、气道高反应性及气道重塑发挥治疗作用。鉴于本研究仅是通过数据挖掘的形式对黄芪治疗哮喘的作用机制进行预测,数据库尚未能收录所有的化学成分,可能会造成部分特异性化合物信息丢失,故存在一定的局限性,后期还需要更加深入的基础实验和临床试验予以佐证。

