PPAR-γ对人胰腺癌BxPc-3细胞增殖的影响
李博 施景龙 邱厚匡 许鸣
【关键词】过氧化物酶体增殖物激活受体-γ;胰腺癌;细胞增殖
胰腺癌是消化系统恶性程度高、预后差的恶性肿瘤之一,由于其侵袭性强,早期往往已经浸润大血管、神经等,造成手术切除难度大,严重降低生存率,5年总体生存率不足1%[1]。过氧化物酶体增殖物-γ(PPAR-γ)除参与脂肪代谢、炎症反应和细胞周期的调控等细胞功能调节外,还与肿瘤发生关系密切[2]。笔者前期试验表明促进PPAR-γ表达可以有效抑制人胰腺癌BxPc-3细胞上皮间充质转化(EMT)及侵袭性[3]。本实验拟明确调控PPAR-γ表达对BxPc-3细胞增殖活性的影响。
材料与方法
一、材料
人胰腺癌BxPc-3细胞购自上海中科院细胞研究所;PPAR-γ激动剂罗格列酮购自美国Sigma;胰酶、高糖DMEM培养基购自美国Gibco公司;四甲基偶氮唑蓝(MTT)试剂盒购自中国碧云天公司;鼠抗人PPAR-γ抗体及GAPDH内参购自南京凯基公司。
二、方法
1.细胞株与培养
人胰腺癌BxPc-3细胞用含10%胎牛血清的DMEM培养液于37℃、5%CO2培养箱中培养,细胞均呈贴壁生长。每2~3d用0.25%胰酶消化传代1次。根据前期研究经验,将BxPc-3细胞分5组处理96h,分别为不加药物的对照组(对照组)、加入终浓度5μmol/L罗格列酮组(5μmol/L罗格列酮组)、加入终浓度10μmol/L罗格列酮组(10μmol/L罗格列酮组)、加入终浓度20μmol/L罗格列酮组(20μmol/L罗格列酮组)、加入终浓度40μmol/L罗格列酮组(40μmol/L罗格列酮组)。
2.PPAR-γ表达水平的检测
采用蛋白免疫印迹法:收集对数生长期BxPc-3细胞,各组BxPc-3细胞加药后加入600μlRIPA细胞裂解液,离心30min,收集上清液即总蛋白,加2倍体积十二烷基酸钠上样缓冲液,电泳后转移至醋酸纤维膜上,脱脂奶粉封闭,加入相应一抗(PPAR-γ抗体,1∶100),4℃孵育过夜,洗膜3次,加入羊抗鼠二抗(1∶10000),37℃孵育2h,电化学发光(ECL)法检测,感光顯影。AlphaImager2200图像系统分析灰度值,以GAPDH为内参,计算各组细胞的PPAR-γ表达水平。实验组每组设4个平行孔,实验独立重复3次,结果取平均值。
3.BxPc-3细胞增殖活性的检测
3.BxPc-3细胞增殖活性的检测采用MTT法检测:收集对数生长期的BxPc-3细胞,各组BxPc-3细胞加药处理后加入20μlMTT溶液,孵育4h,再加入150μl二甲基亚砜(DMSO)震荡10min,使用ELISA检测仪于490nm波长处测量各组吸光度值(增殖活性)。每组设4个平行孔,实验独立重复3次,结果取平均值。
三、统计学处理
使用SPSS16.0处理数据。实验数据用表示,多组间比较采用单因素方差分析,进一步两两比较行LSD-t检验。P<0.05为差异有统计学意义。
结果
一、不同浓度罗格列酮对BxPc-3细胞PPAR-γ表达水平的影响
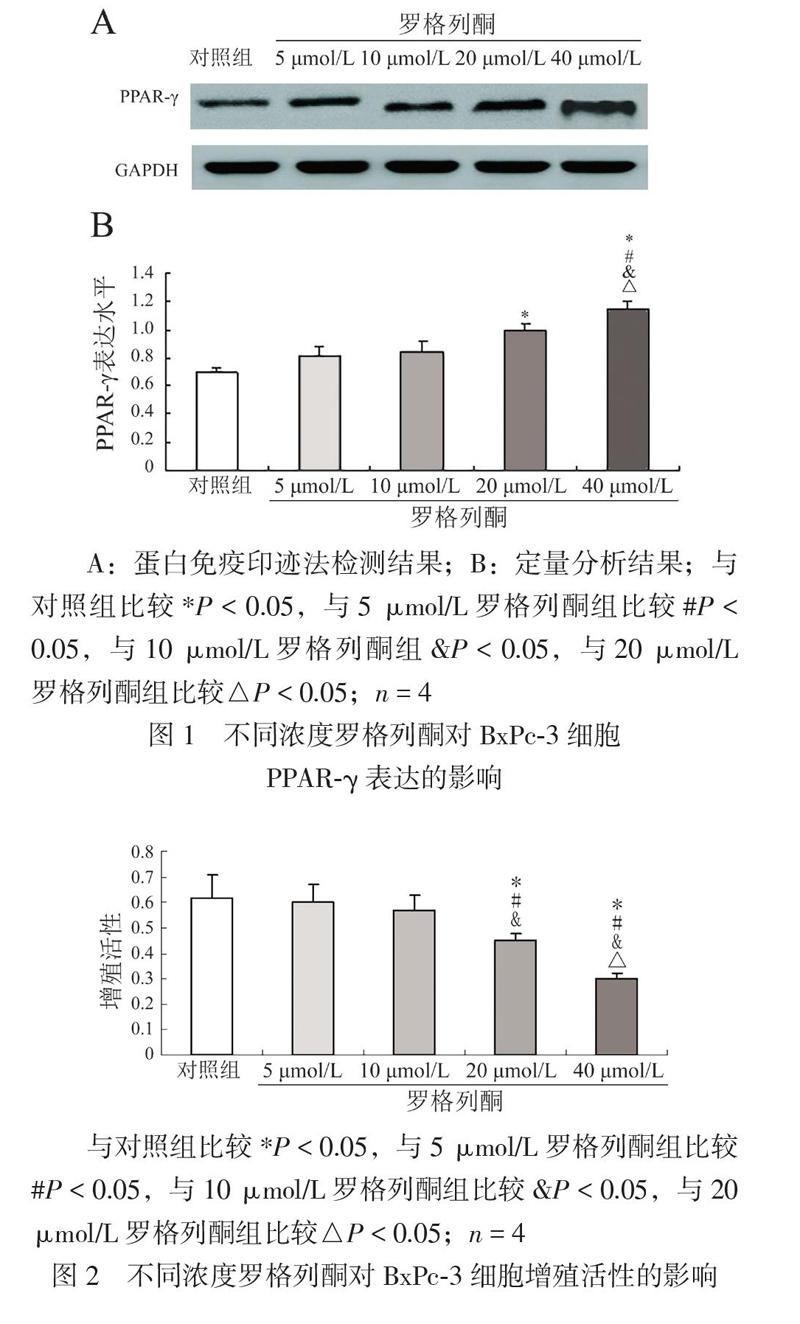
5组BxPc-3细胞PPAR-γ表达水平比较差异有统计学意义(F=40.922,P<0.001)。5μmol/L罗格列酮组、10μmol/L罗格列酮组BxPc-3细胞的PPAR-γ表达水平与对照组比较差异均无统计学意义(P均>0.05),但20μmol/L罗格列酮组、40μmol/L罗格列酮组BxPc-3细胞的PPAR-γ表达水平升高,与对照组比较差异均有统计学意义(P均<0.05),且40μmol/L罗格列酮组BxPc-3细胞的PPAR-γ表达水平高于5μmol/L罗格列酮组、10μmol/L罗格列酮组和20μmol/L罗格列酮组(P均<0.05),见图1。
二、不同浓度罗格列酮对BxPc-3细胞增殖活性的影响
MTT检测显示,5组BxPc-3细胞增殖活性比较差异有统计学意义(F=19.966,P<0.001)。5μmol/L罗格列酮组、10μmol/L罗格列酮处理后BxPc-3细胞增殖活性分别为0.60±0.07、0.57±0.06,与对照组的0.62±0.09比较差异均无统计学意义(P均>0.05);40μmol/L罗格列酮组细胞增殖活性为0.30±0.02,低于20μmol/L罗格列酮组的0.45±0.03,且2组BxPc-3细胞增殖活性均低于对照组、5μmol/L罗格列酮组和10μmol/L罗格列酮组(P均<0.05),见图2。
讨论
PPAR是一类由配体激活的转录因子,有α、β和γ这3种亚型,3种亚型在功能和结构有一定差异[4]。PPAR-γ配体分为外源性和内源性2大类,其中外源性配体以胰岛素增敏剂噻唑烷二酮类药物为代表,包括罗格列酮、吡格列酮等,临床用于治疗胰岛素抵抗、糖尿病等,内源性配体则包括一些不饱和脂肪酸及其代谢产物,如花生四烯酸、亚油酸等,还有前列腺素衍生物、前列腺素D2等,这些天然激动剂活性都较低[5-6]。
PPAR-γ最初发现是与胰岛素抵抗、脂肪细胞分化和器官纤维化等有关。近年研究显示其与肿瘤发生关系密切。已有报道PPAR-γ在胃癌、结肠癌、胰腺癌、肝癌、肾癌、乳腺癌、食管癌和淋巴瘤等多种恶性肿瘤中表达[7]。Tsujie等(2003年)报道PPAR-γ在包括BxPc-3细胞在内的6种胰腺癌细胞株上表达。Kristiansen等(2006年)在129例胰腺癌患者的癌组织中检测PPAR-γ,71.3%的病例中有PPAR-γ的表达,且其表达与胰腺癌的分级和分期呈正相关,推测PPAR-γ与胰腺癌有关。PPAR-γ在胰腺癌中的确切作用机制尚未阐明。Eibl等(2001年)认为,PPAR-γ可能通过诱导胰腺癌细胞凋亡,进而阻止胰腺癌细胞生长。
笔者前期研究使用罗格列酮促进BxPc-3细胞中PPAR-γ表达,结果显示罗格列酮可以有效抑制人胰腺癌BxPc-3细胞EMT及侵袭性。本实验中笔者继续将不同浓度罗格列酮作用于BxPc-3细胞,结果显示20、40μmol/L罗格列酮可以有效促进PPAR-γ的表达,且40μmol/L罗格列酮组BxPc-3细胞的PPAR-γ表达高于20μmol/L罗格列酮组。MTT结果提示20μmol/L罗格列酮组、40μmol/L罗格列酮组BxPc-3细胞增殖活性明显下降,表明PPAR-γ表达可以有效抑制人胰腺癌BxPc-3细胞增殖活性。
综上所述,本研究结果初步揭示了PPAR-γ激动剂的抗胰腺癌细胞增殖特性,而探索PPAR-γ参与人胰腺癌BxPc-3细胞增殖及EMT的信号传导通路将是我们下一步的研究方向。

