沙拉沙星、二氟沙星直接竞争化学发光酶联免疫检测方法的建立
李思,蒋蔚,卢春慧,程婷婷,,孙卫东,王权*
(1. 中国农业科学院上海兽医研究所,上海 200241; 2. 南京农业大学动物医学院,江苏 南京 210095)
氟喹诺酮类药物已广泛运用于人[1-2]与动物[3-4]疾病的治疗当中,其中盐酸二氟沙星、盐酸沙拉沙星为兽类专用药[5]。二氟沙星可通过脱甲基作用生成其活性代谢产物沙拉沙星,从而起到抗菌效果[6]。沙拉沙星是由美国雅培公司在1995年上市,并获得FDA批准的第一个可用于食用动物的氟喹诺酮类药物[7]。临床上以盐酸沙拉沙星的形式用药,因其抗菌谱广、药效良好,所以被广泛用于畜禽及水产类的细菌感染防治[8-9]。此外,盐酸沙拉沙星价格低廉,是畜禽养殖户的用药首选,又由于不规范用药或滥用的现象时有发生,易导致畜禽体内细菌耐药性增强[10],通过食物链对消费者的神经系统、葡萄糖代谢、皮肤等造成潜在的危害[11]。我国农业部已明文规定了二氟沙星、沙拉沙星在鸡肉当中的最大残留量分别为300 μg/kg、10 μg/kg[12],美国已经全面禁止了氟喹诺酮类药物在养殖领域的使用[13]。国内外用于沙拉沙星残留检测的方法主要包括:免疫分析方法[14]、高效液相色谱法(HPCL)[15]、液相色谱-质谱联用法(LC/MS)[16-17]、超高效液相色谱法(UPCL)[18]等,其中后3种方法需要复杂且耗时长的样品前处理,而且检测仪器昂贵,不适用于市场上大量样品的快速检测。免疫分析方法当中主要包括酶联免疫分析方法(ELSIA)[19]、胶体金免疫层析法(GICA)[20]、荧光免疫分析法(IFA)[21]、化学发光酶联免疫法(chemiluminescence enzyme-linked immunoassay,CLEIA)[22],具有快速、高特异性、高灵敏度等特点,可满足市场上大批量快速检测的需求。本研究中建立的直接竞争化学发光酶联免疫分析方法(dc-CLEIA),是将化学发光与酶联免疫分析方法结合在一起,利用酶标记抗体,待免疫反应结束后,以酶催化化学发光底物,根据其化学发光强度进行定性及定量分析。此方法不仅可以缩短检测时长,而且还能提高检测灵敏度。
1 材料与方法
1.1 主要材料
沙拉沙星单克隆抗体(SAR-Ab)及包被抗原(SAR-1-OVA),均由本实验室制备;盐酸沙拉沙星,购自上海源叶生物科技有限公司;二氟沙星、诺氟沙星、恩诺沙星、环丙沙星、氧氟沙星等氟喹诺酮类药物,均购自上海阿拉丁生化科技股份有限公司;辣根过氧化物酶(HRP),购自上海满雪生物科技有限公司;高碘酸钠(NaIO4)、四氢硼酸钠(NaBH4),购自国药集团化学试剂有限公司;化学发光底物A液、B液,均购自湖州英创生物科技有限公司;超高性能发光检测仪(BioTek®)。
1.2 酶标沙拉沙星抗体(McAb-HRP)的合成与鉴定
1.2.1 McAb-HRP的制备
根据文献[23]的方法,采用改良过碘酸钠法合成SAR-Ab辣根过氧化物酶标记物(McAb-HRP)。称取6 mg HRP溶解于1 mL去离子水中,再加入300 μL NaIO4溶液(0.1 mol/L),混匀,室温下避光反应20 min。将反应后的混合液使用醋酸钠溶液(1 mmol/L,pH=4.4)透析过夜,透析后的HRP溶液用碳酸盐缓冲液(CBS,0.2 mol/L,pH=9.5)调节pH至 9.5 作为A液。取6 mg SAR-Ab溶于CBS(0.01 mol/L,pH=9.5)中作为B液,将A液与B液混合,室温避光搅拌反应2 h。 加入80 μL NaBH4溶液(4 mol/L),混匀,室温避光反应1.5 h。再将反应产物以PBS(0.01 mol/L,pH=7.4)溶液于4 ℃透析 3 d,最后,与等体积甘油混合保存于-20 ℃。
1.2.2 McAb-HRP的鉴定
在220~440 nm范围内进行对SAR-Ab、HRP、McAb-HRP的PBS溶液进行紫外光谱扫描鉴定,对比三者之间的最大吸收峰的位移及其吸收曲线变化,鉴定McAb-HRP是否偶联成功。同时采用直接ELISA鉴定偶联物McAb-HRP的效价,采用棋盘法,向酶标板中纵向包被SAR-1-OVA及OVA,横向加入不同稀释度的酶标抗体McAb-HRP,经ELISA常规操作,测得其效价。
1.3 dc-CLEIA检测方法的建立
1.3.1 包被原浓度与酶标抗体稀释比工作浓度确定
首先采用棋盘法,纵向包被不同浓度的包被原(SAR-1-OVA),横向包被不同稀释度的酶标抗体(McAb-HRP),根据RLU值,初步选择数值在1×106左右的包被原浓度以及酶标抗体稀释度作为初步工作浓度。采用二因子交叉试验,在初步的工作浓度上下分别选择3个不同的包被抗原及酶标抗体浓度,使沙拉沙星标准品终浓度为20、10、5、2.5、1.25、0.625、0.312 ng/mL,对不同浓度的沙拉沙星标准溶液作dc-CLEIA,绘制各包被原及酶标抗体工作浓度下的抑制标准曲线,计算其灵敏度IC50(即50%抑制率时对应的沙拉沙星标准品浓度)的值,根据IC50的值选择最佳工作浓度并建立标曲。
1.3.2 检测步骤
用CBS(pH=9.6,0.05 mol/L)将包被原SAR-1-OVA稀释到所需浓度,加入化学发光板中100 μL/孔,4 ℃孵育过夜,1×PBST洗板3遍,间隔5 min。5%脱脂乳200 μL/孔,37 ℃ 孵育 2 h,1×PBST洗板3遍,间隔5 min。洗板后加入50 μL稀释好的标准品(或样品)和50 μL McAb-HRP,置于37 ℃ 孵育1.5 h,1×PBST洗板3遍,间隔5 min。加入100 μL/孔的化学发光的底物液(A液∶ B液=1∶1),5 min内,用超高性能发光检测仪检测,读取化学发光值(RLU值)。
1.4 建立标准曲线
根据最佳工作条件结果,以沙拉沙星标准品浓度的对数值为横坐标,以结合率B/B0作为纵坐标(B表示某一浓度沙拉沙星标准品抑制时对应的RLU值,B0表示空白样品对应的RLU值),建立沙拉沙星直接竞争化学发光标准曲线。
1.5 精密度试验
用不同浓度的盐酸沙拉沙星标准品进行竞争抑制时,以McAb-HRP与包被原SAR-1-OVA结合率的批内误差和批间误差来评价此方法的精密度。在同一次试验中,每个标准品浓度做5组重复,以其批内变异系数表示其批内精密度;在不同的时间连续做5次,以其批间变异系数表示其批间精密度。
1.6 特异性试验
取13种氟喹诺酮类药物以及4种其他抗生素作为竞争抑制物,进行dc-CLEIA。拟出各药物的抑制曲线,并计算出其半数抑制量(IC50)。最后,按公式得出各竞争抑制药物与SAR-Ab的交叉反应率。
交叉反应率=(沙拉沙星标准品的IC50/其他竞争抑制药物的IC50)×100%。
1.7 最低检出限(LOD)试验
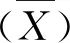
1.8 样品前处理
将鸡胸肉用组织匀浆机打成均质的糊状。取4 g均质样本于50 mL离心管中加入乙腈-二氯甲烷混合液(乙腈∶二氯甲烷=1∶4)16 mL,充分涡旋5 min,15 ℃,5 000 r/min,离心10 min,取8 mL有机相至干燥容器中,旋转蒸发至干,用2 mL 0.02 mol/L PBS溶解干燥的残留物,加入2 mL正己烷,充分混合30 s,15 ℃,5 000 r/min,离心5 min,去除上层,取下层PBS液体用于检测分析。
1.9 添加回收试验
在标准曲线线性范围内,根据高、中、低的添加浓度原则,向空白鸡肉样品中加入不同浓度的沙拉沙星药物,每个浓度设置5组平行试验。按照1.8的样品处理方法,采用dc-CLEIA方法检测实际样品中的药物浓度,最后根据计算公式计算出各添加浓度的回收率和变异系数。
回收率=(实际浓度的平均值/添加浓度)×100%;变异系数=(实际浓度的标准差/实际浓度的平均值)×100%。
2 结果与分析
2.1 酶标抗体McAb-HRP的鉴定
2.1.1 紫外扫描鉴定
取SAR-Ab、HRP和McAb-HRP的PBS溶液,在220~440 nm范围内进行紫外扫描,紫外扫描结果见图1,谱图显示SAR-Ab在波长278 nm处有个最大吸收峰,HRP在403 nm处有个最大吸收峰,McAb-HRP则分别在277和402 nm处各有个最大吸收峰,可初步判断酶标抗体偶联成功。
图1 McAb-HRP偶联紫外扫描分析
2.1.2 间接ELISA鉴定及其效价测定
运用间接ELISA鉴定McAb-HRP是否偶联成功,结果如表1,包被SAR-1-OVA孔的OD450较包被OVA孔大,说明酶标抗体可以与SAR-1-OVA特异性结合,并且能与四甲基联苯胺(TMB)发生显色反应,由此进一步证明了酶标抗体偶联成功,且在包被原SAR-1-OVA浓度为2.5 μg/mL时,酶标抗体效价达到了1∶32 000。

表1 McAb-HRP鉴定结果
2.2 dc-CLEIA检测方法的建立
2.2.1 最佳包被抗原浓度及最佳酶标抗体稀释度的确定
根据初步选择的包被抗原浓度1.25 μg/mL及酶标抗体稀释度1∶8 000,进一步选取3个包被抗原浓度2.5、1.25、0.625 μg/mL以及3个酶标抗体稀释度1∶4 000、1∶8 000、1∶12 000,同时使沙拉沙星标准品的终浓度为20、10、5、2.5、1.25、0.625、0.312 ng/mL,根据dc-CLEIA的操作步骤,进行药物竞争抑制试验,最后根据RLU值,计算出在不同包被原浓度及酶标抗体稀释比下的IC50,结果如表2。在包被原浓度为1.25 μg/mL,酶标一抗的稀释度为1∶8 000时,IC50最低,故选其为最佳工作条件。

表2 不同包被抗原浓度及酶标抗体稀释度下的IC50
2.2.2 dc-CLEIA标准曲线的建立
如图2,沙拉沙星在线性范围浓度0.312~20 ng/mL内建立标准曲线,其结合率与沙拉沙星标准品浓度的对数值呈线性关系,回归方程为y=-0.373x+0.688(R2=0.985),经计算,其IC50为3.19 ng/mL。

图2 沙拉沙星dc-CLEIA 标准曲线
2.3 精密度试验
用不同浓度的盐酸沙拉沙星标准品进行竞争抑制,对所得的RLU值进行批内和批间变异系数分析,来表示此方法的精密度。变异系数=[SD的平均值/(1.414×平均结合率)]×100%。沙拉沙星标准品各浓度下的结合率和变异系数见表3。经计算,平均批内变异系数为4.68%,平均批间变异系数为6.13%,平均批内批间变异系数均低于7%,由此说明该方法精密度良好。
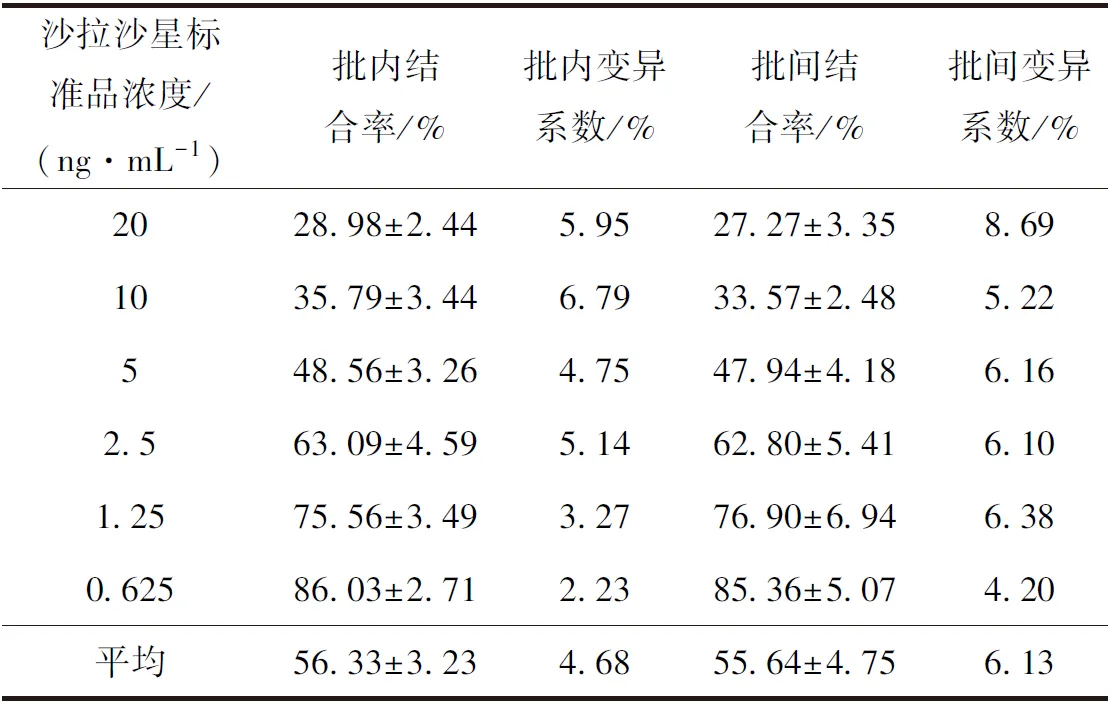
表3 dc-CLEIA批内批间误差
2.4 特异性试验
由表4可知,SAR-Ab与二氟沙星的交叉率较高,与其他10种氟喹诺酮类药物的交叉反应率均低于8%,与其余4种其他抗生素的交叉反应率极低,表示SAR-Ab能特异性的识别沙拉沙星与二氟沙星。

表4 SAR-Ab特异性试验检测结果
2.5 二氟沙星标准曲线的建立
以二氟沙星不同浓度标准品的对数值为横坐标,以结合率B/B0作为纵坐标,建立了二氟沙星直接竞争化学发光标准曲线,如图3。二氟沙星在线性范围浓度0.312~20 ng/mL内,其结合率与二氟沙星不同浓度标准品的对数值呈线性关系,回归方程为:y=-0.369x+0.719(R2=0.994),经计算,其IC50为3.94 ng/mL。
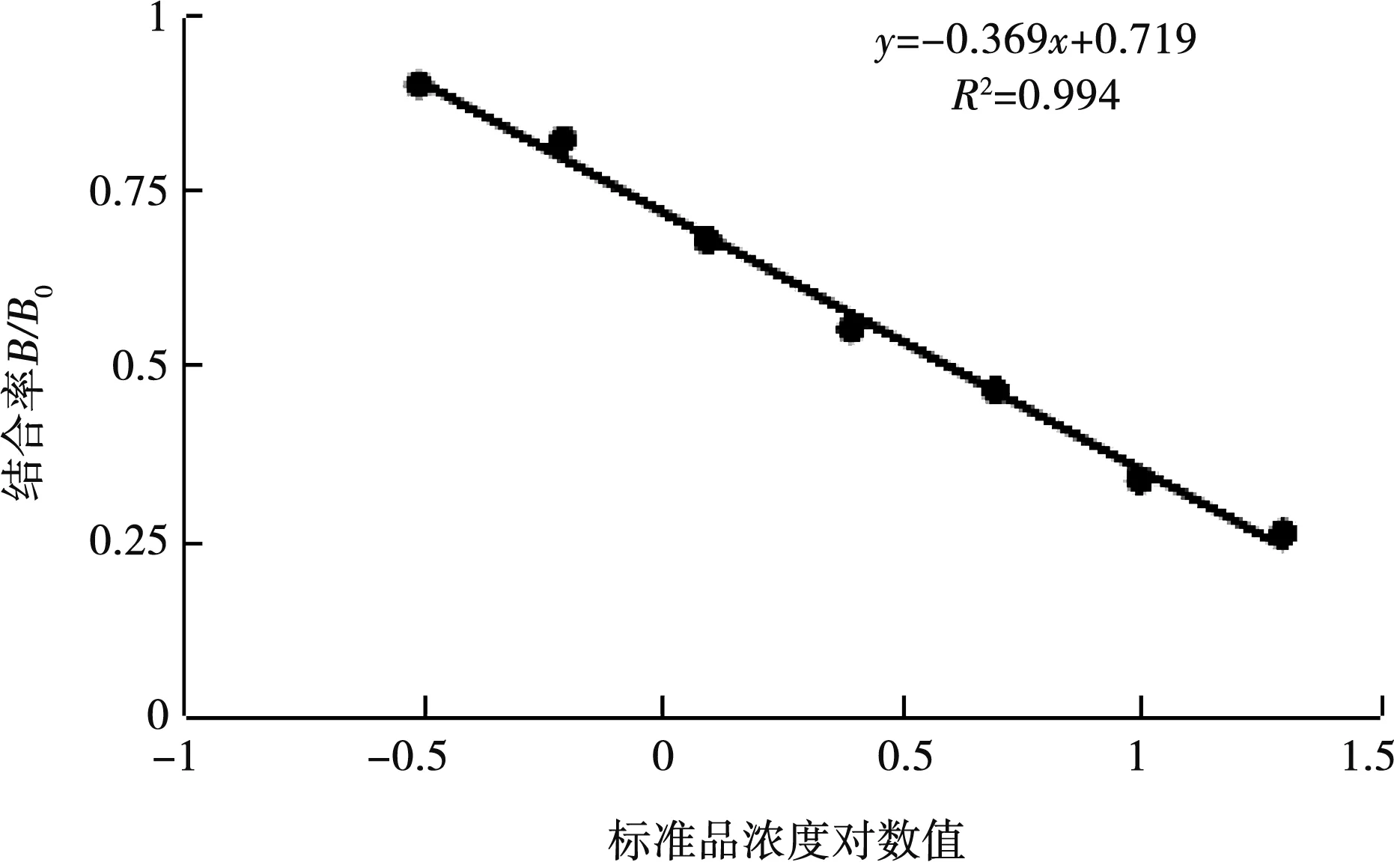
图3 二氟沙星 dc-CLEIA 标准曲线
2.6 最低检出限试验
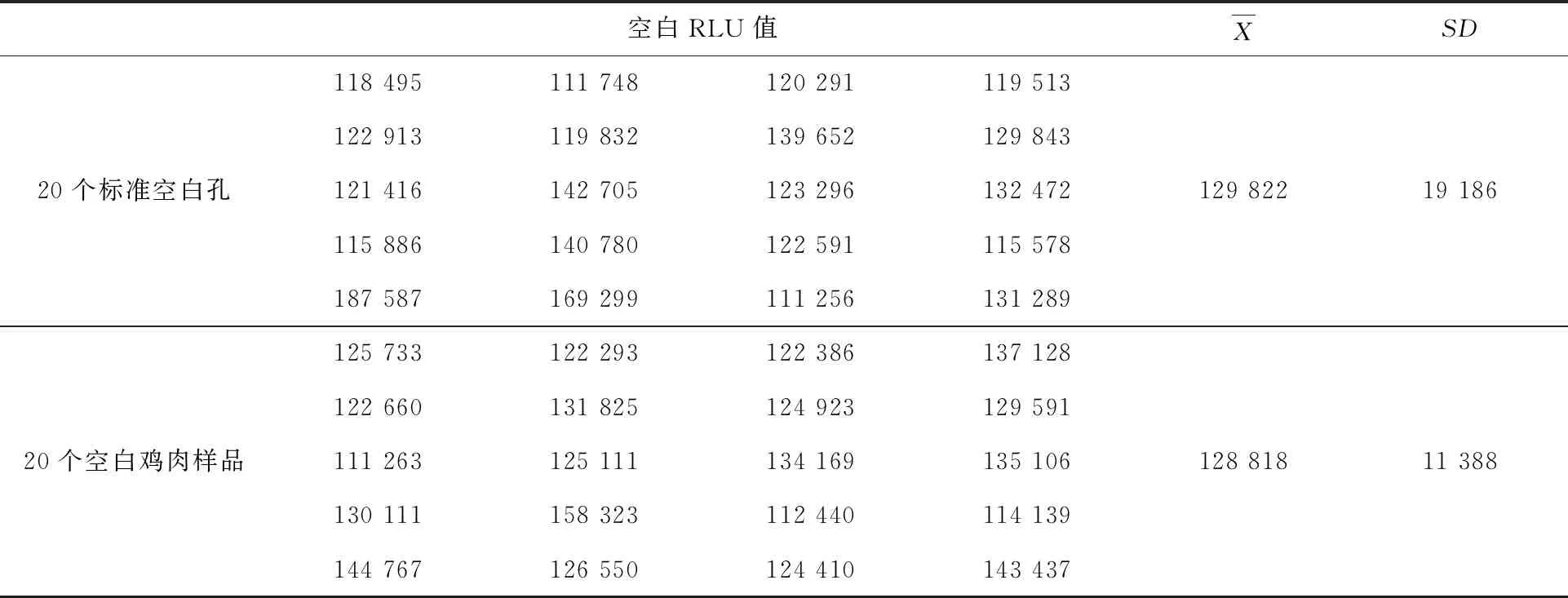
表5 各空白值检测结果
2.7 添加回收试验
在空白鸡肉中,分别添加沙拉沙星和二氟沙星,在0.312~20 ng/mL的线性范围内,均设置20、5、2.5、0.5 μg/kg 4个添加浓度,作dc-CLEIA检测,结果见表6。经计算得出沙拉沙星在鸡肉中的回收率为88.2%~108.3%,其变异系数≤10.28%;二氟沙星在鸡肉中的回收率为93.36%~102.7%,其变异系数≤13.4%。

表6 添加回收试验结果
3 讨论
本研究采用改良的过碘酸钠法,合成偶联物McAb-HRP,经紫外扫描及直接ELISA 鉴定偶联成功,且在包被抗原SAR-1-OVA浓度为2.5 μg/mL时,酶标抗体的效价达到了1∶32 000,说明偶联效率较高。通过棋盘法,确定了最佳包被抗原浓度以及最佳酶标抗体稀释度分别为1.25 μg/mL、1∶8 000,在此基础上建立了dc-CLEIA分析方法,其标准抑制曲线y=-0.373x+0.688 (R2=0.985),灵敏度IC50为3.19 ng/mL,样品最低检出限为1.25 μg/kg。刘儒彪等[24]制备的沙拉沙星ELISA检测试剂盒的灵敏度IC50为4.11 ng/mL,其最低检出限为2.06 ng/mL。根据穆国冬[25]建立的间接竞争ELISA标准曲线y=-24.566x+94.216,R2=0.998,可计算出其灵敏度IC50为3.81 ng/mL,其最低检出限为1.55 ng/mL。由此可看出本研究中建立的dc-CLEIA分析方法,灵敏度高于ELISA方法。本试验建立的dc-CLEIA检测方法,其精密度试验结果显示,其批内、批间变异系数均低于7%,由此说明此方法重复性良好。而特异性结果显示,除与二氟沙星的交叉反应率高达80.96%外,与其他氟喹诺酮类药物的交叉反应率均低于8%,而这正是因为拉沙星是二氟沙星的活性代谢物。这两种氟喹诺酮类药物不同于其他氟喹诺酮类药物的地方在于前者在其N1位上带有一个苯环结构,从而对整个药物分子的空间结构影响较大,故制备的SAR-Ab对二氟沙星的交叉反应率较其他氟喹诺酮类药物高出许多。由此建立了二氟沙星的抑制标准曲线,线性范围为0.312~20 ng/mL,线性方程为y=-0.369x+0.719(R2=0.994),灵敏度IC50为3.94 ng/mL。最后在鸡肉样本中对沙拉沙星和二氟沙星进行添加回收试验,结果显示,沙拉沙星在鸡肉中的回收率为88.2%~108.3%,其变异系数≤10.28%;二氟沙星在鸡肉中的回收率为93.36%~102.7%,其变异系数≤13.4%。由此表明,本试验建立的dc-CLEIA分析方法精密度、特异性良好,灵敏度高。
化学发光酶联免疫方法具备灵敏度高、特异性强,且能快速大量的检测,无需复杂耗时的样品前处理,能满足市场大量检测需求,其次化学发光值能够达到6个数量级,测定范围更宽。化学发光酶联免疫分析方法可分为直接法和间接法,各有其优缺点。本研究中建立的dc-CLEIA方法的灵敏度相较于本实验室建立的间接竞争化学发光酶联免疫方法(ic-CLEIA)的灵敏度1.45 ng/mL低,但也完全能满足国家农业农村部对于沙拉沙星样品残留检测要求,dc-CLEIA优点在于省去了酶标二抗的孵育时间,故在检测时间上优于ic-CLEIA。而ic-CLEIA因为有一抗和酶标二抗反应的放大效应,所以其灵敏度明显优于dc-CLEIA。在实际的运用当中,可根据两种方法的优点来选择具体的检测方法。

