胆翘注射液中主要质量指标成分的定性和定量方法的建立
吕 利 , 谢 颖,2 , 林柏良 , 邓招游 , 邓锐涵 , 彭健波 , 吴文健 , 陶 卿 , 何家康,
(1. 广西大学动物科学技术学院 , 广西 南宁 530005 ; 2. 广西壮族自治区动物疫病预防控制中心, 广西 南宁 530001 ; 3. 广西兽药制剂工程技术研究中心 , 广西 南宁 530003)
动物胆汁具有抗菌、抗炎、解热镇痛、抗氧化等多种药理活性,胆汁酸为胆汁的主要成分[1-2]。黄芩是中医临床的常用药之一,具有清热燥湿、解毒等功效[3],在现代医学中,黄芩具有抗菌[4]、抗病毒[5]、抗炎[6]、抗过敏[7]、抗氧化[8]等药理作用。连翘味苦、性微寒,有清热止吐、除湿退黄、清肝利胆等作用[9],现代药理研究表明,连翘具有广谱抗菌、抗炎、解热、利尿的作用[10-12]。中药注射剂是从药材中提取有效成分并纯化后,制成的可注入机体的溶液、乳状液及临用前配制为溶液的粉末或浓溶液的无菌制剂[13]。中药注射剂是现代科学技术与传统中医药理论相结合的产物,可直接注入体内,吸收快,定位准确,疗效高,可以治疗许多急、慢性病例或危重病例,可充分发挥中药的优点[14]。
胆翘注射液是由胆膏、黄芩提取物和连翘提取物经加工制成的中药注射剂,具有清肺止咳、消炎利胆等多种功效。本试验旨在建立胆翘注射液中胆膏、黄芩提取物和连翘提取物的薄层鉴别方法,以及胆膏、黄芩提取物含量测定的高效液相色谱(HPLC)分析方法,为胆翘注射液质量标准的制定提供方法学依据。
1 材料与方法
1.1 仪器设备 ZF-20D暗箱式紫外分析仪,购自上海宝山顾村电光仪器厂;939型全自动薄层制板器,购自重庆南岸贝尔德仪器技术厂;ZDX-35BI自动座式压力蒸汽灭菌锅,购自山东新华医疗器械股份有限公司;BP211D 电子分析天平,购自德国赛多利斯集团;LC-20A高效液相色谱仪,购自日本岛津制作所,配备有SPD-M20A检测器和DAD、SIL-20A自动进样器和柱温箱;TU-1901紫外可见分光光度计,购自北京普析通用仪器有限责任公司;B3200S-T超声仪,购自必能信超声(上海)有限公司;CD-UPT-П-20L超纯水仪,购自成都越纯科技有限公司。
1.2 药品与试剂 甲醇、乙腈为色谱级,其他试剂为分析纯,水为超纯水;胆膏,其药材基原胆汁为猪科动物Sus scrofa domesticus Briss.,经乙醇处理获得稠膏状物,胆膏的标准符合《兽药国家标准》化学药品、中药卷第一册“胆膏”项下规定,产地广西;黄芩提取物(含黄芩苷86.9%)、连翘提取物(含连翘苷1.98%),均购自四川恒瑞通达生物科技有限公司;三批胆翘注射液中试样品(批号:20150601、20150602和20150603)、缺胆膏的胆翘注射液阴性样品、缺黄芩提取物的胆翘注射液阴性样品、缺连翘提取物的胆翘注射液阴性样品,由广西北斗星动物保健品有限公司提供;猪去氧胆酸对照品(中国食品药品检定所研究院,纯度:TLC时99.5%,HPLC时97.5%,批号:100087~200610);鹅去氧胆酸对照品(中国食品药品检定研究院,纯度:98.3%,批号:110806~201708);黄芩苷对照品(中国食品药品检定所研究院,批号:110715~201714)。
1.3 薄层色谱(TLC)鉴别
1.3.1 胆膏的鉴别 精密量取胆翘注射液10 mL,置50 mL锥形瓶中,加10%氢氧化钠溶液10 mL,用牛皮纸将瓶口盖上,置立式灭菌锅中,于120 ℃、压力103 kPa加热4 h,放冷,用盐酸调节pH至6~7,移至100 mL量瓶中,用甲醇稀释至刻度,摇匀,滤过,取续滤液50 mL,蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液;取缺胆膏的胆翘注射液阴性样品,按上述方法制得阴性样品液;另取猪去氧胆酸对照品、鹅去氧胆酸对照品,分别加无水乙醇制成每1 mL各含1 mg的溶液,作为对照品溶液。吸取上述药液各5 μL,于同一硅胶G薄层板上点样,以异辛烷-乙醚-正丁醇-冰乙酸-水(10∶5∶3∶5∶1,v/v/v/v/v)的上层溶液(临用配置)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105 ℃加热至斑点清晰显色视检。
1.3.2 黄芩提取物的鉴别 取胆翘注射液1 mL,加甲醇9 mL,摇匀,作为供试品溶液;取缺黄芩提取物的胆翘注射液阴性样品,按上述方法制得阴性样品液;另取黄芩苷对照品,加甲醇制成每1 mL含1 mg 的溶液,作为对照品溶液。吸取上述药液各2 μL, 于同一聚酰胺薄膜点样,以醋酸为展开剂,展开,取出,晾干,喷以1%三氯化铁乙醇溶液,在105 ℃加热至斑点清晰显色视检。
1.3.3 连翘提取物的鉴别 取胆翘注射液60 mL,加乙酸乙酯振摇(轻摇)提取3次(60 mL、50 mL、40 mL),合并乙酸乙酯液,蒸干,残渣加甲醇5 mL使溶解,蒸至近干,加中性氧化铝0.5 g,拌匀,加置中性氧化铝柱(100~200目,1 g,内径1~1.5 cm)上,用70%乙醇80 mL洗脱,收集洗脱液,浓缩至干,残渣加甲醇1 mL使溶解,作为供试品溶液;取缺连翘提取物的胆翘注射液阴性样品,按上述方法制得阴性样品液;另取连翘苷对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。吸取上述药液各2~5 μL,于同一硅胶G薄层板上点样,以三氯甲烷-甲醇-冰乙酸(17∶2∶1,v/v/v)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105 ℃加热至斑点清晰显色视检。
1.4 胆膏含量测定
1.4.1 色谱条件 Inertsil ODS-3 C18色谱柱(250 mm×4.6 mm,5 μm),以十八烷基硅烷键合硅胶为填充剂;流动相:乙腈-0.1%冰乙酸(50∶50);流速:1 mL/min;检测器:蒸发光散射检测器;进样量:对照品溶液5 μL和10 μL,供试品溶液10 μL;理论板数按猪去氧胆酸峰计算应不低于7 000。
1.4.2 对照品溶液的制备 分别取猪去氧胆酸、鹅去氧胆酸对照品适量,精密称定,各加入甲醇,分别制得0.625 mg/mL的对照品贮备液,备用。
1.4.3 供试品溶液的制备 精密量取本品10 mL,置50 mL锥形瓶中,加10%氢氧化钠溶液10 mL,用牛皮纸将瓶口盖上,置立式灭菌锅中,于120 ℃、压力103 kPa加热4 h,放冷,用盐酸调节pH至6~7,移至100 mL量瓶中,用甲醇稀释至刻度,摇匀,滤过,取续滤液,作为供试品溶液。
1.4.4 专属性试验 取猪去氧胆酸对照品、鹅去氧胆酸对照品、供试品、阴性样品,在“1.4.1” 项色谱条件下进样检测。
1.4.5 线性关系考察 分别配制浓度为0.125、0.250、0.375、0.500 mg/mL和0.625 mg/mL的猪去氧胆酸、鹅去氧胆酸对照品溶液,在“1.4.1”项色谱条件下进样检测。取“1.4.2”项下浓度均为0.625 mg/mL的猪去氧胆酸和鹅去氧胆酸对照品溶液,加甲醇稀释,进样测定,记录色谱图。
1.4.6 重复性试验 精密量取同一批次注射液样品6份,按“1.4.3”项下制备供试品溶液,在“1.4.1”项下色谱条件进样检测。
1.4.7 稳定性试验 精密量取同一批次注射液样品适量,按“1.4.3 ”项下制备供试品溶液,于室温下放置0、4、8、12、16、20 h和24 h后在“1.4.1”项色谱条件下进样检测。
1.4.8 加样回收率试验 精密量取已知含量的供试品1.0 mL,平行6份,每份各精密加入猪去氧胆酸、鹅去氧胆酸对照品贮备液4.0 mL,按“1.4.3”项下方法制备供试品溶液,在“1.4.1” 项色谱条件下进样检测。
1.4.9 样品含量测定 取三批样品,按“1.4.3”项下方法制备供试品溶液,在“1.4.1”项色谱条件下进样检测;另取对照品适量,同法测定,按外标法计算胆翘注射液中猪去氧胆酸、鹅去氧胆酸的含量。
1.5 黄芩提取物含量测定
1.5.1 色谱条件 Inertsil ODS-3 C18色谱柱(250 mm×4.6 mm,5 μm),以十八烷基硅烷键合硅胶为填充剂;流动相:甲醇-水-冰乙酸(50/50/1);体积流量:1 mL/min;检测波长为274 nm;进样量:10 μL。
1.5.2 对照品溶液的制备 取黄芩苷对照品适量,精密称定,加50%甲醇制成浓度为0.750 mg/mL的对照品溶液,即得。
1.5.3 供试品溶液的制备 精密吸取供试品1 mL, 置100 mL量瓶中,加50%甲醇稀释至刻度,摇匀,滤过,弃去初滤液,取续滤液作为供试品溶液。
1.5.4 专属性试验 取黄芩苷对照品、供试品、阴性样品,在“1.5.1” 项色谱条件下进样检测。
1.5.5 线性关系考察 分别配制浓度为0.075、0.150、0.225、0.300 mg/mL和0.375 mg/mL的黄芩苷对照品溶液,在“1.5.1” 项色谱条件下进样检测,以峰面积为纵坐标(y),以黄芩苷对照品浓度(mg/mL)为横坐标(x)进行回归分析。
1.5.6 重复性试验 精密量取同一批次注射液样品6份,按“1.5.3”项下制备供试品溶液,在“1.5.1” 项色谱条件下进样检测。
1.5.7 稳定性试验 精密量取同一批次注射液样品适量,按“1.5.3 ”项下方法制备供试品溶液,于室温下放置0、4、8、12、16、20 h和24 h后在“1.5.1” 项色谱条件下进样检测。
1.5.8 加样回收率试验 精密量取已知含量的胆翘注射液1.0 mL,平行6份,每份精密加入黄芩苷对照品溶液20 mL,按“1.5.3”项下方法制备供试品溶液,在“1.5.1”项色谱条件下进样检测。
1.5.9 样品含量测定 取3批样品,按“1.5.3”项下方法制备供试品溶液,在“1.5.1”项色谱条件下进样检测;另取对照品适量,同法测定,按外标法计算胆翘注射液中黄芩苷的含量。
2 结果
2.1 胆膏、黄芩提取物、连翘提取物的鉴别 由图1、2、3可知,供试品色谱在与对照品相应的位置上,显相同颜色的斑点,背景清晰,分离效果好,无干扰,结果易判断,符合薄层色谱系统适用性检验。

图1 胆翘注射液中胆膏鉴别的薄层色谱分析Fig.1 TLC analysis of bile ointment in Danqiao injection1:缺胆膏的阴性样品; 2:猪去氧胆酸对照品; 3:鹅去氧胆酸对照品; 4:批号20150601供试品; 5:批号20150602供试品;6:批号20150603供试品1:Negative sample without bile ointment; 2:Control substance of hyodeoxycholic acid; 3:Control substance of chenodeoxycholic acid; 4:Batch 20150601 of trial products; 5:Batch 20150602 of trial products; 6:Batch 20150603 of trial products

图2 胆翘注射液中黄芩提取物鉴别的薄层色谱分析Fig.2 TLC analysis of scutellariae extract in Danqiao injection1:黄芩苷对照品; 2:缺黄芩提取物的阴性样品; 3:批号20150601供试品; 4:批号20150602供试品; 5:批号20150603供试品1:Control substance of baicalin; 2:Negative sample without scutellaria extract; 3:Batch 20150601 of trial products; 4:Batch 20150602 of trial products; 5:Batch 20150603 of trial products
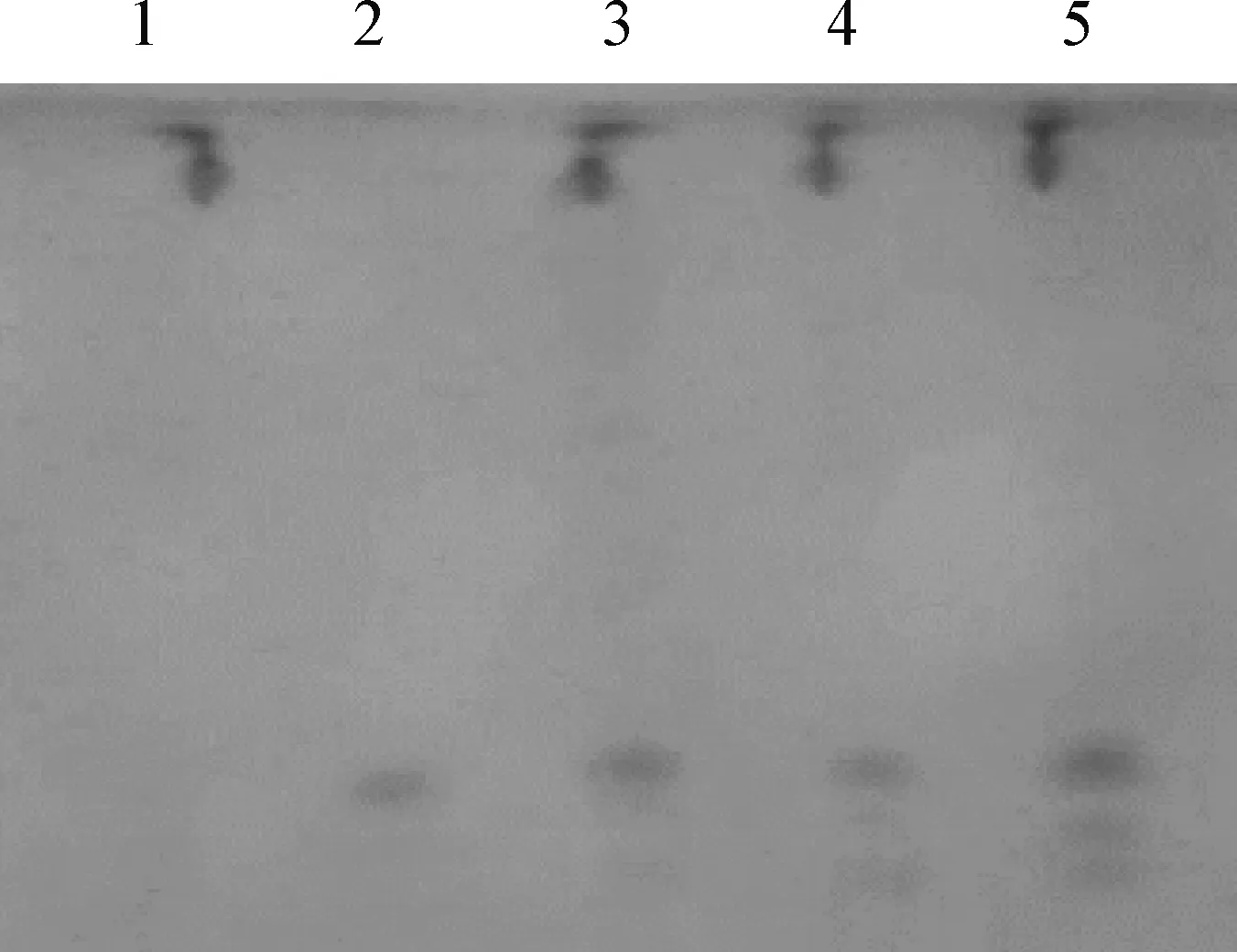
图3 胆翘注射液中连翘提取物鉴别的薄层色谱分析Fig.3 TLC analysis of weeping forsythia extract in Danqiao injection1:缺连翘提取物的阴性样品; 2:连翘苷对照品; 3:批号20150601供试品; 4:批号20150602供试品; 5:批号20150603供试品1:Negative sample without weeping forsythia extract; 2:Control substance of weeping forsythia; 3:Batch 20150601 of trial products; 4: Batch 20150602 of trial products; 5: Batch 20150603 of trial products
2.2 胆膏含量测定
2.2.1 专属性试验 如图4所示,猪去氧胆酸和鹅去氧胆酸的保留时间分别为10.749 min和22.655 min,处方中其他药味对测定无干扰,说明该方法的专属性良好。
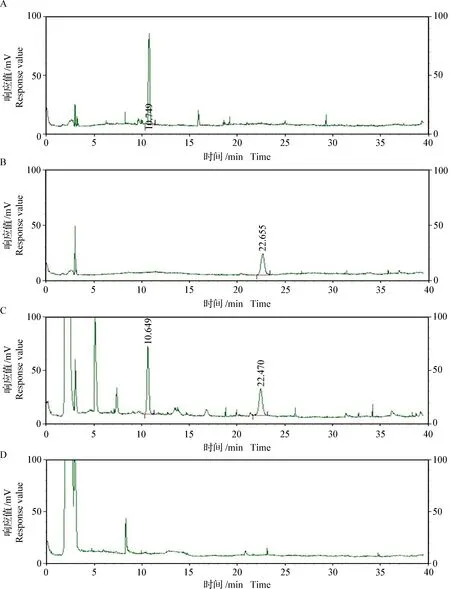
图4 胆翘注射液的高效液相色谱分析Fig.4 HPLC analysis of Danqiao injectionA:猪去氧胆酸对照品溶液; B:鹅去氧胆酸对照品溶液; C:供试品溶液; D:缺胆膏的阴性样A:Control solution of hyodeoxycholic acid; B:Control solution of chenodeoxycholic acid; C:Test solution; D:Negative sample without bile ointment
2.2.2 线性关系 以峰面积的对数为纵坐标(y),以猪或鹅去氧胆酸对照品浓度(mg/mL)的对数为横坐标(x)进行回归分析,得猪去氧胆酸的回归方程为y=1.63x+5.48,R2=0.999 9,鹅去氧胆酸的回归方程为y=1.66x+5.17,R2=0.999 2,表明猪去氧胆酸、鹅去氧胆酸在0.125~0.625 mg/mL范围内时,与峰面积呈良好的线性关系。当信噪比S/N 为3∶1时,猪去氧胆酸和鹅去氧胆酸的检测限分别为7.81 μg/mL和31.25 μg/mL;当信噪比S/N为10∶1时,猪去氧胆酸和鹅去氧胆酸的定量限分别为26.04 μg/mL和104.17 μg/mL。
2.2.3 重复性试验 测得猪去氧胆酸的平均含量为2.83 mg/mL,RSD=0.41%(n=6);鹅去氧胆酸的平均含量为2.30 mg/mL,RSD=0.30%(n=6),表明该方法的重复性良好。
2.2.4 稳定性试验 测得猪去氧胆酸的平均峰面积为1 639 762.43,RSD=0.45%;鹅去氧胆酸的平均峰面积为656 498.71,RSD=0.58%,表明供试品溶液在室温下24 h内稳定。
2.2.5 回收率试验 如表1所示,猪去氧胆酸的平均回收率为100.07%,RSD=0.77%(n=6);鹅去氧胆酸的平均回收率为100.58%,RSD=0.72%(n=6),表明该方法的准确度良好。
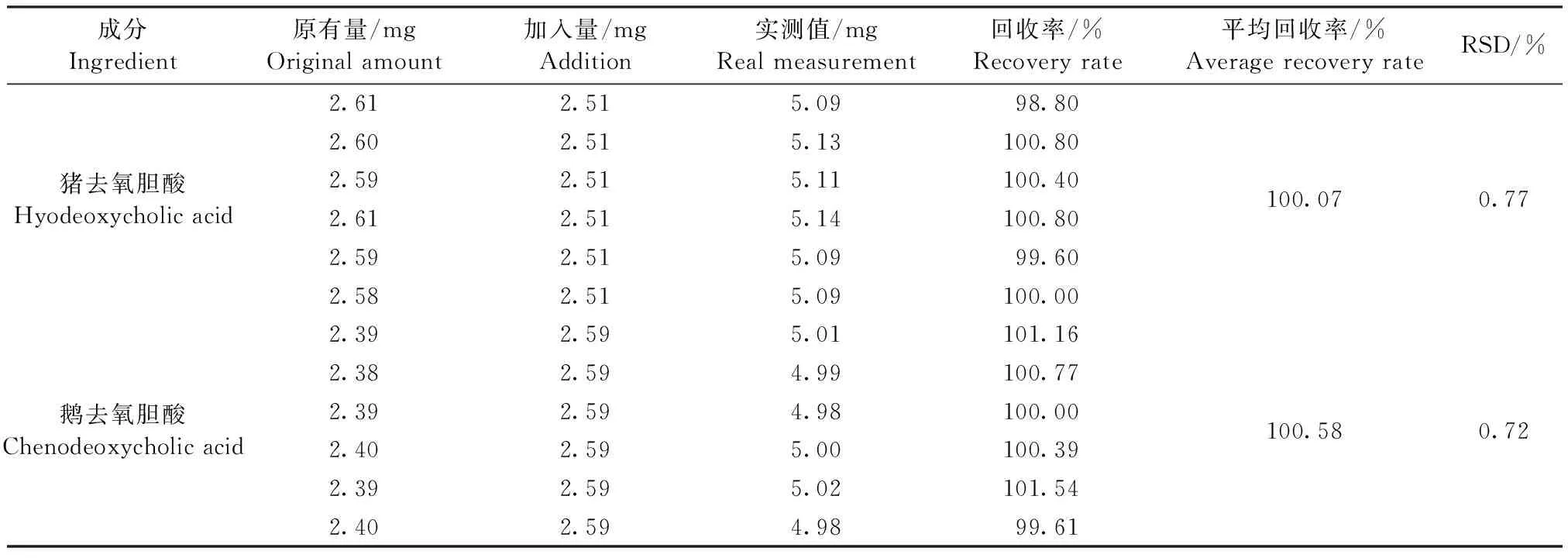
表1 胆翘注射液的加样回收率试验结果(猪去氧胆酸和鹅去氧胆酸)Table 1 Test results of sample recovery rate of Danqiao injection (Hyodeoxycholic acid and chenodeoxycholic acid) (n=6)
2.2.6 样品含量测定 3批样品中猪去氧胆酸和鹅去氧胆酸的含量测定结果见表2。
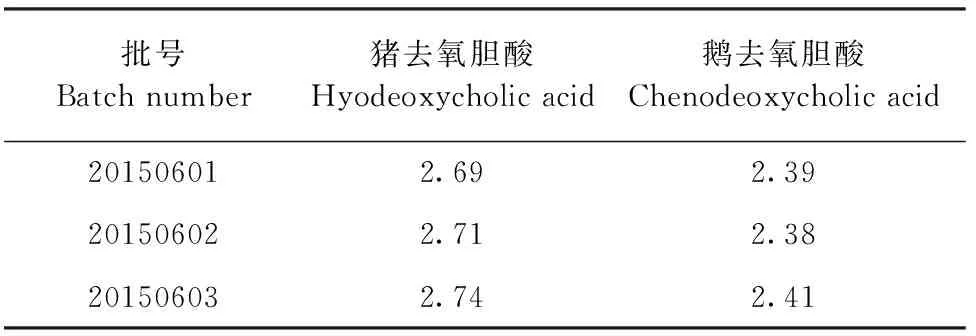
表2 样品含量测定结果(猪去氧胆酸和鹅去氧胆酸)Table 2 Determination results of sample contents(Hyodeoxycholic acid and chenodeoxycholic acid) (mg/mL,n=3)
2.3 黄芩提取物含量测定
2.3.1 方法专属性 如图5所示,黄芩苷的保留时间为7.675 min,处方中其他药味对该项定量测定无干扰,说明该方法的专属性良好。

图5 胆翘注射液的高效液相色谱分析Fig.5 HPLC analysis of Danqiao injectionA:黄芩苷对照品溶液; B:供试品溶液; C:缺黄芩提取物的阴性样品A:Control solution of baicalin; B:Test solution; C:Negative sample without scuteuaria extract
2.3.2 线性关系 以峰面积为纵坐标(y),以黄芩苷对照品浓度(mg/mL)为横坐标(x)进行回归分析,得回归方程为y=3 120 496.6x+45 046,R2=0.999 9。结果表明黄芩苷在0.075~0.375 mg/mL范围内时,与峰面积呈良好的线性关系。
2.3.3 重复性试验 测得黄芩苷的平均含量为15.70 mg/mL,RSD=0.27%,表明该方法的重复性良好。
2.3.4 稳定性试验 测得黄芩苷的平均峰面积为5 434 367.14,RSD=1.28%,表明供试品溶液在室温下24 h内稳定。
2.3.5 回收率试验 如表3所示,加样回收率试验测得黄芩苷的平均回收率为101.71%,RSD=1.00%(n=6),表明该方法用于胆翘注射液中黄芩苷含量测定的准确度良好。

表3 胆翘注射液的加样回收率试验结果(黄芩苷)Table 3 Test results of sample recovery rate of Danqao injection (Baicalin) (n=6)
2.3.6 样品含量检测 3批样品中黄芩苷的含量测定结果见表4。

表4 样品含量测定结果(黄芩苷)Table 4 Determination results of sample contents (Baicalin) (mg/mL,n=3)
3 讨论
3.1 关于胆膏、黄芩提取物和连翘提取物的薄层鉴别 TLC在中药质量控制中具有直观、显著的优势,可同时分离多种样品,固定相和流动相的选择与变换灵活大,操作简单,分离速度快[16-17]。本试验参照《中国药典》(2015年版一部)[18]收载的药材猪胆粉质量标准中的薄层鉴别方法、《中国兽药典》(2015年版二部)[15]收载的黄芩提取物质量标准中的薄层鉴别方法、《中国兽药典》(2015年版二部)[15]收载的连翘提取物质量标准中的薄层鉴别方法,进行三批中试生产胆翘注射液中胆膏、黄芩提取物、连翘提取物的薄层鉴别,结果各个TLC色谱图背景清晰,分离效果好,阴性样品无干扰,易判断,具备专属性,符合薄层色谱系统适用性检验。结果表明该项定性鉴别方法对供试品的处理及展开系统的选择是合理的,可作为胆翘注射液中胆膏、黄芩提取物和连翘提取物的鉴别方法。
3.2 关于胆膏与黄芩提取物的高效液相色谱条件的确定 HPLC具有压力高、速度快、效率高、灵敏度高等特征,特别是在对高沸点、受热后性能不稳定或是分子量较大的中药样品进行测定和分析时有独特的优势[18-19]。由于猪去氧胆酸、鹅去氧胆酸属甾体类化合物,仅在紫外末端有弱的吸收,不适合用紫外检测器检测,因此本试验选用蒸发光检测器进行检测[20]。本文参照《中国药典》(2015年版一部)[21]
收载的藿胆片质量标准中胆酸及相关文献[20]的含量测定方法,并经过多次重复试验,筛选、优化、验证,最终确定胆翘注射液中胆膏含量测定的色谱条件。对黄芩苷对照品溶液进行紫外扫描(扫描范围190~400 nm),结果表明,黄芩苷在274 nm处有明显的强吸收,因此本试验选用274 nm作为检测波长,其他色谱条件参照《中国兽药典》(2015年版二部)[15]收载的银黄提取物注射液黄芩提取物含量测定方法,进行多次筛选、验证,最终确定胆翘注射液中黄芩提取物含量测定的色谱条件。试验结果显示,所建立的定量分析方法简便、快速、专属性强、重现性和准确度好,可作为胆翘注射液中指标成分猪去氧胆酸、鹅去氧胆酸及黄芩苷的含量测定方法。

