去甲万古霉素临床药理学的研究综述
胡佳丽, 范亚新, 郭蓓宁, 张 菁
去甲万古霉素(norvancomycin)原名国产万古霉素,是由华北制药1968年自主研制并投入生产的糖肽类抗生素,由放线菌发酵而来。1986年,原卫生部药品生物制品检定所在检定过程中发现去甲万古霉素的效价比国际标准品万古霉素高约10%,通过质子-核磁共振波谱分析技术进一步测定,发现其化学结构仅比万古霉素在N-56位末端氨基上少一个甲基,为N-去甲基万古霉素 ,并正式命名为去甲万古霉素[1]。去甲万古霉素化学结构与万古霉素相似,其抗菌谱、抗菌活性亦与万古霉素相仿,特别是对耐甲氧西林葡萄球菌(MRS)的抗菌活性尤为显著。与万古霉素一样,去甲万古霉素具耳、肾毒性,且治疗窗窄、治疗指数低,在临床应用时建议进行治疗药物监测(TDM)。目前国内外已有大量万古霉素临床应用专家共识及文献资料支持其合理应用[2-3],但缺乏去甲万古霉素的相关文献汇总。本文就去甲万古霉素的药动学(PK)、药效学(PD)、临床疗效、不良反应、TDM等作一综述,以更好地为临床合理使用该药物提供参考。
1 临床前研究
1.1 作用机制
去甲万古霉素可抑制细菌细胞壁合成,主要直接与细胞壁的肽聚糖前体五肽侧链末端D-丙胺酰-D-丙氨酸结合,由于其烷基较万古霉素短,因此与细胞壁的亲和力略强,抗菌活性也略强[4]。去甲万古霉素还具有一定抑制细菌RNA 合成和损伤细菌细胞膜的作用,属于快速杀菌药物,具有良好的抗菌活性。
1.2 体外PD
郭燕等[5]采用琼脂稀释法测定去甲万古霉素对3 011株临床分离菌的体外抗菌活性,结果显示该药物对葡萄球菌属、链球菌属、肠球菌属等临床常见的革兰阳性球菌均有高度的抗菌活性,包括甲氧西林耐药金黄色葡萄球菌(MRSA)、青霉素耐药肺炎链球菌(PRSP)等多重耐药菌株,抗菌活性与万古霉素、替考拉宁、利奈唑胺相仿,显著优于其他受试抗菌药物。除33株对万古霉素耐药的肠球菌亦对去甲万古霉素耐药外,未见其他去甲万古霉素耐药株。见表1(因去甲万古霉素暂无药敏折点,因此无法计算敏感率和耐药率)。虽然该研究显示去甲万古霉素的MIC90值与万古霉素基本一致,但去甲万古霉素1 mg/L可抑制92.1%无乳链球菌生长,显著优于万古霉素的14.0%;0.5 mg/L的去甲万古霉素可抑制74.5%MRSA或84.6%甲氧西林敏感金黄色葡萄球菌(MSSA)生长,而相同浓度的万古霉素仅能抑制38.6%MRSA或49.1%MSSA生长;去甲万古霉素的累计敏感百分率高于万古霉素,均提示去甲万古霉素的抗菌活性可能比万古霉素略强。李仲兴等[6]测定了去甲万古霉素对202株凝固酶阴性葡萄球菌的MIC,结果显示去甲万古霉素对里昂葡萄球菌、溶血葡萄球菌、表皮葡萄球菌等抗菌活性较好,MIC90值均为4 mg/L,敏感率达100%,与万古霉素相仿。另有研究表明去甲万古霉素及其衍生物对艰难梭菌具有良好抗菌活性,不低于甲硝唑和万古霉素[7]。
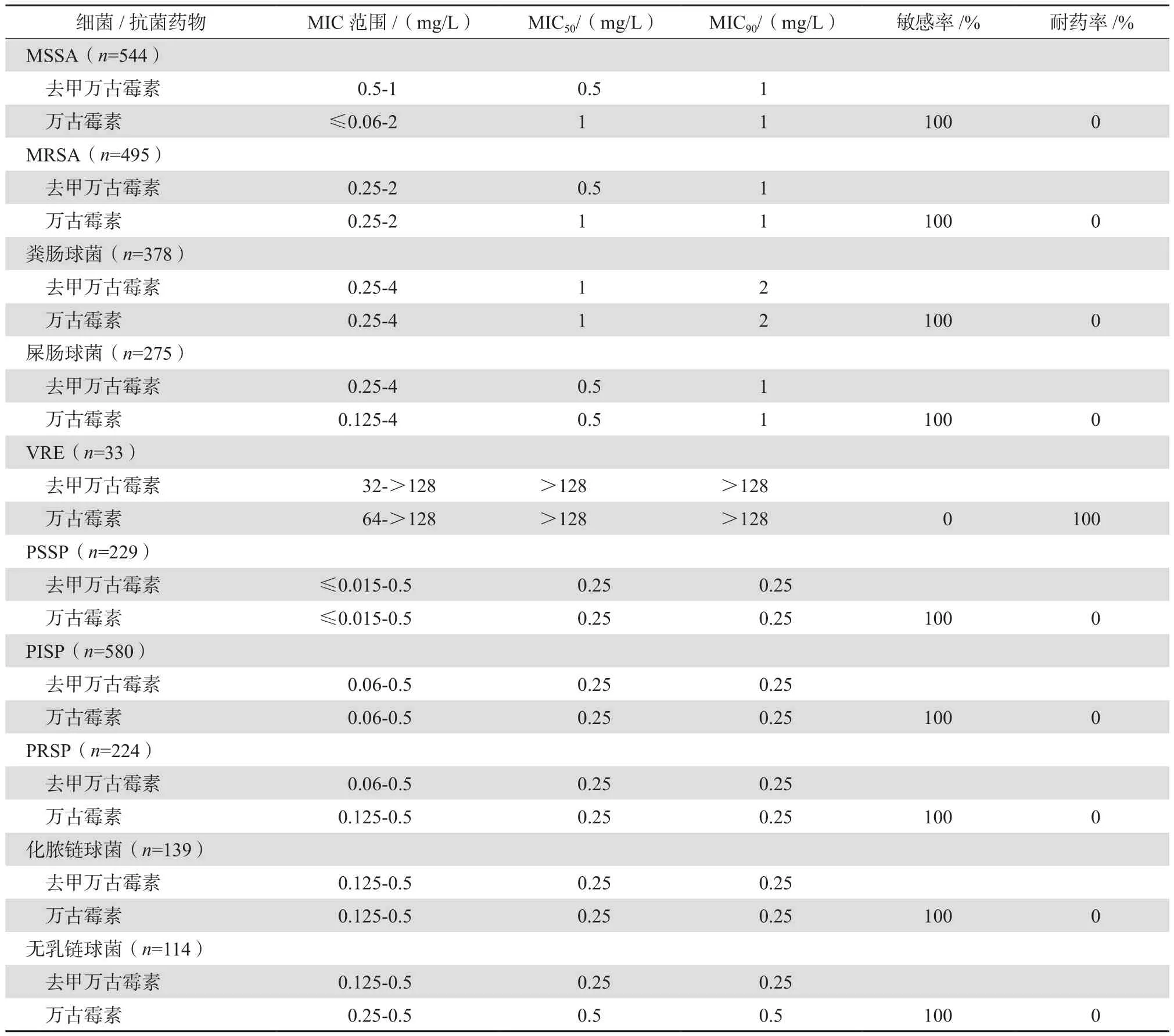
表1 去甲万古霉素与万古霉素对主要革兰阳性菌的药敏结果
目前,去甲万古霉素并未在国外上市使用,因此美国临床和实验室标准化协会(CLSI)、欧洲共同体药敏试验委员会(EUCAST)并无该药的药敏折点。但该药物已在国内上市应用五十余年,随着多重耐药革兰阳性菌的种类和数量仍在迅速增加,万古霉素的药敏结果并不能简单地代表去甲万古霉素,因此需要去甲万古霉素相关的药敏折点以供参考。Yang等[8]对国内4个城市的5所实验室收集的1 199株临床分离葡萄球菌(金黄色葡萄球菌、表皮葡萄球菌、溶血葡萄球菌和人葡萄球菌)进行去甲万古霉素的流行病学折点(epidemiological cutoff, ECOFF)研究。采用标准的肉汤微量稀释法测定去甲万古霉素的MIC值,结果显示所有菌株对去甲万古霉素的MIC均在0.12~2 mg/L。去甲万古霉素对表皮葡萄球菌和溶血葡萄球菌的流行病学折点为2 mg/L,对金黄色葡萄球菌和人葡萄球菌的流行病学折点为1 mg/L,低于EUCAST中万古霉素的药敏折点,可能显示去甲万古霉素具有更佳的抗菌效果。同时由于与肉汤微量稀释法结果的相关性较低,纸片扩散法的抑菌圈直径不适用于药敏折点的制定。临床分离株耐药基因检测结果显示甲氧西林耐药相关的mecA基因在葡萄球菌中的检出率为63.1%,未检出携带mecC、vanA、vanB、vanC、vanD和vanE基因的菌株。去甲万古霉素的流行病学折点与mecA基因无明显相关性。该折点的制定对临床鉴别野生株,合理使用该药有一定的指导意义。
1.3 药物安全性
临床前动物毒理实验结果表明去甲万古霉素具有良好的毒理安全性。高文元等[9]以万古霉素作为对照,对260只豚鼠分组,分别采用缓慢静脉推注去甲万古霉素的高(216 mg/kg)、中(108 mg/kg)、低剂量(54 mg/kg),1次/d,连续 14 d的慢性耳毒性实验。研究结果显示在去甲万古霉素4~16倍的临床剂量给药下,去甲万古霉素对前庭功能行为正常,对耳蜗功能未形成即时或延时性的听力损害,耳蜗内外毛细胞的缺失率在正常范围内,耳蜗形态学未见病理改变。去甲万古霉素和万古霉素的耳毒性相似,基本无耳毒性。
冯怡[10]研究去甲万古霉素对24只Beagle犬的长期毒性试验,分为高(162→108 mg/kg)、中(54 mg/kg)、低剂量(27 mg/kg)三个剂量组,静脉滴注,1次/d,每周给药6 d,连续给药6周,停药后观察4周,探索去甲万古霉素毒性反应的靶器官及其损害的可逆性。该实验所用剂量分别为临床剂量的1~2、2~4、6~12倍,结果表明该药毒性反应最主要的靶器官为肾脏,胃肠道变化为肾损伤引起的继发性反应,这与万古霉素的主要毒性反应为肾毒性的文献报道较为一致[11-12]。低剂量组未见明显肾毒性反应,仅见少量肾脏线粒体嵴减少、断裂;中、高剂量组的线粒体嵴减少、断裂或肿胀,部分基质变空,停药后有自行恢复的趋势。进一步研究发现,去甲万古霉素可致体外培养的人肾小管上皮细胞株的细胞形态异常和增殖抑制。
1.4 组织分布
去甲万古霉素分布于各组织。Zhou等[13]建立了一种灵敏、简便的毛细管电泳电化学方法,研究去甲万古霉素在24只大鼠体内的组织分布,结果显示去甲万古霉素在大鼠体内消除半衰期为42.4742 min, 清 除 率 为 0.0233 mL·kg-1·min-1。 通过测定,去甲万古霉素可分布于肾、肺、胃、肠、脾、心、肝和大脑,浓度依次由高到低。该药在肾脏中浓度最高,可能和该药的肾毒性发生率高有关;而在脑中药物浓度最低,表明该药不易透过血脑屏障。但有研究表明,当感染脑膜炎时,会增加去甲万古霉素的血脑屏障透过率[14]。段宪武等[15]在PRSP致脑膜炎的兔模型中,静脉注射不同剂量的去甲万古霉素,结果显示脑膜炎较非脑膜炎组峰浓度高出约3倍(2.66对0.62 mg/L),且去甲万古霉素在脑膜炎中脑脊液透过率与万古霉素相似,为19.6%。
2 临床研究
2.1 PK
去甲万古霉素标准品效价比进口万古霉素高出10%。成人每日0.8~1.6 g(80万~160万U),分2~3次缓慢静脉滴注;小儿每日按体重16~24 mg/kg(1.6万~2.4万U/kg),分2次静脉滴注,每次静脉滴注时间宜在1 h以上。去甲万古霉素口服几乎不吸收,肌内注射有刺激性,也不宜静脉推注。现有报道鞘内注射去甲万古霉素是治疗颅内感染的重要手段[16]。去甲万古霉素单剂静脉滴注400 mg结束即达到血药峰浓度25.18 mg/L,8 h平均血药浓度为1.90 mg/L,有效血药浓度可维持6~8 h,24 h尿中平均总排泄率为81.1%。去甲万古霉素单剂静脉滴注800 mg,血药峰浓度平均为50.07 mg/L,24 h尿中平均总排泄率为85.9%。该药物除脑组织外可广泛分布于身体各种组织体液,80%以上经肾脏排泄[17]。
不同肾功能、不同年龄患者去甲万古霉素PK参数差别很大。肾功能减退轻、中、重度患者的平均药物清除率分别为(4.01±1.27)、(2.17±0.95)、(0.23±0.09)L/h,平均消除半衰期为(9.57±4.34)、(22.86±20.73)、(154.26±74.28)h, 清 除 率 明 显减慢[18];不同年龄患者的去甲万古霉素PK参数亦有不同,老年与非老年感染者的清除率分别为(3.49±1.73)、(5.89±2.08)L/h,AUC24平均值分别为490.16、283.92 mg·h/L,平均药物清除率分别为12.07、6.79 L/h,老年患者药物清除率明显降低,AUC24明显增大[17]。患者不同的肝功能对去甲万古霉素PK参数无明显影响。
2.2 PK/PD特性
万古霉素为时间依赖性且抗生素后效应长的药物,PK/PD指数主要为AUC24/MIC,当AUC24/MIC≥400时可取得满意的临床疗效和细菌学疗效,国内有研究沿用该指数进行去甲万古霉素的给药方案探索[19]。但去甲万古霉素的用药方案与万古霉素并不完全一致,特别是剂量,万古霉素的PK/PD指数并不代表去甲万古霉素的指数,张菁[18]对去甲万古霉素群体PK/PD进行了研究,PK/PD指数为AUC24/MIC,而%T>MIC与临床疗效和细菌学疗效之间关系不明显;当去甲万古霉素治疗葡萄球菌和肠球菌感染患者达到95%以上治愈率时,去甲万古霉素对葡萄球菌的PK/PD指数为AUC24/MIC>579.90、对肠球菌的PK/PD指数为AUC24/MIC>637.67。吴干斌等[20]以此研究结果为基础,以去甲万古霉素对肠球菌的PK/PD指数AUC24/MIC≥638 为靶值,利用蒙特卡罗软件进行模拟,得到相应的目标达标概率(PTA) 和累积反应分数(CFR),筛选不同肾功能患者的最佳给药方案。不同的疾病和研究设计可能导致不同的结果,Wang等[21]对90例静脉滴注去甲万古霉素(经验初始给药方案为 16~24 mg·kg-1·d-1,分2次给药,之后根据临床情况调整用量)的血液恶性肿瘤患儿进行PK/PD分析,主要以MRSA感染为主,因不同阳性菌感染,混杂因素较多,得出其PK/PD指数为AUC24/MIC≥221.06,并提出MIC 1 mg/L为去甲万古霉素的流行病学折点。
2.3 临床疗效及不良反应
去甲万古霉素临床适应证与万古霉素相似[22],主要适用于耐药革兰阳性菌(MRSA、MRCNS、PRSP等)所致的呼吸系统感染、中枢神经系统感染、血流感染、骨关节感染、感染性心内膜炎、皮肤及软组织等严重感染,也可用于青霉素过敏者或经青霉素类或头孢菌素类抗生素治疗无效的严重革兰阳性菌感染患者。同时口服去甲万古霉素(0.4 g,4次/d)也可有效治疗艰难梭菌所致假膜性肠炎[23]。多项研究显示与万古霉素治疗阳性菌感染相比,两者的临床有效率、细菌清除率相当,不良反应发生率相近,且无统计学意义[24-28]。见表2。但由于去甲万古霉素标准品的效价比进口万古霉素效价高出10%,因此同等剂量的去甲万古霉素作用强度较强, 0.4 g去甲万古霉素约相当于0.5 g万古霉素,两药临床应用时给药方案不尽相同。相比于去甲万古霉素,万古霉素通常每天总剂量2 g,给药方式可分为1 g,1次/12 h或者600 mg ,1次/6 h静脉滴注给药;儿童、婴儿每天40 mg/kg,分2~4次静脉滴注,新生儿每次给药剂量 10~15 mg/kg,2~3次;万古霉素还对老年人的临床应用作了特殊说明,老年人一般0.5 g,1次/12 h或1 g,1次/d;当患者处于不同肾功能损害时,万古霉素的给药调整方案也不尽一致,具体可参考第48版《热病》中的治疗指南。
去甲万古霉素是治疗革兰阳性球菌感染的较安全的国产抗生素。自2001年进行工艺改进,去甲万古霉素的纯度达到95%以上,所导致的皮疹,耳、肾毒性发生率大大降低。见表2。刘晓东等[29]报道去甲万古霉素不良反应发生时间最早为首次用药后5 min,最迟发生时间为连续用药后第22天,与万古霉素相似。刘杨等[30]对965例静脉滴注去甲万古霉素的住院患者进行临床和实验室安全性评价,不良反应发生率为8.29%。肾功能损害占4.04%,常在用药后1周内出现,表现为血肌酐和尿素氮升高,仅有2例表现为急性肾功能衰竭,可能与去甲万古霉素使用有关;肝功能损害占2.38%,多为轻中度、可耐受;过敏反应占1.76%,主要表现为皮疹,常见于用药1周左右后;消化道反应占0.83%,主要表现为轻度恶心、纳差、腹胀等。偶见听力减退(2例)、周围血象白细胞降低(2例)、静脉炎(1例)。另有一项北京20家医院、前瞻性的去甲万古霉素临床试验安全性评价[31],结果基本与刘杨等[30]报道相似。且有研究提示[29]若静脉滴注速度过快可能引起红人综合征(1.9%)、呼吸困难、低血压等,因此输注时间应>1 h。
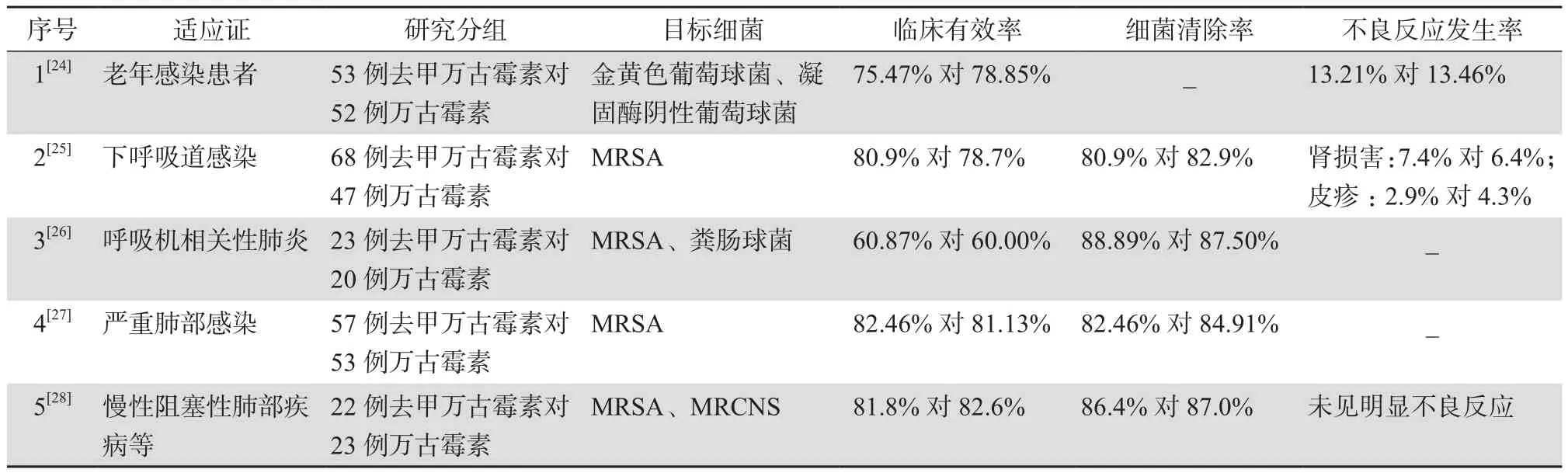
表2 去甲万古霉素与万古霉素的临床疗效及不良反应比较
2.4 特殊人群
去甲万古霉素因其耳、肾毒性,在特殊人群中使用可能需要调整给药剂量。由于该药主要是通过肾脏清除,因此不同肾功能状态患者应采用不同的给药方案。张菁等[32]对诊断或拟诊为革兰阳性菌感染的146例患者的PK/PD分析显示患者内生肌酐清除率的变化对去甲万古霉素清除率会有一定影响,不同肾功能状态减退患者可根据肌酐清除率调整给药方案,见表3。
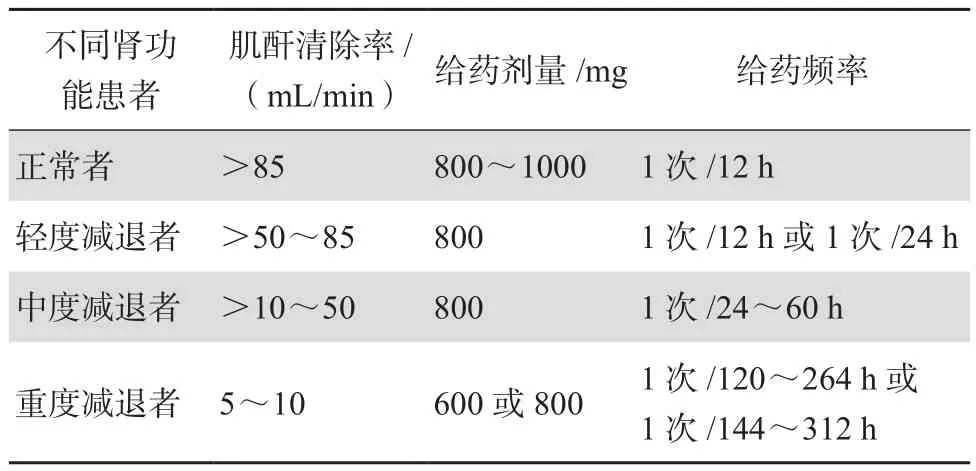
表3 不同肾功能状态患者去甲万古霉素给药方案推荐
张菁等[33]报道两组健康受试者静脉滴注去甲万古霉素800 mg后的体内PK过程符合二室模型,老年与年轻受试者相比,AUC增加,消除半衰期延长,表观分布容积增大,总清除率及肾清除率降低,上述差异可能主要因老年人肾脏血流量减少,肌酐清除率降低,易致药物在体内积蓄。侯沐欣等[24]对105例老年感染患者比较了使用去甲万古霉素与万古霉素肾毒性的差异,结果显示去甲万古霉素组患者尿素氮、肌酐水平均短暂升高,两药均对患者的肾功能有一定影响,但停药后即恢复,不良反应均较轻且差异无统计学意义。另有研究显示老年人群的肾脏毒性较年轻人发生率明显升高[34]。但老年人应用去甲万古霉素大多数是安全的,建议老年感染患者在应用去甲万古霉素时,即使肾功能测定在正常范围内,也应适当减少药物剂量或延长给药间隔,同时也可监测某些预测早期肾损害的指标[35]、听力变化,进行TDM。
去甲万古霉素是儿科治疗革兰阳性菌严重感染的重要抗生素。王俊等[36]将49例使用去甲万古霉素的患儿按体质量中位数校正,将成人去甲万古霉素群体药动学(PPK)模型外推得到儿童模型,通过拟合优度图、可视化预测检验及正态化预测分布误差验证外推模型的稳定性和预测性能,模型结果显示说明书中的小儿给药方案中剂量可能偏低。当去甲万古霉素用于治疗不同MIC值(0.25、0.5、0.75、1 mg/L)的细菌感染时,要使PTA达到90%以上,对葡萄球菌属的日剂量应分别为16、32、48、>48 mg/kg,治疗肠球菌属感染的日剂量应分别为16、24、32、40 mg/kg。
2.5 TDM
去甲万古霉素个体差异较大,治疗窗较窄。临床实践中建议对去甲万古霉素进行TDM,对于患者预后、病原菌清除、减少不良反应都有重要意义,特别是对肾功能减退、老年人、新生儿等特殊群体患者,或者大剂量且长疗程的重症患者,或者合用其他耳肾毒性药物的患者[37-40]。也有研究表明有必要对神经外科术后患者的血清和脑脊液同时进行TDM[41]。
去甲万古霉素TDM采样时机,临床一直参考万古霉素指南[2]。具体的TDM判断标准也是沿用万古霉素,之前国内万古霉素TDM的谷浓度参考区间为5~10 mg/L,但在2009年之后美国传染病学(IDSA)在万古霉素应用指南和2011年MRSA治疗指南中提出,血药谷浓度临床上应控制在10 mg/L以上,对于复杂性感染,血药谷浓度应达到15~20 mg/L。但由于大量成人和儿童重症感染患者谷浓度达15~20 mg/L,增加了肾毒性发生的报道,因此2020年国际指南更新修订了万古霉素给药和监测内容,推荐万古霉素治疗严重MRSA感染时,AUC/MIC应维持在400~600,以达到临床疗效并保证患者安全性[3]。2020年国内更新版万古霉素专家共识[42]推荐监测谷浓度或AUC;24推荐成人患者的稳态谷浓度维持在10~15 mg/L;建议儿童患者或新生儿的稳态谷浓度维持在5~15 mg/L;对于严重MRSA感染的成人患者,建议万古霉素稳态谷浓度维持在10~20 mg/L;建议AUC24维持在400~650 mg·h/L。由于去甲万古霉的PK/PD指数与万古霉素不尽相同,还需大量临床试验来探究其合理的TDM指标及参数。
3 总结与展望
近年来,医院感染中革兰阳性菌仍以金黄色葡萄球菌、肠球菌、肺炎链球菌等常见,细菌耐药问题越来越严重,多重耐药菌传播的形势日益严峻,近期CHINET研究报道除三级医院检出极少数万古霉素耐药肠球菌外,其他均未发现万古霉素耐药革兰阳性菌株[43-45],去甲万古霉素和万古霉素依然是治疗革兰阳性菌感染的“最后一道防线”。且去甲万古霉素更具有成本-效果优势,在取得良好疗效的同时可更加合理使用卫生医疗资源,减轻患者负担,挽救患者生命[46]。

