芹菜素丝素蛋白纳米粒的制备及其安全性、抗肿瘤活性研究
季鹏 张进香 王祥龙 葛健文 黄海琴

摘 要 目的 制备芹菜素丝素蛋白(API@SF)纳米粒,并评价其安全性和抗肿瘤活性。方法 采用纳米沉淀法制备API@SF纳米粒,并对其形态、粒径、Zeta电位、载药量、体外释放等進行表征;采用溶血实验和HE染色法评价该纳米粒的安全性;采用MTT法评价该纳米粒对小鼠乳腺癌4T1细胞的抑制作用。结果 本研究所制得的API@SF纳米粒呈类球形,粒径分布均匀,平均粒径为406.61 nm,多分散性指数为0.154,Zeta电位为-18.4 mV,平均载药量为5.20%。体外释放结果显示,该纳米粒在pH 5.0的释放介质中释放速率相对较快,在pH 7.4的释放介质中释放速率相对较慢。溶血实验和HE染色结果显示,该纳米粒具有良好的生物相容性。MTT实验结果显示,API@SF纳米粒对4T1细胞的抑制作用显著高于API原料药(P<0.05),其作用机制可能与提高细胞中活性氧水平有关。结论 本研究成功制备了API@SF纳米粒,该纳米粒具有良好的安全性和抗肿瘤活性。
关键词 芹菜素;丝素蛋白;纳米粒;制备;安全性;抗肿瘤活性
中图分类号 R944 文献标志码 A 文章编号 1001-0408(2022)01-0058-06
DOI 10.6039/j.issn.1001-0408.2022.01.10
ABSTRACT OBJECTIVE To prepare apigenin silk fibroin (API@SF) nanoparticles and to evaluate their safety and anti-tumor activity. METHODS API@SF nanoparticles were prepared by nanoprecipitation method, and their morphology, particle size, Zeta potential, drug loading amount and in vitro release were characterized. The safety of nanoparticles was evaluated by hemolysis test and HE staining. MTT assay was adopted to evaluate inhibitory effects of API@SF nanoparticles on breast cancer 4T1 cells in mice. RESULTS The prepared API@SF nanoparticles were spherical with uniform distribution. The average particle size was 406.61 nm, the polydispersity index was 0.154, the Zeta potential was -18.4 mV, and the average drug-loading amount was 5.20%. The in vitro release results showed that the release rate of the nanoparticles was relatively fast in the release medium of pH 5.0 and relatively slow in the release medium of pH 7.4. Results of hemolysis test and HE staining showed that the nanoparticles had good biocompatibility. Results of MTT assay showed that the inhibitory effect of API@SF nanoparticles on 4T1 cells was significantly higher than that of API raw materials (P<0.05), and its mechanism may be related to increasing the level of reactive oxygen species in cells. CONCLUSIONS API@SF nanoparticles are prepared successfully, which possess good safety and anti-tumor activity.
KEYWORDS apigenin; silk fibroin; nanoparticles; preparation; safety; anti-tumor activity
癌症作为一种长期困扰人类的恶疾,其致死率仅次于心血管类疾病;且由于肿瘤细胞具有强大的代谢补偿和侵袭转移能力,导致在其治疗过程中会频繁复发并累及多个器官,严重降低了患者的生活质量[1]。目前,临床治疗癌症以手术切除、化疗和放疗为主,其中作为非侵入性治疗的化疗方式已被广泛应用,可有效地抑制癌细胞的生长和转移[2]。虽然现有化疗药物效果较强,但生物相容性较差,在杀灭肿瘤细胞的同时也会给正常器官带来损伤[3]。因此,开发更多低毒高效的化疗药物迫在眉睫。
芹菜素(apigenin,API)别名芹黄素,是一种黄酮类化合物,具有抗炎、抗氧化、抗菌和抗肿瘤等多种药理活性[4-5]。API已被证明对多种肿瘤细胞均具有显著的抑制作用,其作用机制可能与抑制肿瘤细胞迁移或侵袭、促进细胞周期阻滞、诱导细胞凋亡以及干扰肿瘤细胞信号通路有关[6]。由于API的水溶性较差,对肿瘤细胞缺乏选择性,且其半衰期短、生物利用度相对较低,极大地限制了其进一步临床应用[7]。因此,有必要改善API的溶解性和生物利用度,以获得更好的抗肿瘤效果。
丝素蛋白(silk fibroin,SF)作为一种天然高分子生物材料,具有良好的生物相容性、降解性和可再生性;当其作为药物载体时,可增强药物的控释性、减少药物的副作用和用药次数[8]。基于此,本研究制备芹菜素丝素蛋白(API@SF)纳米粒,并评价其安全性和抗肿瘤活性,以期为该纳米粒的临床应用提供实验依据。
1 材料
1.1 主要仪器
本研究所用主要仪器有UV-1200型紫外可见分光光度计[尤尼柯(上海)仪器有限公司]、FA2004型万分之一电子天平(瑞士Mettler-Toledo公司)、pHS-3C型pH计(上海仪电科学仪器股份有限公司)、KQ-500DB型数控超声仪(昆山市超声仪器有限公司)、1510-02820C型酶标仪(美国Thermo Fisher Scientific公司)、JEM-F200型透射电子显微镜(日本Jeol公司)、CKX53型倒置荧光显微镜(日本Olympus公司)、Mastersizer-2000型粒度分析仪(英国Malvern公司)。
1.2 主要药品与试剂
溴化锂(LiBr)、API对照品、二甲基亚砜(dimethyl sulfoxide,DMSO)(批号分别为C12143081、A800499、20191228,纯度均大于98.0%)均购自上海麦克林生化科技有限公司;API原料药(批号Le031663875,纯度99.22%)购自上海皓鸿生物医药科技有限公司;磷酸二氢钾(KH2PO4,批号20200818)购自中国医药集团有限公司;无水磷酸氢二钠(Na2HPO4,批号20181207)购自上海沪试化工有限公司;无水碳酸钠(Na2CO3,批号20210401)购自无锡市亚盛化工有限公司;桑蚕丝素(批号180301)购自湖州新天丝生物科技有限公司;MTT试剂(批号20201105)购自美国Sigma公司;2,7-二氯二氢荧光素二乙酸酯(2,7-dichlorodihydrofluorescein diacetate,DCFH-DA,批号20210505)购自上海碧云天生物技术有限公司;其余试剂为实验室常用规格,水为去离子水。
1.3 动物
本研究所用动物为BALB/c小鼠,雌性,体质量18~24 g,购自上海市计划生育科学研究所,动物生产许可证号为SCXK(沪)2018-0006。小鼠饲养于温度22~25 ℃、相对湿度50%的环境中,期间自由饮食。
1.4 细胞
本研究所用小鼠乳腺癌4T1细胞购自中国科学院上海生科院细胞资源中心。
2 方法与结果
2.1 SF的制备
参考文献[9]方法,将0.02 mol/L Na2CO3溶液加热煮沸后,加入桑蚕丝素1 g,继续煮沸30 min,以60 ℃水洗涤3次,然后置于60 ℃烘箱中烘干过夜,即得丝素纤维;将丝素纤维溶于9.3 mol/L LiBr溶液中,置于60 ℃烘箱中烘干2 h;将上述溶液转移至截留分子量为14 000 Da的透析袋中透析12 h,每隔4 h更换1次水,即得SF溶液;将SF溶液置于60 ℃烘箱中烘干过夜,即得SF。
2.2 API@SF纳米粒的制备
采用纳米沉淀法进行制备。称取SF适量,以水制成质量浓度为1 mg/mL的SF溶液;将一定量API加入2 mol/L pH 8.0的磷酸盐缓冲液(phosphate buffer solution,PBS)中溶解,再加入5倍体积的SF溶液,混合均匀,于4 ℃条件下静置4 h后,置于40 ℃水浴条件下磁力搅拌12 h;以12 000 r/min离心3 min,弃上清液,即得API@SF纳米粒。
2.3 API的含量测定
采用紫外可见分光光度法测定API的含量[7]。
2.3.1 溶液制备 精确称取API对照品适量,置于10 mL量瓶中,加入30%乙醇-DMSO混合溶液(9 ∶ 1,V/V,下同),超声(频率40 kHz,功率200 W,下同)溶解并稀释成质量浓度为250 μg/mL的API贮备液。另取“2.2”项下的API@SF纳米粒适量,置于10 mL量瓶中,加入30%乙醇-DMSO混合溶液2 mL,超声溶解并定容,以0.45 μm微孔滤膜滤过,即得供试品溶液(API质量浓度为250 μg/mL)。
2.3.2 标准曲线绘制 精密量取“2.3.1”项下API贮备液适量,以30%乙醇-DMSO混合溶液逐级稀释,即得API质量浓度分别为50、40、30、20、10、5 μg/mL的系列溶液;以30%乙醇-DMSO混合溶液为空白,采用紫外可见分光光度计于342 nm波长处测定吸光度。以吸光度(y)为纵坐标、API质量浓度(x,μg/mL)为横坐标进行线性回归,得到回归方程y=0.021 8x+0.009 0(R2=0.999 2),表明API的检测质量浓度在5~50 μg/mL范围内线性关系良好。
2.3.3 方法学考察 (1)精密度试验:取“2.3.1”项下API贮备液适量,以30%乙醇-DMSO混合溶液制成API低、中、高质量浓度(10、20、30 μg/mL)溶液,采用紫外可见分光光度计于342 nm波长处测定吸光度,以考察日内精密度。结果显示,API低、中、高质量浓度溶液吸光度的日内RSD分别为1.41%、0.70%、0.55%(n=6),均小于2%,表明该方法精密度良好。(2)稳定性试验:取供试品溶液适量,于室温下放置0、2、4、8、12、24 h后,采用紫外可见分光光度计于342 nm波长处测定吸光度,以考察稳定性。结果显示,吸光度的RSD為1.17%(n=6),表明供试品溶液在室温下放置24 h内稳定性良好。(3)重复性试验:取“2.2”项下API@SF纳米粒,按“2.3.1”项下供试品溶液制备方法平行制备6份样品溶液,采用紫外可见分光光度计于342 nm波长处测定吸光度,以考察重复性。结果显示,吸光度的RSD为0.73%(n=6),表明该方法重复性良好。(4)加样回收率试验。取“2.3.1”项下供试品溶液100 μL,共6份,分别置于10 mL量瓶中,均加入“2.3.1”项下API贮备液100 μL,以30%乙醇-DMSO混合溶液定容,制成供试品溶液,采用紫外可见分光光度计于342 nm波长处测定吸光度并计算加样回收率。结果显示,平均加样回收率为98.78%(RSD=1.39%,n=6),表明该方法准确度良好。
2.4 API@SF纳米粒的表征
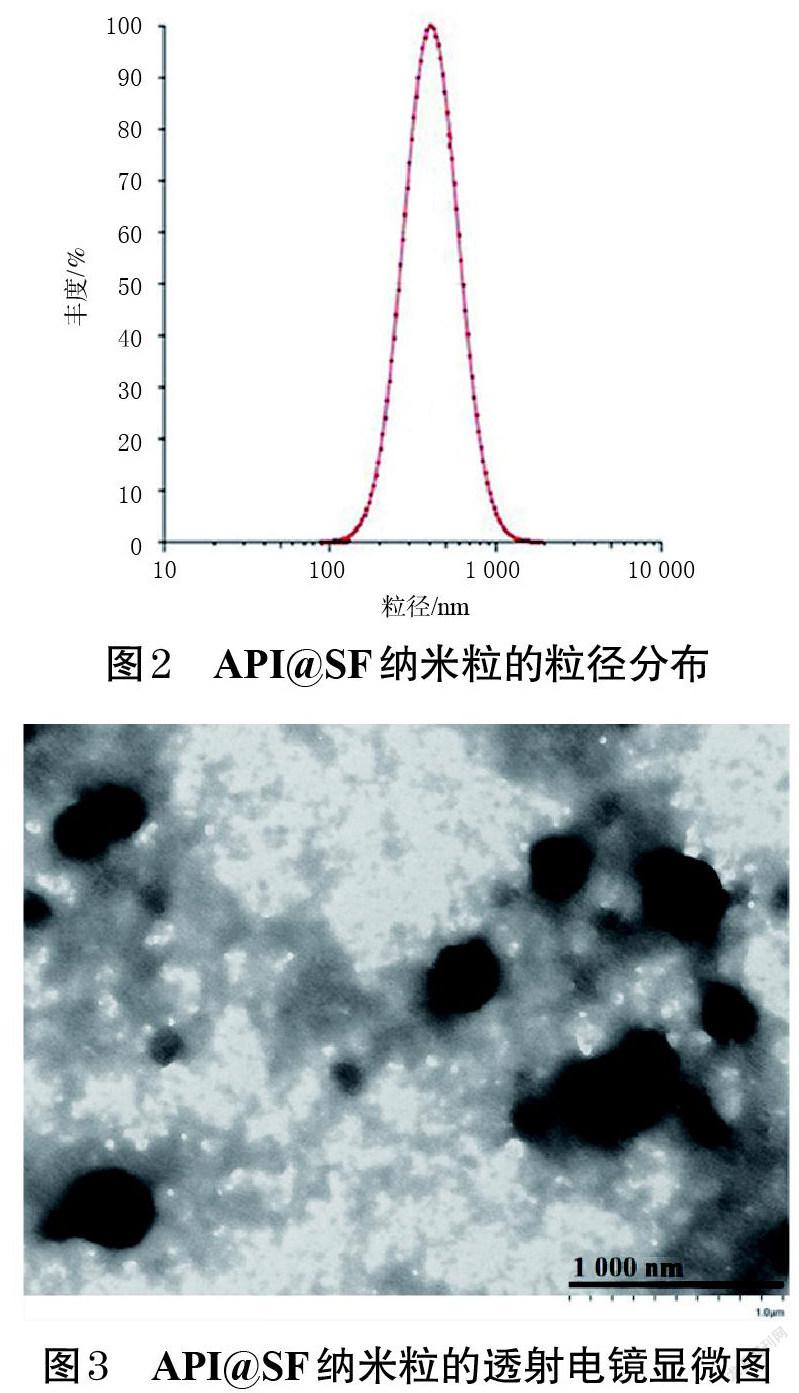
2.4.1 形态、粒径及电位的考察 分别取API贮备液、SF溶液和API@SF纳米粒适量,置于西林瓶中,观察其外观颜色。取API@SF纳米粒适量,以水稀释后,采用粒度分析仪测定其粒径、Zeta电位及多分散性指数(polydispersity index,PDI)。另外,将上述稀释后的API@SF纳米粒混悬液滴在铜网上,以1%磷钨酸溶液染色60 s,用滤纸吸除多余染色液,于室温条件下自然干燥后,采用透射电镜进行观察。结果显示,本研究所制备的API@SF纳米粒为淡黄色混悬液,呈单分散状态,且无明显沉淀;其粒径分布均匀,呈正态分布,平均粒径约为406.61 nm,PDI为0.154,Zeta电位为-18.4 mV;透射电镜观察发现,该纳米粒呈类球形。结果见图1、图2、图3。
2.4.2 API@SF纳米粒载药量的测定 精确称取API@SF纳米粒2.1 mg,共3份,加入30%乙醇-DMSO混合溶液5.2 mL,超声使其充分溶解后,以0.45 μm微孔滤膜滤过;取续滤液,采用紫外可见分光光度计于342 nm波长处测定其吸光度,根据标准曲线计算API的含量,并计算API@SF纳米粒的载药量[载药量(%)=We/Wm×100%,式中We表示包封于该纳米粒中的药量,Wm表示该纳米粒的总质量)。结果显示,3份API@SF纳米粒的载药量分别为5.24%、5.19%、5.18%,平均载药量为5.20%(RSD=0.68%,n=3)。
2.5 API@SF納米粒的体外释放考察
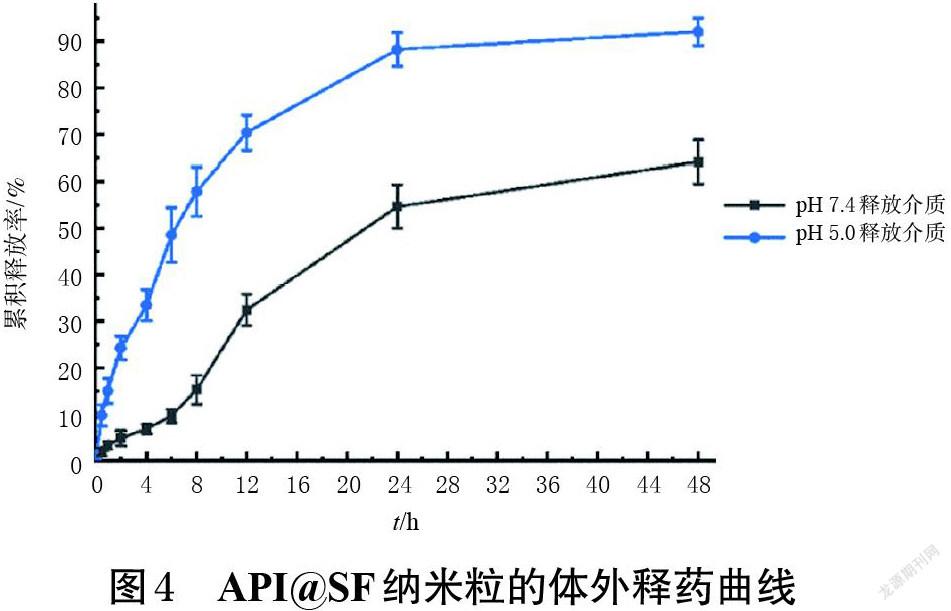
参考文献[7,10]方法,以含20%乙醇的PBS (pH分别为5.0、7.4)为释放介质,将API@SF纳米粒置于截留分子量为14 000 Da的透析袋中,然后浸入上述不同释放介质(180 mL)中,并于37 ℃条件下以100 r/min的搅拌速率进行释放实验。在预定的时间点(0、0.5、1、2、4、6、8、12、24、48 h)取样4 mL(同时补充4 mL释放介质),以0.45 μm微孔滤膜滤过;将滤液以30%乙醇-DMSO混合溶液适当稀释后,采用紫外可见分光光度计于342 nm波长处测定吸光度,计算API的累积释放率,并绘制该纳米粒的体外释药曲线,结果见图4。由图4可知,在pH 5.0的释放介质中,该纳米粒释放API的速率相对较快,在48 h时的累积释放率约为90%;而在pH 7.4的释放介质中,该纳米粒释放API的速率相对较慢,在48 h时的累积释放率约为60%。
2.6 API@SF纳米粒的安全性评价
2.6.1 溶血实验 参考文献[11]方法,将BALB/c小鼠适应性喂养1周后,摘眼球取血;将血样置于盛有玻璃珠的锥形瓶中,振摇10 min,以除去纤维蛋白原获得血细胞。将所得血细胞以氯化钠注射液清洗,然后以3 500 r/min离心10 min,弃去上清液,重复清洗、离心操作,直至上清液不显红色为止,即得红细胞。将所得红细胞加入氯化钠注射液制成2%的混悬液,置于4 ℃冰箱中冷藏备用。取上述红细胞混悬液分为阴性对照组(氯化钠注射液)、阳性对照组(纯化水)和不同浓度API@SF纳米粒组(以API计,质量浓度分别为0.05、0.075、0.1、0.15、0.2、0.4、0.6 mg/mL),每组设3个平行样品。各组样品分别加入相应药物2 mL,于37 ℃孵育30 min后,以3 500 r/min离心10 min;取上清液,采用紫外可见分光光度计于540 nm波长处测定其吸光度,并计算溶血率[溶血率(%)=(各给药组吸光度-阴性对照组吸光度)/(阳性对照组吸光度-阴性对照组吸光度)×100%][12]。结果显示,API@SF纳米粒在API质量浓度0.05~0.6 mg/mL范围内,其溶血率均低于5%,表明API@SF纳米粒与血液的相容性较好,详见图5。
2.6.2 心肌毒性实验 由于化疗药物普遍存在心肌毒性[13],因此,本研究也考察API@SF纳米粒的心脏毒性。取BALB/c小鼠3只,尾静脉注射API@SF纳米粒(以API计,20 mg/kg,剂量根据文献[14-15]设置),每2天给药1次,连续10 d。第11天时,处死小鼠,摘除心脏,剥取心肌组织,置于4%多聚甲醛溶液中固定,经70%、80%、90%、95%乙醇和无水乙醇梯度脱水,再以二甲苯透明替换、浸蜡、包埋、切片(厚度约5 μm),经HE染色后置于显微镜下观察小鼠心肌组织的病理形态学变化。结果显示,在小鼠心肌组织中未观察到炎症损伤,表明API@SF纳米粒没有心肌毒性,详见图6。
2.7 API@SF纳米粒抗肿瘤活性考察
2.7.1 API@SF纳米粒对4T1细胞的抑制作用 采用MTT法进行考察。将4T1细胞以含有10%胎牛血清的RPMI 1640培养基(以下简称“培养基”)于37 ℃、5% CO2的条件下培养,当细胞融合度达80%~90%时进行实验。取上述细胞,调整密度为5 000 mL-1,接种于96孔板中,每孔100 μL,培养过夜。将细胞随机分为空白对照组、API原料药不同质量浓度组(5、10、20、30、40、50 μg/mL,以API计,质量浓度根据前期预实验设置)和API@SF纳米粒不同质量浓度组(5、10、20、30、40、50 μg/mL,以API计,质量浓度根据前期预实验设置),每组设3个复孔。空白对照组加入培养基100 μL,其余各组加入相应含药培养基100 μL,培养24 h后,弃去上清液,加入5 mg/mL MTT溶液10 μL,继续孵育4 h;弃去MTT溶液,以PBS洗涤2次,加入DMSO 100 μL,振荡10 min,使结晶充分溶解。采用酶标仪于490 nm波长处测定各孔的光密度(optical density,OD)值,并计算细胞存活率[细胞存活率(%)=OD给药组/OD空白对照组×100%]。采用SPSS 21.0软件进行统计分析,数据均以x±s表示,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验,检验水准α=0.05。结果显示,与空白对照组比较,API原料药不同质量浓度组和API@SF纳米粒不同质量浓度组细胞存活率均显著降低(P<0.05),且呈明显的浓度依赖趋势;与同质量浓度的API原料药组比较,API@SF纳米粒组细胞存活率均显著降低(P<0.05)。结果见表1。
2.7.2 API@SF纳米粒对4T1细胞中活性氧水平的影响 参考文献[16]方法进行考察。将4T1细胞调整密度为2 × 104 mL-1,接种于24孔板中,每孔0.5 mL,培养过夜。将细胞随机分为空白对照组、API原料药组(25 μg/mL,以API计,质量浓度根据前期预实验设置)、API@SF纳米粒组(25 μg/mL,以API计,质量浓度根据前期预实验设置),每组设3个复孔。空白对照组加入培养基0.5 mL,其余各组加入相应含药培养基0.5 mL,培养24 h后,弃去上清液,以PBS洗涤2次,加入10 μmol/L DCFH-DA溶液250 μL,继续培养30 min;吸弃染色工作液,以PBS洗涤3次,采用荧光显微镜进行观察并拍摄荧光图像,使用Image J 1.48v软件分析荧光强度,来表示活性氧(reactive oxygen species,ROS)水平。结果显示,与空白对照组(荧光强度为0)比较,API原料药组(荧光强度为3.45±1.33)、API@SF纳米粒组(荧光强度为5.58±2.00)细胞中ROS水平均显著升高(P<0.05);与API原料药组比较,API@SF纳米粒组细胞中ROS水平显著升高(P<0.05)。结果见图7。
3 讨论
API是一種天然黄酮类化合物,具有抗癌潜力,但因其水溶性差、细胞摄取率低、生物利用度低,从而限制了其在临床上的应用[7]。基于生物材料载体开发纳米递药系统是药剂学研究热点之一,将药物封装在纳米载体中可增强渗透和保留效应,增加肿瘤组织内的药物积累,提高药物的生物利用度和治疗效果[17]。源自家蚕的SF是一种天然高分子生物材料,具有独特的生物特性,如两亲性、无毒性、生物相容性和降解性,因此其在药物载体相关研究中具有巨大潜力[18]。目前已经有部分天然化合物(如紫杉醇、姜黄素、柚皮素、五羟黄酮、白藜芦醇)被包载于SF纳米载体中,且与这些游离药物相比,被SF纳米粒包载后的药物具有更强的抗氧化和抗肿瘤活性[17]。
本研究基于SF载体,构建了API@SF纳米粒,该纳米粒粒径分布均匀,呈正态分布,平均粒径为406.61 mm,平均载药量为5.20%,Zeta电位为-18.4 mV。其中,Zeta电位是胶体分散稳定性的关键决定因素,表示相邻类似带电粒子之间的静电排斥程度,当其绝对值大于15时,表明该粒子的稳定性良好[19-20]。由此可知,本研究所制得的API@SF纳米粒稳定性良好。进一步经体外释放考察发现,API@SF纳米粒的释放具有pH依赖性,且在酸性环境中可迅速释放药物,这提示该纳米粒在酸性肿瘤微环境中可快速释药,进而发挥抗肿瘤活性。
经安全性评价发现,本研究所制得的API@SF纳米粒与血液具有较好的相容性,且无心肌毒性,提示该纳米粒具有良好的安全性和临床应用价值。基于此,笔者探讨了其对小鼠乳腺癌4T1细胞的抑制作用,结果显示,将API包载于SF中可增强API对4T1细胞的体外抑制作用,提示API@SF纳米粒具有良好的抗肿瘤作用。ROS是一种含有氧自由基的高活性化学物质,已被证明与癌症的发展、转移、进展有关[21]。高浓度的ROS具有细胞毒性,可损伤细胞中的DNA、蛋白质等,从而促使肿瘤细胞凋亡,抑制肿瘤生长[22]。本研究结果显示,相比于API原料药,API@SF纳米粒可在4T1细胞内产生更高水平的ROS,从而增强API的抗肿瘤活性。
综上所述,本研究成功制备了API@SF纳米粒,该纳米粒具有良好的安全性和抗肿瘤活性。后续笔者将从动物水平深入探讨该纳米粒的药动学和药效学。
参考文献
[ 1 ] 马晓星,李永吉,朱文全,等.小檗碱联合化疗药物的协同抗肿瘤作用及其共递送纳米载体的研究进展[J].中国药房,2021,32(17):2171-2176.
[ 2 ] HUSSAIN Z,KHAN S,IMRAN M,et al. PEGylation:a promising strategy to overcome challenges to cancer-targeted nanomedicines:a review of challenges to clinical transition and promising resolution[J]. Drug Deliv Transl Res,2019,9(3):721-734.
[ 3 ] ZHONG Y Y,LI X S,CHEN J H,et al. Recent advances in MOF-based nanoplatforms generating reactive species for chemodynamic therapy[J]. Dalton Trans,2020,49(32):11045-11058.
[ 4 ] 李进霞,王佳,康明丽,等.芹菜素γ-环糊精包合物的表征和抗氧化活性研究[J].现代药物与临床,2020,35(4):647-651.
[ 5 ] 徐世一,吕畅,霍元子,等.芹菜素纳米混悬剂在小鼠体内的组织分布研究[J].中国药房,2020,31(4):457-463.
[ 6 ] 徐世一,吕畅,李雪莹,等.芹菜素纳米混悬剂对肝癌HepG2细胞体内外抗肿瘤药效学研究[J].辽宁中医药大学学报,2020,22(10):40-44.
[ 7 ] ZHAO T,HE Y,CHEN H L,et al. Novel apigenin-loaded sodium hyaluronate nano-assemblies for targeting tumor cells[J]. Carbohydr Polym,2017,177:415-423.

