探索次氯酸钠在存储使用过程中出现沉积物的原因
何晓欣(东莞市水务集团供水有限公司,广东 东莞 523112)
0 引言
次氯酸钠(NaClO)溶液是澄清的微黄色液体,与水反应生成次氯酸(HClO)和氢氧化钠(NaOH)[1-2]。生成的次氯酸具有强氧化性,能杀灭细菌、病原体等微生物[1],氢氧化钠能有效调节水中pH[3]。此外,次氯酸钠还具有采购易得、管控方便、成本低等特点,且进行水体消毒中生成的消毒副产物比使用氯气消毒产生的消毒副产物含量更低[2],大大降低了对人体的危害性。因此,次氯酸钠常被运用于污水厂、自来水厂的水体消毒。然而由原使用氯气消毒经改造后用次氯酸钠消毒的自来水厂在存储使用过程中发现次氯酸钠能产生沉淀并堵塞管道。为进一步保障水厂能顺利安全生产,本研究主要探索次氯酸钠出现沉积物的原因,旨在对改善生产提供指导。
1 自来水厂使用次氯酸钠的状况
南方某供水公司拥有7家自来水厂,原使用液氯进行消毒工艺处理,出于安全性考虑自2017年始对各家水厂陆续进行改造,采用浓度为10%的液体次氯酸钠替代液氯进行消毒。运行几年后发现每个自来水厂储存次氯酸钠溶液灌的出口管、输送管等地方均发现有沉淀结晶等现象,并有不同程度的堵塞状况。取出部分沉积物用浓硝酸浸泡仅能部分溶解。通过酸洗、冲管等方法能暂时疏通部分管道保证设备的正常使用,但很快会再次出现堵塞问题,而且堵塞次数越来越频繁。图1是供水公司其中5家自来水厂出现的次氯酸钠沉淀图片。

图1 5家自来水厂的次氯酸钠沉淀
2 次氯酸钠生产工艺流程和相关指标
南方某供水公司向某生产厂家所采购的次氯酸钠是通过原盐提纯后进行电解,电解产物一部分通过蒸发得到氢氧化钠,一部分通过氯氢化作用生成氯气。冷却的氢氧化钠经过与水合理配比后再与氯气混合反应生成符合国家标准浓度要求的次氯酸钠成品,具体工艺流程如图2所示。其化学反应式为[4]:
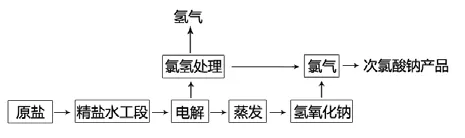
图2 次氯酸钠生产工艺
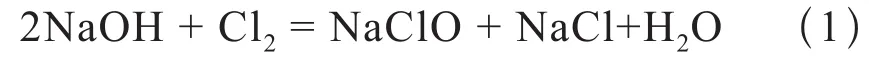
采购回来的次氯酸钠澄清、微黄色、无杂质,密度为1.15~1.24 g/cm3,检测有效氯浓度(以Cl计)为10.7%±0.24%,游离碱(以NaOH计)为0.1%~1.0%,铁<0.000 2%,重 金 属( 以 Pb计 )<0.001%,砷<0.000 1%,所有指标均符合GB/T 19106—2013《次氯酸钠》表1要求,具体信息如表1所示。

表1 次氯酸钠国家标准与合同标准
3 试验材料
总硬度标准样品(环境保护部标准样品研究所)标准值2.00±0.07 mmol/L,采用生活饮用水标准检验方法(GB/T 5750.4—2006 )7.1的乙二胺四乙酸二钠滴定法测得204 mg/L(以CaCO3计),即原液浓度为5 104.6 mg/L;生产厂家送货后马上进行试验,次氯酸钠验收的有效氯浓度(以Cl计)为10.48%;实验室专用超纯水机(重庆利迪LD-75G-E(RR除盐型));烧杯;白色容量瓶;密封避光箱。
4 试验方法
由于缺乏定量衡量沉淀含量的试验条件,因此采用观察法和描述法。控制不同的因素变量,每隔一段时间观察液体产生沉淀的变化情况,用0~5级表述沉淀出现的多少,0为没有出现沉淀,5为相比较而言出现最多沉淀的量。0~1级再细分5个描述等级,采用微量、极少量、少量、较多、非常多进行描述。
5 试验结果
5.1 钙镁离子的影响
自来水中会存在少量Ca2+、Mg2+,而且Ca2+、Mg2+与次氯酸钠接触后能与空气中的CO2和水反应产生沉淀,其化学式如下:

取4个100 mL烧杯分别装入50 mL次氯酸钠,分别加入0 mL、0.5 mL、1.0 mL、1.5 mL总硬度标准样品原液,放置于桌面。其观察结果如图3所示,记录结果如表2所示。
结合表2和图3,未添加Ca2+、Mg2+的烧杯中始终未发现沉淀,添加总硬度后的次氯酸钠随着时间变化沉淀慢慢形成,沉淀大块易聚集,并且添加总硬度浓度越大出现沉淀的时间越早,最终产生的沉淀也越多。这说明Ca2+、Mg2+的存在能影响沉淀的产生,在未存在Ca2+、Mg2+或 Ca2+、Mg2+含量极少时,次氯酸钠的稳定性能更加持久,但随着Ca2+、Mg2+含量越多,次氯酸钠稳定性越差。

图3 含不同浓度Ca2+、Mg2+的次氯酸钠沉淀
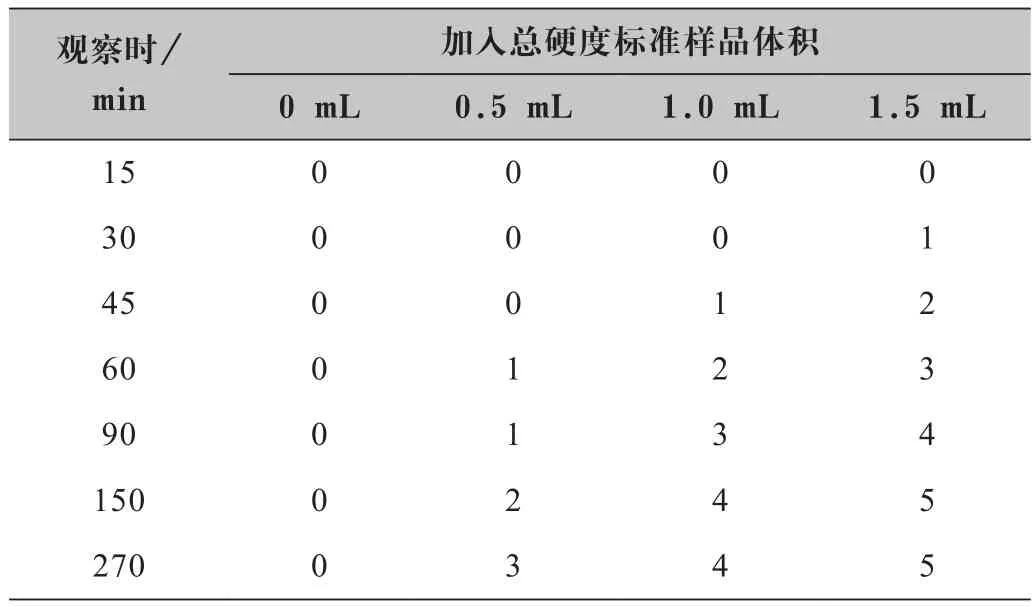
表2 次氯酸钠产生沉淀与钙镁离子的关系
5.2 光照的影响
次氯酸钠稳定性十分差,遇光容易分解,其反应式为[5]:

按照上述5.1试验步骤,改变放置环境,将烧杯放置于密封避光箱中,其结果如表3和图4。
结合表2、表3和图4结果,未添加Ca2+、Mg2+的烧杯中始终未发现沉淀。同时,随着Ca2+、Mg2+浓度的提高,产生沉淀的速度和含量大小也与5.1结论一致。但添加不同总硬度浓度的次氯酸钠溶液中在避光条件下生成沉淀速度均明显降低,光照条件下60 min观察结果与在避光条件下150 min的观察结果类似。说明光照是加快次氯酸钠沉淀产生的一个十分重要的因素,光能迅速破解次氯酸钠的稳定性。

图4 光照对次氯酸钠沉淀的影响
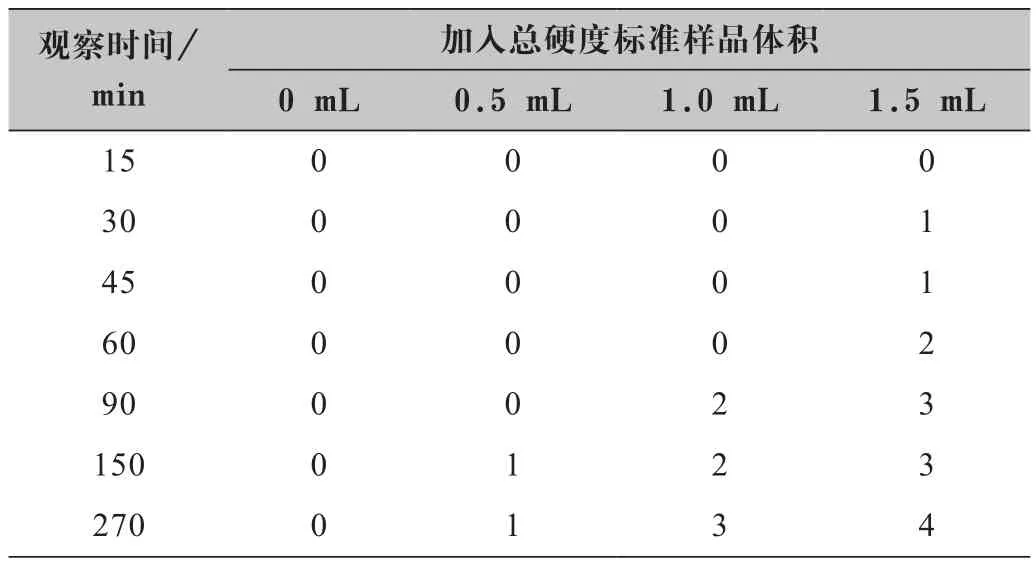
表3 避光下次氯酸钠产生沉淀与钙镁离子的关系
5.3 密封性的影响
由于避光条件产生沉淀时间较长,因此探索密封性的影响采取透光形式。取4个50 mL白色容量瓶,分别加入0 mL、0.5 mL、1.0 mL、1.5 mL总硬度标准样品原液,用次氯酸钠定容至50 mL,放置在与5.1相同操作的环境中,其结果见表4。
试验结果并未出现5.1与5.2较大凝聚团的沉淀,只形成了微小颗粒沉淀,液体的清亮度受到了影响。从表4的结果中得出,次氯酸钠形成的沉淀较慢,不同总硬度浓度的容量瓶中形成沉淀所需时间比避光的还长。究其原因,容量瓶瓶颈窄,与空气接触面减少,空气流动性减弱。氧气或者反应的接触面比光照因素更加强烈。
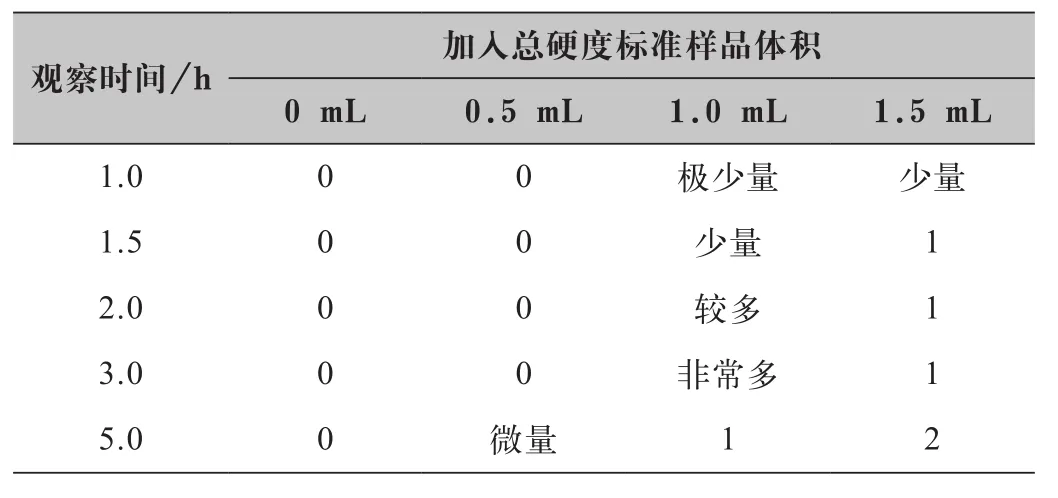
表4 密封性对次氯酸钠产生沉淀的影响
5.4 不同次氯酸钠浓度与稀释水质的影响
取4个烧杯依次装入10 mL、20 mL、30 mL、50 mL次氯酸钠,用超纯水加至50 mL。同时另一组用自来水代替超纯水同时进行对比。每个烧杯加入0.5 mL总硬度标准样品。其结果如表5、表6和图5。
从图5观察和表5、表6描述看,次氯酸钠浓度较稀的(10+40、20+30)更容易产生沉淀,但随着时间增长,产生沉淀最多的不在浓度稀的次氯酸钠上,也不在浓度最高的次氯酸钠上,而是在30+20的稀释浓度上。在稀释情况下,其产生的沉淀量随着稀释倍数降低而增加。未经稀释过的次氯酸钠产生沉淀的速度和沉淀含量均比稀释了的低。对比超纯水与自来水稀释结果,用自来水稀释所产生的沉淀速度比超纯水稀释的迅速,其产生的含量也较多。说明自来水中存在的物质能促导沉淀形成。若生产时配比氢氧化钠浓度采用的是自来水,会降低次氯酸钠保存期。
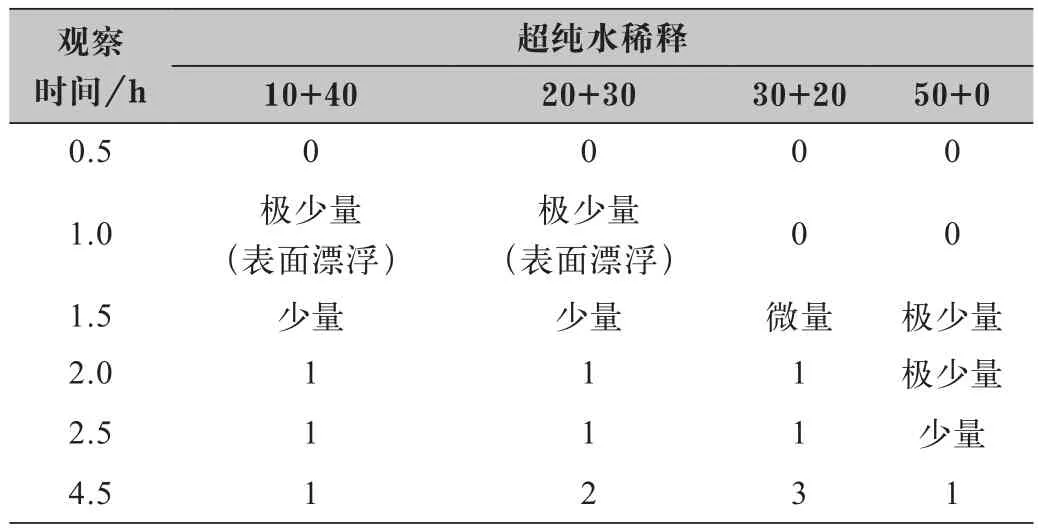
表5 次氯酸钠浓度(超纯水稀释)对产生沉淀的影响
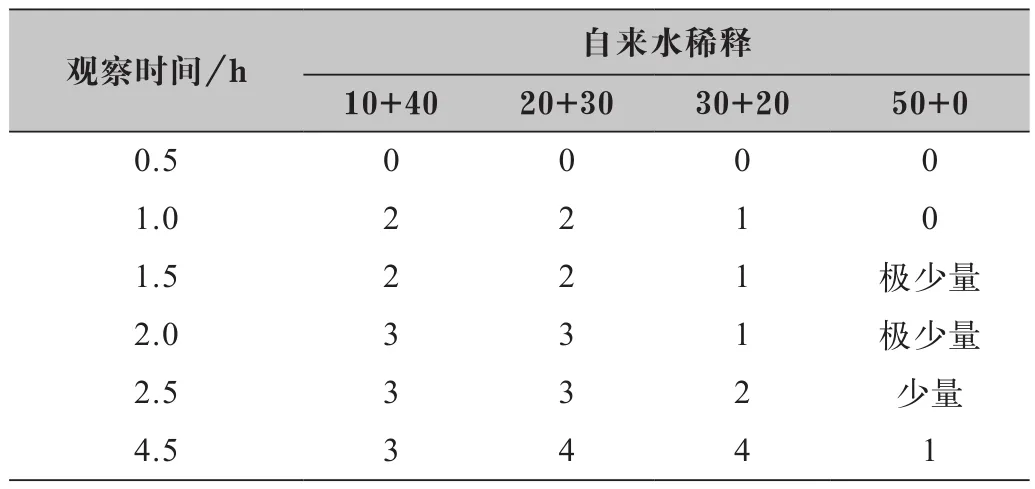
表6 次氯酸钠浓度(自来水稀释)对产生沉淀的影响

图5 不同次氯酸钠浓度与稀释水质的对比
6 结语
(1)次氯酸钠在存储使用过程中出现沉淀不是偶然,与本身生产工艺、浓度含量、水中杂质、保存条件密切相关。
(2)钙镁离子的存在能促使次氯酸钠产生沉淀,并且产生的沉淀量与钙镁离子的含量有关。
(3)光照条件下能加速次氯酸钠与钙镁离子的沉淀反应。
(4)减少次氯酸钠与空气的接触,加强密封性可以使次氯酸钠在有钙镁离子的条件下更加稳定,生成沉淀速度减慢。要使次氯酸钠减慢沉淀的形成,密封性比避光性更值得注意。
(5)次氯酸钠在超纯水中比自来水生成沉淀较慢且较少,因此生产稀释过程中最好使用纯水配溶。
(6)次氯酸钠存储最好不经稀释,以原液存放。若需要稀释使用且需要暂时存放的应注意稀释比例和尽快使用完毕。

