天然生物材料在组织工程化血管构建中的作用及研究进展
陈国宝,杨 欢,周江一,田吉迅,邓雅心
(重庆理工大学 药学与生物工程学院, 重庆 400054)
如今,心血管疾病成为发达国家中主要的死亡原因之一[1],中国的心血管疾病患病率也是常年居高不下。据统计推算表明,中国现存心血管疾病人数已达到3.3亿人,每5例死亡人数中有2例死于心血管病[2]。心血管疾病的高死亡率原因与其引起的一系列并发症以及不良反应有关,表现在感染病毒风险的提高以及意外事故,如剧烈运动而导致猝死的机率增大[3]。心血管糖积聚导致的动脉粥样硬化则是主要的心血管疾病之一[4],除了通过施加药物改善血管内膜血栓的凝结的状况外,血管的修复与置换也成为当今流行的解决方案。
目前,针对心血管疾病的主要治疗策略是对外周动脉瘤进行插管处理,对颈动脉进行支架搭桥手术处理,从而改善局部动脉血管的堵塞情况[5],而搭桥支架手术的关键在于血管创伤处的组织血管化建立。其中用于搭桥的支架生物相容性就成为关键点。异种血管移植的方法无论是在短期的相容性或者长期的力学性能上都不能满足天然血管的要求[6]。同样,通过人工合成的高分子聚合物以及金属支架也无法有效地解决血管支架降解和相容性问题,而通过组织工程学原理构建的含有天然生物材料的复合支架为解决这一难题提供了可能。
组织工程学是通过将细胞生物学和材料学相结合,从而开发出恢复、修护、改善组织功能的生物替代物的新兴学科[7]。通过这种策略制备的支架材料具有良好的自组织能力,能形成结构和功能都与天然组织相似的生物组织,使受损组织或器官重获新生。其中,天然生物材料具有良好的生物相容性、可降解性、低免疫原性以及快速诱导血管新生而展现出巨大的临床应用潜能。
目前,用于心血管支架的天然生物材料主要分为细胞外基质衍生物类生物材料、蛋白质类生物材料与多糖类生物材料等。其中,蛋白质类生物材料包括胶原、丝素蛋白、角蛋白等,多糖类生物材料包括壳聚糖、纤维素、海藻酸盐等。不同类别的天然组织在力学性能、化学性能和生物学性能等方面均存在较大的差异,如何利用各类天然生物材料的特性研制出优良的支架材料成为组织工程的关键。
本文综述了近几年天然生物材料在血管组织工程中的研究进展,包括对各类生物材料的特点与优势、局限性及应用等进行了总结与讨论,并展望了天然生物材料在血管组织工程的应用前景。
1 脱细胞血管基质来源类生物材料
组织工程中血管网络的构建需要经历漫长的时间,目前已经出现了许多模仿天然细胞外基质(extracellular matrix,ECM)结构和成分的方法以促进血管生成。但内皮细胞很难从合成的ECM中出芽形成新的血管。脱细胞基质是将来源于各种物种的组织/器官通过物理、化学、酶等方法进行细胞分离并消除免疫原后保留得到的细胞外基质。脱细胞基质不仅能为细胞提供结构支持,还能提供各种生化信号,从而促进细胞黏附、增殖和分化等[8]。由于不同基质的结构和组成各不相同,来源于不同组织/器官中的脱细胞基质具有诱导向特定组织重塑的潜力[9]。因此,脱细胞血管以及脱细胞血管基质复合支架已成为促进血管再生的理想材料,如图1所示。
1.1 脱细胞血管
脱细胞血管具有与天然血管相似的顺应性,以承受血压的变化,并且包含了大量促血管生成因子,可直接作为移植物用于血管修复[10]。血管组织的力学性能很大程度上来自高度保守的ECM蛋白,Dahl等[11]制备出了在体外培养的猪主动脉脱细胞基质支架,从此开启了脱细胞血管基质支架的大门。在大直径(>8 mm)和中等直径(6~8 mm)动脉制造中,人工聚合物合成血管可作为有效的血管替代物,而在小直径(<6 mm)动脉中,人工聚合物血管替代物的通畅率较低,且较容易发生血栓或增生等现象,使其应用受到了限制[12]。相较于人工聚合物血管替代物,ECM衍生类生物材料拥有巨大优势。在结构蛋白的空间结构保留相对完整的同时[13-14],脱细胞血管基质还能提供细胞组织间的信息通讯,促进细胞黏附、增殖、迁移与分化[15]。另外,脱细胞血管基质支架可以通过调节基质中含有的胶原、弹性蛋白含量,从而改善较为欠缺的力学性能[16]。不仅如此,通过灵长类动物实验结果看出,在长达6个月的脱细胞血管基质支架移植实验后,支架的直径和长度未发生明显变化,表明脱细胞基质血管替代物拥有良好的耐用性[17]。另外,Syedain等[18]的实验表明,脱细胞血管基质支架在植入年轻受体体内后,可能具有生长的能力,在植入脱细胞血管基质支架的幼羊模型的一年随访结果中显示,最初植入的脱细胞血管支架经历了真正的躯体生长,而不是简单地机械扩张。
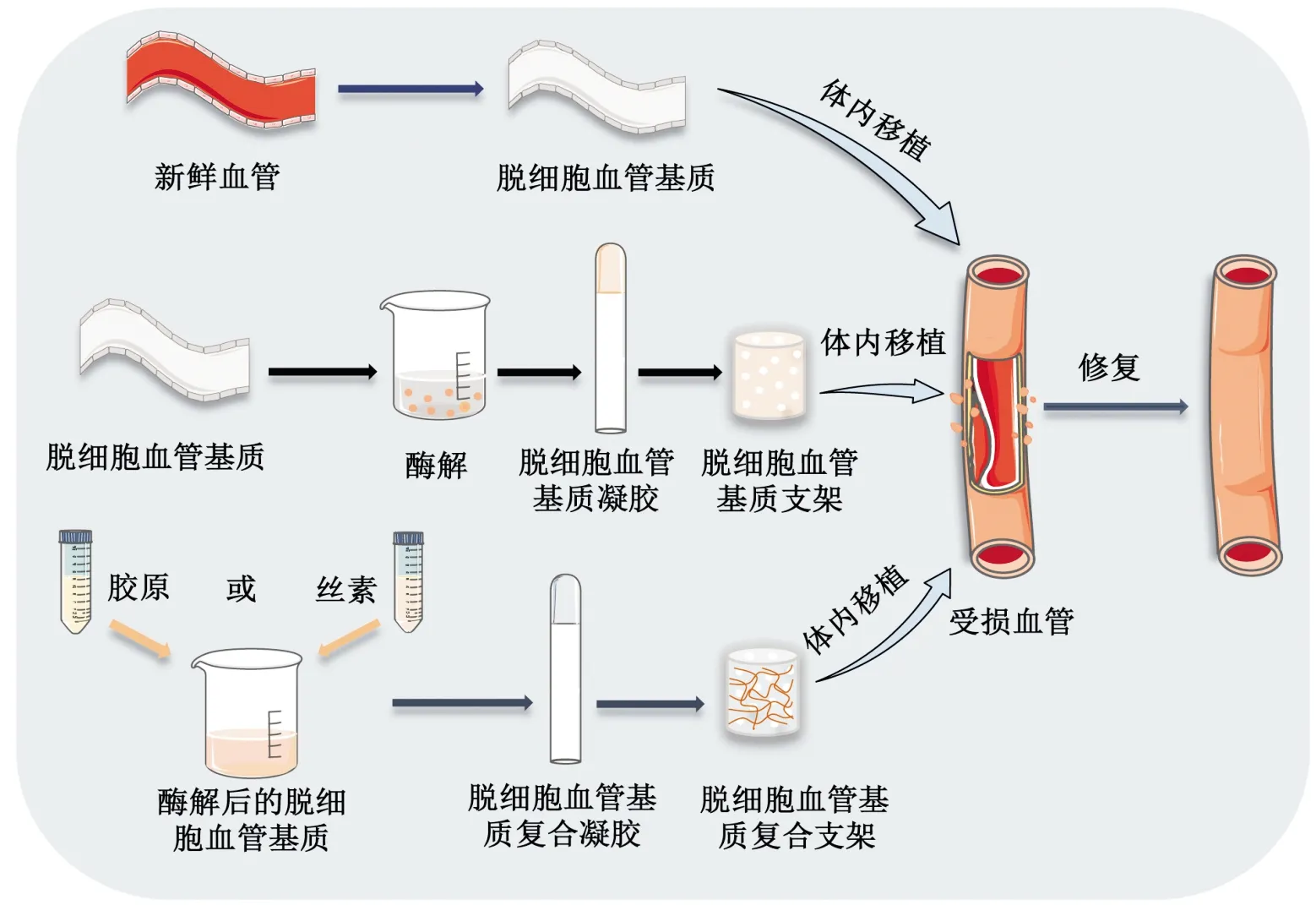
图1 用于血管组织工程的脱细胞血管基质来源类生物材料
1.2 脱细胞血管基质复合支架
脱细胞血管虽然在生物相容性及诱导血管再生方面具有天然的优势,但是仅把脱细胞血管作为移植物限制了其在临床上对不规则组织修复的应用。通过酶解的方法将脱细胞血管水解成凝胶后,不但能扩大其使用范围,而且脱细胞血管基质中促血管生成能力也得到一定程度的保留[19]。由于酶解后会对结构蛋白造成破坏,导致脱细胞血管基质凝胶的力学性能无法与组织相匹配。将其他材料与脱细胞血管基质共混成为了最简易的改善其力学性能的方式。天然高分子材料,如丝素蛋白与脱细胞血管基质凝胶共混后,制备得到的支架能有效地提高整体的力学性能。与纯丝素支架相比,共混支架在植入大鼠皮下4周后形成了极为丰富的血管网络[20]。将胶原与脱细胞血管基质共混形成凝胶,不但弥补了脱细胞血管基质中流失的胶原成分,同时改善了它的生物力学强度,并且该复合凝胶通过调节间充质干细胞的旁分泌作用加速了受损肾脏中血管网络的形成,从而诱导肾脏再生[21]。总之,脱细胞血管凝胶在组织工程血管化方面具有巨大的应用前景。
虽然高分子材料具有理想的机械强度和生物力学性能,但仍然存在与种子细胞的生物相容性不佳、降解产物会影响种子细胞的生物学特性和工程化组织的形成等关键问题[22]。相比之下,以ECM为主的脱细胞血管基质及其复合支架为种子细胞提供了超微结构的三维培养空间,提高了种子细胞的生物相容性、黏附、增殖和迁移能力,成为构建组织工程血管的理想支架材料。
2 蛋白质类生物材料
蛋白质作为生命体最重要的物质基础,广泛存在于自然界中。相比于人工合成的聚合物材料,蛋白质类生物材料具有良好的生物相容性与生物降解性等优点,所以被广泛应用于包括制备组织工程血管支架在内的各个研究领域中。目前组织工程化血管支架的制备常用的蛋白质类生物材料包括胶原、角蛋白、弹性蛋白、纤维蛋白、明胶、蛋清及丝素蛋白等,如图2所示。

图2 用于组织工程血管的蛋白质类生物材料
2.1 胶原
胶原蛋白是人体及动物ECM中一种非常重要的结构蛋白,是构成血管、皮肤和韧带等身体部分的主要组织成分。近年来,因其具有弱的抗原性、良好的生物相容性、无细胞毒性、高可降解性以及促进细胞生长等优点,所以在组织工程血管支架研究领域中应用较为广泛。
研究表明,由小肠粘膜下层获得的胶原可在体外成功参与血管支架的制作,并且在血管支架的制备过程中,利用胶原蛋白作为机械支撑,可成功克服弹性蛋白等生物材料极限拉伸强度较低的缺点[23-24]。对于胶原类血管的力学性能,Zhou等[25]进行了深入测试,利用细胞外基质成分胶原、肝素和透明质酸通过交联技术共同构建双层血管导管,对交联后的导管在干燥情况下的最大拉伸强度及最大断裂伸长率与湿态情况下平均抗拉强度与断裂伸长率进行测试记录,数据显示该双层血管导管在干燥情况下与在湿态情况下的断裂伸长率分别为84.88%、72.05%,湿态情况下的断裂伸长率仍达到真实血管的最低标准,说明该胶原类血管支架具有良好的力学性能。但胶原易导致血栓形成,所以在血管支架制备方面,其应用受到了一定的限制[26]。后续研究发现,可以在胶原支架进行体外研究实验时,对其进行有效的表面涂层或者预先植入一种具有活性的细胞,达到减少该类胶原支架在体内退化引起血管疾病及发生血栓可能性的目的[27]。
2.2 角蛋白
角蛋白是构成生皮表皮、毛皮毛囊的主要蛋白质。角蛋白生物材料具有良好的生物可降解性、生物相容性及无免疫原性,是一种有效的天然生物材料[28]。目前,角蛋白基材料常被用于制造微针、药物输送、伤口敷料以及血管支架等。角蛋白作为一种结构蛋白,含有大量的二硫化物,具有较好的机械强度和还原反应性。角蛋白中丰富的二硫键可被谷胱甘肽(Glutathione,GSH)还原成半胱氨酸残基,然后长期催化亚硝基谷胱甘肽(Nitrosoglutathione,GSNO)的内源性供体产生一氧化氮,产生的一氧化氮在加速血管重构中发挥了关键作用。有研究采用静电纺丝法制备含有角蛋白的聚己内酯(Polycaprolactone,PCL)血管支架,研究结果表明:PCL/角蛋白支架能够成功催化GSNO释放NO,可促进人脐静脉内皮细胞(human umbilical vein endothelial cells,HUVECs)增殖的同时抑制人脐动脉平滑肌细胞(human umbilical artery smooth muscle cells,HUASMCs)增殖,从而达到促进血管重构的目的[29]。此外,磺化角蛋白-PCL纳米纤维支架被证明能够促进内皮细胞的生长,同时抑制平滑肌细胞的增殖并降低血小板的黏附[30]。这一研究结果证实磺化的角蛋白能够改善角蛋白的凝血功能,进一步提高在血管组织工程中的应用前景。
2.3 弹性蛋白
弹性蛋白是弹性纤维的主要成分,其可赋予所在组织器官良好的弹力及抗张能力,且具有良好的生物相容性,在生物材料领域得到了广泛的应用。
弹性是弹性蛋白的最重要物理化学性质,在天然胶原蛋白支架中添加适当的弹性成分,能够使支架的整体性能得到改善。对脱细胞肌腱切片衍生的天然胶原支架进行研究发现,当胶原蛋白支架与不同浓度的弹性蛋白交联时,支架的弹性得到了显著改善[16]。评估不同浓度弹性蛋白对胶原蛋白支架力学性能的影响,并根据结果选择合适的弹性蛋白浓度进行进一步分析发现,在胶原蛋白支架中添加适宜浓度的弹性蛋白后,支架的延展性和杨氏模量发生明显的变化,构件在最大载荷时的杨氏模量和拉伸应力显著降低,并且在最大载荷时的拉伸应变得到一定程度上的增加。此外,研究表明,弹性蛋白也能够使血管的顺应性增强。动脉壁含有丰富的弹性蛋白,有储存弹性能量及高应变等特性,可以确保血流畅通[31]。由可溶性弹性蛋白和胶原复合制成的支架具有孔隙率和表面积,适合小直径移植物的制作。不溶性弹性蛋白的应变恢复率高于胶原蛋白。研究表明,在胶原凝胶中加入弹性蛋白可以增强内皮细胞的增殖能力,同时显著抑制动脉平滑肌细胞的增殖[19]。综上,可见弹性蛋白是一种极具潜力的、用于血管组织工程的支架材料。
2.4 纤维蛋白
纤维蛋白为凝血酶作用于纤维蛋白原而成的产物,不仅具有良好的生物相容性、生物可降解性及无毒性等优点,而且能促进血管生成与组织修复,因此被广泛应用于组织工程血管支架材料的制备[32]。
在纤维蛋白类材料血管支架的理想型探究方面,Pankajakshan等[32]釆用溶剂浇铸的方法制备出了一种新型的纤维蛋白类血管支架。将内皮细胞与该类支架材料进行复合培养,2 h后观察到内皮细胞附着于支架表面,24 h后观察到附着的内皮细胞明显扩散,15 d后,支架表面出现一层连续的内皮细胞单层,30 d时,支架上具有较大表面积内皮细胞层,此时能较为清楚地观察到内皮细胞层迁移到孔表面且细胞边界清晰,该研究说明该纤维蛋白类支架材料极有可能成为一种较为理想的人工血管支架材料。为避免血管植入体内发生异物反应,研究表明,事先由从患者血液中获得纤维蛋白从而制成支架,同时种植自体来源的细胞,可有效避免异物植入带来的排斥反应[33]。目前用于心血管组织工程中的可生物降解脚支架常表现出有毒降解和炎症反应,Ye等[34]通过把纤维蛋白凝胶作为可降解三维支架进行组织工程血管研究发现,细胞在该类支架上生长情况良好,无炎性反应且产生无毒性降解产物,进一步证实了纤维蛋白类支架材料在组织工程血管制备中的潜在可行性[26]。
但是,纤维蛋白类材料血管缺乏较好的机械性能和稳定性,其应用在一定程度上受到了限制[27]。因此,纤维蛋白支架材料如何提高机械性能及稳定性是未来的研究重点之一。
2.5 明胶
明胶是胶原变性的产物,没有固定的结构和相对分子量,属于一种大分子的亲水胶体,具有良好的生物相容性和生物可降解性,其降解产物易被吸收且不产生炎症反应,被广泛应用于临床医学研究中。
支架能否实现自身的“血管化”是组织工程血管能否成功应用于生物体内最重要的一项指标[26]。Frerich等[35]以明胶作为血管支架,以脉动灌流培养内皮细胞,16 d后,观察到内皮细胞在支架上的黏附性良好,支架内出现广泛的“毛细血管”网状结构,并且部分毛细血管样网络高度连通。此研究说明以明胶作为组织工程血管支架材料能够解决支架腔内或壁内细胞的营养及氧气供给问题。
明胶的内在机械强度较低,所以现在大多作为制备复合支架的材料,可以在明胶中加入明胶甲基丙烯酰可以增加交联度,从而提高机械性能。明胶的另一个缺点是它的溶解性,在37 ℃或以上温度条件下会以胶体溶胶的形式溶解,在较低温度下(室温)形成凝胶,这个缺点限制了它的长期移植应用。相关研究表明,用低毒的京尼平交联明胶纳米纤维垫可以显著提高其杨氏模量和断裂应力分别至990 MPa和21 MPa[36]。此外,使用血管壁间充质干细胞进行初步体外复合发现细胞在明胶支架上具有良好的细胞活力及粘附性[36]。所以,可以通过对明胶的交联增强其稳定性,进一步延长明胶的降解时间,同时达到增强明胶耐水性的目的。
2.6 蛋清
蛋清指蛋内的半透明液体,因其有天然无毒、生物相容性好、无明显炎症反应、可利用性强、成本低廉、来源丰富等特点,被广泛用于生物材料。不同蛋白有着不同的功能,如卵清蛋白在刺激细胞增殖方面具有一定优势[37],卵巨球蛋白在抑制炎症、促进细胞增殖和迁移方面具有一定的优势等[38],蛋清也是一种制备血管支架材料的可用材料[39]。
天然血管主要由内膜、中层和外膜3层构成。呈单层结构的血管不能满足组织工程血管移植物应用的要求。采用静电纺丝和同轴3D打印相结合的方法制备3层血管支架(triple-layered vascular scaffold,TVS),即聚己内酯-胶原(polycaprolactone-collagen,PCL-Col)通过静电纺丝法制备TVS的内层,使用蛋清参与TVS中间层的形成[40]。但由于蛋清很难保持其生物活性,而海藻酸钠在钙离子的催化下可以迅速形成凝胶,所以,混合是生产更完整的生物材料的有效方法之一。通过同轴3D打印和交联机制挤出蛋清/海藻酸钠(egg white/sodium alginate,EW/SA)共混水凝胶,形成中空纤维,沿圆周方向缠绕内层表面,作为TVS的中间层。最后,将静电纺丝PCL-Col纳米纤维包裹在水凝胶层表面作为TVS的外层。所制备的TVS与天然血管相比,极限拉应力、断裂应变等机械性能均与天然血管相近。此外,通过HUVECs对TVS的生物相容性进行的研究表明,细胞能够成功附着在移植物表面,并保持较高的存活率[40]。蛋清参与制备得到的新型3层血管支架具有适当的力学性能和良好的生物学性能,在组织工程血管移植中具有非常大的应用潜力。
2.7 丝素蛋白
丝素蛋白是从蚕丝中提取的一种天然高分子纤维蛋白,因其具有良好的生物相容性、稳定的化学性能及机械性能等优点,所以在组织工程中可为各种类型的细胞提供理想的支架,在血管组织工程支架的制备方面应用尤为广泛[41]。
Suzuki等[42]以家蚕和野生柞蚕的蚕茧为原料,采用脱胶法分离出丝素蛋白,测量结果表明丝素蛋白具有较强的机械力学性能。Marcolin等[43]将电纺丝素管状基质良好的生物相容性及力学性能与明胶优异的细胞相互作用特性相结合,成功制备出一种丝素类复合管状材料,对该材料进行拉伸等力学测试,结果显示所制备出的丝素类复合管状材料的柔顺性及粘弹性等机械性能均与天然血管相当,此结果证实丝素类复合管状材料可用作小口径血管支架材料。也有相关研究表明,由纯的丝素溶液进行静电纺丝得到的纤维机械强度均比原始丝的机械性能有所降低,不能达到人工血管等材料的强度要求。将丝素蛋白分别与PCL和聚二恶烷酮共混进行静电纺丝,可使得到的丝素蛋白纤维纺丝抗断强度及延展性能等有明显的改善[44-45],该研究说明将丝素蛋白与其他高聚物共纺,可以提高血管假体的机械强度。但丝素蛋白在体内的降解速度也将成为一个问题,Horan等[46]通过体外酶类实验表明丝素蛋白会在一个相对较长的时间内缓慢降解,可以为组织生成提供足够的时间,但降解速度缓慢容易导致宿主反应,这将影响丝素蛋白在血管组织工程领域的进一步发展。
3 多糖类生物材料
天然多糖类物质作为一类资源丰富、易于获得的天然高分子生物材料,因其具有优秀的生物相容性和良好的生物可降解性,且分、降解产物对人体安全无害的特性,所以在生物材料领域应用广泛,包括制备组织工程血管支架。目前组织工程化血管支架的制备常用的多糖类生物材料包括壳聚糖、细菌纤维素、海藻酸盐以及透明质酸等,如图3所示。
3.1 壳聚糖
壳聚糖又称脱乙酰甲壳素,具有优秀的生物相容性、生物降解性、无毒性与抗菌性。作为一种组织工程的支架材料,因其具有易形成多孔结构、易于修饰及体内大分子亲和力高等特点,在血管支架材料研究方面应用广泛。

图3 用于组织工程血管支架的多糖类生物材料
在制备小孔径血管方面,壳聚糖与PCL通过静电纺丝法复合制成的血管支架具有类似天然ECM微/纳米结构的多孔结构,这样的结构利于细胞的黏附及生长[47]。同时,壳聚糖也可与细菌纳米纤维素中复合,从而制成力学性能和生物相容性都有明显提升的复合血管支架[48]。在制备大孔径血管方面,其与明胶复合制备的大孔水凝胶复合支架能够很好地模拟血管的性能,支架具有的双层结构也能够很好地促使细胞黏附增殖[49]。因此,壳聚糖在组织工程血管支架制备的应用中有很大的可能性。未来,在探究壳聚糖的复合运用等方面势必将成为研究热点。
3.2 细菌纤维素
细菌纤维素是在不同条件下,由醋酸菌属、土壤杆菌属、根瘤菌属和八叠球菌属等微生物合成的纤维素的统称。因其具有无毒、细纤维网络、高纯度、良好的抗拉性能及可塑性特点,在血管支架材料运用中具有巨大潜力[50]。
Malm等[51]为探究细菌纤维的实用可能性,在绵羊颈动脉中植入由细菌纤维素制成的小口径血管支架,结果发现血管支架保持了长达13个月的通畅期,同时也无血栓形成的迹象,这表明细菌纤维素具备作为血管支架材料的潜力。但植入早期血管闭塞率过高、细胞内皮化不足等问题仍待解决。周霄楠[52]对细菌纤维素管状材料制备与表面改性方法进行了优化,将其在体外预先进行内皮化,减少了体内血栓形成与内皮增生的问题,而后将REDV多肽修饰在细菌纤维素表面,增加了材料表面内皮化的能力。
3.3 海藻酸盐
产自藻类的海藻酸不溶于水,但其盐溶液溶于水后遇钙离子易形成凝胶,这种材料的稳定性、粘性、安全性使之拥有成为血管支架材料的可能性。王薇等[53]使用以涤纶编织管为增强基的海藻酸钙/聚丙烯酰胺水凝胶血管材料拥有低溶胀率、良好力学性能等特性,且经过长时间浸泡,这些性能均未出现明显变化。这种血管支架材料的形态、溶胀性、力学性能等方面虽符合临床要求,但因以涤纶为基,所以在生物相容性及降解性能等方面需要进一步研究。
Ruther等[54]将海藻酸二醛明胶生物墨水通过3D打印的方法制备出血管支架,体外细胞实验发现这种支架不会对成纤维细胞与内皮细胞造成损害,具有良好的细胞相容性。此外,通过构建具有不同孔径大小的蜂窝状海藻酸盐血管支架并在其表面用纤连蛋白固定,随后涂有基质胶。接种内皮细胞到这种支架上后可以稳定的生长且可以承受生理水平的流体剪切力的刺激并保持支架完整[55]。这些研究表明:海藻酸盐支架为建立持久的血管生成模块提供了合适的基质,可以用于增强器官的血运重建。
3.4 透明质酸
透明质酸作为一种酸性多糖,自从其从牛眼玻璃体中提取出来后,因其天然可降解且降解产物可以被机体吸收的特性在临床上用途广泛。而高分子透明质酸能够诱导体内血管生成,降解而成的低分子透明质酸也具有促进血管生成的作用[56],因而透明质酸拥有作为组织工程血管支架材料的可能性。孙秀娟等[57]将类人胶原蛋白与透明质酸混合经过真空冻干制作出的血管支架材料拥有良好的孔隙率(>90%),经细胞毒性实验、细胞种植实验、皮下植入实验得到透明质酸的组织相容性、细胞相容性、生物降解性良好的结论。此外,使用高速旋转收集器用PCL制备了排列良好的纳米纤维支架,并用透明质酸修饰了这些表面,研究支架在体外对内皮细胞行为的协同作用[58]。体外细胞实验发现透明质酸涂层排列的PCL纳米纤维支架可以高度促进附着并引导HUVECs与平行排列的纳米纤维双极扩散。此外,支架上的HUVECs形成了汇合的单内皮细胞层,并表现出血管性血友病因子(von Willebrand factor,vWF)较高的蛋白质表达水平[58]。这一研究表明:排列整齐的纳米结构联合透明质酸更能促进用于血管组织工程的功能性内皮的再生。
4 结论
天然生物材料在组织工程血管支架的构建中扮演着重要角色,不仅是在生物相容性、信息通讯、药物传送、生物降解方面表现良好,更是在支架机械特性方面拥有先天优势,这使得天然生物材料在治疗心血管疾病中的运用越发广泛,其优缺点如表1所示。近些年来,关于天然生物材料的研究发展迅速,在临床试验中也表现出良好的运用前景,越来越多的生物支架研究者开始把目光投向天然生物材料的复合运用。

表1 用于组织工程化血管构建的常见天然生物材料的优缺点
尽管天然生物材料在力学性能、组织相容性等方面表现出色,但由于在移植后期容易诱发血栓形成,是导致试验失败的原因[59],所以目前还没有成功的人造小口径血管支架移植试验案例。如何解决支架移植时炎症的发生、降低移植后期血栓发生机率、掌握支架降解速率、减少移植物周围组织血管化等问题仍需要进一步研究。此外,取自实验动物的天然生物材料更需要注意个体之间的不同性与多变性等不可预见的问题[60]。只有在充分了解各类天然生物材料的特性,掌握有效的制备方法后,才能设计出拥有良好的各项指标的组织工程支架。
未来,随着组织工程学进一步发展,天然生物材料在再生医学的运用将愈来愈多,研究开发具有生物活性的组织工程材料将势必成为热点。因此,由生物学与临床医学共同支撑的再生医学将会大步迈进。设计出具有细胞亲和性、力学性能良好、抑制血栓及新生内膜增生等特点的血管支架,不仅能推动学术科研的大前进,更能促进医药产业的发展,为人类健康事业服务。

