隔山消的指纹图谱建立、化学模式识别分析及多指标含量测定
孙佳 勾健 秦兰 刘亭 潘洁 韦宇 刘春花






中圖分类号 R284.1 文献标志码 A 文章编号 1001-0408(2022)06-0673-07
DOI 10.6039/j.issn.1001-0408.2022.06.05
摘 要 目的 建立隔山消药材的指纹图谱并进行化学模式识别分析,同时测定其中4种成分的含量。方法 采用高效液相色谱(HPLC)法。色谱柱为ACE UExcel C18,流动相为乙腈-0.1%磷酸溶液(梯度洗脱),流速为1.2 mL/min,检测波长为210 nm,柱温为40 ℃,进样量为10 μL。以青阳参苷元为参照,采用《中药色谱指纹图谱相似度评价系统(2012版)》绘制16批隔山消药材的HPLC指纹图谱并进行相似度评价,确定共有峰。采用SPSS 26.0软件和SIMCA 14.0软件进行聚类分析、主成分分析和正交偏最小二乘-判别分析,以变量重要性投影(VIP)值大于1为标准筛选影响隔山消药材质量的差异性成分;采用相同的HPLC法测定丁香酸、去酰基萝藦苷元、白首乌二苯酮和青阳参苷元的含量。结果 16批隔山消药材中共有29个共有峰,相似度为0.723~0.998;共指认了4个共有峰,分别为丁香酸(7号峰)、去酰基萝藦苷元(9号峰)、白首乌二苯酮(13号峰)、青阳参苷元(15号峰)。聚类分析结果显示,16批隔山消药材可聚为3类,其中S1为一类,S3为一类,S2、S4~S16为一类。主成分分析结果显示,5个主成分的累计方差贡献率为88.706%,分类结果与聚类分析结果一致。正交偏最小二乘-判别分析结果显示,VIP值大于1的共有峰由大到小依次为20号峰、10号峰、25号峰、12号峰、15号峰(青阳参苷元)、21号峰、14号峰、16号峰、26号峰、22号峰、17号峰。丁香酸、去酰基萝藦苷元、白首乌二苯酮和青阳参苷元检测质量浓度的线性范围分别为0.715 3~45.778 0、2.379 4~152.281 0、0.642 0~41.085 0、14.541 6~930.662 0 µg/mL(R 2均大于0.999);定量限分别为0.357 7、0.475 9、0.642 0、2.423 6 μg/mL,检测限分别为0.146 0、0.164 1、0.248 8、0.833 3 μg/mL;精密度、重复性、稳定性(24 h)试验的RSD均小于3%;平均加样回收率分别为99.11%(RSD=2.00%,n=9)、98.54%(RSD=2.21%,n=9)、96.33%(RSD=2.54%,n=9)、95.96%(RSD=2.93%,n=9);含量分别为17.12~147.80、95.23~583.10(S8低于定量限)、16.91~210.88、211.68~3 587.15(S1低于定量限)μg/g。结论 所建HPLC指纹图谱和含量测定方法稳定、可靠、准确度高且重复性好,结合化学模式识别分析可用于隔山消药材的质量控制。
关键词 隔山消;高效液相色谱法;指纹图谱;化学模式识别分析;含量测定
Establishment of fingerprint, analysis of chemical pattern recognition and multi-index content determination of Cynanchum auriculatum
SUN Jia1,GOU Jian2,QIN Lan2,LIU Ting1,PAN Jie3,WEI Yu2,LIU Chunhua3(1. Provincial Key Lab of Pharmaceutics in Guizhou Province/State Key Lab of Functions and Applications of Medicinal Plants, Guizhou Medical University, Guiyang 550004, China; 2. College of Pharmacy, Guizhou Medical University, Guiyang 550004, China; 3. Engineering Research Center of the Ministry of Education for the Development and Application of Ethnic Medicine and Traditional Chinese Medicine, Guizhou Medical University, Guiyang 550004, China)
ABSTRACT OBJECTIVE To establish the fingerprint of Cynanchum auriculatum, to conduct its chemical pattern recognition analysis, and to determine the contents of four components at the same time. METHODS High performance liquid chromatography (HPLC) method was adopted. The determination was performed on ACE UExcel C18 column with mobile phase consisted of acetonitrile-0.1% phosphoric acid solution (gradient elution) at the flow rate of 1.2 mL/min. The determination wavelength was set at 210 nm, and the column temperature was 40 ℃. The sample size was 10 μL. Taking qingyangshengenin as the reference, HPLC fingerprints of 16 batches of C. auriculatum medicinal materials were drawn and similarity was evaluated by using the Similarity Evaluation of Chromatographic Fingerprints of Traditional Chinese Medicine (2012 edition), and the common peaks were determined. SPSS 26.0 software and SIMCA 14.0 software were used for cluster analysis, principal component analysis and orthogonal partial least squares- discriminant analysis. The differential components affecting the quality of C. auriculatum were screened by taking the value of variable importance in projection (VIP) greater than 1 as the standard; same HPLC method was used to determine the contents of syringic acid, acyl asclepiadelenin, baishouwubenzophenone and qingyangshengenin. RESULTS There were 29 common peaks in 16 batches of C. auriculatum, with a similarity of 0.723-0.998. Four common peaks were identified, namely syringic acid (peak 7), acyl asclepiadoidin (peak 9), baishouwubenzophenone (peak 13) and qingyangshengenin (peak 15). The results of cluster analysis showed that 16 batches of C. auriculatum could be clustered into three categories, among which S1 were grouped into one category, S3 were grouped into one category, S2, and S4-S16 were grouped into one category. The results of principal component analysis showed that the cumulative variance contribution rate of the five principal components was 88.706%, and the classification results were consistent with the results of cluster analysis. The results of orthogonal partial least squares-discriminant analysis showed that the common peaks (from large to small) with VIP value greater than 1 were peak 20, peak 10, peak 25, peak 12, peak 15 (qingyangshengenin), peak 21, peak 14, peak 16, peak 26, peak 22 and peak 17. The linear ranges of syringic acid, acyl asclepterin, baishouwubenzophenone and qingyangshengenin were 0.715 3-45.778 0, 2.379 4-152.281 0, 0.642 0- 41.085 0, 14.541 6- 930.662 0 µg/mL respectively (all R 2>0.999). The quantitative limits were 0.357 7, 0.475 9, 0.642 0 and 2.423 6 μg/mL; the detective limits were 0.146 0, 0.164 1, 0.248 8 and 0.833 3 μg/mL, respectively. RSDs of precision, repeatability and stability (24 h) tests were less than 3%; the average recoveries were 99.11% (RSD=2.00%, n=9), 98.54% (RSD=2.21%, n=9), 96.33% (RSD=2.54%, n=9) and 95.96% (RSD=2.93%, n=9); the contents were 17.12-147.80, 95.23-583.10 (S8 below the quantitative limit), 16.91-210.88 and 211.68-3 587.15 (S1 below the quantitative limit) μg/g, respectively. CONCLUSIONS Established HPLC fingerprint and the method of content determination are stable, reliable, accurate and reproducible. Combined with analysis of chemical pattern recognition, it can be used for the quality control of C. auriculatum.
KEYWORDS Cynanchum auriculatum; high performance liquid chromatography; fingerprint; analysis of chemical pattern recognition; content determination
隔山消又名飞来鹤、过山消、隔山撬等,为萝藦科植物耳叶牛皮消Cynanchum auriculatum Royle ex Wight的干燥块根,味甘、苦,性微温,主要分布于我国云南、贵州、四川等地的少数民族聚居区[1-2]。研究发现,隔山消含有苯乙酮类、甾体苷类、有机酸类、香豆素类、木脂素类等化学成分[1,3],具有补肝肾、强筋骨、益精血、乌须发和消积止痛等功效,民间多用于治疗痢疾、食积饱胀、胃气痛等胃肠道疾病,临床用于治疗虚损劳伤、腹痛腹胀、急慢性胁痛、腹水等症[4-5]。隔山消现收载于《贵州省中药材、民族药材质量标准》《中华本草·苗藥卷》《贵阳民间药草》等标准/书籍中[6-8],但上述标准/书籍仅对隔山消药材的性状、性味、鉴别等方面进行了描述。本课题组前期研究发现,隔山消提取物具有促进胃肠道蠕动的作用,其主要活性成分为白首乌二苯酮、去酰基萝藦苷元、青阳参苷元和丁香酸等[9]。由于中药所含化学成分较为复杂,且质量易受生产地域、采摘时间、炮制方式等因素的影响,从而导致药材质量参差不齐,加之目前关于隔山消药材的研究多集中在化学成分及药理作用等方面[9-11],有关含量测定的研究有限且仅以单一成分或单一种类化合物作为指标[12-13],因此,该药材缺乏更全面、专属性更强的质量评价方法。
中药指纹图谱具有整体性、稳定性的优点,可完整、系统地表征药材样品中主要化学成分的相似性[14-15]。化学模式识别方法近年来被广泛应用于中药材及中药制剂的质量评价中,可对多种现代仪器分析所得数据进行客观分析,并将其量化[14,16-17]。基于此,本研究建立了隔山消药材的高效液相色谱(high performance liquid chromatography,HPLC)指纹图谱,同时结合化学模式识别进行分析,并采用相同HPLC法测定了药材中白首乌二苯酮、去酰基萝藦苷元、青阳参苷元和丁香酸的含量,旨在为隔山消药材的质量控制提供参考。
1 材料
1.1 主要仪器
本研究所用主要仪器有U3000型HPLC仪及配备的四元泵、自动进样器、柱温箱、脱气器、光电二极管阵列检测器(美国Thermo Fisher Scientific公司),Allegra X-30R Centrifuge型高速离心机(美国Beckman Coulter公司),DK-98-Ⅱ型电热恒温水浴锅(天津市泰斯特仪器有限公司),KQ-300DE型数控超声波清洗器(昆山市超声仪器有限公司),EL204型电子天平[梅特勒-托利多仪器(上海)有限公司],WP-UP-Ⅱ-20型超纯水机(四川沃特尔水处理设备有限公司)等。
1.2 主要药品与试剂
丁香酸对照品(批号PS010564,纯度≥98%)购自成都普思生物科技股份有限公司;去酰基萝藦苷元对照品(批号CS-200723,纯度≥99.66%)购自北京世纪奥科生物技术有限公司;白首乌二苯酮对照品(纯度≥98%)由贵州医科大学贵州省药物制剂重点实验室自制;青阳参苷元对照品(批号AF20062803,纯度≥98%)购自成都埃法生物科技有限公司;甲醇、乙醇、乙腈、磷酸均为色谱纯,其余试剂均为分析纯,水为超纯水。
16批隔山消药材(编号S1~S16)中,S11~S14批样品购自贵州飞云岭药业股份有限公司,其余批次药材购自贵州、四川及云南等地的药材市场。上述药材购于2018年3月-2020年8月,经贵州医科大学药学院生药学教研室刘春花副教授鉴定为萝藦科植物隔山消C. auriculatum Royle ex Wight的干燥块根。16批隔山消药材的来源信息见表1。
2 方法与结果
2.1 隔山消药材的HPLC指纹图谱建立
2.1.1 色谱条件 以ACE UExcel C18(250 mm×4.6 mm,5 μm)为色谱柱,以乙腈(A)-0.1%磷酸溶液(B)为流动相进行梯度洗脱(0~5 min,10%A→15%A;5~25 min,15%A→30%A;25~35 min,30%A→42%A;35~55 min,42%A→90%A;55~60 min,90%A;60~70 min,90%A→10%A);流速为1.2 mL/min;检测波长为210 nm;柱温为40 ℃;进样量为10 μL。
2.1.2 混合对照品溶液的制备 取丁香酸、去酰基萝藦苷元、白首乌二苯酮、青阳参苷元对照品适量,精密称定,加甲醇溶解并定容,制成上述4种成分质量浓度分别为45.778 0、152.281 0、41.085 0、930.662 0 µg/mL的混合对照品溶液,于-20 ℃储存,备用。
2.1.3 供试品溶液的制备 取隔山消药材粉末(过60目筛,下同),约1.0 g,置于具塞锥形瓶中,加入0.1 mol/L盐酸6 mL、30%乙醇50 mL,加热回流提取4 h,滤过,用30%乙醇20 mL洗涤滤渣,合并滤液和洗液,水浴挥至近干,残渣加甲醇溶解并定容至5 mL,以20 000 r/min离心10 min,取上清液,即得供试品溶液。
2.1.4 精密度试验 取“2.1.3”项下供试品溶液(编号S7),按“2.1.1”项下色谱条件连续进样测定6次,以青阳参苷元为参照,计算各共有峰的相对保留时间和相对峰面积。结果显示,29个共有峰相对保留时间的RSD为0.02%~1.53%,相对峰面积的RSD为0.56%~2.50%(n=6),表明方法精密度良好。
2.1.5 重复性试验 取隔山消药材(编号S7)粉末1.0 g,共6份,精密稱定,按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,以青阳参苷元为参照,计算各共有峰的相对保留时间和相对峰面积。结果显示,29个共有峰相对保留时间的RSD为0.15%~1.41%,相对峰面积的RSD为1.20%~2.86%(n=6),表明方法重复性良好。
2.1.6 稳定性试验 取“2.1.3”项下供试品溶液(编号S7),分别于室温下放置0、2、4、8、12、24 h时按“2.1.1”项下色谱条件进样测定,以青阳参苷元为参照,计算各共有峰的相对保留时间和相对峰面积。结果显示,29个共有峰相对保留时间的RSD为0.07%~2.53%,相对峰面积的RSD为1.41~2.81%(n=6),表明供试品溶液于室温下放置24 h内稳定性良好。
2.1.7 指纹图谱的建立 取16批隔山消药材,按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,采用《中药色谱指纹图谱相似度评价系统(2012版)》对所得隔山消的色谱图进行分析,以各成分色谱响应均较强的S2样品为参照图谱,采用中位数法生成对照指纹图谱,设定时间窗宽度为0.1 s,经多点校正和mark峰匹配生成隔山消指纹图谱的共有模式并建立16批隔山消药材的叠加指纹图谱。结果显示,16批隔山消药材共有29个共有峰。16批隔山消药材的HPLC叠加指纹图谱见图1,对照指纹图谱见图2。
2.1.8 共有峰指认 取“2.1.2”项下混合对照品溶液,按“2.1.1”项下色谱条件进样测定,记录色谱图(图3A)。将16批隔山消药材的HPLC叠加指纹图谱与上述混合对照品溶液色谱图进行对比,共指认了其中4个色谱峰,分别为丁香酸(7号峰)、去酰基萝藦苷元(9号峰)、白首乌二苯酮(13号峰)、青阳参苷元(15号峰)。由于青阳参苷元(15号峰)的分离度较好、峰面积较稳定且保留时间适中,故以其为参照。
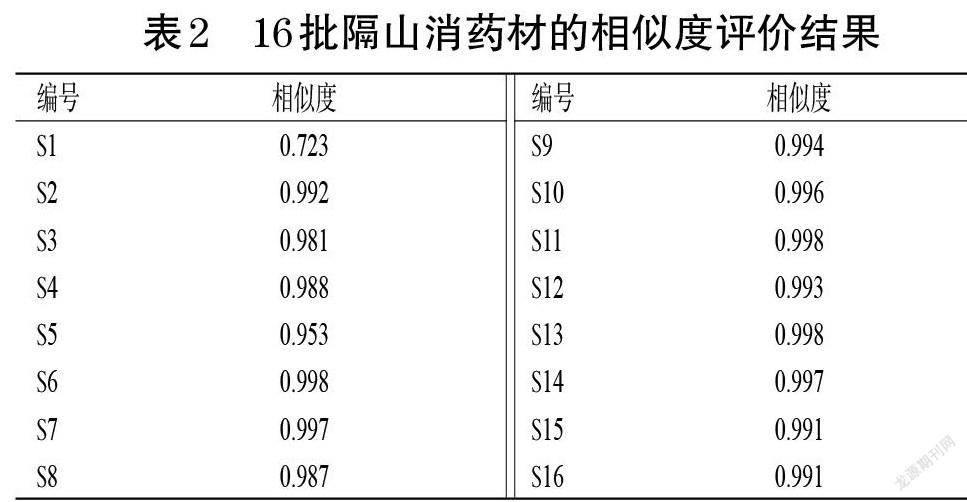
2.1.9 相似度评价 以对照指纹图谱为参照,采用《中药色谱指纹图谱相似度评价系统(2012版)》对16批隔山消药材的指纹图谱进行相似度评价。结果显示,16批隔山消药材的相似度为0.723~0.998,其中仅S1的相似度为0.723,其余均大于0.950,表明除S1外,其余15批隔山消药材的质量稳定、化学成分差异较小。结果见表2。
2.2 聚类分析
以16批隔山消药材指纹图谱的共有峰峰面积为变量,使用SPSS 26.0软件,采用瓦尔德连接方法(即离差平方和法),以平方欧氏距离为测度进行聚类分析。结果显示,当距离为10时,16批隔山消药材可聚为3类,其中S1为一类,S3为一类,S2、S4~S16为一类,表明S1、S3与其余14批隔山消药材质量存在差异。结果见图4。
2.3 主成分分析
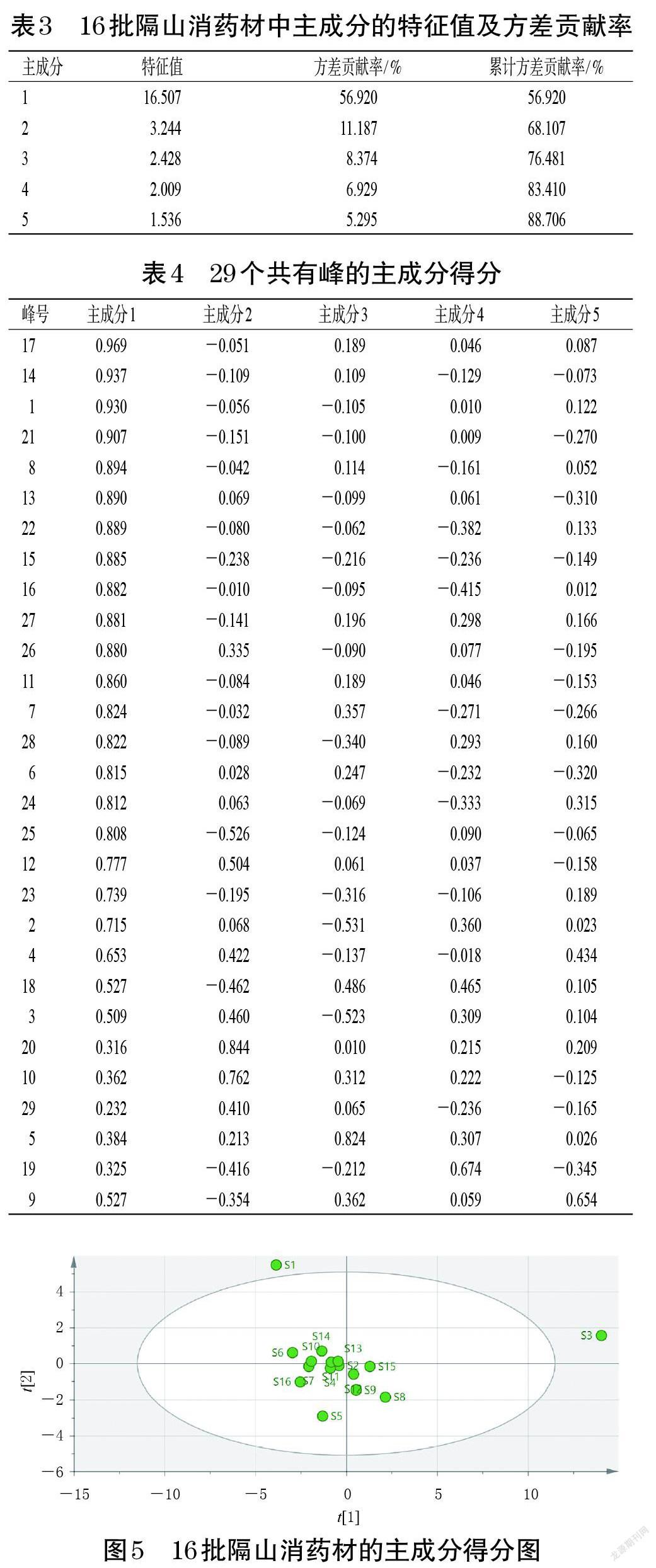
以16批隔山消药材指纹图谱的共有峰峰面积为变量,使用SPSS 26.0软件进行主成分分析。结果显示,共提取5个主成分,其中主成分1的特征值最大,为16.507,方差贡献率为59.920%,主要反映1~4、6~8、11~18、21~28号峰的信息。主成分2~5的特征值分别为3.244、2.428、2.009、1.536,方差贡献率分别为11.187%、8.374%、6.929%、5.295%,其中主成分2反映10、20、29号峰的信息,主成分3反映5号峰的信息,主成分4反映19号峰的信息,主成分5反映9号峰的信息。5个主成分的累计方差贡献率为88.706%,表明提取的这5个主成分可以反映样品数据中的绝大部分信息,能代表16批隔山消药材样品中29个共有峰峰面积,提示隔山消药材质量受多个成分的影响。结果见表3、表4 。
以16批隔山消药材指纹图谱的共有峰峰面积为变量,采用SIMCA 14.0软件绘制主成分得分图,详见图5。由图5可知,16批隔山消药材可分为3类,S1样品位于得分图的左上方,为一类;S3样品位于得分图的最右侧,为一类;S2、S4~S16样品位于得分图的中部,为一类。
2.4 正交偏最小二乘-判别分析
以16批隔山消药材指纹图谱的共有峰峰面积为变量,使用SIMCA 14.0软件进行正交偏最小二乘-判别分析。结果显示,累计解释能力参数R 2X、R 2Y分别为0.867、0.975,累计模型预测能力参数Q 2为0.552,均大于0.5,表明该模型稳定、可靠[18]。16批隔山消药材被分为3类,其中S1为一类,S3为一类,S2、S4~S16为一类。结果见图6。
变量重要性投影(variable importance in projection,VIP)值是筛选差异性成分的重要指标,VIP值越高,成分对组间差异的影响越大,故本研究以VIP值>1为标准筛选影响隔山消药材质量的差异性成分[14,18]。结果显示,VIP值>1的共有峰由大到小依次为20号峰、10号峰、25号峰、12号峰、15号峰(青阳参苷元)、21号峰、14号峰、16号峰、26号峰、22号峰、17号峰。结果见图7。
2.5 隔山消药材中4个有效成分的含量测定
2.5.1 色谱条件 同“2.1.1”项。
2.5.2 混合对照品溶液的制备 同“2.1.2”项。
2.5.3 供试品溶液的制备 同“2.1.3”项。
2.5.4 系统适用性试验 取上述混合对照品溶液、供试品溶液、空白对照溶液(按“2.5.3”项下方法制备不含隔山消药材的空白对照溶液),按“2.5.1”项下色谱条件进样测定,记录色谱图,详见图3。由图3可知,在供试品溶液中,丁香酸等4个成分的保留时间与对照品溶液的保留时间一致,分离度均大于1.5,理论板数均不低于7 000,空白对照溶液不影响待测成分的含量测定。
2.5.5 线性关系考察 取“2.5.2”项下混合对照品溶液適量,用50%甲醇逐级稀释,制得丁香酸质量浓度分别为22.889 0、11.444 5、5.722 2、2.861 1、1.430 6、0.715 3 µg/mL,去酰基萝藦苷元质量浓度分别为76.140 5、38.070 2、19.035 1、9.517 6、4.758 8、2.379 4 µg/mL,白首乌二苯酮质量浓度分别为20.542 5、10.271 3、5.135 6、2.567 8、1.283 9、0.642 0 µg/mL,青阳参苷元质量浓度分别为465.331 0、232.665 5、116.332 8、58.166 4、29.083 2、14.541 6 µg/mL的系列线性工作溶液。精密吸取上述系列线性工作溶液和“2.5.2”项下混合对照品溶液,按“2.5.1”项下色谱条件进样测定,记录色谱图。以各待测成分质量浓度(x)为横坐标、峰面积(y)为纵坐标进行线性回归,结果见表5。
2.5.6 定量限与检测限考察 取“2.5.2”项下混合对照品溶液,用50%甲醇倍比稀释,按“2.5.1”项下色谱条件进样测定,记录峰面积。以信噪比分别为10 ∶ 1、3 ∶ 1计算定量限和检测限,结果见表4。
2.5.7 精密度试验 取“2.5.3”项下供试品溶液(编号S7),按“2.5.1”项下色谱条件连续进样测定6次,记录峰面积。结果显示,丁香酸、去酰基萝藦苷元、白首乌二苯酮、青阳参苷元峰面积的RSD分别为1.00%、2.20%、1.80%、0.54%(n=6),表明方法精密度良好。
2.5.8 重复性试验 取隔山消药材(编号S7)粉末1.0 g,共6份,精密称定,分别按“2.5.3”项下方法制备供试品溶液,再按“2.5.1”项下色谱条件进样测定,记录峰面积并按外标法计算样品含量。结果显示,丁香酸、去酰基萝藦苷元、白首乌二苯酮、青阳参苷元含量的RSD分别为0.67%、2.00%、2.80%、0.58%(n=6),表明方法重复性良好。
2.5.9 稳定性试验 取“2.5.3”项下供试品溶液(编号S7),分别于室温下放置0、2、4、8、12、24 h时按“2.5.1”项下色谱条件进样测定,记录峰面积。结果显示,丁香酸、去酰基萝藦苷元、白首乌二苯酮、青阳参苷元峰面积的RSD分别为1.40%、1.60%、2.40%、0.98%(n=6),表明供试品溶液于室温下放置24 h内稳定性良好。
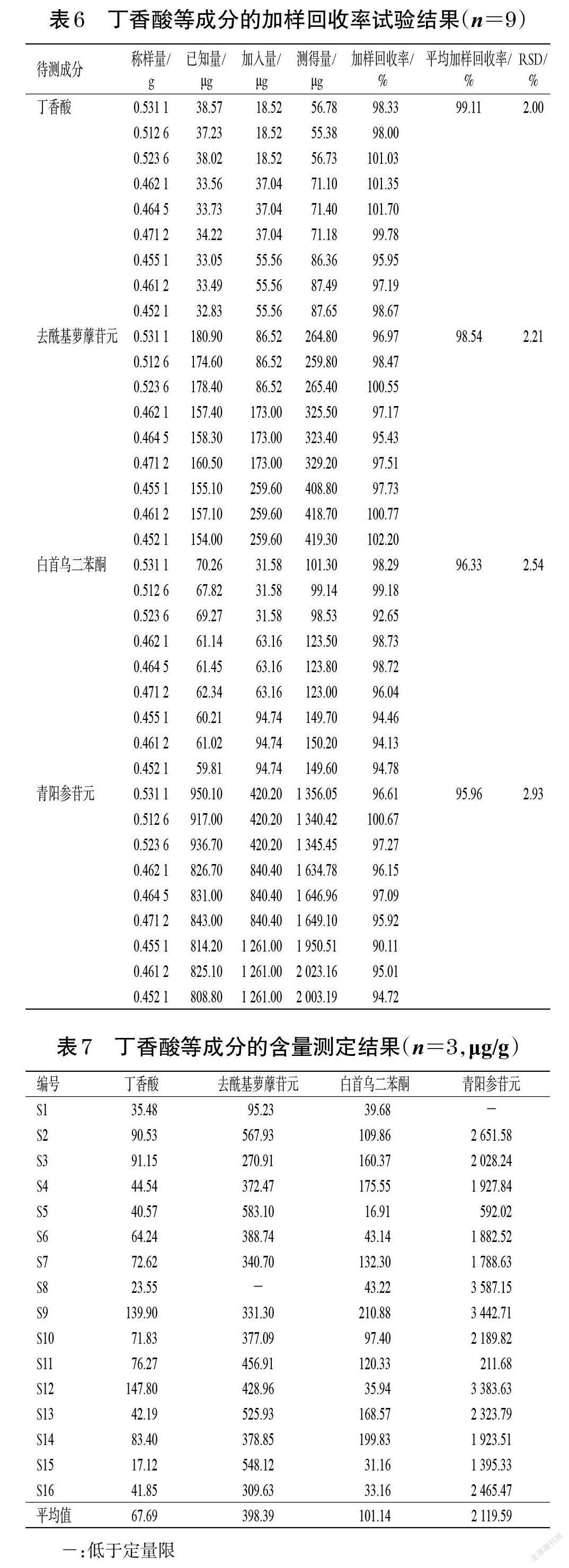
2.5.10 加样回收率试验 称取已知含量的隔山消药材(编号S7)粉末,每份约0.5 g,共9份,按已知量的0.5、1、1.5倍精密加入与待测成分含量相当的混合对照品溶液(按“2.5.2”项下方法配制),按“2.5.3”项下方法制备供试品溶液,再按“2.5.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表6。
2.5.11 样品含量测定 取16批隔山消药材粉末约1.0 g,分别按“2.5.3”项下方法制备供试品溶液,再按“2.5.1”项下色谱条件进样测定,记录峰面积并按外标法计算样品含量。每样品平行测定3次,取平均值,结果见表7。
3 讨论
3.1 提取溶剂及提取方法的选择
在前期预实验中,本课题组分别考察了不同提取溶剂(水、30%乙醇、50%乙醇、70%乙醇、乙醇、30%甲醇、50%甲醇、70%甲醇、甲醇)对隔山消药材指纹图谱的影响。结果发现,当以30%乙醇为提取溶剂时,各成分色谱峰的响应和峰形均较好,基线较平稳,故选择30%乙醇为提取溶剂。崔乐伟[19]采用HPLC法测定了不同批次断节参中青阳参苷元含量,当回流提取溶剂中加入盐酸时,青阳参苷元等活性成分的色谱响应更强。基于此,本研究参考上述文献的方法,考察了提取溶剂中加盐酸与不加盐酸对各成分色谱响应的影响。结果显示,与不加盐酸相比,在提取溶剂中加入0.1 mol/L盐酸后,各成分的色谱响应更强且峰形较好,故最终选择提取溶剂为0.1 mol/L盐酸和30%乙醇。本课题组又对不同提取时间(0.5、1.0、2.0、3.0、4.0、5.0 h)、提取方法(加热回流法、超声提取法)进行了考察,结果显示,加热回流4 h时的提取效果较好且操作简单。
3.2 色谱条件的考察
本课题组前期预实验考察了不同色谱系统(甲醇-水、甲醇-0.05%磷酸溶液、甲醇-0.1%甲酸溶液、乙腈-水、乙腈-0.05%磷酸溶液、乙腈-0.1%磷酸溶液)、不同洗脱程序、不同柱温(30、40、45 ℃)、不同流速(0.8、1.0、1.2 mL/min)对指纹图谱的影响。结果显示,采用本研究所用色谱条件时,所得色谱图中的色谱峰数量较多、分离度较好且基线平稳。通过在210~280 nm波长下对隔山消药材进行扫描后发现,在210 nm波长处所得色谱图基线较平稳、出峰信息量大、峰形较好,故选择210 nm为检测波长。
3.3 指纹图谱及化学模式识别分析
16批隔山消药材共有29个共有峰。相似度评价结果显示,仅S1样品的相似度为0.723,其余15批样品的相似度均大于0.950,表明除S1外,其余15批隔山消药材的质量较稳定、化学成分种类的差异较小。聚类分析结果显示,16批隔山消药材可聚为3类,其中S1聚为一类,S3聚为一类,S2、S4~S16聚为一类;该结果与主成分分析结果一致,表明S1、S3样品与其余14批样品存在差异,可能与这两批药材的采收时间、地点、加工方式等不同有关。正交偏最小二乘-判别分析结果显示,20号峰、10号峰、25号峰、12号峰、15号峰(青阳参苷元)、21号峰、14号峰、16号峰、26号峰、22号峰、17号峰对应的成分是影响隔山消药材质量的差异性成分。
3.4 含量测定结果分析
虽然丁香酸、白首乌二苯酮、去酰基萝藦苷元不是影响隔山消药材质量的差异性成分,但根据本课题组前期研究结果,上述化合物为隔山消药材水溶性部位的主要成分,具有促进胃肠道胃动素和胃泌素释放、抑制血管活性肠肽和肿瘤坏死因子α分泌、增加肠道蠕动、兴奋胃肠平滑肌、促进胃排空和肠推进、改善功能性消化不良的作用[9]。因此笔者认为,这3种成分也可作为隔山消药材质量控制的主要指标成分。含量测定结果显示,丁香酸、去酰基萝藦苷元、白首乌二苯酮、青阳参苷元的含量分别为17.12~147.80、95.23~583.10(S8低于定量限)、16.91~210.88、211.68~3 587.15(S1低于定量限)μg/g,各成分含量存在差异,分析其原因可能与不同产地、不同来源的隔山消药材的栽培环境、采收期、种植模式、加工储存条件等不同有关。
综上所述,所建HPLC指纹图谱和含量测定方法稳定、可靠、准确度高且重复性好,结合化学模式识别分析可用于隔山消药材的质量控制。
参考文献
[ 1 ] 陈艳,徐必学,曹佩雪,等.隔山消化学成分的研究[J].天然产物研究与开发,2013,25(11):1522-1524.
[ 2 ] 王新婕,李振麟,钱士辉,等.耳叶牛皮消中C21甾体类成分研究进展[J].中国野生植物资源,2018,37(3):51-55,63.
[ 3 ] 秦兰,孙佳,刘春花,等. UPLC-ESI-MS/MS法测定苗药隔山消中8个成分含量[J].贵州医科大学学报,2021,46(8):886-892.
[ 4 ] 李艳,黎开燕.隔山消的药理作用研究进展[J].现代中西医结合杂志,2015,24(2):213-215.
[ 5 ] 吴一振,周明高,周顺,等.土家药隔山消的炮制规范研究[J].中国民族医药杂志,2018,24(1):37-39.
[ 6 ] 贵州省药品监督管理.贵州省中药材、民族药材质量标准[S].贵阳:贵州科技出版社,2003:384.
[ 7 ] 国家中医药管理局,《中华本草》编委会.中华本草:苗药卷[M].贵阳:贵州科技出版社,2005:283-284.
[ 8 ] 貴阳市卫生局.贵阳民间药草[M].贵阳:贵州人民出版社,1959:139.
[ 9 ] 秦兰,游景瑞,潘洁,等.隔山消提取物对功能性消化不良模型大鼠脑肠肽及胃肠道功能的作用机制研究[J].中国药业,2021,30(13):23-26.
[10] 谢凯强,苑春茂,蹇军友,等.隔山牛皮消、耳叶牛皮消和戟叶牛皮消中四个C21-甾体苷元含量比较研究[J].天然产物研究与开发,2018,30(2):261-267.
[11] 曹雨,李金花,刘海波,等.隔山消抗神经氨酸酶活性及化学成分研究[J].中草药,2017,48(21):4485-4492.
[12] 肖培云,蓝海,李龙星. HPLC法测定隔山消中没食子酸的含量研究[J].大理学院学报,2009,8(6):9-11.
[13] 孙佳,赵珊,邹欢,等. HPLC同时测定隔山消中5个成分的含量[J].药物分析杂志,2015,35(10):1801-1805.
[14] 韩忠耀,向军,陈建宇,等.不同产地水冬瓜叶HPLC指纹图谱建立、化学模式识别分析及含量测定[J].中国药房,2021,32(10):1224-1229.
[15] 戚华文,徐鑫,高德嵩,等.吴茱萸HPLC指纹图谱的建立及基原鉴别研究[J].中草药,2021,52(14):4341-4347.
[16] 孙立丽,王萌,任晓亮.化学模式识别方法在中药质量控制研究中的应用进展[J].中草药,2017,48(20):4339- 4345.
[17] 刘敏,曹国琼,张仕林,等.杜仲补天素丸的HPLC指纹图谱建立、化学模式识别分析及含量测定[J].中国药房,2021,32(8):961-966.
[18] 梁慧,潘晓君,杨文惠,等.基于UPLC指纹图谱和一测多评法的虎杖药材质量评价[J].中国药房,2021,32(15):1842-1848.
[19] 崔乐伟.基于物质基础的断节参药材质量标准研究[D].昆明:云南中医学院,2014.
(收稿日期:2021-09-09 修回日期:2021-12-29)
(编辑:陈 宏)

