红磷的纳米化及其在钠离子电池中的应用
张 宇,白 金,赵海雷
北京科技大学材料科学与工程学院,北京 100083
自1991年索尼率先商业化锂离子电池以来,锂离子电池凭借着电压高、循环稳定、自放电低、无记忆效应等诸多优点,在大规模储能、电动汽车及消费电子领域得到了广泛的应用.但是锂在地壳中的含量较少,只占0.0065%,随着对锂离子电池需求的快速增长,锂资源日益紧缺,因此开发新型储能电池体系成为了亟待解决的问题之一.
在众多新型储能电池体系中,钠离子电池有着与锂离子电池相似的储能机理,安全性更高,同时钠储量丰富,钠离子电池制备亦可借鉴锂离子电池的设备和产线.因而钠离子电池近年在世界范围内受到研究者的关注.然而由于钠离子半径(0.106 nm)远大于锂离子(0.076 nm),因而许多锂离子电池的电极材料,对钠离子电池并不适用.高性能钠离子电池正负极材料的研究开发,是目前该领域的研究热点之一.目前研究的钠离子电池正极材料主要包括层状结构氧化物[1]、隧道结构氧化物[2]、聚阴离子型化合物[3]、普鲁士蓝类化合物[4]等.负极材料主要有硬碳[5]、钛酸钠[6]、金属及合金[7-8]、金属硫化物[9]、金属氧化物[10]、金属磷化物[11]、单质磷[12-13]等.相比于其他的负极材料,单质磷有着极高的理论比容量(2596 mA·h·g-1)和合适的氧化还原电位(0.4 VvsNa/Na+),同时其储量丰富,因而是一种极具潜力的钠离子电池负极材料.
磷主要有三种同素异形体,白磷、黑磷以及红磷.白磷是一种易燃的剧毒物质,化学性质十分活泼,40 ℃左右即可燃烧,不适宜用于钠离子电池负极.黑磷是半导体,具有石墨状片层结构,并且可以被剥离成二维的磷烯,是一种理想的钠离子电池负极材料.但是黑磷的制备条件十分严苛,往往需要高温、高压和催化剂的作用,这极大的限制了黑磷在钠离子电池中的实际应用.
红磷(RP)的成本低廉、化学性质相对稳定且易于制备,其最有希望实现在钠离子电池中的实际应用.然而红磷也存在一些问题,如其电导率(约10-12S·m-1)极低,且在充放电过程中伴随着的巨大体积效应(≥400%),这极大的制约了红磷的倍率性能和长循环稳定性.针对这些问题,目前的主要改进策略包括:(1)制备纳米红磷(NRP)缓解由于体积效应引起的红磷粉化,同时缩短Na+的传输路径,改善材料的电极反应动力学;(2)将红磷与高导电相材料复合,可以对红磷的进行物理限域,防止充放电过程中的电化学团聚;同时高导电相可以改善电子传导,均化活性颗粒表面电流密度,使得红磷均匀膨胀,减少应力集中,防止红磷粉化.这两类方法通常结合使用,共同改善红磷负极的电化学性能.
目前,纳米红磷的制备仍然面临着许多挑战.本文总结了纳米红磷的制备方法,包括球磨法、升华冷凝法、还原法、气相生长法、溶剂热法、化学沉淀法等,并对各种方法的优缺点进行了比较、总结.本文最后,讨论了纳米红磷负极目前面临的挑战和未来的发展方向.希望这篇综述可以使读者较为全面地了解目前纳米红磷的特性以及研发现状,以促进红磷在钠离子电池中的实际应用.
1 机械力法—球磨
球磨可以通过机械力的不断作用将大尺寸材料破碎、研磨至纳米尺度,是制备纳米材料最常见的方法之一,也被广泛的用于纳米红磷的制备.鉴于红磷存在的导电性差和体积效应问题,通常将红磷与高导电相材料一起球磨制备复合材料,以改善材料的电化学活性和循环稳定性.常见的高导电相材料主要为碳材料,如炭黑[12,14]、碳纳米管[15-17]、石墨烯[18-19]等.此外,因为强机械力的持续作用,在某些情况下红磷可以和碳材料形成P-C 键[20-21]或P-O-C键[15,18-19,22],这有利于增强红磷和碳材料之间的结合,改善红磷的循环性能.如将红磷与堆叠石墨烯一起球磨,柔韧而大比表面积的石墨烯在提高红磷导电性、缓释充放电过程中体积变化的同时,还与红磷形成P-O-C键,促进红磷和石墨烯之间的紧密结合[18].制备出的磷碳(P/G)复合纳米结构负极表现出2077 mA·h·g-1的可逆容量,循环60圈后仍能保持1700 mA·h·g-1的可逆比容量(图1(a)和(b)).
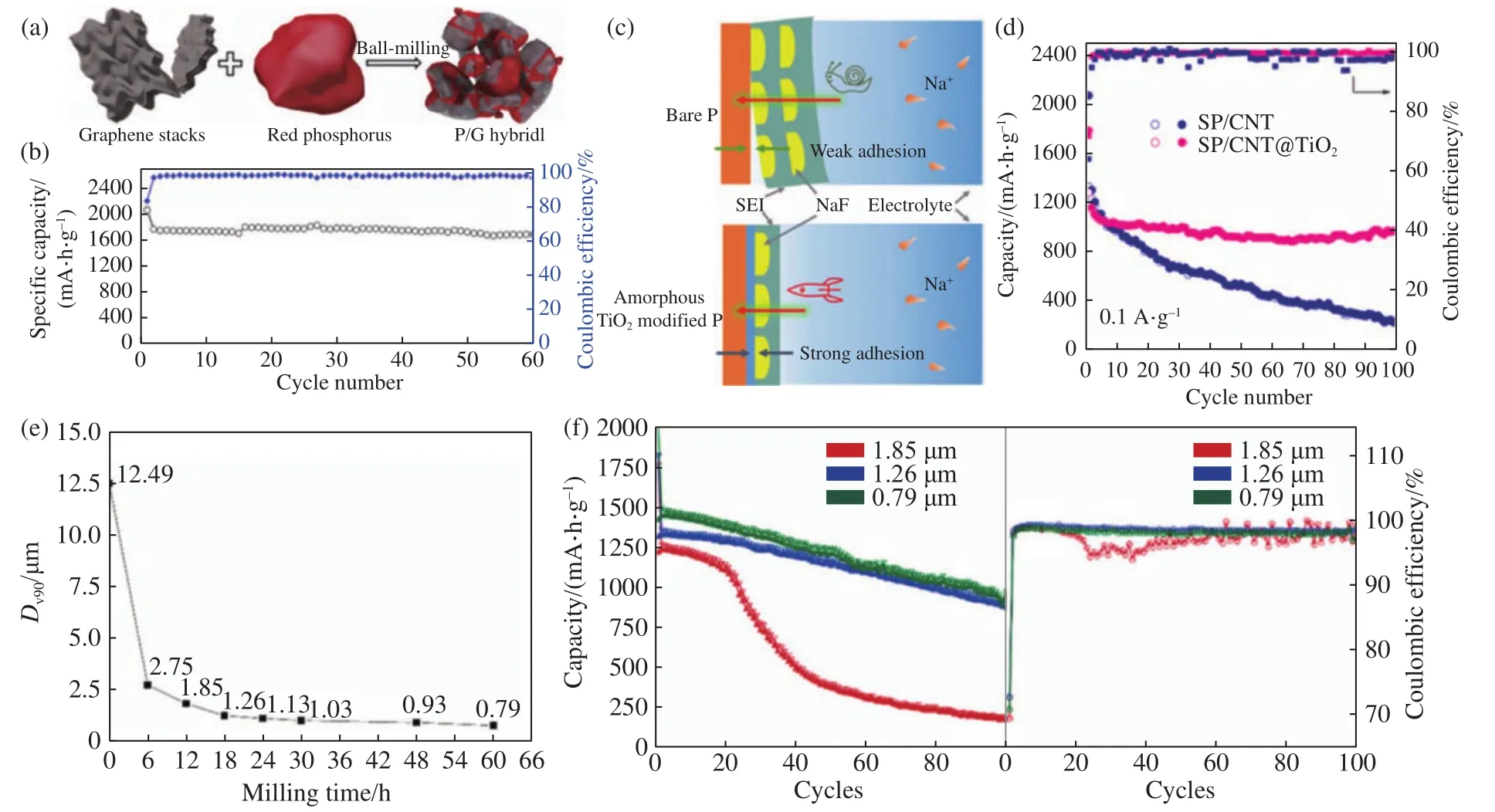
图1 (a)P/G 复合材料制备示意图[18];(b)P/G 复合材料在 260 mA·g-1下的循环性能[18];(c)SEI组分对钠离子存储性能的影响[29];(d)SP/CNT和SP/CNT@TiO2的循环性能[29];(e)Dv90随球磨时间的变化曲线[30];(f)不同Dv90的球磨红磷的循环性能和库仑效率[30]Fig.1 (a) Schematic of synthesis of P/G hybrid[18]; (b) cycling performance of P/G hybrid anode at a current density of 260 mA·g-1[18]; (c) illustration of different components of the SEI film and their contribution to sodium storage in different electrodes[29]; (d) cycling performance of SP/CNT and SP/CNT@TiO2[29]; (e) change curve of Dv90 with ball milling time[30]; (f) cycling performance and Coulombic efficiencies of ball-milled red phosphorus with different Dv90[30]
此外,导电高分子[23]、金属[24-27]、金属氧化物[14,22]、金属氮化物[20]、钛酸盐[28]等也被用于与红磷球磨以改善其电化学性能.Zhang等[29]发现使用无定形的TiO2在红磷表面构建保护层不仅可以在表面构建快速的钠离子传输层,还可以增强与固体电解质界面膜(SEI膜)中NaF的作用力,改善SEI膜与电极之间的结合提高电极的循环稳定性(图1(c)和(d)).
研究发现,红磷尺寸与球磨时间,并非呈线性关系.球磨初期尺寸下降较快,球磨后期颗粒尺寸变化缓慢.颗粒尺寸对电化学性能有显著影响.Dv90为1.86 μm的红磷负极在循环20圈后容量快速衰减,而Dv90为1.26 μm的红磷负极的循环寿命显著提高,循环100次后仍保持初始比容量的67%.但随着研磨时间的进一步增加,红磷的粒径减小只会导致比容量增加,而不会显著改善循环寿命(图1(e)和(f)).球磨过程中,使用乙二醇或者水可以有效提高球磨效率,但是因为水易与红磷反应,容易在球磨过程中引入杂质,因此并不适合用作球磨介质[30].
球磨法制备纳米红磷复合材料有着方法简单、易于操控、适用范围广的特点,但是也存在着一些问题:(1)红磷遇明火、高热、摩擦、撞击有燃烧、爆炸的危险,需要湿法球磨或者在惰性气氛的保护下球磨,增加了操作难度;(2)红磷在球磨过程中会有部分不可避免的氧化,形成磷的氧化物,造成容量的不可逆损失;(3)球磨法制备的纳米红磷颗粒尺寸均一性差,且团聚严重.
2 热化学法
2.1 升华冷凝
对易气化的材料,升华冷凝法常被用于制备其纳米材料.红磷可以在416 °C时升华为小分子的白磷P4气体,冷却时白磷气体可以在基体材料表面沉积为纳米白磷,并在后续的保温过程中(260~320 °C)再次转变为红磷,从而形成纳米红磷的复合材料.
与球磨法相似,为了在减小红磷粒径的同时改善红磷的导电性,目前升华冷凝法常用的基体材料也主要为碳材料,如多孔碳[31-33]、石墨烯[34-35]、碳纳米管[36-38]、碳纤维[39-42]、空心碳球[43-44]等.如Liu等[35]使用柔性的还原氧化石墨烯(rGo)为基体材料制备了具有61.4%高磷载量的柔性的P@rGO自支撑薄膜,直接用作钠离子电池负极材料,在1593.9 mA·g-1电流密度下循环300圈后仍能保持914 mA·h·g-1的高可逆比容量(图2(a)和(b)).
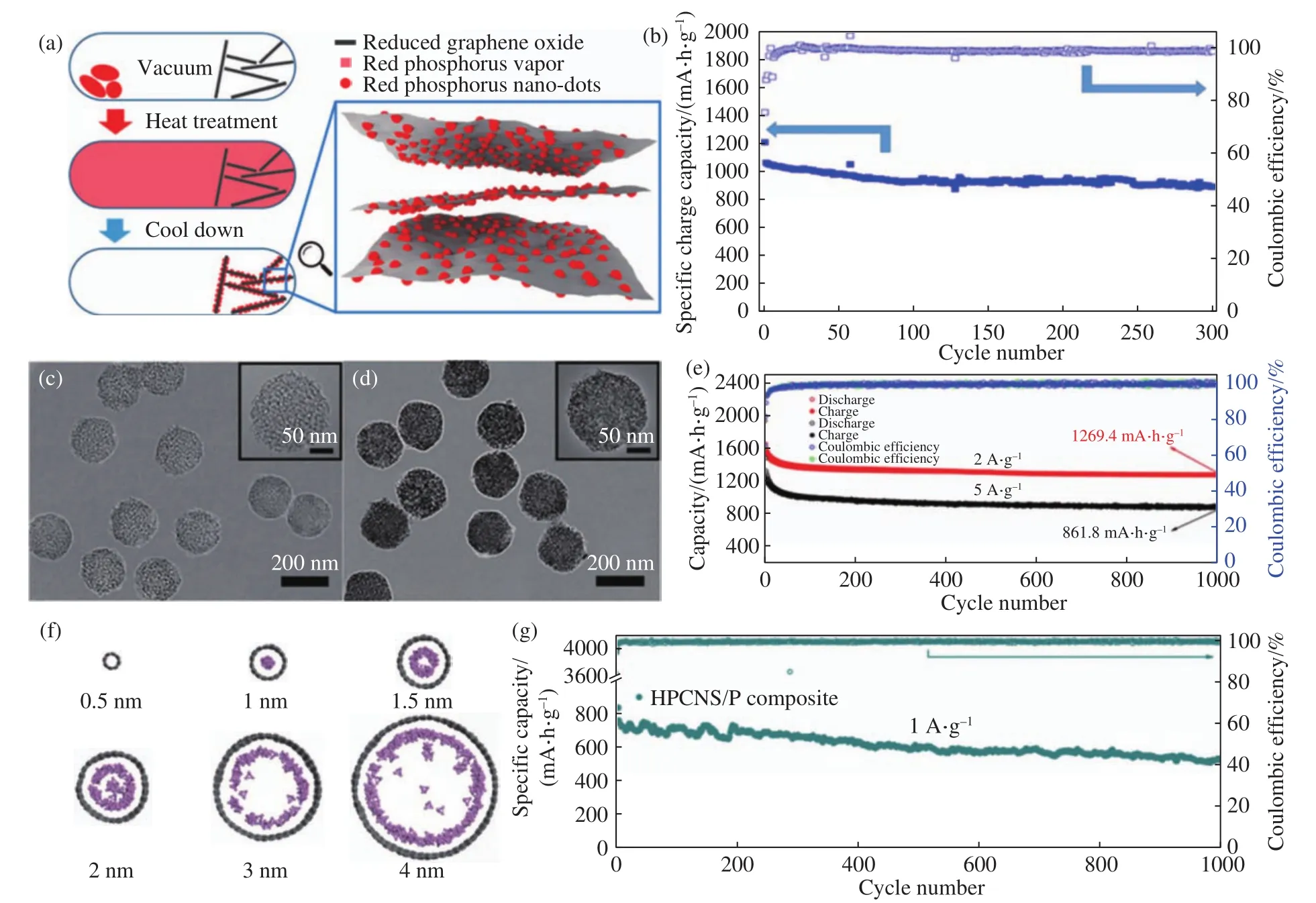
图2 (a)P@rGO 的制备示意图[35];(b)P@rGO 在 1593.9 mA·g-1下的循环性能[35];(c, d) HHPCNSs和HHPCNSs/P 的 TEM 照片[45];(e)HHPCNSs/P 在 2 A·g-1和5 A·g-1下的循环性能[45];(f)P4吸附到直径为0.5、1、1.5、2、3和4 nm 的纳米管后平衡形态顶视图[43];(g)HPCNS/P 在 1 A·g-1下的长期循环性能图[43]Fig.2 (a) Schematic of P@rGO synthesis[35]; (b) cycling performance of P@rGO at a current density of 1593.9 mA·g-1[35]; (c, d) TEM image of HHPCNSs and HHPCNSs/P[45]; (e) cycling performance of P@rGO at a current density of 2 and 5 A·g-1[45]; (f) top view of the equilibrium morphologies after P4 adsorption into the nanotubes of 0.5, 1, 1.5, 2, 3, and 4-nm diameter[43]; (g) long-term cycle stability of the HPCNS/P composite electrode for 1000 cycles at 1.0 A·g-1[43]
碳纤维、石墨烯或者其他的一些一维、二维材料有着巨大的比表面积,可以吸附大量的红磷.然而吸附在其表面的红磷,部分会因为充放电过程中的反复体积变化而从其表面脱落,失去电接触,造成容量的不可逆损失.相比于碳纤维以及石墨烯,多孔碳可以通过毛细作用力吸附白磷气体并最终将红磷沉积在其孔道之中,可以对红磷起到物理限域的作用,避免红磷在充放电过程中从多孔碳中脱落、失去电接触[31-33,46-47].对于具有超高孔体积(3.258 cm3g-1)的中孔介孔纳米碳球(HHPCNSs),大的孔体积可为负载红磷和缓冲红磷的膨胀提供充足的空间,并可对红磷起到物理限域的作用,HHPCNSs/P在2A·g-1下循环1000圈后仍然保持 1269.4 mA·h·g-1的可逆比容量,容量保持率 81.2%[45](图2(c)~(e)).
在多孔碳材料中,孔径分布对红磷的沉积形态也有很大的影响,通过模拟P4分子在直径0.5~4 nm的碳纳米管中的沉积情况发现,当直径<0.9 nm时P4分子无法在孔中沉积.当直径达到1 nm时,P4分子在孔中呈链状分布,并随着直径的增加P4分子由链状分布向着管状分布变化(图2(f)).1~2 nm的孔洞可以提升磷的负载量,并对磷起到更好的物理限域作用.当微孔尺寸主要为1~2 nm的微孔碳球(HPCNS)作为基体材料时,HPCNS/P表现出了良好的循环稳定性[43](图2(g)).
在一些特定条件下,升华冷凝也可以通过形成P-C键或P-O-C键来提高红磷和碳材料之间的作用力,从而改善电极的循环稳定性[38,40,43-45,47-50].但是形成P-C 键或P-O-C键的具体条件目前仍不清楚.
通过升华冷凝法制备的红磷复合材料负极往往红磷的粒径细小,甚至几个纳米,空间分布均匀、粒径均一,有着良好的循环稳定性.但是也存在以下几个主要问题.(1)升华冷凝法制备纳米红磷必须用到基体材料,无法制备单一的纯纳米红磷;(2)红磷复合材料负极的红磷含量往往受制于基体材料的比表面积和孔体积,含量往往很难超过50%,极大的限制了其能量密度;(3)红磷升华冷凝后会转化为白磷.为了防止白磷的泄露、自燃并使白磷充分转化为红磷,制备过程需要在密闭的容器中长时间的保温,且在热处理结束后需要清洗除去材料中多余的白磷.这增加了该方法大规模应用的难度.
2.2 热还原
工业上,通常在1400 °C以上碳热还原Ca3(PO4)2制备白磷,其反应式为:2Ca3(PO4)2+ 6SiO2+ 10C =6CaSiO3+ P4+ 10CO.基于碳热还原的基本想法,Sun等[51]将 P4O10作为磷源,PEG作为碳源,在900 °C碳热还原制备纳米红磷填充于三维球形碳网络中的磷/碳(P/C)复合材料(P4O10+ 10C ↔ 4P +10CO).所制备的P/C复合材料在520 mA·g-1电流密度下循环160圈后仍具有920 mA·h·g-1的可逆比容量(图3(a)~(c)).

图3 (a)P/C复合材料的制备示意图;(b)P/C复合材料的SEM照片;(c)P/C复合材料在不同电流密度下的循环性能[51]Fig.3 (a) Schematic and digital photographs of the synthesis procedure for P/C composite; (b) SEM image of the P/C composite; (c) cycling performance of the P/C composite at different current densities[51]
为了降低还原时的温度,Li等[52]发现在AlCl3存在的情况下,金属Zn可以在50 °C的低温下还原 PCl5制备纳米红磷(2PCl5·AlCl3+ 5Zn = 2P +5ZnCl2+ 2AlCl3).共价盐 AlCl3和PCl5可以形成基团和基团的加成化合物PCl5·AlCl3,将体系熔点从200 °C降低至50 °C,简化了制备工艺.有意思的是,此方法也可以在180 °C下还原P2O5和Ca3(PO4)2,还可以用于制备金属磷化物.此外,研究发现使用NaCl-KCl-AlCl3为低温共熔盐,金属Mg为还原剂和模板,可以利用Kirkendall效应在220 °C还原制备多孔纳米红磷(5Mg + 2PCl5→5MgCl2+ 2P)[53].
2.3 气相生长
气相生长法主要用于晶体纳米红磷的制备,目前常见的方法为化学气相沉积(CVD)、化学气相输运(CVT)以及气-液-固生长法(VLS).CVD法常用的基质材料包括SiO2管[54]、SiO2纤维[55]、Si纳米纤维板[55]、钛板[55]等.以红磷或者白磷为原料,通过较为简单的热处理就可以得到针状或者棒状的纳米纤维红磷.
VLS法是利用在合金熔体液滴的约束下,气相基元在液相的金属催化剂基元中的不断溶解与析出,生长一维晶体结构[56-57].因为金属铋熔点较低且对P4蒸汽有着低但显著的溶解性,基于VLS的生长机理,可以制备出多晶红磷纳米线和单晶红磷纳米带(图4(a)~(c))[58-59].
CVT法以碘作为输运剂和矿化剂,高温侧(480 °C)无定形红磷升华形成的P4气体与碘蒸汽反应生成气态的PIx,PIx在温度梯度的作用下输送到温度较低的成核侧(450 °C),然后分解为晶体红磷和碘.形成的晶体红磷通过超声处理可以得到晶体红磷纳米带(图4(d)~(f))[60].
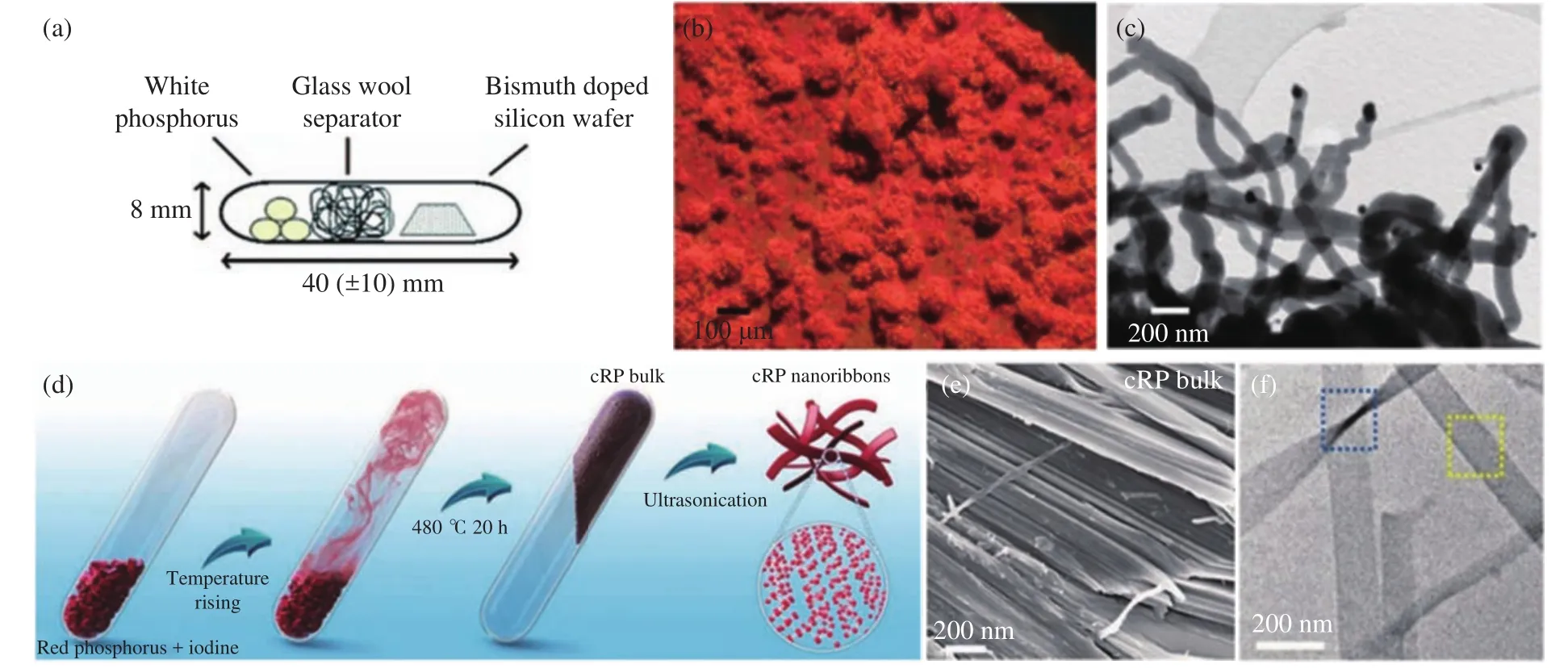
图4 (a)晶体红磷纳米线的制备示意图[58];(b)热处理后的光学照片[58];(c)晶体红磷纳米线的 TEM照片[58];(d)块状晶态红磷和晶体红磷纳米带的制备示意图[60];(e)块状晶体红磷的SEM照片[60];(f)晶体红磷纳米带的TEM照片[60]Fig.4 (a) Schematic of the synthesis of crystalline red phosphorus nanowire[58]; (b) optical micrographs of the product after heat treatment[58]; (c) TEM image of the crystalline red phosphorus nanowire[58]; (d) schematic of the synthesis of red phosphorus bulk and nanoribbons[60]; (e) SEM image of red phosphorus bulk[60]; (f) TEM image of red phosphorus nanoribbons[60]
由于晶体红磷的产率和成本问题,目前,晶体红磷多用于催化领域,在锂/钠离子电池领域的应用较少.
3 湿化学法
3.1 溶剂热
溶剂热法是制备纳米材料的常用方法,在高温、高压溶剂热条件下,可以为各种前驱体的溶解、反应和结晶提供一个在常压条件下无法实现的特殊物理和化学环境,使得一些在常温常压下很难甚至无法进行的化学反应得以发生.Zhou等[61]将NaN3作为还原剂,PCl5作为磷源,甲苯作为溶剂,通过溶剂热还原制备了直径约300 nm、壳厚约40 nm的中空多孔红磷纳米球(HPNs).其反应方程式为:10NaN3+2PCl5→2P+10NaCl+15N2.反应过程中生成的N2气体可以作为模板为红磷提供形核位点,而当温度冷却、压力降低后,被红磷壳包裹的N2气体被释放,形成了中空多孔纳米红磷球(图5(a)和(b)).当用作钠离子电池负极时,HPNs在520 mA·g-1循环 80 圈后仍能保持1364.7 mA·h·g-1的可逆比容量,2600 mA·g-1下循环600 圈后仍能保持 969.8 mA·h·g-1的可逆比容量(图5(c)).
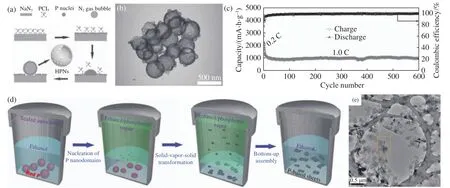
图5 (a)HPNs的生成机理图[61];(b)HPNs的 TEM 照片[61];(c)HPNs在 2.6 A·g-1下的循环性能图[61];(d)磷纳米片的生成机理图[62];(e)磷纳米片的TEM照片[62]Fig.5 (a) Schematic of the formation mechanism of HPNs[61]; (b) TEM image of HPNs[61]; (c) cycling performance of HPNs at a current density of 2.6 A·g-1[61]; (d) schematic of the formation of phosphorus nanosheets[62]; (e)TEM image of phosphorus nanosheets[62]
Zhang等[62]将商用红磷作为磷源,乙醇作为溶剂进行溶剂热反应.在400 °C、5.07 MPa的超临界状态下,红磷不断的升华—冷凝,持续的固-气-固转变促使孤立的磷纳米畴形成临界晶核,并进一步的通过自下而上的组装形成磷纳米片(图5(d)和(e)).所形成的纳米片主要由无定形红磷、黑磷以及磷的氧化物组成,多孔且薄(<5 nm),表现出良好的电化学性能[62].然而,此方法需要将乙醇密闭加热至400 °C,条件严苛且危险,限制了其实际应用.
与之相似的是以水作为溶剂,在200 °C下水热反应24 h,也可以制备红磷纳米颗粒(RPQDs)和具有网状结构的红磷纳米线(RPNWs).当与rGO进行复合后,RPQDs/ rGO复合电极表现出约900 mA·h·g-1的可逆比容量和良好的循环性能[63].作者对RPQDs和RPNWs形成机理的解释与Zhang等相同,但是我们认为这可能是一种类似文献中提到的水刻蚀机理[64].一方面,红磷与水中的氧反应生成磷的氧化物,并进一步与水反应生成磷酸.另一方面,红磷可以直接和水反应生成磷酸和PH3气体[65].这首先造成大块红磷被腐蚀成多孔结构,并进一步的溶解、破碎成RPQDs和RPNWs.
相比于球磨法和升华冷凝法,溶剂热法可以制备形貌特殊的纳米红磷,制备过程也较为简单.然而,较高的反应温度和压力以及较低的产率极大地限制了该技术的实际应用.
3.2 化学沉淀
相比于其他纳米材料制备方法,化学沉淀法制备成本低、方法简单快捷、易于工业化生产.目前化学沉淀法制备纳米红磷主要有两个方向:(1)基于含磷化合物的还原反应;(2)基于单质磷在溶剂中的溶解沉淀.
2017年,Chang等[66]首先找到了一种通过液相法大规模制备纳米红磷的方法.他们发现,PI3可以溶解在碘苯溶液中形成均匀溶液,将这一溶液加入到含有十六烷基三甲基溴化铵(CTAB)的乙二醇溶液中,可以在几秒钟内沉淀出球型度良好、粒径 100~150 nm 的纳米红磷颗粒(RPNPs)(图6(a)~(c)).与此同时,少量的碘离子可以掺杂到红磷中,显著提高纳米红磷的导电率,使其导电性接近半导体锗(图6(d)).纯的RPNPs电极表现出良好的循环稳定性(图6(e)),PRNPs的产率可达20%,并且制备工艺便于放大,表现出不错的实用前景.
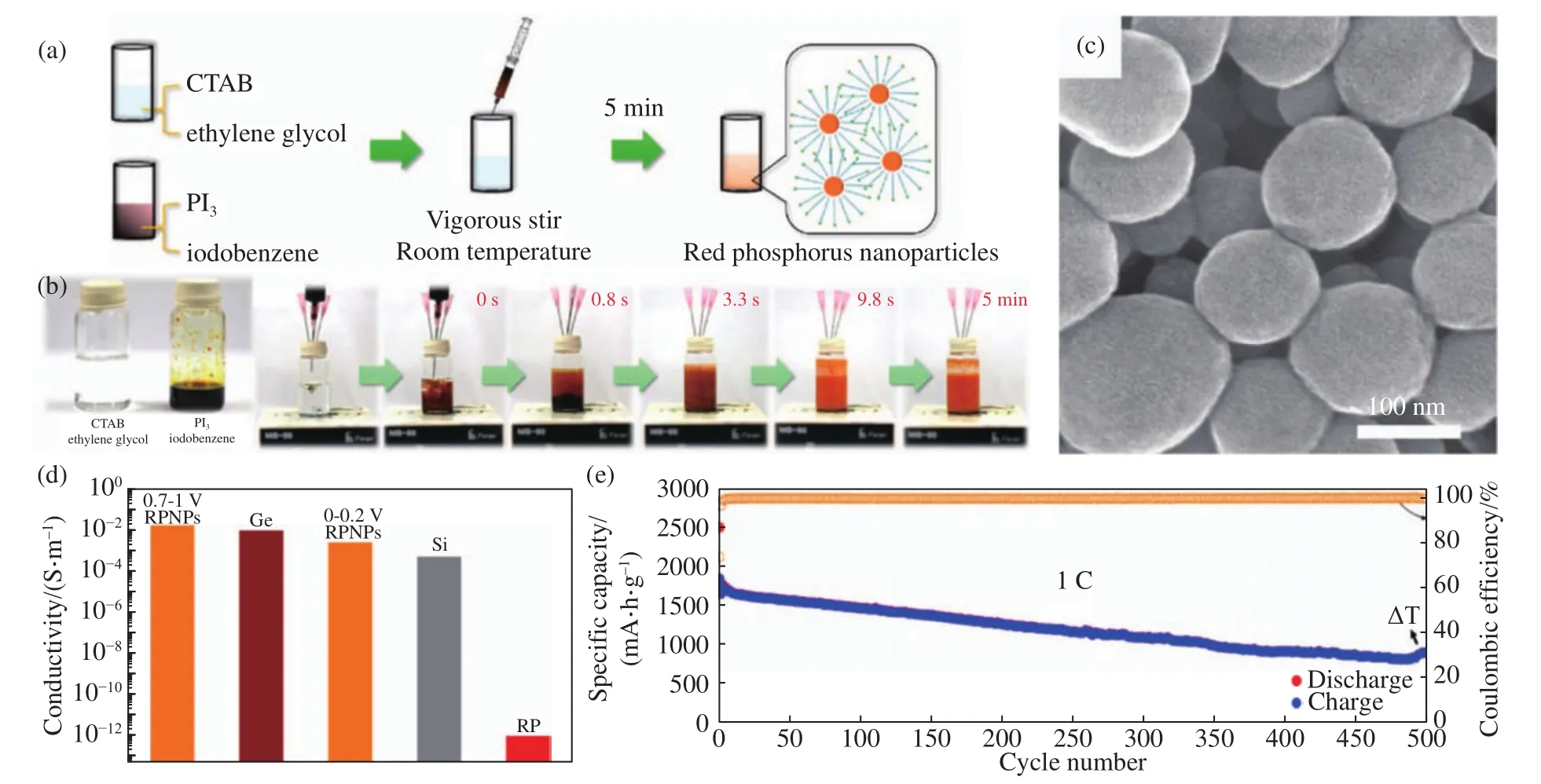
图6 (a, b)RPNPs的制备示意图;(c)RPNPs的 SEM 照片;(d)Ge、Si、RPNPs以及 RP 的电导率;(e)RPNPs在 2 A·g-1下的循环性能图[66]Fig.6 (a, b) Schematic of the synthesis of RPNPs; (c) SEM image of RPNPs; (d) conductivity of Ge, Si, RPNPs, and RP; (e) cycling performance of RPNPs at a current density of 2 A·g-1[66]
基于这一方法,多孔纳米红磷[67],中空纳米多孔红磷[68],多孔道纳米红磷[69]也被制备出来.其中,Liu等[67]在CTAB中加入氧化石墨烯(GO),并在氨水还原后得到RP@rGO.离心后将浸入在碘苯、乙二醇和氨水混合残液中的RP@rGO真空干燥,溶液沸腾产生气泡,rGO表面的红磷颗粒依附于气泡自发组装形成多孔纳米红磷(NPRP),形成的NPRP@rGO复合材料在173.26 mA·g-1下循环150 圈后任保持 1249.7 mA·h·g-1的可逆比容量,并表现出良好的倍率性能.
与上述方法相似,将PCl3加入到HSiCl3-Pr3NCH2Cl2的混合溶液中,也可以在几秒内快速地沉淀出纳米红磷颗粒[70].与使用PI3的制备方法相比,该方法制备的纳米红磷的球型度较差,但是尺寸更小(50~100 nm)、产率更高(38%).且与 PI3相比,PCl3的价格低廉,更适合工业生产.
基于PI3和PCl3的方法可以批量制备纳米红磷,然而其产率仍然偏低.且PI3价格昂贵、易水解,HSiCl3极易燃、易爆,限制了以上两种方法的实际应用.磷—胺法则较好的避免了这些问题.2019年, Li等[71]首先报道了胺可以诱导白磷相转变至红磷和黑磷.伯胺和叔胺可以通过自我电离产生胺基阴离子,胺基阴离子作为亲核试剂攻击白磷分子的3d未占满轨道,使得P-P键断裂,生成四面体的磷胺阴离子.作为中间体的四面体磷胺阴离子可以继续作为亲核试剂攻击白磷分子,生成聚磷阴离子.当使用H+中和多余的胺之后,聚磷阴离子沉积下来生成无序的纳米磷,而通过控制加热的时间可以获得不同结构的纳米磷.
不久后,Liu等[72]发现也可以通过将红磷溶解在乙二胺(EN)中制备纳米红磷(图7(a)和(b)).通过控制加入H+的浓度,可以调节纳米红磷颗粒的生成速率和粒径大小,且产率高达80%.使用rGO作为基体材料,5~10 nm的纳米红磷颗粒可以均匀沉积在rGO的表面,在降低纳米红磷粒径的同时增强其电子传导,改善其电化学性能(图7(c)和(d))[72].利用碳纳米笼(CNCs)作为基体材料,拥有85.3%超高红磷负载量的RP@CNC复合材料,在5000 mA·g-1下循环1300 圈后仍能保持750 mA·h·g-1的可逆比容量,容量保持率超过80%,表现出优异的循环稳定性和倍率性能(图7(e)~(g))[73].
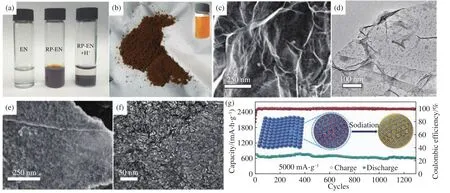
图7 (a)EN溶液、RP-EN溶液、RP-EN溶液混合稀HCl的光学照片[72];(b)NRP粉体和NRP胶体的光学照片[72];(c)NRP-rGO的SEM照片[72];(d)NRP-rGO 的 TEM 照片[72];(e, f)RP@CNC 的 SEM和TEM 照片[73];(g)RP@CNCs在 5 A·g-1下的循环性能图[73]Fig.7 (a) Photographs of the EN solution, RP-EN complex solution, and RP-EN complex mixed with dilute hydrochloric acid[72]; (b) photographs of the NRP powder and NRP colloid[72]; (c) SEM image of NRP-rGO; (d) TEM of NRP-rGO[72]; (e, f) SEM and TEM images of RP@CNC[73]; (g) cycling performance of RP@CNC at a current density of 5 A·g-1[73]
相较于其他方法,化学沉淀是最有潜力的纳米红磷的制备方法.其中,基于含磷化合物还原反应的方法,具有前处理时间短、无须加热、制备周期短等优势.但其产率较低、原料价格昂贵、化学性质活泼,这些影响了该方法的广泛应用.基于磷—胺法的溶解沉淀技术路线具有产率高(80%)、制备过程安全、便捷,原料成本低等优势.但该方法主要问题在于以白磷作为原料极度危险,制备过程中磷的溶解缓慢、制备周期长.
4 总结与展望
红磷作为钠离子电池负极材料,有着极高的理论比容量、合适的氧化还原电位以及丰富的资源储量,可以大幅度提升钠离子电池能量密度,是极具潜力的钠离子电池负极材料.纳米化,作为制备红磷负极材料的关键一环,是缩短钠离子传输路径、改善红磷倍率性能,减小红磷体积效应、实现长期循环稳定的重要手段.纳米红磷的制备方法包括球磨、升华冷凝、热还原、气相生长、溶剂热、化学沉淀等,各方法均有优势和不足.未来针对红磷纳米化的研究可以围绕以下几个方面开展:(1)提升复合材料中的磷含量以提升电极材料整体的能量密度.尤其针对升华冷凝法,其磷含往往低于50%,可着重寻找合适的基体材料或对基体材料进行表面改性以提升磷载量.(2)注重结构设计,将纳米化和结构设计结合起来,以共同改善电极的电化学性能.尤其针对纳米红磷较低的首次库仑效率,应更注重结构设计的实用化.(3)化学沉淀法未来应重点关注.一方面可以着重研究基于廉价且稳定的磷氯化物(如PCl3、PCl5)的还原法,以代替昂贵的磷碘化物.另一方面可重点关注强极性溶剂[74]和亲核试剂[75]的选择,以缩短磷的溶解时间,提高磷-胺法的制备效率.

