吡非尼酮早期干预特发性肺纤维化的疗效和安全性评估
夏泽海 吕群


[摘要]目的評估吡非尼酮早期干预特发性肺纤维化(IPF)的疗效和安全性。方法回顾性分析2016年1 月至2019年8月在杭州师范大学附属医院接受治疗的40例 IPF 患者的临床资料,其中接受吡非尼酮治疗的20例 IPF 患者为吡非尼酮组,未接受吡非尼酮治疗的20例 IPF 患者为对照组。随访观察治疗6、12个月后吡非尼酮组及对照组患者的临床数据,观察吡非尼酮的疗效及不良反应。结果治疗6、12个月后,两组 FVC、DLCO 占预计值百分比与治疗前比较,差异无统计学意义(P >0.05),而对照组6 min 步行距离与治疗前比较有所降低(P <0.05),吡非尼酮组6 min 步行距离与治疗前比较,差异无统计学意义(P >0.05)。治疗6个月后,吡非尼酮组的 FVC、DLCO 占预计值百分比及6 min 步行距离高于对照组,差异有统计学意义( P <0.05);治疗12个月后,吡非尼酮组的 FVC、DLCO 占预计值百分比及6 min 步行距离高于对照组,差异有统计学意义(P <0.05)。吡非尼酮组患者在12个月治疗期间共有9例(45.00%)患者出现1种及以上轻中度不良反应,所有患者均未停药。结论随访12个月,口服吡非尼酮能够减缓 IPF 患者肺功能下降以及6 min 步行距离的减少速度,并具有较好的耐受性。
[关键词]特发性肺纤维化;吡非尼酮;不良反应;安全性
[中图分类号] R563 [文献标识码] A [文章编号]2095-0616(2022)07-0012-05
Efficacy and safety evaluation with pirfenidone in early intervention of idiopathic pulmonary fibrosis
XIA Zehai LV Qun2
1.School of Medicine, Hangzhou Normal University, Zhejiang, Hangzhou 310015, China;2.Department of Respiratory Medicine, the Affiliated Hospital of Hangzhou Normal University, Zhejiang, Hangzhou 310015, China
[Abstract] Objective To evaluate the efficacy and safety of early intervention with pirfenidone in idiopathic pulmonary fibrosis (IPF). Methods A retrospective analysis was performed on the clinical data of 40 IPF patients with who received treatment at the Affiliated Hospital of Hangzhou Normal University from January 2016 to August 2019, 20 IPF patients with who received pirfenidone as the pirfenidone group and 20 IPF patients were not treated with pirfenidone as the control group. The clinical data of the patients in the pirfenidone group and the control group after 6 and 12 months of treatment were followed up to observe the efficacy and adverse effects of pirfenidone. Results After 6 and 12 months of treatment, the percentages of FVC and DLCO in the two groups were not significantly different from those before treatment (P >0.05), while the 6-minute walking distance in the control group decreased compared with that before treatment (P <0.05), the 6-minute walking distance in the pirfenidone group was not significantly different from that before treatment (P >0.05). After 6 months of treatment, the percentages of FVC, DLCO and 6-minute walking distance in the pirfenidone group were higher than those in the control group, and the differences were statistically significant (P <0.05). The percentages of FVC, DLCO and 6-minute walking distance in the group were higher than those in the control group, and the difference was statistically significant (P <0.05). A total of 9 patients (45.00%) in the pirfenidone group had one or more mild to moderate adverse reactions during the 12-month treatment period, and all patients did not stop taking the drug. Conclusion At 12-month follow-up, oral pirfenidone was able to reduce the decay speed of lung function and the reduce speed of 6-minute walk distance of IPF patients, with a good tolerance.
[Key words] Idiopathic pulmonary fibrosis; Pirfenidone; Adverse events; Safety
特发性肺纤维化(idiopathic pulmonary fibrosis, IPF)是一种病因不清、慢性进展性的纤维化性间质性肺炎,患者以呼吸困难及肺功能障碍为主要临床表现[1-3]。临床主要采用胸部高分辨率计算机断层扫描(high resolution computed tomography, HRCT)对 IPF 进行诊断,若影像学表现为间质性肺疾病的临床特征,不具特异性,则需行肺活检进一步诊断。吡非尼酮可抑制转化生长因子-β等炎性因子合成,达到抑制成纤维细胞增殖和胶原合成的效果[4]。研究显示[5-6],吡非尼酮能够延缓轻中度 IPF 患者肺功能减退速度,对控制疾病进展起到一定作用,且可能对重度 IPF 患者具有同样的治疗效果。随机对照研究能够提供可靠的临床证据,但其需进行严格的质量控制,无法准确反映医疗技术的真实效果。本研究对 IPF 患者使用吡非尼酮治疗12个月的疗效和安全性进行分析,为吡非尼酮治疗 IPF 提供依据。
1资料与方法
1.1 一般资料
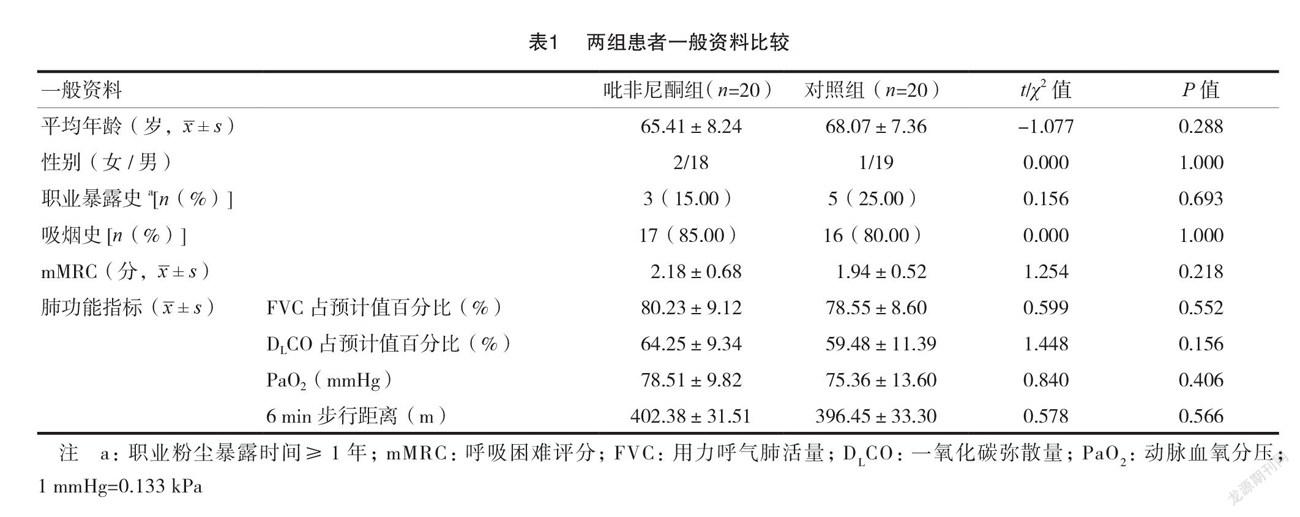
回顾性分析2016年1月至2019年8月在杭州师范大学附属医院接受治疗的40例 IPF 患者的临床资料,其中接受吡非尼酮治疗的20例 IPF 患者为吡非尼酮组,未接受吡非尼酮治疗的20例 IPF 患者为对照组。吡非尼酮组年龄58~84岁,对照组年龄53~79岁。两组的一般资料比较,差异无统计学意义(P >0.05),具有可比性。见表1。本研究为回顾性研究,已由医院医学伦理委员会批准通过。纳入标准:①年龄18~80岁,男女不限;②符合特发性肺纤维化诊断标准[7]。排除标准:①对吡非尼酮成分过敏或无法耐受者;②其他因素引起的间质性肺炎;③既往使用吡非尼酮时间>30 d 者;④合并严重心功能、肝肾功能障碍及其他重要脏器损害者;⑤因各种原因不能长期规律服药且按时复查者。
1.2 方法
所有入组患者均行肺功能检查、胸部 HRCT、动脉血气分析以及6 min 步行试验(表1)。所有患者在治疗6、12个月后返院复查肺功能、胸部 HRCT 和6 min 步行试验。对照组给予止咳、平喘、吸氧等对症治疗,吡非尼酮组在此基础上,加用口服吡非尼酮(北京康蒂尼药业有限公司,国药准字 H20133376,规格:100 mg)治疗,以900 mg/d 为初始剂量,2~4周内根据患者耐受程度增加剂量至1200~1800 mg/d,所有患者均建议规律口服吡非尼酮12个月。在吡非尼酮治疗期间,发生药物不良反应、疾病进展及其他等情况者,可减少剂量或停止服药,经医生评估后可再次使用吡非尼酮,注意需严谨使用药物。
1.3 观察指标及评价标准
参照《特发性肺纖维化诊断和治疗中国专家共识》[7]中的诊断标准判定 IPF 急性加重和病情进展。两组患者均至医院随访,1次/6个月,复查临床症状和肺功能指标及6 min 步行距离,同时观察并记录吡非尼酮相关不良反应,并予以相应措施进行处理。①肺功能指标:两组患者采用德国格莱特Spirostik Complete 型肺功能仪行肺功能检查,包括用力呼气肺活量(forced expiratory vital capacity, FVC)占预计值百分比、一氧化碳弥散量(carbon monoxide dispersion, DLCO)占预计值百分比。②6 min 步行距离:两组患者在平坦路面上,根据自身正常速度持续行走6 min,每隔1 m 作一个标记,记录患者6 min 内行走的距离。③记录吡非尼酮组患者出现的不良反应,包括消化系统(上腹部不适、肝功能不全)、皮肤(日光性皮疹、皮肤瘙痒)、全身症状(乏力、消瘦)不良反应,并计算不良反应发生率。
1.4 统计学方法
使用 SPSS 23.0统计学软件进行分析。正态分布的计量资料以均数±标准差(x ± s)表示,采用 t 检验。计数资料以[n (%)]表示,采用χ2检验。 P <0.05为差异有统计学意义。
2结果
2.1 两组患者治疗前后肺功能和6 min步行距离比较
治疗6、12个月后,两组 FVC、DLCO 占预计值百分比与治疗前比较,差异无统计学意义(P >0.05),而对照组6 min 步行距离与治疗前比较有所降低,差异有统计学意义(P <0.05),吡非尼酮组6 min 步行距离与治疗前比较,差异无统计学意义(P >0.05);治疗6个月后,吡非尼酮组的 FVC、DLCO 占预计值百分比及6 min 步行距离高于对照组,差异有统计学意义(P <0.05)。治疗12个月后,吡非尼酮组的 FVC、DLCO 占预计值百分比及6 min 步行距离高于对照组,差异有统计学意义(P <0.05)。在观察期内,两组均未出现患者病死的情况。见表2。
2.2 两组患者IPF急性加重和病情进展比较
吡非尼酮组出现急性加重1名,为吡非尼酮治疗10个月后出现急性加重,对照组出现 IPF 急性加重3例,从基线治疗到出现急性加重的时间为8.5(8~11)个月,差异无统计学意义(χ2=0.278, P=0.598)。吡非尼酮组出现病情进展2例,对照组出现病情进展4例,差异无统计学意义(χ2=0.196, P=0.658)。
2.3 吡非尼酮组疗效分层分析
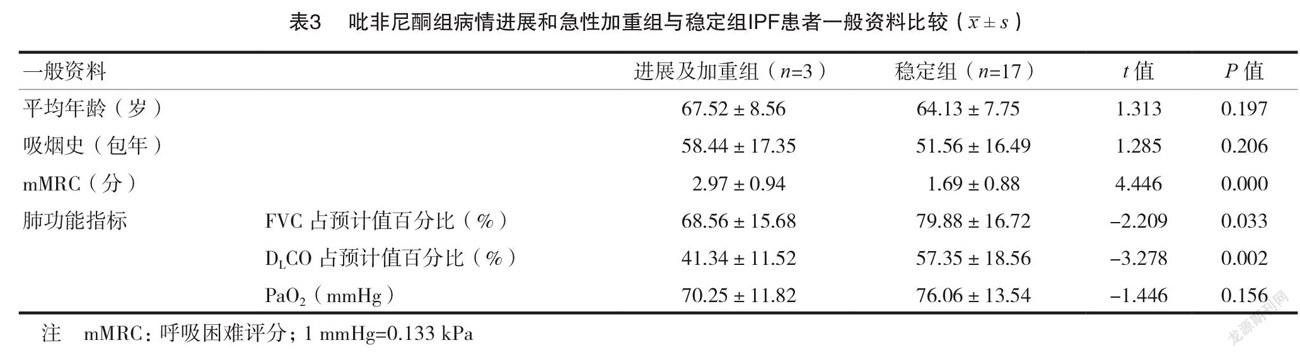
随访过程中,口服吡非尼酮期间有1例 IPF 患者出现急性加重,其运动耐力显著降低,血气分析提示低氧血症;2例患者胸部 HRCT 提示肺纤维化较基线进展,无急性加重表现,考虑疾病进展。3例病情进展和急性加重患者的年龄、吸烟包年和 PaO2同其余病情稳定者比较,差异均无统计学意义(P >0.05),而两组呼吸困难评分(modified British medicalresearch council,mMRC)、FVC 占预计值百分比、DLCO 占预计值百分比比较,差异均有统计学意义( P <0.05)。见表3。
2.4 吡非尼酮不良反应情况及处理措施
吡非尼酮组共有9例患者出现不同程度的不良反应,其中5例出现1种不良反应,2例出现2种不良反应,且有2例出现3种不良反应,大多数为轻中度不良反应,在接受相应的处理措施后均未中断治疗。在不良反应中发生率最高的为消化系统不良反应,6例患者出现上腹部不适,表现为服药后轻微腹痛、恶心等症状,程度可耐受,对此类患者建议采用餐中口服的给药方式;1例患者出现肝功能不全,口服护肝药物后复查正常。共发生5例皮肤相关不良反应,其中3例患者出现日光性皮炎,建议患者采用遮阳帽、防晒霜、穿长袖衣物等措施避免阳光直射。3例患者出现全身症状,如头晕,乏力等,建议患者观察随诊,并给予相应对症处理。见表4。
3讨论
IPF 是一种慢性进行性疾病,其以纤维化组织在肺实质中异常积聚为特征,总体预后不良[8],但随着过去几十年中,对 IPF 病理生物学的理解取得重大进展,诊断过程的标准化和延缓疾病进程治疗的可及性, IPF 的前景发生了极大逆转。尽管仍然难以达到对 IPF 致病机制的全面理解,但不断地研究仍使医务工作者对其的理解更进一步。吸烟是 IPF 的一个危险因素,会导致自我维持的肺损伤,因此在戒烟后,其仍被视为 IPF 的危险因素。此外,与不吸烟者相比,有吸烟史的 IPF 患者中位生存期为3~5年,5年生存率仅为20%~40%[9]。本研究纳入的多数 IPF 患者均有吸烟史,比例达75%。 IPF 与农业、牲畜业、木屑和石头、沙子和二氧化硅之间显著相关。本研究入组 IPF 患者中,20%(8/40)有职业暴露史。病毒、真菌及细菌等病原菌均与 IPF 发病具有一定关系。
自1993年进行第一次试验以来, IPF 的药理治疗领域发生了重大变化,反映出对其发病机制的理解、诊断标准的标准化以及大型随机对照研究设计的改进。因针对炎症和免疫反应或干扰凝血药物的安全性和有效性的大量证据,导致在 IPF 治疗临床实践指南的最新更新中强烈建议不要使用该药物。而吡非尼酮经随机对照研究证实能够改变 IPF 自然病程,得到指南推荐使用的吡非尼酮是一种口服吡啶,能够下调转化生长因子-β的表达及活性,对成纤维细胞的增殖有抑制作用,还能抑制胶原的合成[10]。有研究表明吡非尼酮通过调节Wnt/GSK-3β/β-catenin 和 TGF-β1/Smad2/3这两条信号通路来减轻肺纤维化[11]。多项研究证实吡非尼酮对 IPF 患者的有益作用,接受吡非尼酮治疗后,患者相关肺功能指标均得到改善[12-13]。本研究结果显示,经吡非尼酮治疗6、12个月后,吡非尼酮组患者 FVC、DLCO 占预计值百分比及6 min 步行距离未出现下降,并得到了一定程度的提高,尤其在治疗的最初6個月。在吡非尼酮治疗期间,发生疾病进展和急性加重的 IPF 患者,呈现出肺功能差、活动耐力低、呼吸困难等表现,同时大多数 IPF 患者对该药物具有良好的耐受性。Russll等[14]研究结果显示,FVC 占预计值百分比可作为 IPF 死亡预测的指标,当其降低幅度≥10%时,患者的病死风险明显增加,故可用于 IPF 疾病进展的评价。另外,有研究指出[15],吡非尼酮可减缓 FVC 下降速度,并在1年内将病死风险降低48%。本研究结果显示,吡非尼酮组患者与对照组相比,在经过6、12个月的规范干预后,其 FVC 占预计值百分比较基线明显升高,与雷凯春等[16-17]的研究结论相一致。
已有临床实践表明[18],吡非尼酮可减缓 IPF 患者肺功能指标下降速度,在使用该药物后,患者可获得更长的疾病无进展生存期,但对其是否可以减少患者急性加重,目前临床尚无统一定论。本研究结果显示,吡非尼酮组 IPF 急性加重发生率为5%,低于对照组的15%。Nathan 等[19]的报道显示,FVC 水平与疾病进展密切相关,其水平越高,患者出现疾病进展的次数越多,病死率越高。此外,本研究结果显示,在吡非尼酮治疗期间,发生疾病进展和急性加重的 IPF 患者,其呼吸困难症状严重,肺功能明显减退,进一步佐证了上述研究结论。
6 min 步行试验可用于心肺功能及体能状况的评估,因其实用且实施方便等优点,得到了广泛的应用。6 min 步行距离是评估 IPF 患者病死率的临床常用指标,若其结果减小及行走过程中患者血氧饱和度下降,则说明 IPF 患者临床预后较差,病死风险较高[20]。本研究结果显示,吡非尼酮组治疗6、12个月后其6 min 步行距离的缩短较对照组减缓,差异有统计学意义(P <0.05)。
吡非尼酮具有良好的长期安全性和耐受性。一项大型(n=1299)且定义明确的 IPF 患者队列综合安全性分析[21]提示,吡非尼酮具有良好的耐受性,以胃肠道和皮肤不良反应较为常见。大多数不良反应发生在治疗的前6个月内,严重程度一般为轻度至中度。胃肠道和皮肤相关不良反应的发生率在治疗6个月后下降。多数病例的不良反应通过不同的策略可以控制。本研究中,吡非尼酮组共有9例(45%)患者出现不同程度的不良反应,但大多数为轻中度不良反应,在接受相应的处理措施后均得到控制并继续治疗,体现出吡非尼酮良好的安全性。
本研究仍存在一定不足,为单中心非随机的病例对照研究,纳入样本例数相对较少,且观察时间较短等,可能存在数据偏倚,研究结论的可靠性需进一步验证。IPF 患者通常伴有其他疾病,需采取不同治疗方案,同时,合并用药情况复杂,可能也会对吡非尼酮的应用造成一定影响,导致研究结果出现误差。当下,吡非尼酮仅能维持现状或延缓肺功能减退,并不能从根本上控制 IPF 的疾病发展,更无法逆转 IPF 的病理改变。随着对 IPF 疾病本质的进一步深入,可为未来开发有效药物提供科学依据,而有效药物的开发能在一定程度上控制 IPF 病情发展,并对提高患者生存质量及降低其病死率有较大的帮助。
[参考文献]
[1]董秀,解染,李若茗,等.吡非尼酮治疗特发性肺纤维化的快速卫生技术评估[J].中国新药杂志,2020,29(20):2389-2394.
[2]陈乾,熊旭东.免疫细胞在特发性肺纤维化中的研究进展[J].中国现代应用药学,2018,35(10):1586-1590.
[3]方楚玲,徐作军.特发性肺纤维化的细胞和分子生物学标志的研究进展[J].中华结核和呼吸杂志,2018,41(4):303-307.
[4]吕紫薇,黄凯,甘文华,等.吡非尼酮和尼达尼布抑制博来霉素诱导的小鼠肺纤维化药效比较[J].中国病理生理杂志,2020,36(1):112-118.
[5] Maher TM,Lancaster LH,Jouneau S, et al.Pirfenidonetreatment in individuals with idiopathic pulmonary fibrosis: impact of timing of treatment initiation[J].Ann Am Thorac Soc,2019,16(7):927-930.
[6]王春彬,张爽,张倩,等.两种新型抗纤维化药物治疗特发性肺纤维化的研究进展[J].中国药学杂志,2019,54(9):682-686.
[7]中华医学会呼吸病学分会间质性肺疾病学组.特发性肺纤维化诊断和治疗中国专家共识[J].中华结核和呼吸杂志,2016,39(6):427-432.
[8] Sgalla G,Iovene B,Calvello M,et al.Idiopathicpulmonary fibrosis: pathogenesis and management[J]. Respir Res,2018,19(1):32.
[9]杜开锋,张来,贺红梅,等.3D-胸部 CT 估算肺纤维化程度在特发性肺纤维化预后分析中的应用[J].复旦学报(医学版),2021,48(2):217-223.
[10]郑小兵,金琳羚,黄文,等.进展性纤维化性间质性肺疾病与抗纤维化治疗[J].中华结核和呼吸杂志,2021,44(6):569-573.
[11] Lv Q,Wang J,Xu C,et al.Pirfenidone alleviatespulmonary fibrosis in vitro and in vivo through regulating Wnt/GSK-3β/β-catenin and TGF-β1/Smad2/3 signaling pathways[J].Mol Med,2020,26(1):49.
[12] Marcos Ribes B,Sancho-Chust JN,Talens A, et al.Effectiveness and safety of pirfenidone for idiopathic pulmonary fibrosis[J].Eur J Hosp Pharm,2020,27(6):350-354.
[13]梁丽萍.吡非尼酮治疗特发性肺纤维化急性加重期对患者肺功能及预后的影响[J].中国医药科学,2020,10(13):210-212,216.
[14] Russll AM,Adamali H,Mlyneanx PL, et al.DailyHomeSpirometry: An Effective Tool for Detecting Progression in Idiopathic Pulmonary Fibrosis[J].Am JRespir Crit Care Med,2016,194(8):989-997.
[15] Song MJ,Moon SW,Choi JS,et al.Efficacy of lowdose pirfenidone in idiopathic pulmonary fibrosis: real world experience from a tertiary university hospital[J]. Sci Rep,2020,10(1):21218.
[16]雷凯春,岳红梅,周婷婷.吡非尼酮治疗特发性肺纤维化的临床疗效及不良反应[J].中国新药与临床杂志,2018,37(3):160-163.
[17] Krauss E,Tello S,Wilhelm J,et al.Assessing theEffectiveness of Pirfenidone in Idiopathic Pulmonary Fibrosis : Long-Term , Real-World Data from European IPF Registry (eurIPFreg)[J].J Clin Med,2020,9(11):3763.
[18]闫永吉,范亚丽,余诗雯,等.吡非尼酮治疗特发性肺纤维化疗效及安全性的单中心真实世界研究[J].中华结核和呼吸杂志,2018,41(5):327-332.
[19] Nathan SD,Costabel U,Glaspole I,et al.Efficacyof Pirfenidone in the context of multiple disease progression events in patients with idiopathic pulmonary fibrosis[J].Chest,2019,155(4):712-719.
[20]沈沁雪,彭紅.特发性肺纤维化病情的临床评估[J].中南大学学报(医学版),2021,46(3):309-315.
[21] Lancaster L,Albera C, Bradford WZ, et al.Safetyof pirfenidone in patients with idiopathic pulmonary fibrosis: integrated analysis of cumulative data from 5 clinical trials[J].Bmj Open Respiratory Research,2016,3(1):e000105.
(收稿日期:2021-12-06)

