Li3PS4固态电解质的研究进展
魏超超,余 创,吴仲楷,彭林峰,3,程时杰,谢 佳
(1华中科技大学电气与电子工程学院强电磁工程与新技术国家重点实验室;2华中科技大学化学与化工学院;3华中科技大学物理学院,湖北 武汉 430074)
二次锂离子电池具有高能量/功率密度、低成本和长循环寿命等特点,被广泛应用于电动汽车、智能电网、备用电源(UPS)等领域[1-3]。但是随着电动汽车及规模化储能领域的快速发展,市场对电池安全性、能量密度提出了更高的要求。相比液态锂离子电池,全固态锂离子电池在安全性方面具有明显的优势,成为了动力电池和电化学储能技术领域的研究热点[4-6]。固态电解质的不易燃性和稳定性是实现全固态锂离子电池高安全性的关键,也是推进全固态锂离子电池技术发展的保证[7-8]。目前研究较多的固态电解质主要是聚合物电解质[9]和无机固态电解质[10]。聚合物电解质具有高安全性、力学柔性等优点,但其较低的室温离子电导率、较窄的电化学窗口、较低的离子迁移数以及负极侧对锂金属稳定性较差等缺点,限制了该类电解质在高性能全固态锂离子电池领域的应用[11]。相比较而言,无机固态电解质更具优势,不但拥有更高的室温离子电导率且热稳定性更好。常见的无机固态电解质有氧化物[12]、硫化物[13-14]、磷酸盐[15]、氮化物[16]、氢化物[17]和卤化物固态电解质[18]等,其中硫化物固态电解质因其超高的室温锂离子电导率(约10-2S/cm)[4,19],且电化学窗口宽、机械加工性能好等优点成为固态电解质领域的研究重点[20-22]。根据硫化物固态电解质的原料组成可将其分为二元硫化物和三元硫化物电解质,目前研究较多的为前者。二元硫化物固态电解质主要有Li2S-P2S5[23-24]、Li2S-SiS2[25-26]、Li2S-GeS2[27-28]等 几类体系,它们在室温下的离子电导率较高、电化学窗口宽,成为硫化物固态电解质研究的热点[29]。
Li2S-SiS2体系中SiS2是由四面体[SiS4]组成的网络结构的共价化合物,当其与离子化合物Li2S发生化学反应时,可以产生更多供锂离子迁移的间隙数,因此Li2S-SiS2电导率较高,但是其与工业上常用的石墨负极材料的兼容性较差且Li2S-SiS2极易吸潮,化学稳定性较差。Li2S-GeS2硫化物固态电解质在空气中吸湿性不强,可以在一定程度上解决组装电池的难题,但是其室温离子电导率并不高,需要进行后续的掺杂改性[14]。而Li2S-P2S5虽然也存在其他硫化物电解质一样的弊端:空气稳定性较差,制备成本偏高,离工业化的生产与应用还有距离等,但是(100-x)Li2S-xP2S5是目前研究最多的硫化物电解质体系,其具有较高离子电导率、较低电子电导率、较宽的电化学稳定性窗口以及对金属锂和石墨负极稳定性相对较好等一系列优点,是深入研究硫化物固态电解质性能及应用的最佳选择[30]。而Li3PS4(x=25)具有较高的室温离子电导率(约10-4S/cm),且对锂金属负极兼容性较好,是被广泛关注的硫化物固态电解质之一[31]。
1 Li3PS4 电解质结构和锂离子传导机理
1.1 Li3PS4电解质的结构
Li3PS4电解质属于含硫快离子导体(thio-LISICON),包括α-Li3PS4、β-Li3PS4和γ-Li3PS4三种晶相[32-33](如图1)。α、β和γ三相间随温度变化而转变,室温时主要以γ-Li3PS4相存在,当温度上升到195 ℃时转变为β-Li3PS4相,随后在更高的温度(473 ℃)下转变为高温α-Li3PS4相,并且该相转变过程是不可逆的,其中β-Li3PS4相具有最高的室温离子电导率(约为10-4S/cm)。
1.2 Li3PS4电解质的离子传导机理
Li3PS4电解质内部锂离子的迁移构成了离子传导,其他离子组成传导锂离子的晶体框架,结构中的PS3-4四面体排布方式影响锂离子的迁移路径和通道,三种不同晶相的Li3PS4迁移路径不同,需要克服的迁移势垒也不同,导致锂离子电导率各不相同。如图1(a)所示,α-Li3PS4结构中有序的T+/T-四面体(T+代表PS3-4四面体顶点向上方向,T-代表PS3-4四面体顶点向下方向)相互隔离,分别沿[110]和[001]方向排列。而如图1(b),β-Li3PS4由六方密堆积的硫化物离子组成,PS3-4呈锯齿形排列,结构中包含两个Li+位点,这有利于促进间隙位的锂离子迁移,从而获得较高的锂离子电导率;γ-Li3PS4结构中的PS3-4四面体的所有顶点仅在同一方向呈有序排列,因此PS3-4彼此隔离而不利于锂离子迁移[图1(c)],相应的电导率较低[33]。

图1 几种晶体结构(a)α-Li3PS4;(b)β-Li3PS4;(c)γ-Li3PS4[28-29]Fig.1 Several crystal structures(a)α-Li3PS4;(b)β-Li3PS4;(c)γ-Li3PS4[28-29]
2 Li3PS4电解质制备方法
2.1 固相法合成
固相法是制备无机固态电解质最常用的方法[34],固相路径合成Li3PS4电解质主要有熔融淬火法[35-36]和高能球磨法[37]两种。熔融淬火法是指将Li2S与P2S5等原料混合后密封在内壁沉积有碳材料的石英管中,然后进行高温煅烧,而后在冰水中淬火。这种方法可以通过控制煅烧温度来制备不同玻璃态的硫化物电解质,但也存在以下缺点:①制备流程复杂,P2S5的蒸气压较高,必须在真空条件下密封的石英管中进行熔融;②条件苛刻,难以精确控制参与反应的原材料的比例,尤其是容易在淬火过程中产生杂质。Tachez等人[38]采用熔融淬火法成功合成了高离子电导率的β-Li3PS4,但发现该电解质在室温下难以稳定保存,制备的高电导率的β-Li3PS4容易转变为低电导率的γ-Li3PS4。相较而言,固相法合成的高离子电导的β-Li3PS4电解质主要采用高能球磨法制备[31,39]。高能球磨法相较于熔融淬火法具有很多优势,例如Li2S与P2S5反应原料在常温球磨过程中就会发生一系列包括高能研磨、混合、粉碎、非晶化和固态反应等复杂反应,合成出的β-Li3PS4固态电解质具有更高的室温离子电导率[38],并且该方法也可适用于其他组成的硫化物固态电解质,例如Li7P3S11[40]。但高能球磨法存在合成过程繁琐,热处理时易出现硫挥发造成化学计量偏差等问题。
2.2 液相法合成
固相合成路径存在能耗高、均匀性差、大规模制备困难等问题,液相合成法能较好地克服上述缺点。例如液相合成能耗较低、原子级别混合均匀性较好、有利于规模化制备等,且适用于对电极材料表面进行修饰改性,形成较好的固-固界面接触[41]。液相合成法主要分为悬浮液法和溶液法,前者通过在非质子溶剂中搅拌原料,如N-甲基甲酰胺(NMF)[42]、乙腈(ACN)[43]、乙酸乙酯(EA)[44]、四氢呋喃(THF)[45]和丙酸甲酯(MP)[46]等。Liu 等人[45]报道选取THF 作为溶剂制备的Li3PS4电解质具有高电导率且电化学稳定性优异。溶液法合成则是通过将材料溶解在质子溶剂中,如乙醇、乙二胺(EDA)等,形成透明的溶液,然后去除有机溶剂得到均匀混合的材料,经后续热处理得到最终的目标电解质。溶液法得到均匀的电解质溶液可应用于电极材料表面包覆,形成电解质包覆电极材料结构,该结构具有良好的固-固界面接触和锂离子传导动力学。乙醇常被用作溶液法合成硫化物固态电解质的溶剂[47],但是选取乙醇作为溶剂制备Li3PS4很困难,这是因为羟基会与原料P2S5中的P—S 键发生反应[48-49]。Ito 等[50]选择沸点较低(<150 ℃)的质子溶剂EDA作为分散介质,采用溶液法合成Li3PS4。EDA结构组成中不含易与原料发生副反应的羟基和氧,且能够提高产物Li3PS4电解质的锂离子电导率。溶剂的选择对于采用液相法合成的Li3PS4固态电解质的离子电导率影响较大,根据报道的结果总结如表1所示。

表1 不同有机溶剂合成Li3PS4电解质室温下离子电导率Table 1 Ionic conductivity of Li3PS4 electrolytes synthesized by different organic solvents
但是在通常情况下,Li3PS4电解质通过液相合成法制备的离子电导率普遍低于固相合成法,这主要是因为在液相合成过程中有机溶剂易残留在电解质表面降低其电导率[51]。针对固相及液相合成路径各自的优缺点,研究人员也在尝试探索其他合成Li3PS4电解质的新思路和新方法。例如Suto等人[52]利用微波辅助法快速制备出Li3PS4电解质,全过程只需耗时3小时,与传统球磨法耗时较长相比,大大缩短合成时间,提升了制备效率。
3 Li3PS4电解质改性研究
目前Li3PS4电解质实用化面临的主要问题有:对空气/水汽稳定性差、与电极材料的界面兼容性较差、电解质自身的电化学稳定性有待改善、室温离子电导率与有机电解液相差较大等。鉴于此,研究人员采取了多种策略对Li3PS4电解质上述理化性能进行了针对性改进。
3.1 离子电导率改善
(100-x)Li2S-xP2S5系硫化物固态电解质因具有较高的室温锂离子电导率而成为固态电解质的研究热点,但其离子电导率与当前有机电解液相差较大,并且随着电化学储能系统的快速发展,对于固态电池的倍率性能有了更高的要求,这就需要研究人员进一步提升固态电解质的离子电导率。当前,研究人员采取了不同的策略提高Li3PS4电解质的离子电导率,具体研究结果总结于表2。
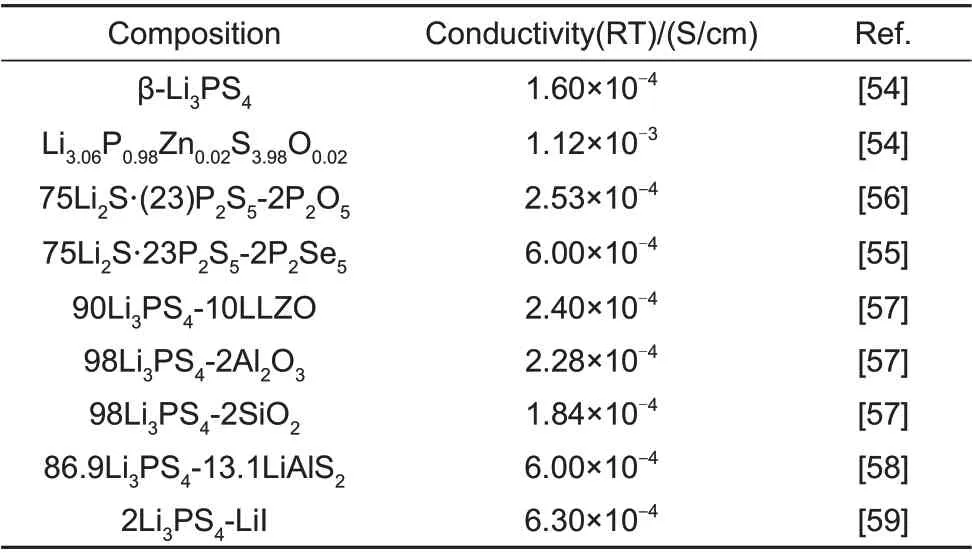
表2 Li3PS4电解质掺杂后离子电导率Table 2 Ionic conductivities of Li3PS4 sulfide electrolytes
研究发现用氧(O)或者硒(Se)部分取代硫(S)可以提高电解质的离子电导率。常见的向电解质结构中引入O 元素的方法有掺杂Li2O 和ZnO 等,这些掺杂能有效提高Li3PS4电解质的离子电导率。Xiao团队[53]通过系统的DFT研究表明,O掺杂最重要的作用是在其周围形成一个入口,它不仅降低了局部空位跳跃势垒,而且为b 位空位与d 位锂离子的交换创造了一条新的路径。几何空间的扩展和O掺杂周围势场的变化最终推动了Li3PS4离子导电结构行为从2D 向3D 的转变,进而增强了锂离子电导率[图2(a)]。Liu 等人[54]通过掺杂ZnO 得到组成为Li3.06P0.98Zn0.02S3.98O0.02的电解质,其室温离子电导率高达1.12×10-3S/cm,这主要得益于引入O原子导致Li3PS4的晶格增大,扩展了锂离子的传导路径。此外研究还发现在Li3PS4结构中掺杂离子半径更大的Se 得到的75Li2S·(25-x)P2S5-xP2Se5系列改性电解质,其最高室温离子电导率可达6×10-4S/cm[55]。其实氧化物除了可以通过利用O 掺杂的方式改善Li3PS4电解质离子电导率,还可以作为一种填料形式掺杂,与Li3PS4混合得到离子电导率更高的复合电解质,复合电解质同时受到空间电荷效应和阻塞效应双重影响,离子导电的氧化物与Li3PS4硫化物之间形成离子和电子点缺陷的空间电荷层,导致带电粒子的电阻减小,电解质的离子电导率增强,而阻塞效应会阻塞带电粒子迁移,导致电导率降低。Li 等人[56]通过研究P2O5掺杂量得到不同组成的75Li2S·(25-x)P2S5-xP2O5电解质,发现当x=0~5 时,电解质的锂离子电导率随P2O5掺杂量增加先上升后下降,当x=2时,改性的电解质达到最高室温离子电导率(2.53×10−4S/cm)[图2(b)],且通过XRD与拉曼光谱可以看出电解质结构并未发生变化[图2(c)、(d)]。Hood 等人[57]系统研究了三种不同的氧化物(Li7La3Zr2O12、Al2O3、SiO2)对Li3PS4电解质进行混料效果对比,如图2(e)所示,发现随混合比例的增加都会导致离子电导率先上升后下降,这其中受到的两种效应分别对应离子电导率上升和下降部位。因此采用控制引入的氧化物的类型及比例能实现对Li3PS4电解质离子电导率的提升。掺杂不仅可以产生点缺陷或间隙离子,而且还可以扩大锂离子的扩散通道,这些措施都有利于硫化物电解质的离子电导率提高。

图2 (a)β-Li3PS4中O驱动的从2D到3D传输行为转变以及O掺杂对Li界面稳定性的改善的示意图;(b)75Li2S·(25-x)P2S5-xP2O5中室温离子电导率和平均晶粒尺寸随x值的变化;(c)干燥的75Li2S·25P2S5样品和热处理的75Li2S·(25-x)P2S5-xP2O5(x=0,1,2,3,5 mol%)样品的XRD图谱;相应(d)拉曼光谱;(e)氧化物添加对Li3PS4(LPS)电解质的影响模型;“A”代表不添加氧化物;“B”代表空间电荷效应;“C”代表氧化物的阻塞效应Fig.2 (a)Schematic illustration of the O-driven transition from 2D to 3D transport behaviour in β-Li3PS4 and the improvement of the interfacial stability against Li by O doping,(b)The variation of room-temperature ionic conductivities and the average crystallite size with the value of x in 75Li2S·(25-x)P2S5-xP2O5,(c)Raman spectra and b the corresponding XRD patterns and(d)of the dried 75Li2S·25P2S5sample and heat-treated 75Li2S·(25-x)P2S5-xP2O5(x=0,1,2,3,5 mol%)samples,(e)Model for the oxide filler’s effect on the parent Li3PS4(LPS)electrolyte,‘A’represents the addition of no oxide filler,‘B’represents the space-charge effect,and‘C’shows the blocking effect of the oxide filler
除了上述氧化物掺杂外,还有一些硫化物掺杂,如Al2S3、NiS2、MoS2等也能提高(100-x)Li2SxP2S5系硫化物固态电解质的离子电导率。有报道就发现在(100-x)Li2S-xP2S5系电解质中存在非桥联硫抑制锂离子的扩散,通过Al2S3掺杂能够消除非桥联硫,形成(100-x)Li3PS4-xLiAlS2系列电解质,当x=13.1 时,86.9Li3PS4-13.1LiAlS2具备最高的锂离子电导率和最低的活化能[58]。
最近还有一些卤化物掺杂的报道,研究发现向Li3PS4固态电解质中引入卤化物也能够有效提高其室温离子电导率[35],Liang等人[59]通过在Li3PS4电解质中引入LiI,得到几组不同化学组分的硫化物电解质,其中组成为2Li3PS4-LiI 的电解质观察到新相Li7P2S8I 形成,它表现出Li3PS4和LiI 间的固溶体特征,且具有较高的室温离子电导率(6.3×10−4S/cm)和较宽的电化学稳定性窗口。研究表明,碘离子进入配位结构,不仅改善了电解质对正极的氧化稳定性,而且增强了对金属锂负极的稳定性,同时改善了电解质的界面动力学和离子电导率。
此外,从离子价态角度,研究发现较大离子半径的阳离子掺杂可以部分取代P5+的位置,也能提升Li3PS4离子电导率,阳离子掺杂分为同价阳离子掺杂与异价阳离子掺杂。目前Li3PS4电解质主要以异价阳离子掺杂为主,Kanno等人[60]采用Ge4+掺杂得到Li3.25Ge0.25P0.75S4,室温离子电导率高达2.20×10−3S/cm;已有报道的文献还有Zn2+[61]、Mo4+[62]等。Li3PS4同价阳离子掺杂也有一定的进展,例如许晓雄团队[63]成功将Sb5+掺杂到Li3PS4中,其中Li3P0.98Sb0.02S3.95O0.05电解质实现1.08×10−3S/cm 的高离子电导。
3.2 稳定性改善
稳定性是衡量固态电解质实用化前景的一个重要的参数。目前硫化物电解质的稳定性主要包括电解质对空气/水汽的稳定性和电解质对正负极材料的电化学兼容性。
3.2.1 空气/水汽稳定性改善
大多数硫化物电解质在空气中的稳定性较差,主要是因为硫化物电解质易与空气中的水分子发生化学反应,产生有毒的H2S气体,且反应会导致硫化物电解质结构破坏,离子电导率大幅下降,还可能引发一系列安全问题[64]。因此硫化物电解质制备和应用都必须在惰性气体氛围下处理,这也增加了其生产制造成本和应用的工艺复杂性,说明提高硫化物电解质对空气/水汽的稳定性是硫化物电解质实现商业化的关键问题。目前主要通过氧原子掺杂、金属氧化物混合和软酸原子取代等方式进行改善。
氧原子掺杂主要是在硫化物电解质体系中引入比桥键S 更稳定的非桥键O,Ohtomo 等人[65]利用Li2O 部分取代75Li2S·25P2S5中Li2S 来抑制H2S的产生。硫化物电解质暴露在空气中生成H2S气体的量被用来衡量电解质对空气的稳定性,生成的H2S气体越多,电解质在空气中越不稳定。在xLi2O·(75-x)Li2S·25P2S5体系中,随着Li2O 引入量的增加,暴露在空气中的改性电解质产生的H2S气体含量逐渐降低,相应的离子电导率也随之提高,所以为了提高硫化物电解质对空气/水汽的稳定性同时保持较高的离子电导率,研究人员分组研究对稳定性和电导率的影响,发现7Li2O·68Li2S·25P2S5具有较高的离子电导率(2.5×10−4S/cm)且产生的H2S含量最低。
Hayashi 等人[66]研究发现将Li3PS4电解质与金属氧化物MxOy(M=Fe,Zn 和Bi)混合能够吸收副反应产生的H2S气体,进而提高电解质暴露在潮湿空气中的化学稳定性,具体反应机理如下

研究人员将Li3PS4电解质暴露在干燥的氧气和氮气氛围中,结果显示Li3PS4电解质在干燥空气中很稳定,并未检测到H2S气体的产生,表明硫化物电解质并不会与氧气或氮气发生反应[图3(a)];随后将掺杂金属氧化物的Li3PS4电解质长时间暴露于空气中,发现吉布斯自由能(△G)越负的金属氧化物对H2S的吸附效果越好,对电解质化学稳定性改善效果越明显。通过使用气相色谱法准确定量测定反应体系生成的H2S[图3(b)],发现三种金属氧化物中Bi2O3(ΔG=-232.0 kJ/mol)反应的吉布斯自由能最小,所生成的H2S气体最少,对Li3PS4电解质的稳定性改善效果最佳。实验发现虽然ZnO(ΔG=-78 kJ/mol)体系没有特别低的吉布斯自由能,但是根据软硬酸碱理论,其对酸性气体H2S也有很好的吸附效果,因此对Li3PS4电解质的稳定性改善也有很好的效果。研究人员经过优化ZnO与Li3PS4电解质掺杂比例得到最佳组成为90Li3PS4-10ZnO 的复合电解质,其在潮湿空气中长时间暴露后复合电解质的电导率基本不变,证明ZnO能有效改善Li3PS4电解质的稳定性[图3(c)]。此外,应用该90Li3PS4-10ZnO电解质构筑的全固态电池显示出优异的倍率和循环性能[图3(d)]。
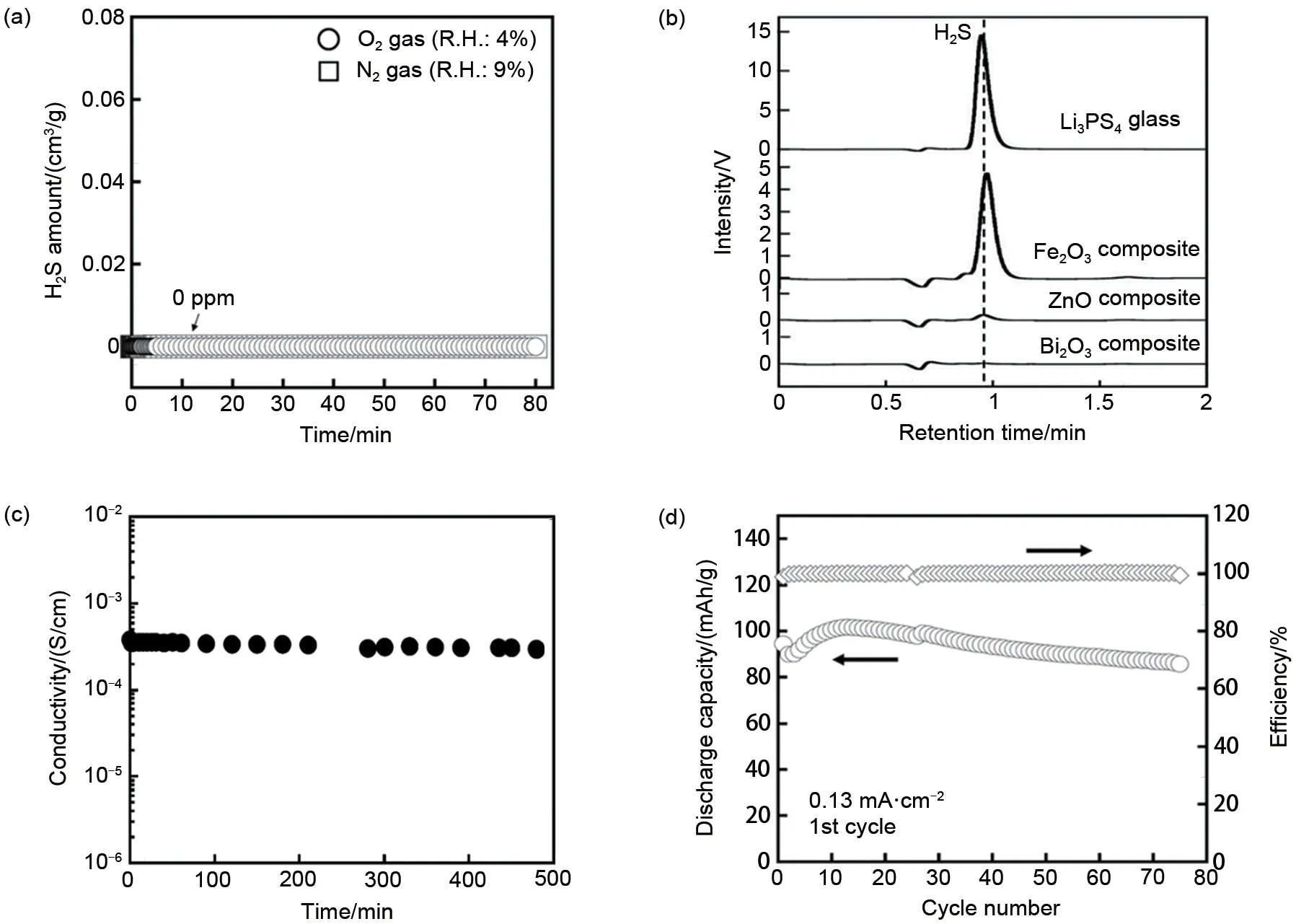
图3 (a)氧气或氮气气氛下Li3PS4电解质生成H2S量随时间的变化量;(b)90Li3PS4-10MxOy(MxOy∶ZnO,Fe2O3和Bi2O3)混合物以及玻璃态Li3PS4生成H2S气相色谱图;(c)90Li3PS4-10ZnO复合电解质的电导率与在空气中暴露时间的关系;(d)使用90Li3PS4-10ZnO复合电解质的In/LiCoO2电池的循环性能[57]Fig.3 (a)Time dependence of H2S amounts generated from the Li3PS4 glass under O2 or N2gas flow,(b)H2S gas chro-matograms for the 90Li3PS4-10MxOy(MxOy:ZnO,Fe2O3,and Bi2O3)composites and the Li3PS4 glass,(c)Electrical conductivity of the pelletized 90Li3PS4-10ZnO composite as a function of exposure time to air,(d)Cycle performance of the In/LiCoO2 cell using the 90Li3PS4-10ZnO composite electrolyte[57]
软酸原子取代也是一种改善硫化物电解质空气稳定性的常用方法,根据软硬酸碱(HASB)理论,Sb 相对于P 来说是更软的酸,与软碱S 结合更稳定,Kimura 等人[67]通过机械球磨的方式分别得到Li3SbS4和Li3PS4电解质,结果显示Li3SbS4电解质长时间暴露在空气中产生的H2S量远低于Li3PS4所产生的H2S的量,具有优异的空气稳定性。
3.2.2 电化学稳定性改善
改善硫化物电化学稳定性,主要是针对Li3PS4电解质对正负电极稳定性及自身电化学稳定性的提升。由于金属锂负极与Li3PS4电解质在热力学条件下不稳定,会发生化学反应,并且金属锂与Li3PS4电解质直接接触生成Li2S界面层能够抑制两者间化学反应的进一步发生,进而形成稳定共存状态。为提高Li3PS4电解质对金属锂负极的稳定性,Tao 等人[68]通过掺杂一定量的P2O5使Li3PS4电解质对锂稳定性及电解质自身的电化学稳定性得到提高,其中最佳组成为75Li2S·P2S5-1P2O5的电解质可与金属锂形成稳定的界面层。除此之外,通过向Li3PS4电解质体系中引入LiI和LiF等锂的卤化物能有效抑制锂枝晶生长,改善电解质与锂金属负极的界面稳定性。Fan等人[69]利用LiF修饰层抑制锂枝晶向Li3PS4电解质中渗透,提高了锂负极与Li3PS4电解质的界面稳定性。
硫化物电解质与含锂过渡金属氧化物正极材料(例如磷酸铁锂、钴酸锂、层状锂镍锰钴等)发生副反应导致电解质/正极界面阻抗增加,并且O 与S的电负性差异导致空间电荷层效应,因此正极材料/硫化物电解质界面不稳定性和空间电荷层效应是制约硫化物基固态电池发展的重要因素[70]。为改善过渡金属氧化物正极与硫化物电解质的界面问题,通常采用湿化学法、激光沉积等策略在两者间引入离子导电而电子绝缘的界面缓冲层[71],随着界面缓冲层的引入,硫化物电解质和正极氧化物之间的电势差被大幅减弱,Li 从氧化物侧转移减少,界面阻抗减少,如用于改善钴酸锂正极与硫化物电解质界面的缓冲层有Li4Ti5O12[72]、LiNbO3[73]、Li2SiO3[74]等,这些界面缓冲层有效地减小了界面电阻,提高正极/硫化物电解质的界面兼容性。Kim等人[75]研究了界面缓冲层对Li3PS4电解质分解程度的影响,通过对比未包覆的、Li2CO3包覆的、Li2CO3/LiNbO3共包覆的LiNi0.6Mn0.2Co0.2O2三种正极活性材料,发现电解质的分解程度与界面缓冲层密切相关。如图4(a)所示,对于未包覆的LiNi0.6Mn0.2Co0.2O2,Li3PS4电解质发生明显的分解反应,导致电极材料和电解质间的界面电阻随着循环的增加而增大。当在LiNi0.6Mn0.2Co0.2O2正极活性材料表面引入适量的Li2CO3时,可以显著提高固态电池的充放电容量和循环稳定性。最后,当在正极材料的表面同时引进Li2CO3/LiNbO3包覆层发现能大幅度改善相应的固态电池的首圈库仑效率[图4(b)]、充放电比容量及循环稳定性和容量保持率[图4(c)]。
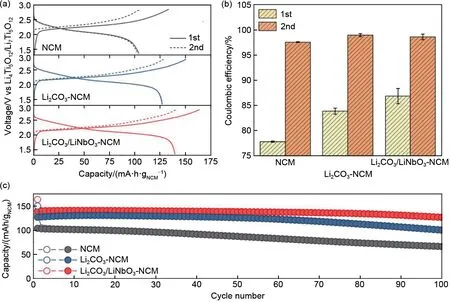
图4 (a)前两次循环对应的电压-比容量曲线;(b)相应的库仑效率变化;(c)使用未包覆(灰色)、Li2CO3包覆(蓝色)和Li2CO3/LiNbO3共包覆的LiNi0.6Mn0.2Co0.2O2(红色)的组装的固态电池在0.1 C速率和25 ℃下的循环性能[66]Fig.4 (a)Initial and second cycle voltage profiles,(b)corresponding Coulombic efficiencies,and(c)cycling performance at a 0.1 C rate and 25 ℃of SSB cells using bare(gray),Li2CO3-coated(blue),and Li2CO3/LiNbO3-coated NCM622(red).Error bars in(b)indicate the standard deviation from two independent cells[66]
此外,正极活性材料/硫化物电解质界面兼容性也与电解质和活性材料间的副反应有关,Chen等[76]将Li3PS4和90Li3PS4-10LiI 电解质分别与正极活性物质LiNi0.8Mn0.1Co0.1O2和LiNi0.6Mn0.2Co0.2O2按照1∶1 的质量比混合,研究热处理对混合物离子电导率的影响,发现未经热处理的混合物随时间推移,离子电导率急剧下降,而先热处理后的混合物离子电导率虽低却几乎稳定不变,这主要由于硫化物电解质和正极活性材料间的副反应在加热处理过程中已经结束造成的。
3.3 力学性能改善
为了构建高性能全固态电池,固态电解质除了具备高离子电导率和良好的稳定性之外,还要求具备优异的力学性能即合适的杨氏模量。一方面,这对于形成良好的电极/电解质间固-固界面尤为关键,在电池充放电过程中,固态电解质具备合适的杨氏模量能够保持活性材料和固态电解质之间的固-固界面接触良好而延长固态电池的循环寿命。硫化物电解质的杨氏模量一般为18~25 GPa,它能够缓冲正极活性物质的体积变化,因此大多数硫化物基固态电池相较其他无机固态电解质基固态电池具有更好的循环性能[77]。另一方面固态电解质具备一定的机械强度能够减少锂枝晶的产生。无机固态电解质普遍存在刚性易碎等问题,而有机-无机复合固态电解质[78-79]因为有机聚合物的介入具有更好的延展性和分散机械应力的作用,可以有效抑制锂枝晶的生长,因此当前受到广泛的关注。Xu等[80]在聚环氧乙烷(PEO)溶液中原位合成出PEO/Li3PS4有机-无机复合固态电解质,在保证较高的离子电导率的同时显示出良好的机械加工性能。通过应力应变测试发现合成的PEO/Li3PS4复合电解质的杨氏模量比Li3PS4电解质高两倍多,且具有良好的弹性和韧性,在一定程度上能有效阻止锂枝晶的生长,从而降低固态电池短路的风险。
另有研究发现,Li3PS4体系中引入卤化锂LiX(X=I,Br,Cl)也能降低固态电解质的弹性模量。Kato等人[81]研究了LiX的掺杂量对Li2S-P2S5硫化物电解质的力学性能的影响,如表3所示,改性后的Li3PS4电解质的杨氏模量及电导率与加入的LiI含量密切相关,体系中引入适量的LiI能有效地将Li3PS4电解质的杨氏模量从23 GPa降低至19 GPa,从而减小Li3PS4电解质与电极间的界面阻抗。
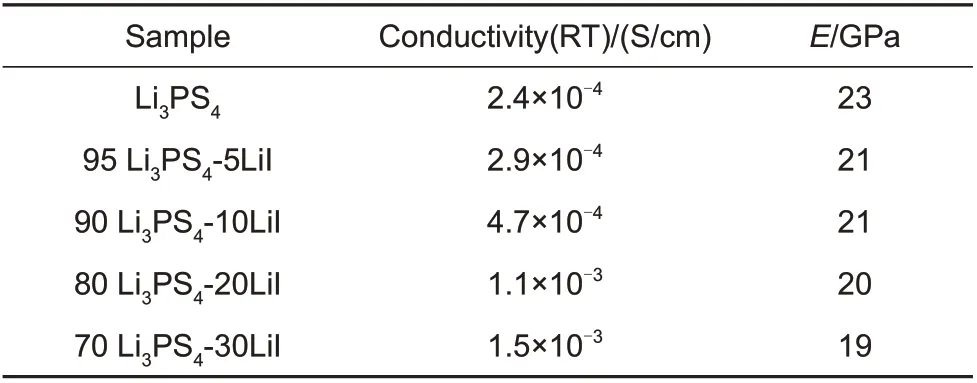
表3 Li3PS4电解质掺杂LiI后杨氏模量及离子电导率Table 3 Young’s modulus and ionic conductivity of Li3PS4 electrolyte doped with LiI
4 基于Li3PS4电解质的全固态电池
4.1 与单质硫及复合硫结合的全固态锂硫电池
硫因其高理论比容量(1675 mAh/g)和低成本成为一种非常有前景的锂硫电池电极材料[82-84],但在液态锂硫电池中,硫正极容易生成易溶解在电解液中的多硫化物(Li2Sn)[85],进而影响电池充放电性能;然而在固态锂硫电池中硫作为正极材料,在充放电过程中产生的多硫化物不会溶解在固态电解质中,不会出现多硫化物的离子穿梭机制[86-87],因此硫及复合硫材料可以作为理想的全固态锂硫电池电极材料[图5(a)]。硫及硫基复合材料均有很高的比容量和较高的对锂电位,但硫作为电子绝缘体,使用硫做正极材料通常需要与铜或碳等混合来增加材料的电子传导性。Kinoshita等人[88]使用硫/碳复合材料作为正极与Li3PS4电解质结合组装全固态锂硫电池,在0.9~2.6 V电压范围和0.1 mA/cm2的恒流密度下显示出良好的电化学性能,在50次充放电后放电比容量仍高达1200 mAh/g。Tatumisago 等人[40]选取Li3PS4作为电解质,利用单质硫的高比容量,将硫单质与电解质、导电剂按一定比例混合作为复合正极材料,组装全固态电池Li-In/S。如图5(b)所示,该电池在室温下0.064 mA/cm2的电流密度下放电比容量高达1500 mAh/g,远高于商业化的钴酸锂电池。
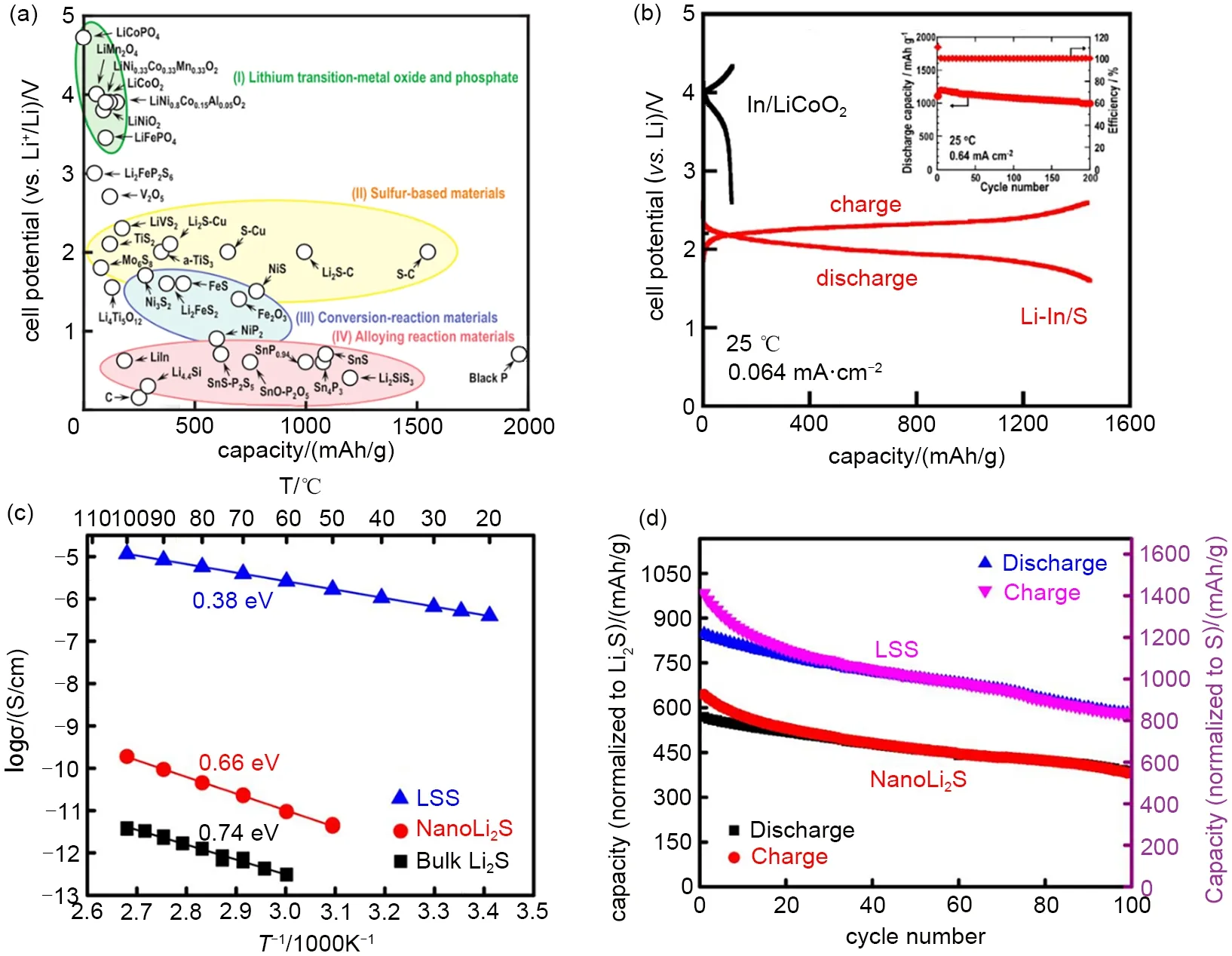
图5 (a)至今报道的使用硫化物固态电解质的固态电池,其电池电位(vs.Li+/Li)和可逆比容量之间的关系;(b)Li-In/S固态电池和In/LiCoO2 固态电池在0.064 mA/cm2时的充放电曲线(内嵌图为Li-In/S 固态电池在0.64 mA/cm2时的循环性能);(c)块状Li2S、NanoLi2S和LSS离子电导率随温度变化曲线图;(d)LLS电池和NanoLi2S电池在60 ℃时,以0.1 C倍率充放电的循环性能[77,80]Fig.5 (a)Correlation between cell potential(vs.Li+/Li)and reversible specific capacity in all-solid-state cells with a sulfide solid electrolyte reported so far,(b)Charge-discharge curves of an all-solid-state Li-In/S cell at 25 ℃under the current density of 0.064 mA/cm2(The embedded diagram shows the cycle performance of Li-In/S solid state battery at 0.64 mA/cm2),(c)Temperature dependency of ionic conductivities of the bulk Li2S,NanoLi2S,and LSS,(d)Cycling performance of LLS cell,NanoLi2S cell at 60℃under the rate of C/10[77,80]
4.2 与硫化锂及其类似物结合的全固态锂硫电池
硫化锂是硫单质完全放电后的产物,与硫正极一样,其理论比容量远高于商业上常用的LiFePO4、LiCoO2等正极材料。相对于硫单质正极材料,硫化锂有着更多的优势,例如热稳定性好,体积膨胀效应较小。Lin等人[89]选取几种Li2S做正极活性材料,β-Li3PS4做电解质层,锂金属做负极。分别组装块状Li2S (bulk Li2S)电池、纳米级Li2S (Nano Li2S)电池、Li2S@Li3PS4(LLS)电池,其中Li2S@Li3PS4正极材料由于Li3PS4包覆层的存在,其锂离子电导率(约10-6S/cm)远高于块状Li2S电解质(约10-13S/cm),以及正负极具有更好的电化学兼容性[图5(c)],因而Li2S@Li3PS4(LLS)固态电池展示出高的充放电比容量及优异的容量保持率[图5(d)]。
4.3 与过渡金属硫化物结合构筑全固态锂硫电池
过渡金属硫化物也可以作为全固态锂硫电池用活性材料,例如硫化钛(TiS3)[90]、硫化钼(MoS3)[91]、硫化铁(FeS2)[92]等,主要是因为这些过渡金属硫化物具有较高的离子电导率和电子电导率,同时充放电比容量也较高,构筑的全固态锂硫电池容易获得优异的电化学性能。Pan等人[93]利用FeS2的复合正极组装Li-In/Li3PS4/FeS2-SE-VGCF 固态电池,该电池在0.13 mA/cm2的充放电电流密度下,显示出高达420 mAh/g的可逆放电比容量,在更高的电流密度(0.64 mA/cm2)下,该固态电池在循环200次后容量保持率高达88%。
4.4 与商业化正极材料结合构筑全固态电池
目前常用的商业化正极材料多为含锂过渡金属氧化物,如钴酸锂、锂镍锰钴三元正极材料等。三元正极材料因其较大的放电比容量和高的工作电压成为动力电池正极材料的研究热点,它主要包括LiNi1-x-yCoxMnyO2(NCM)[94]和LiNi1-x-yCoxAlyO2(NCA)[95]两大类型。高锂离子电导率的硫化物固态电解质与三元正极材料相结合构筑的全固态电池具有较大的能量密度优势。Machida等人[96]基于Li3PS4电解质,分别选取未包覆的和ZrO2包覆的LiNi1/3Co1/3Mn1/3O2作为正极材料进行对比,发现以ZrO2包覆的正极材料构筑的固态电池Li4.4Si|Li3PS4|ZrO2@LiNi1/3Co1/3Mn1/3O2显示出较小的界面阻抗,其初始放电比容量高达120 mAh/g,循环50次后容量保持率高达95%,上述参数均远高于以LiNi1/3Co1/3Mn1/3O2为正极材料的固态电池。Kim 等人[97]也选取Li3PS4为电解质,分别以未包覆和Li2CO3/LiNbO3包覆的LiNi0.6Co0.2Mn0.2O2作为正极材料构筑全固态电池,对比发现Li2CO3/LiNbO3缓冲层能有效减小正极活性材料与电解质之间的界面阻抗,进而提升固态电池的电化学性能。包覆后的固态电池在室温下0.1 C 倍率下循环100 圈后容量保持率由64%提升至91%。此外,研究发现三元正极材料的粒径同样会影响Li3PS4基固态锂电池的性能,作者选取LiNi0.6Co0.2Mn0.2O2(NCM622)为正极活性材料,分别制备大尺寸的NCM622、中等尺寸的NCM622 和小尺寸的NCM6222 正极材料,与Li3PS4电解质和In 负极构筑全固态电池,实验结果显示以小尺寸NCM622正极构筑的全固态电池表现出更大的可逆比容量以及更为优异的循环性能[98]。
4.5 与负极材料结合构筑全固态电池
当前锂离子电池常用的负极材料主要为石墨[99],其理论比容量只有370 mAh/g左右,无法满足交通电气化和规模化储能的快速发展对高能量密度电化学储能器件的需求。硅因其4200 mAh/g 的高理论比容量,有望替代石墨成为新一代的负极材料,被认为是最具潜力的高比容量负极材料之一[100]。然而硅负极材料在充放电过程中会发生严重的体积变化,导致容量快速衰减,并且硅基负极材料的电子电导率较低,这些问题影响硅基负极材料的电化学性能。因此,应用于锂离子电池的硅基负极材料都需要经过改性处理。Okuno等人[101]合成出多孔硅作为负极材料,与Li3PS4电解质及Li-In合金负极组装全固态电池。孔隙的存在缓解了硅基负极材料在充放电过程中的体积膨胀效应,从而保证了硅基固态电池良好的电化学性能,组装的全固态电池初始放电比容量高达2300 mAh/g 且循环100 圈后容量保持率达93%。
4 总结和展望
高安全性、高功率/能量密度的固态电池受到研究人员的广泛关注,但是当前其电化学性能离商业化液态锂离子电池差距还较大。固态电解质是固态电池内部的关键材料之一,开发高性能的固态电解质是推动固态电池实用化的前提条件。Li3PS4硫化物电解质因其相对较高的离子电导率和对锂稳定性受到广泛关注,但其仍然存在空气稳定性差、电极/电解质界面不稳定等问题。这些问题直接制约了Li3PS4硫化物固态电解质的发展和应用。
本文系统地总结了Li3PS4硫化物电解质的合成方法:液相合成法和固相合成法。并基于此归纳了Li3PS4电解质提高离子电导率的方法有:①氧化物掺杂;②硫化物掺杂;③卤化物掺杂。这些掺杂形式均能有效拓宽锂离子传导路径,进而提高离子电导率。改善电解质的稳定性方法有:①通过氧原子掺杂、金属氧化物混合和软酸原子取代等方式减少Li3PS4电解质在空气中的副反应,降低H2S 气体的生成量,改善其空气稳定性;②掺杂氧化物、卤化物改善其对金属锂负极的稳定性;③引入电子绝缘的界面缓冲层改善对正极活性材料的稳定性。改良电解质力学性能的方法有:①引入卤化锂降低材料杨氏模量;②引入有机聚合物电解质,制备力学性能更好的有机无机复合电解质。并且归纳了Li3PS4电解质与硫、金属硫化物、含锂过渡金属氧化物正极等电极材料相结合组装的全固态电池的电化学性能。希望通过本文的总结和归纳能够帮助研究人员更加深入地了解Li3PS4电解质,并针对该电解质存在的对空气/水汽稳定性较差及与正负极固/固界面稳定性不好等问题提出新的改善策略, 为构筑基于Li3PS4电解质的高安全性、高能量密度、长寿命固态锂电池提供重要的技术支撑和理论指导。
基于前文总结,Li3PS4硫化物固态电解质在未来的研究和应用还有很大的改进空间,在优化合成工艺方面还需要进一步降低合成成本、简化合成步骤;在改善离子电导率方面无论是复合改性还是掺杂改性还需要引入更多的元素并充分发挥各元素的性能;在改进稳定性方面还需要更多地兼顾整体的稳定性,这包括界面稳定性及电解质本身的稳定性,这是构筑Li3PS4基固态电池的基础。虽然目前硫化物固态电池还处于研发阶段,还没有相应的产业化方案,大规模的产业化还需要与电极材料、组装工艺等方面共同进步,但随着近年来固态电池技术壁垒的不断突破,已经出现越来越多的全固态储能设备,相信不远的将来硫化物固态电池会出现在人们的视野,而Li3PS4硫化物电解质无论是成本还是发展空间,在后期大规模商业化有着巨大的市场潜力。

