大剂量甲氨蝶呤治疗血液系统恶性肿瘤发生排泄延迟的危险因素分析
纪硕 李小娜 周珊珊 王麟奇 赵朋飞 刘坤

【摘要】 目的 分析影響大剂量甲氨蝶呤(HD-MTX)化疗患者发生排泄延迟的可能危险因素,为临床合理使用甲氨蝶呤提供参考依据。方法 以2013年7月至2022年7月医院血液科收治的55例大剂量甲氨蝶呤化疗的患者为研究对象,根据血药浓度监测结果将患者分为排泄延迟组(33例)和非排泄延迟组(22例),采用单因素筛选,多因素Logistic回归模型分析影响大剂量甲氨蝶呤排泄延迟的危险因素。结果 行大剂量甲氨蝶呤化疗患者共55例,发生排泄延迟的33例,排泄延迟发生率为60%。单因素分析结果显示性别、是否发热、是否呕吐、饮食量、疾病危险度、体质系数和疾病类型不是大剂量甲氨蝶呤排泄延迟的危险因素(P>0.05),年龄、合并使用抗菌药物、甲氨蝶呤剂量以及体表面积剂量是大剂量甲氨蝶呤排泄延迟的危险因素(P<0.05)。多因素分析结果显示,合并抗菌药物是甲氨蝶呤发生排泄延迟的影响因素(P<0.05),合并抗菌药物的患者发生排泄延迟的危险性是不合并抗菌药物患者的9.899倍。结论 合并使用青霉素、头孢菌素、氟喹诺酮类抗菌药物是大剂量甲氨蝶呤排泄延迟的危险因素,应警惕危险因素以降低大剂量甲氨蝶呤排泄延迟风险。
【关键词】 甲氨蝶呤;排泄延迟;血药浓度;白血病
中图分类号 R473.6 文献标识码 A 文章编号 1671-0223(2022)23--03
Analysis of risk factors for delayed excretion in the treatment of hematological malignancies with high-dose methotrexate Ji Shuo,Li Xiaona,Zhou Shanshan,Wang Linqi,Zhao Pengfei,Liu Kun. School of Pharmacy, North China University of Science and Technology, Tangshan 063210, China
【Abstract】 Objective To analyze the possible risk factors of delayed excretion in patients with high-dose methotrexate (HD-MTX) chemotherapy , and to provide evidence for the rational use of methotrexate in clinic. Methods Fifty-five patients with HD-MTX chemotherapy who were admitted to the Department of Hematology of hospital from July 2013 to July 2022 were taken as the research object. According to the monitoring results of blood concentration, the patients were assigned to the excretion delay group (33 cases)and non-excretion delay group(22 cases). Univariate screening and multivariate Logistic regression model were used to analyze the risk factors for delayed excretion of high-dose methotrexate. Results A total of 55 patients underwent high-dose methotrexate chemotherapy,33 cases occurred delayed excretion , with the delayed excretion rate of 60%. The results of univariate analysis showed that gender, fever, vomiting, diet, disease risk, and physique coefficient and disease type not affected the delayed excretion of HD-MTX(P>0.05), and age, combined use of antibiotics,body surface area dose and methotrexate dose affected the delayed excretion of HD-MTX(P<0.05). The results of multivariate analysis showed that the combined antibacterial drugs were the influencing factors of the delayed excretion of methotrexate (P<0.05). The risk of delayed excretion in patients with antibiotics was 9.899 times higher than that in patients without antibiotics. Conclusion Concomitant use of penicillin, cephalosporin and fluoroquinolone antibiotics is a risk factor of delayed excretion of HD-MTX, and caution should be exercised.Risk factors should be alerted to reduce the risk of delayed excretion of high-dose methotrexate.
【Key words】 Methotrexate; Excretion delay ; Blood concentration; Leukemia
甲氨蝶呤为抗叶酸药物,作为第一个靶向抗癌药物被开发[1],通过与二氢叶酸还原酶竞争性可逆性结合,阻止二氢叶酸转换为四氢叶酸,推迟和阻碍脱氧核糖核酸(DNA)和核糖核酸(RNA)的合成,从而发挥抗肿瘤的作用[2]。甲氨蝶呤通过主动转运渗入细胞,但是由于肿瘤细胞血液运输较差,甲氨蝶呤只能通过被动扩散途径进入肿瘤细胞,因此只有应用大剂量的甲氨蝶呤才能使肿瘤细胞内的药物浓度达到有效值[3]。大剂量甲氨蝶呤联合亚叶酸钙解救治疗方案(HD-MTX-CF)已广泛应用于临床[4]并具有独特优势,可以透过人体血脑屏障和血睾屏障,在髓外浸润和全身强化治疗中起到重要作用[5];并且大剂量甲氨蝶呤可以抵抗由于二氢叶酸还原酶数量增多或亲和力降低产生的甲氨蝶呤耐药性[6]。HD-MTX治疗中甲氨蝶呤剂量通常比常规剂量大10倍以上,在达到较好治疗效果的同时,部分患者極易出现排泄延迟的现象,一旦发生排泄延迟,极易出现骨髓抑制、肝功能损害、白细胞减少等不良反应[7],不仅会增加患者的躯体痛苦,还会影响其治疗效果[8]。通过对患者体内甲氨蝶呤血药浓度进行监测,可以判断患者是否发生排泄延迟,进而决定是否增加亚叶酸钙的解救次数和解救剂量,以及是否继续水化碱化治疗。但是,治疗药物监测具有滞后性,故通过深入分析排泄延迟的危险因素,可以为临床更有效地预测排泄延迟的发生,安全大剂量使用甲氨蝶呤并实现个体化给药提供依据。本研究针对临床血液系统恶性肿瘤患者,分析排泄延迟的危险因素。
1 对象与方法
1.1 调查对象
选取2013年7月至2022年7月在医院血液科进行HD-MTX方案化疗并行血药浓度监测的患者55例为研究对象,行HD-MTX化疗,根据血药浓度监测结果将患者分为排泄延迟组(33例)和非排泄延迟组(22例),其中急性淋巴细胞白血病42例,淋巴瘤13例,年龄13~67岁。患者知情同意本研究并签署知情同意书。
(1)纳入标准:行大剂量甲氨蝶呤化疗;相关基础资料完整;无其他血液系统严重疾病;无药物过敏反应者;患者及家属签署知情同意书。
(2)排除标准:病历资料和基本信息不完整者;出现免疫缺陷综合征者;出现严重不良反应未能完成甲氨蝶呤治疗者;合并重度骨髓抑制者;合并严重肝肾功能损害者。
(3)排泄延迟定义:HD-MTX开始后48h(即HD-MTX化疗结束后24h)甲氨蝶呤水平≥1μmol/L72h (即HD-MTX化疗结束后48h)甲氨蝶呤水平≥0.1μmol/L,符合上述二者之一即为排泄延迟[9]。
1.2 资料收集
内容包括性别、年龄、是否发热、是否呕吐、饮食量、是否合并抗菌药物、疾病危险度、体质系数、甲氨蝶呤体表面积剂量、甲氨蝶呤剂量、甲氨蝶呤的血药浓度、疾病类型。其中甲氨蝶呤血药浓度监测,采用高效液相色谱法监测甲氨蝶呤的血药浓度。
1.3 治疗方法
所有患者均经静脉给药,剂量为0.8~6.0g,均在24h内输注完毕,甲氨蝶呤输注完毕后12h开始给予亚叶酸钙解救,1次/6h,暂定给予5次,并根据MTX浓度调整解救次数及剂量,期间动态观测患者是否出现黏膜损伤并监测肝肾功能变化。
1.4 统计学方法
应用SPSS 23.0统计学软件进行数据分析,计量资料检验变量是否服从正态分布,计量资料服从正态分布的采用“均数±标准差”表示,组间均数比较行t检验,不服从正态分布的采用“中位数(P25~P75)”表示,组间中位数比较行非参数检验;计数资料组间率比较行卡方检验。多因素分析采用Logistic回归模型。双侧概率检验,以P<0.05为差异有统计学意义。
2 结果
2.1 排泄延迟情况
行HD-MTX化疗的55例患者发生排泄延迟的33例,排泄延迟发生率为60%。
2.2 排泄延迟影响因素的单因素分析
单因素分析结果显示,排泄延迟组与非排泄延迟组患者在性别、是否发热、是否呕吐、饮食量、疾病危险度、体质系数、疾病类型方面差异无统计学意义(P>0.05);在年龄、是否合并抗菌药物、体表面积剂量以及甲氨蝶呤剂量方面差异有统计学意义(P<0.05)。见表1。
2.3 排泄延迟影响因素的多因素分析
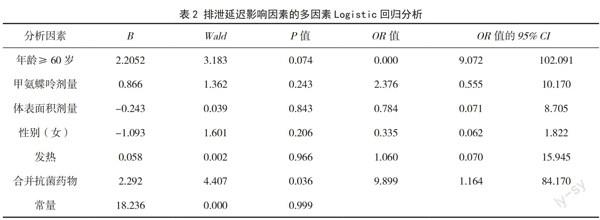
以是否排泄延迟为因变量(是=1,否=0),以单因素分析具有统计学意义的因素(年龄、是否合并抗菌药物、甲氨蝶呤剂量、体表面积剂量)及性别、发热为自变量,进行多因素Logistic回归分析。结果显示,合并抗菌药物是甲氨蝶呤发生排泄延迟的影响因素(P<0.05),合并抗菌药物的患者发生排泄延迟的危险性是不合并抗菌药物患者的9.899倍。见表2。
3 讨论
国内外文献报道的HD-MTX排泄延迟的影响因素各不相同,Kentaro Narita等[10]研究认为性别、年龄是MTX排泄延迟的危险因素,Jahnke[11]和Crews[12]的研究均不支持年龄是MTX排泄延迟的影响因素。陆华等[13]的研究认为药物剂量并非MTX排泄延迟的影响因素,钱卿等[14]的研究认为MTX的用药剂量与甲氨蝶呤的排泄延迟相关。分析产生争议的原因,首先不同研究者对MTX排泄延迟的定义不同,其次不同研究对象之间由于种族、地区等的差异而存在基因多态性的不同,再次,纳入的患者数量也会对结果造成影响。
本研究资料显示,行HD-MTX化疗方案的55例患者中排泄延迟发生率为60%,排泄情况较差,单因素分析结果显示排泄延迟组和非排泄延迟组在患者性别、是否发热、是否呕吐、饮食量、疾病危险度、体质系数和疾病类型方面差异无统计学意义,在年龄、合并抗菌药物、体表面积剂量以及甲氨蝶呤剂量方面差异有统计学意义;多因素分析结果显示,两组在合并抗菌药物方面差异有统计学意义。由此可知合并使用青霉素、头孢菌素、喹诺酮类抗菌药物会影响甲氨蝶呤的排泄延迟。分析原因:有机阴离子转运蛋白(OATs)主要分布于肾脏,参与MTX向肾近端小管的转运[15],青霉素和头孢菌素类抗菌药物通过抑制OATs来抑制MTX的肾排泄[16];氟喹诺酮类药物可能通过损伤肾小球滤过功能使MTX排泄延迟[17]。
本研究中HD-MTX化疗排泄延迟的发生率高于其他研究[18-19],一方面可能与本研究纳入的样本量小有关,另一方面可能与质子泵抑制剂的使用有关,本研究中合并使用质子泵抑制剂(PPIs)排泄延迟的发生率高于未合并使用PPIs,但是差异无统计学意义。PPIs可能通过抑制乳腺癌抗性蛋白(BCRP)来抑制甲氨蝶呤的消除[20],MTX与PPIs之间相互作用的临床意义存在着争议,有研究认为PPIs的存在与MTX排泄延迟无关[21],一项关于质子泵抑制剂致大剂量甲氨蝶呤排泄延迟的Meta分析[22]指出,联合PPIs的患者出现MTX排泄延迟的频率高于未联合使用PPIs的患者,且差异有统计学意义。
本研究纳入的样本量较少,可能导致研究结果存在偏倚,需要进一步开展前瞻性大样本研究,探究PPIs对于MTX排泄延迟的影响。
综上所述,行大剂量甲氨蝶呤化疗的患者,对于合并使用青霉素、头孢菌素、氟喹诺酮类抗菌药物的患者应提高警惕,发现排泄延迟时可通过调整亚叶酸钙的解救剂量和浓度,加强水化碱化等处理来减少不良反应的发生。
4 参考文献
[1] Visentin M,Zhao R,Goldman I D.The antifolates[J].Hemato Oncol Clin North Am, 2012,26(3): 629-648.
[2] 康敏,黃榕彬,刘文辉.亚叶酸钙解救用于大剂量甲氨蝶呤疗法的研究进展[J].中南药学,2019,17(8):1247-1250.
[3] Cohen IJ, Wolff JE. How long can folinic acid rescue be delayed after high-dose methotrexate without toxicity[J]. Pediatr Blood Cancer, 2014, 61(1): 7-10.
[4] Tubiana-Mathieu N, Monjanel-Mouterde S, Lejeune C, et al. Pharmacokinetics of folinic acid and 5-methyltetrahydrofolic metabolite after repeated oral administration of calcium folinate following methotrexate treatment[J]. Eur J Cancer, 1994, 30(9): 1281-1284.
[5] 吴斌,胡荣,李旸,等.成人大剂量甲氨蝶呤治疗后排泄延迟因素的分析[J].中国现代医学杂志,2015,25(10):59-61.
[6] 大剂量甲氨蝶呤亚叶酸钙解救疗法治疗恶性肿瘤专家共识[J].中国肿瘤临床,2019,46(15):761-767.
[7] 王艳萍,卢愿,仲任,等.大剂量甲氨蝶呤治疗儿童急性淋巴细胞白血病的不良反应及影响因素分析[J].山东医药,2015,55(39):90-92.
[8] 洪杏,盛超.小儿急性淋巴细胞白血病大剂量甲氨蝶呤化疗血药浓度监测与不良反应观察[J].现代仪器与医疗,2018,24(6):152-153,156.
[9] Xu WQ,Tang YM,Fang CQ,et al.Study on elimination delay in high dose methotrexate therapy in childhood acute lymphoblastic leukemia[J].Zhonghua Xueyexue Zazhi, 2005, 26(1): 15-18.
[10] Narita K, Kobayashi H, Abe Y, et al. Evaluation of risk factors and survival effect of delayed excretion of high-dose methotrexate in patients with leukemia and lymphoma[J]. Blood, 2017, 130: 4132.
[11] Jahnke K, Korfel A, Martus P, et al. High-dose methotrexate toxicity in elderly patients with primary central nervous system lymphoma[J]. Ann Oncol, 2005, 16(3): 445-449.
[12] Crews KR,Liu T,Rodriguez-Galindo C,et al.High-dose methotrexate pharmacokinetics and outcome of children and young adults with osteosarcoma[J].Cancer,2004,100(8): 1724-1733.
[13] 陆华,钟小斌,黄振光,等.大剂量甲氨蝶呤治疗儿童急性淋巴细胞白血病排泄延迟分析[J].中国药房,2009,20(29):2265-2267.
[14] 钱卿,胡楠,陈荣,等.大剂量甲氨蝶呤治疗血液系统恶性肿瘤后排泄延迟的影响因素及其与不良反应的相关性研究[J].中国医院用药评价与分析,2020,20(1):56-59.
[15] Türková A,Zdrazil B.Current advances in studying clinically relevant transporters of the solute carrier (SLC) family by connecting computational modeling and data science[J].Comput Struct Biotechnol J,2019(17): 390-405.
[16] 刘爽,宋再伟,易湛苗,等.联合用药对大剂量甲氨蝶呤安全性影响的系统评价[J].中国临床药理学杂志,2019,35(14):1522-1525.
[17] 赵嘉澍,赵志刚,王睿韬,等.大剂量甲氨蝶呤化疗后延迟排泄的影响因素和发生机制的研究进展[J].现代肿瘤医学,2021,29(17):3104-3108 .
[18] 张晗.白血病患儿甲氨蝶呤治疗后并发排泄延迟的影响因素[J].现代诊断与治疗,2021,32(5):730-731.
[19] 边爽,李程辉,高晖.分析甲氨蝶呤治疗小儿白血病发生排泄延迟的影响因素[J].当代医学,2020,26(3):175-176.
[20] Boerrigter E , Crul M . A non-interventional retrospective cohort study of the interaction between methotrexate and proton pump inhibitors or aspirin-Science Direct[J]. Ann Pharm Fr, 2017, 75(5):344-348.
[21] Chan A J, Rajakumar I.High-dose methotrexate in adult oncology patients: a case-control study assessing the risk association between drug interactions and methotrexate toxicity[J].J Oncol Pharm Pract,2014,20(2): 93-99.
[22] 宋艳琴.质子泵抑制剂致大剂量甲氨蝶呤排泄延迟的Meta分析[D].昆明:昆明医科大学,2019.
[2022-08-07收稿]
作者单位:063210 河北省唐山市,华北理工大学药学院(纪硕、李小娜、周珊珊、王麟奇、赵朋飞);华北理工大学附属医院药学部(刘坤)
*通讯作者

