间质性肺疾病合并糖尿病患者发生认知功能障碍的危险因素分析
新图叶 刘晖 张莹 米合热古力·司马义
间质性肺疾病(Interstitial pulmonary disease,ILD)是一种慢性、进行性、实质肺疾病,其特征在于肺实质中不同程度的炎症和纤维化,具有高发病率和死亡率,并且长期ILD患者常伴有一定程度的认知功能障碍[1]。随着深入研究,糖尿病(diabetes mellitus,DM)相关肺损伤和认知功能障碍,已经得到证实,肺也被认为是糖尿病的靶器官之一,主要表现为肺纤维化[2]。并且DM也被认为是影响ILD治疗和不良预后的危险因素[3]。因此本研究拟寻找ILD合并DM患者发生认知功能的危险因素。
资料与方法
一、一般资料
选取2017年6月至2021年6月期间我院接受治疗的ILD患者72例,其中包括特发性ILD5例,结缔组织病相关ILD 41例,过敏性肺炎相关ILD 7例,急性间质性肺炎13例,血管炎相关ILD 6例,其中合并糖尿病29例。根据蒙特利尔认知评估(Montreal cognitive assessment,MoCA)量表判定有无合并认知功能障碍,39例为认知障碍组,33例为非认知障碍组,其中男46例,女26例;年龄34~73岁,平均年龄(49.85±4.25)岁;体质指数(Body mass index,BMI)21.3~25.6 kg/m2,平均BMI(22.32±2.41)kg/m2;病程0.5~21.0年,>5.0年31例。所有患者家属均签署了临床研究治疗知情同意书。并通过我院医学伦理委员会审查(批号:D210929-01)。
1 纳入标准
(1)根据2002年美国胸科学会/欧洲呼吸病学会诊断标准和2013年对ILD的分类和诊断共识明确诊断为ILD[4-5];(2)不伴随躯体恶性肿瘤,急性感染或肺动脉高压等疾病;(3)年龄≥18岁。
2 排除标准
(1)伴随有严重的心功能不全,肝肾功能不全等危及生命的疾病,如心力衰竭,肾衰竭等;(2)合并颅脑创伤,颅内肿瘤或精神类疾病;(3)长期饮酒或精神类药物滥用者;(4)已经接受正压通气治疗的患者。
3 剔除标准
患者死亡、自动出院、中途退出则停止研究。
二、方法
收集患者的一般临床资料,包括者性别,年龄,BMI,合并症,血氧饱和度(Oxygen saturation SpO2),心率,呼吸频率,肺功能及影像学结果等。所有患者入院后次日清晨抽取空腹状态下肘静脉血10mL,用于测定白细胞计数(White blood cell count,WBC),C反应蛋白(C-reactive protein,CRP)、降钙素原(Preprocalciton,PCT)、低密度脂蛋白(Low density lipoprotein,LDL-C),肌酐(Cr),空腹血糖,糖化血红蛋白(hemoglobin A1c,HbA1c)水平等指标。认知功能评估采用蒙特利尔认知评估(Montreal cognitive assessment,MoCA)量表,该量表包括视空间与执行功能、注意力、定向力等7个项目,总分0~30分,评分越低表明认知功能越差,MoCA量表>26分为认知功能正常,≤26分为认知功能障碍[6]。
患者入院后一周内完成肺功能检查,同时记录第1秒用力呼气容积(1 second forced expiratory volume,FEV1)、用力肺活量(Forced vital capacity,FVC),肺一氧化碳弥散量(diffusion capacity for carbon monoxide of lung,DLCO), 数据均用实测值占预计值百分比表示。
患者取仰卧位,高分辨CT参数设置为层厚1mm。根据病变累及的范围及程度计算 Warick评分:磨玻璃影 1分,不规则胸膜边缘2分,小叶间隔增厚或胸膜下线征3分,蜂窝状影4分,胸膜下囊肿5分。累及1~3个肺段1 分,4~9个肺段2分,>9个肺段3分,最高30分[7]。
三、统计学方法
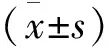
结 果
一、一般临床资料
合并DM的ILD患者的MoCA量表各维度评分除语言和定向力外,均显著低于单无DM的ILD患者,差异均具有统计学意义,P<0.05(见表1)。与非认知障碍组相比,认知障碍组的糖尿病的比例,Warrick评分、空腹血糖、HbA1c均显著升高,FEV1,FVC和DLCO均显著降低,差异均具有统计学意义,P<0.05(见表2)。

表1 有无合并糖尿病的ILD患者MoCA量表各维度评分比较

表2 患者一般临床资料比较
二、ILD患者发生认知功能障碍的多因素回归分析
以是否发生认知功能障碍为因变量,将表1中的具有统计学差异的因素作为自变量进行赋值,多因素Logistic回归分析结果显示DLCO,HbA1c均为ILD患者发生认知功能障碍的危险因素,均P<0.05(见表3)。

表3 ILD患者认知功能障碍的多因素Logistic回归分析
三、不同危险因素预测ILD发生认知功能障碍的ROC曲线分析
ROC分析结果显示HbA1c、DLCO的AUC分别为0.752,0.768。敏感度分别为69.2%,64.1%。特异度分别为63.7%,63.6%。(见表4,图1)。HbA1c和DLCO的联合检测结果显示AUC为0.805,敏感度和特异度分别为76.9%,72.7%。

表4 ILD患者发生认知功能障碍的ROC曲线分析

图1 不同危险因素预测认知功能障碍的ROC曲线分析
讨 论
肺部疾病对神经认知障碍影响的研究表明,多种肺部疾病患者的认知过程受损,继发于肺部疾病的神经认知功能受损,可能对患者的整体生活质量,尤其是治疗依从性产生负面影响[8]。ILD包括影响肺间质的各种肺部疾病,它可能由吸入物质、药物、感染、结缔组织病或特发性原因等多种因素引起,对患者的生活质量有明显的负面影响[9]。尽管既往研究认为认知功能障碍主要与呼吸衰竭的持续时间和缺氧程度有关[10],但由于ILD的异质性,在非缺氧患者中也存在一定的认知功能障碍,如伴随糖尿病等全身性疾病,也可能对中枢神经系统产生直接不利影响[3,10]。因此本研究拟寻找合并DM的ILD患者发生认知功能障碍的危险因素,为后续的机制研究提供方向。
本研究结果显示合并DM的ILD患者的MoCA量表各维度评分除语言和定向力外均显著低于无DM的ILD患者,多因素分析结果也显示HbA1c升高是ILD患者发生认知功能障碍发生的危险因素,表明合并有DM会加重ILD患者的认知功能损害。尽管目前尚无直接针对ILD和糖尿病的共同发病机制的研究,但ILD和DM的肺部并发症在临床特征,HRCT成像和组织病理学变化上均有共同特征,如FVC、FEV1和 DLCO均显著降低[11],肺基底层毛细血管增厚、肺泡壁中胶原蛋白含量增加等[12]。伴随着研究的深入,还发现ILD和DM之间的作用是相互的,均会加重患者的认知功能障碍[13],并且DM会导致ILD肺纤维化症状逐渐加重,二者之间可能还存在共同的作用基因和易感位点,并且作用机制高度复杂性和多样性[14]。高血糖会导致氧化应激和细胞趋化,并导致自由基生成和抗氧化活性之间的不平衡[15],导致肺中的微血管损伤,肺泡上皮和肺毛细血管基底层增厚,肺毛细血管血容量减少,肺泡壁增厚和灌注减少的结合,导致通气灌注不匹配,从而导致扩散能力受损[16]。而氧化应激、内皮微损伤和血小板活化伴随细胞因子趋化,被认为是ILD起始和发展的重要机制[17]。此外伴随着胰岛素敏感性下降,海马、下丘脑、纹状体和额叶等富含胰岛素受体的大脑区域极易发生神经变性[18],这种神经元生成以及潜在的生化改变,可能会进一步加重患者的认知障碍。
本研究单因素分析结果显示合并认知功能障碍的ILD患者肺功能检查结果均显著低于认知功能正常的ILD患者,ILD患者主要表现为限制性通气功能障碍,由于肺泡间隔增生和胸膜纤维化加重,导致胸膜粘连,肺扩张受限,因此FVC和FEV1均明显降低,而呼吸膜伴随着纤维增生增加了气体的弥散距离, 导致弥散功能障碍,即DLCO显著降低[19]。当通气功能障碍加重时伴随患者脑氧供减少,可能导致继发于缺氧导致的脑小血管病的解剖结构和功能变化,进而发生认知功能障碍[20]。有关脑弥散张量成像研究显示限制性通气功能障碍患者的脑组织中弥散模式显著异常,与认知功能的强烈相关,表明脑组织微观结构广泛恶化[21]。但多因素分析结果显示仅DLCO是ILD患者发生认知功能障碍的独立危险因素,这可能是因为FVC和FEV1是肺疾病的标准生理指标,但反映肺气肿和血管异常的敏感性不如DLCO[22]。而DLCO不仅与限制性通气功能障碍的动脉硬化密切相关[23],而且还是ILD进展的敏感指标[19]。
本研究局限性在于首先本研究为单中心研究,样本量较小,仍需进一步的多中心大样本量研究证实该结论。其次有关ILD和DM的共同发病机制尚未明确,仍需进一步的体内外实验进行验证。总之,本研究结果显示合并DM能增加ILD患者认知功能障碍的发生风险,DLCO,HbA1c水平是ILD合并DM患者发生认知功能障碍的独立危险因素。

