超声剪切波频散成像对代偿期肝硬化高风险食管胃静脉曲张的诊断价值
王佳音, 周洪雨, 李庭红, 赵 蕾, 徐佰国, 尹伟利, 王 芳,梁 静, 经 翔, 向慧玲
1 天津医科大学三中心临床学院, 天津 300170; 2 天津市第三中心医院, 天津市重症疾病体外生命支持 重点实验室, 天津市人工细胞工程技术研究中心, 天津市肝胆疾病研究所 a.超声科,b.消化(肝病)科, 天津 300170
食管胃底静脉曲张(esophageal gastric varices,EGV)是肝硬化门静脉高压患者常见症状之一,而曲张静脉破裂出血的患者6周病死率仍高达20%左右[1]。因此,早期识别高风险食管胃底静脉曲张(high risk esophageal gastric varices,HREGV),对改善患者预后有着重要意义。多家指南[2-4]推荐肝硬化患者定期应接受胃镜检查,以筛查有无静脉曲张以及判断静脉曲张出血风险。但因胃镜检查的侵入性和痛苦,患者的耐受性及依从性较差。随着检测设备和技术的发展,无创监测并早期识别HREGV成为近年来的研究热点。二维超声剪切波弹性成像(shear wave elastography,SWE)与组织硬度相关,对预测肝硬化患者是否存在静脉曲张有一定临床价值,但对HREGV的诊断价值有限[5]。SWE受频散斜率影响,有研究[6-8]表明,剪切波频散成像(shear-wave dispersion,SWD)与组织炎症坏死相关,可用于评估组织的黏度,但在预测肝硬化患者HREGV中未见报道,因此本研究在代偿期肝硬化患者中检测肝SWD/SWE,并探讨其预测HREGV的临床价值。
1 资料与方法
1.1 研究对象 选取2020年2月—2021年2月在天津市第三中心医院就诊的各种病因接受胃镜检查的代偿期肝硬化患者。同时排除:(1)入组时及既往存在消化道出血者;(2)入组时及既往出现腹水者;(3)入组时及既往出现II级以上肝性脑病、脓毒症及肝肾综合征者;(4)既往接受过内镜治疗、脾切除手术及经颈静脉门腔静脉分流术(TIPS)者;(5)入组时诊断肝脏恶性肿瘤者。
代偿期肝硬化诊断依据《肝硬化诊治指南》标准[9]:(1)组织学符合肝硬化诊断;(2)内镜显示食管胃静脉曲张或消化道异位静脉曲张,除外非肝硬化性门静脉高压;(3)B超、肝脏硬度测定(LSM)或CT等影像学检查提示肝硬化或门静脉高压特征;(4)无组织学、内镜或影像学检查者,需符合以下4条中2条,①PLT<100×109/L,无其他原因可以解释;②血清白蛋白<35 g/L,排除营养不良或肾脏疾病等其他原因;③INR>1.3或PT延长;④AST/PLT比率指数(APRI)>2。出现腹水、食管胃静脉曲张破裂出血、脓毒症、肝性脑病、肝肾综合征任何一种并发症即为失代偿期。
1.2 腹部超声检测肝SWD/SWE 由1名具备10年以上超声操作经验的超声科医生在不知患者其他检查及化验结果的情况下使用彩色超声仪(Aplio i800, Canon Medical Systems, Tochigi, Japan)进行常规腹部超声及肝脏的SWE/SWD检查。探头为3.5 MHz,凸振。SWE/SWD操作方法:受试者禁食6 h,平卧位,右臂最大程度外展,置于头顶,探头垂直于肝表面,在右叶寻找最佳肋间窗并避开大的血管及胆道,训练受试者轻轻屏住呼吸,超声系统显示双视图,冷却5 s后切换到四视图模式,包括剪切波速度或剪切波弹性(速度图)、剪切波到达时间轮廓(传播图)、超声图像和剪切波频散斜率图;3 cm×3 cm大小的取样框放在肝被膜下1 cm,1 cm大小的圆形测量区域(ROI)放置取样框内,得到以kPa测量的硬度和以m·s-1·kHz-1测量的频散斜率。所有操作按照佳能操作手册完成。以上所有检查,测量5次,取平均值(图1)。

注:包括剪切波速度图、剪切波到达时间轮廓(传播图)、超声图像、剪切 波频散斜率图。
1.3 胃镜检查 所有患者空腹接受常规胃镜(GIF-Q260J,Olympus,日本)检查,检查结果由同1名具备20年以上操作经验的胃镜医师完成胃镜统一阅片,判断有无食管胃静脉曲张,并根据LDRf[2]分型标准评估食管胃静脉曲张的部位、直径以及风险程度等。根据AASLD[3]标准,直径≥5 mm的静脉曲张或红色症(+)的静脉曲张或任何失代偿性的小静脉曲张被定义为HREGV。不符合以上情况的归为非高风险食管胃静脉曲张(NHREGV)。

2 结果
2.1 一般资料比较 本研究共收集各种病因肝硬化并接受胃镜检查患者235例,其中同期接受SWD/SWE检查患者171例,排除既往消化道出血、腹水、肝性脑病、肝肾综合征及脓毒血症;既往接受内镜治疗、脾切除手术治疗、TIPS及肝脏恶性肿瘤患者123例,最后纳入符合标准的代偿期肝硬化患者58例。其中,NHREGV组36例,HREGV组22例,平均(53.48±10.91)岁,男35例,女23例。乙型肝炎肝硬化39例,丙型肝炎肝硬化7例,酒精性肝硬化5例,其他原因肝硬化7例。HREGV组与NHREGV组相比,SWD、病因、脾脏直径、门静脉直径、TBil差异均有统计学意义(P值均<0.05)。肝脏SWE离散度较大,中位数9.45 kPa,HREGV组与NHREGV组的SWE差异无统计学意义(P=0.223)。两组其余相关临床基线特征见表1。

表1 NHREGV组与HREGV组一般资料比较
2.2 肝硬化HREGV无创指标的logistic分析 将文中涉及到的指标进行单因素分析,结果显示,病因、SWD、脾脏直径、门静脉直径差异具有统计学意义(此处P值放宽至0.1),将单因素分析结果有统计学意义的无创指标进行二元logistic回归分析,显示,SWD为代偿期肝硬化患者出现HREGV的独立危险因素(P<0.05),SWD每增加1 m·s-1·kHz-1,发生HREGV的概率增加67%(表2)
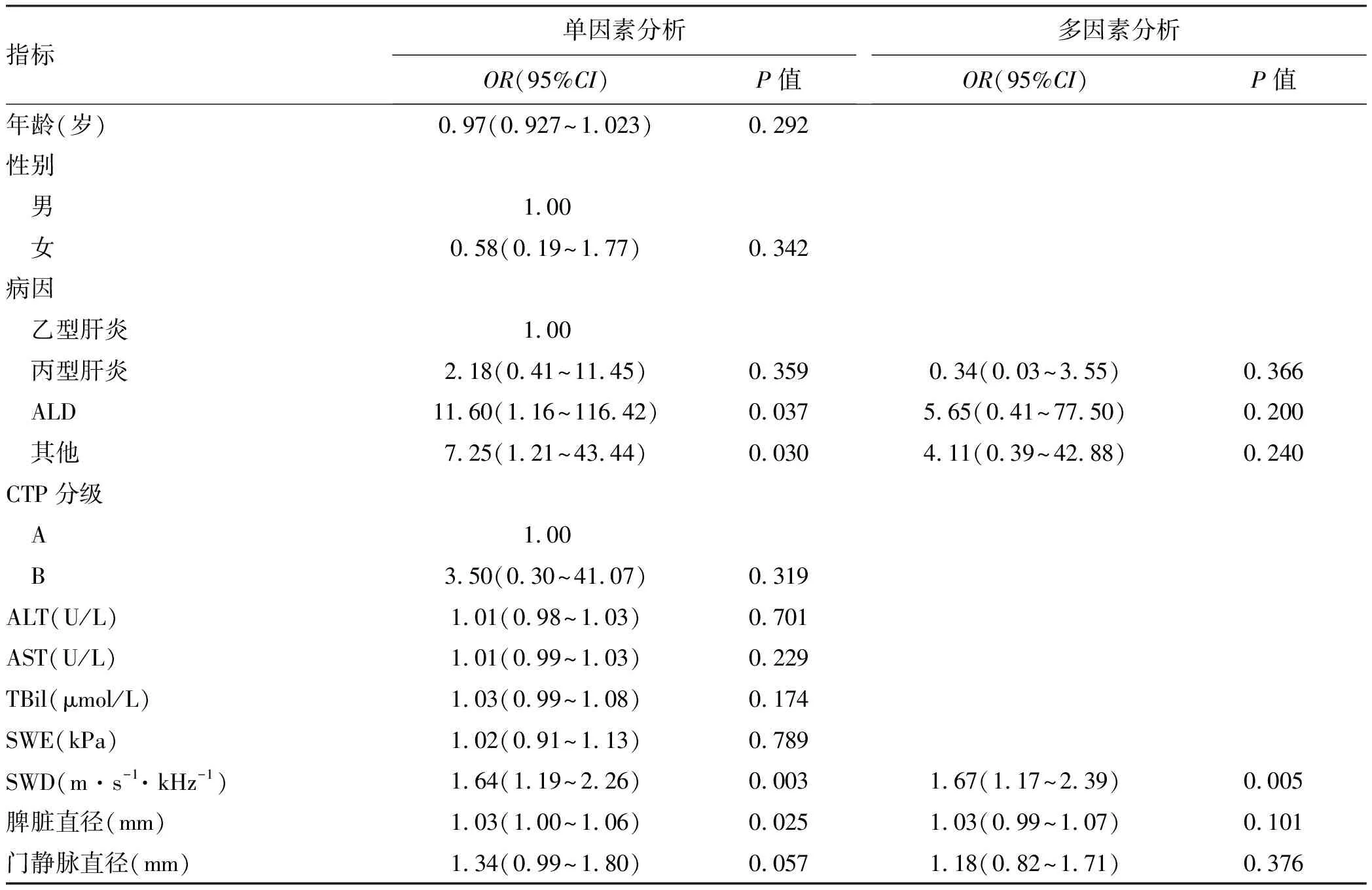
表2 代偿期肝硬化患者HREGV无创指标的logistic分析
2.3 肝脏SWE及SWD对HREGV的诊断效能 绘制ROC曲线评价肝脏SWD与SWE在诊断代偿期肝硬化患者HREGV的效能,结果显示在代偿期肝硬化患者中,SWD诊断HREGV的曲线下面积(AUC)为0.786,最佳临界值为15.35 m·s-1·kHz-1,特异度80.56%,敏感度81.82%;SWE诊断HREGV的AUC为0.596,特异度52.78%,敏感度68.18%,最佳临界值为9.25 kPa(表3,图2)。

图2 肝脏SWE/SWD诊断代偿期肝硬化患者HREGV的ROC曲线

表3 肝脏SWD/SWE诊断代偿期肝硬化患者HREGV的ROC分析
3 讨论
约50%的肝硬化患者存在食管胃静脉曲张,5%~15%肝硬化患者合并食管胃底静脉曲张破裂出血,一旦发生,常危及患者生命。基础肝病的严重程度、静脉曲张的大小和红色征是食管胃底静脉曲张破裂出血的主要危险因素。内镜是判断曲张静脉大小和出血风险最直观的检查手段,被认为是诊断静脉曲张尤其是高出血风险静脉曲张的“金标准”[10-11]。但内镜检查的侵入性及不舒适性,被患者接受程度低,尤其是无任何症状的代偿期肝硬化患者,往往导致干预治疗延后,甚至出现上消化道出血等急诊,因此无创诊断肝硬化患者静脉曲张越来越受到重视。
无创评估肝硬化患者静脉曲张的研究主要围绕血小板、超声、CT、核磁、仿真肝静脉压力梯度技术[12-16]等。血小板减少是肝硬化门静脉高压患者最常见的表现,它与门静脉压力和EGV的存在有一定关系,但是,单独使用血小板来诊断或排除EGV不够准确。联合血小板计数与其他非侵入性检查如肝硬度、脾脏大小和直径计算肝硬度脾/血小板评分、血小板/脾比、可以提高无创指标预测食管静脉曲张的价值,但在预测是否存在EGV方面的准确性有限,AUC为0.71~0.84[17]。瞬时弹性成像技术(TE),单独或结合血小板计数、脾脏大小,具有较好的临床显性门静脉高压诊断效能,可用于无创诊断肝硬化食管胃静脉曲张,并已被写入Baveno共识[1]和中国共识[18],但TE容易受到ALT、肥胖、肋间隙窄及腹水等影响。MRI、虚拟肝静脉压力梯度等技术程序比较复杂、并且价格较为昂贵[16,19],基层医院难以完成。
SWE是将弹性成像集成到常规超声图像中,具有可视、取样面积大,不受腹水、肋间隙、肥胖等因素影响的优点,可同时完成肝硬化患者常规肝脾形态结构、血流及占位病变检查,同时实现肝脏硬度检查,评估肝纤维化程度,实现对患者病情的“一站式”评估[20],避免TE的重复检查,临床适用性较高。SWE通过对肝硬度的测量对是否存在静脉曲张有很好的诊断效能,但对HREGV诊断价值有限[5]。SWE测定是假设所检测的组织是一个纯弹性体,在完全弹性组织中,无论剪切波频率如何,剪切波速度都是恒定的,然而,在黏弹性组织中,剪切波速度随频散而变化。研究[6,21-24]表明,SWE获得的频散斜率与肝脏坏死性炎症活动有关,小叶炎症活动程度是剪切波频散斜率的唯一决定因素。也有文献[25]报道用SWE诊断中重度肝纤维化的最佳阈值为剪切波频率依赖性。肝硬化是一个炎症坏死不断发展的过程,肝脏疾病如非酒精性脂肪性肝病和急性肝炎已被报道增加肝黏度,因此通过评估肝脏的弹性和黏度,即黏弹性特性,可以获得对肝硬度更准确的评估。
SWD在诊断肝硬化HREGV中的价值国内外尚未见报道。本研究结果显示,代偿期肝硬化患者肝脏SWD平均(15.17±2.45) m·s-1·kHz-1,其中HREGV组肝脏SWD显著高于NHREGV组;logistic回归分析显示,SWD为代偿期肝硬化患者发生HREGV的独立危险因素,SWD诊断HREGV的AUC为0.786,诊断价值中等。已知代偿期肝硬化患者静脉曲张程度与肝硬化程度相关,本研究的结果支持SWD与肝纤维化相关的观点[26],提示SWD可以用于预测代偿期肝硬化患者静脉曲张风险程度。本组患者肝脏SWE离散度较大,对诊断HREGV无价值,AUC为0.596,与以往研究结果不一致[26-29]。文献[20,30]报道不同超声的检查方法和所用参数各不相同,结果存在差异。一项Meta分析[31]显示超声SWE对肝纤维化严重程度的诊断准确性较高,但对门静脉高压和食管静脉曲张严重程度的诊断准确性中等,与本文的结果较类似。另外,指南中明确指出对于ALT升高的SWE对纤维化的诊断效能较低。本研究人群中ALT、AST及TBil有部分超过正常值可能导致本组SWE离散度较大。SWD因考虑了炎症坏死因素,结果相对SWE更加稳定,可能更能真实反映伴有炎症肝脏的纤维化程度。同时当门静脉压力梯度超过10~12 mmHg时,肝脏硬度与门静脉高压之间的相关性显著降低[32],这与在门静脉高压进展过程中,血管活性因子、自发分流通道形成、门静脉血栓形成等肝外因素对门静脉压力影响所占比例越来越大,导致静脉曲张的出现和加重与肝脏本身硬化程度的相关性降低有关,这也可能是SWE在预测HREGV中价值不大的原因。
本研究探讨了SWD在预测代偿期肝硬化患者HREGV中的临床价值,为无创评估肝硬化患者静脉曲张程度提供了一种新的思路,值得扩大样本进一步研究。 但本研究有以下不足:首先,样本数较少;其次,涉及肝硬化病因较多,以病毒性肝炎(乙型肝炎、丙型肝炎)为主,酒精性脂肪肝及非酒精性脂肪肝所致肝硬化样本量较少,不同病因肝硬化发展过程中炎症表现及脂肪变程度不同,需进一步开展单一病因肝SWD与HREGV的关系研究以得出不同病因预测HREGV的界值;第三,本研究仅在佳能Aplio i800超声设备中进行,结果仅能适用于本型号超声,不能推广到其他超声设备。
总之,本研究首次证实佳能Aplio i800超声的SWD可以在一定程度上预测代偿期肝硬化患者高风险静脉曲张的存在,有望为临床医师判断代偿期肝硬化患者是否存在HREGV提供一种简单的初筛工具,但尚不足以替代胃镜。
伦理学声明:本研究于2019年12月27日经由天津市第三中心医院伦理委员会审批,批号为IRB2019-022-02,所有患者都签订了知情同意书。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突。
作者贡献声明:王佳音负责数据收集,统计分析及论文写作;周洪雨、赵蕾负责对文章内容进行批判性审阅;徐佰国参与文章统计分析;李庭红、尹伟利、王芳、梁静负责数据收集,对文章内容进行批判性审阅;经翔负责本研究设计及实施研究;向慧玲负责本研究设计及论文审核。

