镍铜砷复合污染对土壤微生物和酶活性的影响
郭全恩, 曹诗瑜, 南丽丽, 展宗冰, 王 卓, 汪 堃, 李景峰
(1.甘肃省农业科学院土壤肥料与节水农业研究所,甘肃 兰州 730070;2.甘肃农业大学草业学院,甘肃 兰州 730070;3.甘肃省农业科学院,甘肃 兰州 730070)
土壤重金属污染已经成为当今世界重要的环境问题之一,受到世界各国学者的关注[1-2]。由于土壤重金属相比于其他污染物具有隐蔽性、不可逆性、长期性和潜伏性,一旦重金属含量超过了土壤自身的承载力,将会导致土壤生产力下降,从而引起土壤质量下降[3]。金昌市是全国重要的镍、铜、钴生产基地,尤其以硫化镍为主,居世界同类矿床第二位。在长期的矿产开采、选矿、冶炼及使用过程中产生了不少有害重金属,这些重金属通过粉尘、交通运输、污水灌溉、生活垃圾等途径对周边农田生态环境产生一定的影响[4]。因此,加强矿区周边农田土壤监管对保障区域粮食安全和生态环境建设具有重要的意义。
目前,有关金昌市土壤重金属污染特征的研究已有大量报道[5-7]。如廖晓勇等[8]研究表明,金昌市土壤样品Ni 和Cu 的超标率分别为70%和57%,污染面积分别为26 km2和24 km2;徐琪等[9]研究表明,金川区土壤Hg、Cr、Ni、Cu、Cd 和Pb 高于甘肃省土壤背景值,Ni 含量超过了国家二级标准。近年来,我国一直推进重金属污染防治方面的工作,2015年中央下达重金属专项资金36×108元,支持30个地市重点区域重金属治理和37 个重金属土壤污染治理与修复示范工程。金昌市金川区宁远堡镇白家咀村七队现有污染农田面积37 hm2,被列为首批全国土壤污染治理与修复试点之一,反映了其典型性、代表性和示范性。
土壤微生物作为土壤的重要组成部分,对土壤中的有机质、腐殖质以及养分的分解、形成、循环和转化起到了关键性驱动作用[10],在一定程度上保障着生态服务的可持续性[11]。胞外酶的分泌通常是土壤微生物代谢的限速步骤,胞外酶活性常用于指示微生物能量和营养需求与土壤养分状况的变化[12],在众多的土壤酶种类中,受关注程度比较高的是与碳、氮、磷循环密切相关的几种生态酶(过氧化氢酶、脱氢酶、脲酶、碱性磷酸酶)[13],它们功能的大小直接决定了碳、氮、磷原子从有机物大分子中释放的速率[14-15]。因此,充分认识重金属与土壤生物的相互作用机制,预知土壤重金属污染引起的生态效应,是科学有效地开展土壤污染防控与治理修复的重要前提[16]。贺玉晓等[17]对河南省焦作市韩王煤矿沉陷区土壤重金属含量与土壤酶活性的关系进行了研究,认为重金属对酶活性的影响取决于重金属的类型与含量。张涪平等[18]对西藏拉屋矿区(Cu-Zn-Pb)重金属污染与土壤微生物学特性之间的关系进行了研究,指出随着矿区土壤重金属含量增加,土壤酶活性、微生物量C、N、P均逐渐降低。闫文德等[19]对湘潭锰矿废弃地土壤酶活性与重金属含量之间的关系进行了研究,结果表明土壤过氧化氢酶与Zn、Mn、Pb 呈正相关,与Ni 呈负相关,脲酶与Pb呈负相关关系。因此,可以看出有关煤矿沉陷区、Cu-Zn-Pb 矿区和锰矿废弃地土壤重金属对酶活性和微生物多样性的研究已有文献报道,但有关镍铜砷复合污染矿区土壤重金属含量与生物学性状之间的关系鲜见报道。为此,本研究以金川区宁远堡镇白家咀村七队镍铜砷复合污染土壤为研究对象,采用大田调查的方法,探讨土壤重金属对土壤微生物和酶活性的影响,旨在为较早预知重金属毒害下土壤环境质量的变化和认识生态环境退化过程提供理论依据。
1 材料与方法
1.1 研究区概况
白家咀村隶属于甘肃省金昌市金川区宁远堡镇,地处甘肃省河西走廊东端,属大陆性温带干旱气候,全年日照时数2884 h,年平均气温10 ℃,年平均降雨量139 mm,无霜期156 d,平均海拔1553 m。区域内矿产资源丰富。土壤类型为灰棕漠土,耕层土壤基本理化性状为:有机质26.7 g·kg-1,pH 8.39,碱解氮54.7 mg·kg-1,速效磷21.6 mg·kg-1,速效钾243 mg·kg-1,碳酸钙质量分数为123.2 g·kg-1,砂粒(0.02~2 mm)质量分数为395.3 g·kg-1,粉砂粒(0.002~0.02 mm)质量分数为333.0 g·kg-1,黏粒(<0.002 mm)质量分数为280.2 g·kg-1,属壤质黏土。
1.2 样品采集与分析
在邻近矿区的宁远堡镇白家咀村七队,通过走访相关科研单位,确定了13个采样点、3个分区(A、B、C)(图1),采用GPS定位五点法取样,于2019年8月采集0~20 cm和20~40 cm土层土样,重复3次,封袋带回实验室风干过100目尼龙筛网保存。
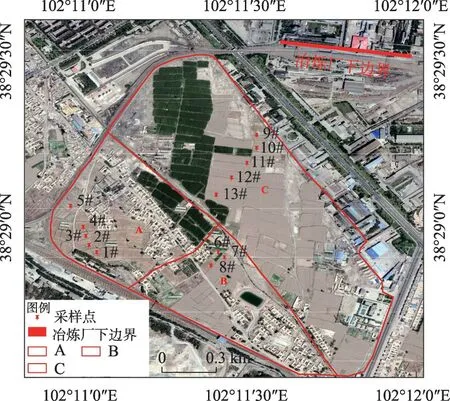
图1 研究区采样点分布Fig.1 Distribution of sampling points in the study area
Zn、Pb、Cd、Cr、Cu、Ni 采用四酸(盐酸+硝酸+氢氟酸+高氯酸)电热板消解,电感耦合等离子体质谱(ICP-MS)法检测;As和Hg是王水水浴消解,原子荧光光谱(HGF-V)法检测[20]。碱性磷酸酶—磷酸苯二钠(用硼酸缓冲液)比色法,以24 h后1 g土壤中释放出的酚质量(mg)表示;脲酶—靛酚蓝比色法,以24 h后1 g 土壤中NH3-N 质量(mg)表示;脱氢酶—三苯基四氮唑氯化物(TTC)比色法,以24 h后1 g土壤生成TTC的质量分数表示(mg)[21];过氧化氢酶—紫外分光光度法,以20 min 内1 g 土壤中分解的过氧化氢的质量(mg)表示[22]。细菌数量—采用牛肉膏蛋白胨琼脂培养基,以平板表面涂抹法计数;真菌数量—采用马丁孟加拉红培养基,以平板表面涂抹法计数[23];放线菌数量—采用改良高氏一号培养基[24],以平板表面涂抹法计数。以下列公式计算真菌、细菌和放线菌数量[25]。
菌数=(菌落平均数×稀释倍数)/干土质量
1.3 数据分析方法
用软件Sigmaplot 10.0作图,用SPSS 20.0软件对数据进行单因素方差分析,用邓肯多重比较法对数据进行多重比较。用软件CANOCO 5.0对土壤生物学性状与重金属含量之间的关系进行典范对应分析(CCA)。
2 结果与分析
2.1 土壤重金属总量
在0~20 cm 土层,13 个采样点的Cr、Ni、Cu、Zn、Pb、As、Cd 和Hg 的平均含量依次为:108.3、174.2、183.6、91.8、31.7、18.7、0.47 mg·kg-1和0.077 mg·kg-1;在20~40 cm土层,13个采样点的Cr、Ni、Cu、Zn、Pb、As、Cd 和Hg 的平均含量依次为106.1、129.0、119.4、84.3、27.1、16.8、0.34 mg·kg-1和0.056 mg·kg-1。依据《土壤环境质量/农用地土壤污染风险管控标准(试行)》(GB15618-2018)[26]中的风险筛选值分析,8 种重金属的风险值依次为:Cr(350 mg·kg-1)、Ni(190 mg·kg-1)、Cu(200 mg·kg-1)、Zn(300 mg·kg-1)、Pb(240 mg·kg-1)、As(20 mg·kg-1)、Cd(0.8 mg·kg-1)、Hg(1 mg·kg-1)。因此,依据土壤污染风险管控标准,13个采样点的8种重金属含量平均值未超过风险管控标准。
由图2可知,在0~20 cm和20~40 cm土层,土壤中Cr、Zn、Pb、Cd 和Hg 重金属含量均在风险筛选值以下,Ni、Cu和As个别点位超标。在0~20 cm土层,Ni、Cu 和As 点位超标率依次为:15.4%、30.8%和38.5%。超过风险值的点位Ni 是9 和11,Cu 是9、10、11和13,As是9、10、11、12和13,均处于C区域,这一区域距离冶炼厂最近,可能是由于冶炼厂烟囱长期排放烟气导致该区域重金属含量较高;在20~40 cm土层,Ni、Cu和As点位超标率均为7.7%,超标样点均是9号。因此,研究区土壤存在Ni、Cu、As污染的风险。
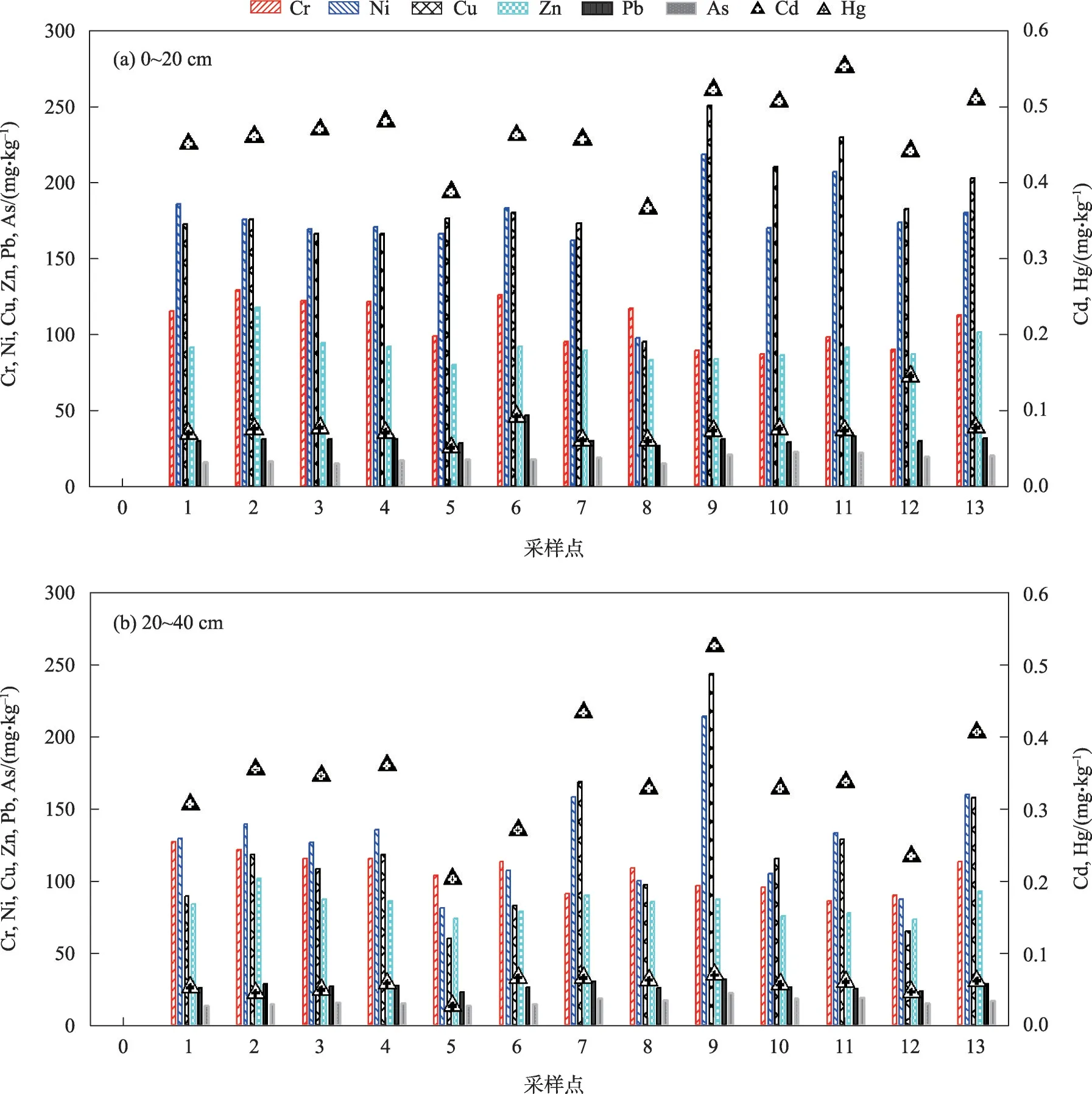
图2 不同采样点土壤重金属含量Fig.2 Content of soil heavy metals at different sampling sites
2.2 土壤生物学性状
2.2.1 土壤微生物数量 土壤微生物以真菌、细菌和放线菌为主,是土壤最具有活性的成分[25]。由表1可知,研究区土壤中主要以细菌为主,其次是放线菌,真菌数量最少,且随着土层深度的增加其数量显著减少。在0~20 cm土层,细菌数量在采样点1、3和10 之间,2 和13 之间差异均不显著,其余采样点之间差异显著(P<0.05,最大相差3.1倍);放线菌在采样点2、8、10 和12 之间,3、4 和5 之间,7 和13 之间,9和10之间差异均不显著,其余采样点之间差异显著(P<0.05);真菌数量在采样点1、7、12 和13 之间,2、3、4、9 和10 之间,5 和11 之间差异均不显著,其余采样点之间差异显著(P<0.05)。在20~40 cm土层,细菌数量在采样点2、3和7之间,4和10之间,8、9、11、12 和13 之间差异均不显著,其余采样点之间差异显著(P<0.05);放线菌数量在采样点1、2、4、7、8、9 和13 之间,5、10 和12 之间,6 和11 之间差异均不显著,其余采样点之间差异显著(P<0.05);真菌在采样点1、2、3、4、7、8、9、10 与5、6、11、12、13之间差异显著(P<0.05)。从A、B、C 3 个研究区的平均值来看,在0~20 cm 土层,细菌、真菌和放线菌均是B区最高,在20~40 cm土层,细菌是A区最高,真菌是B区最高,放线菌是C区最高。
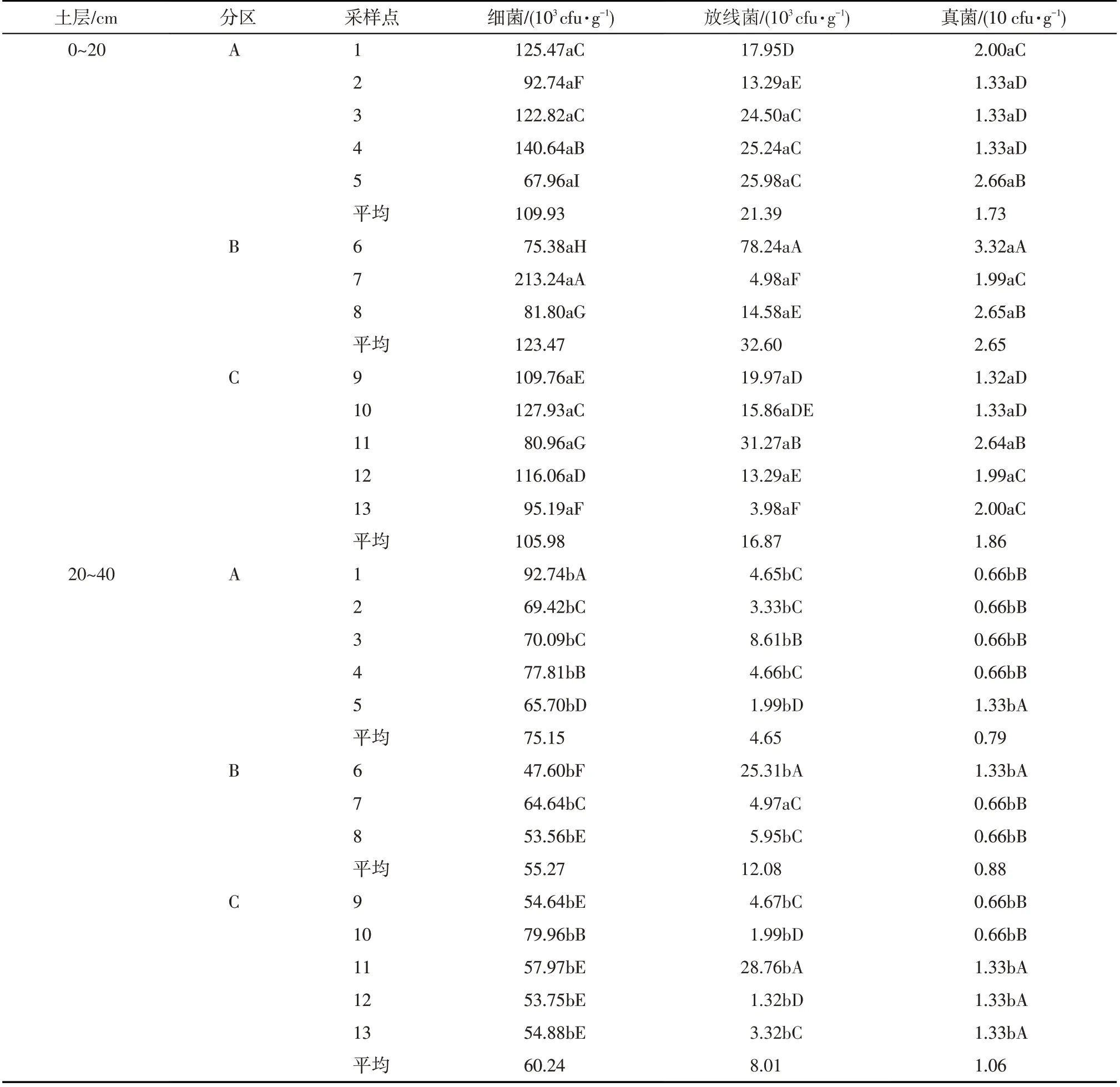
表1 不同采样点微生物数量变化Tab.1 Variation of soil microorganisms at different sampling sites
2.2.2 土壤酶活性 土壤酶是参与土壤新陈代谢的重要物质,主要来源于增殖和死亡的微生物,也可能来自植物根系、土壤动物区系和动植物残体释放[27],其参与有机质分解、土壤微生物能量和营养获取、污染物降解等重要的生态过程[28]。由表2 可知,脲酶、碱性磷酸酶基本呈现随着土层深度的增加而显著减小(P<0.05),而脱氢酶的含量随着土层深度的增加呈显著增加(P<0.05),过氧化氢酶除采样点5和11上下土层之间差异显著外,其余采样点上下土层差异均不显著。从A、B、C 3个研究区的平均值来看,在0~20 cm 土层,C 区脲酶含量最高,其次是A区,B区脲酶含量最低,从区域A到C,碱性磷酸酶含量逐渐降低,而过氧化氢酶和脱氢酶含量逐渐升高;在20~40 cm 土层,脲酶、碱性磷酸酶、过氧化氢酶均是C区最低,而脱氢酶是C区最高。
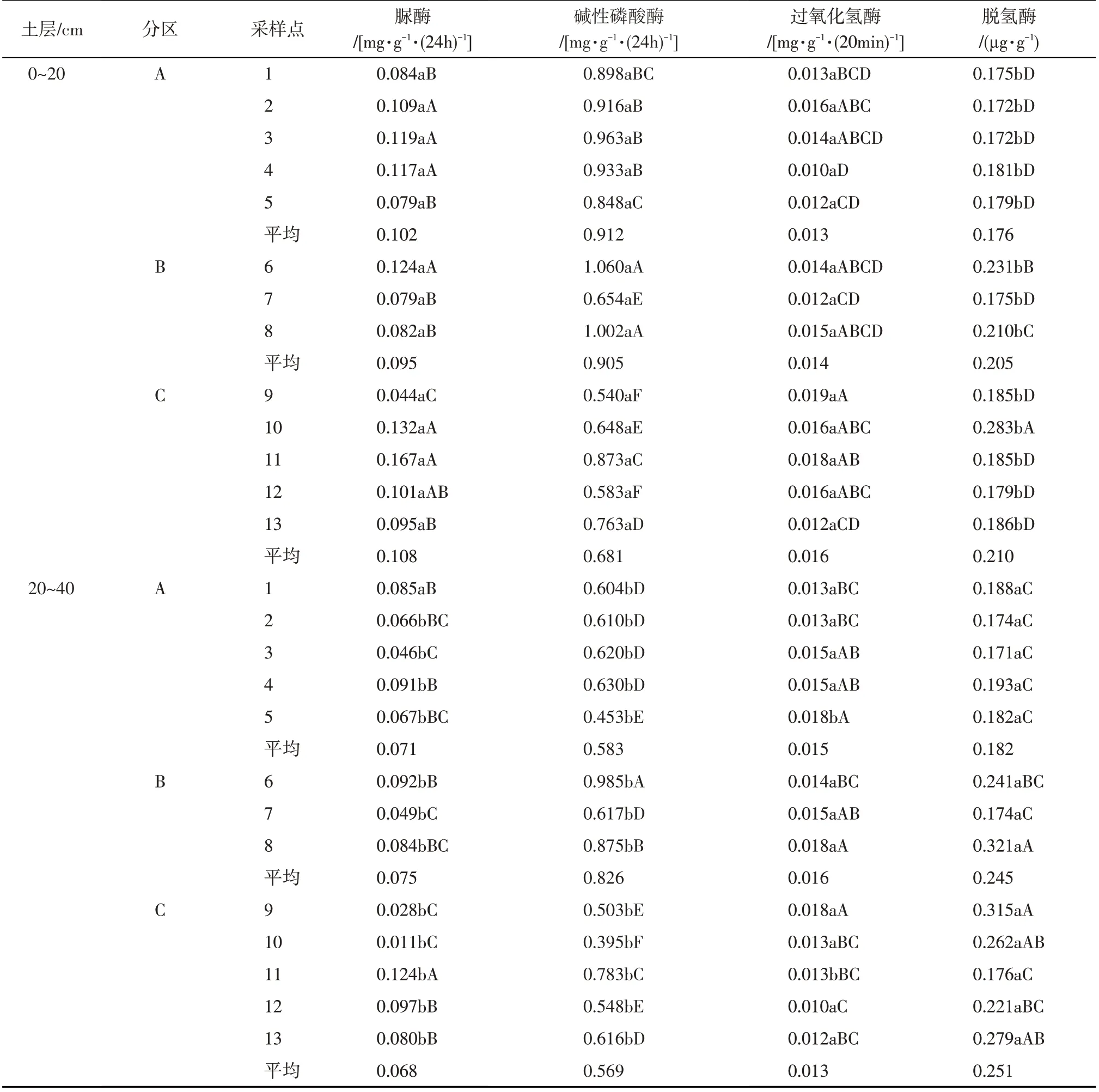
表2 不同采样点土壤酶活性变化Tab.2 Variation of soil enzyme activities at different sampling sites
2.2.3 土壤化学、生物性状及重金属含量之间的相关分析 通过相关分析表明(表3):土壤pH和有机质、Ni、Cu、Zn、Cd 之间呈极显著负相关关系(P<0.01);土壤有机质与Ni、Cu、Zn、Cd、Pb、放线菌、碱性磷酸酶之间呈极显著正相关关系(P<0.01),与Hg、真菌、脲酶、过氧化氢酶之间呈显著正相关关系(P<0.05);Cr与Zn、碱性磷酸酶之间呈极显著正相关关系(P<0.01),与As 之间呈极显著负相关关系(P<0.01)。Ni 与Cu、Zn、Cd、Pb、As、Hg、过氧化氢酶之间呈极显著正相关(P<0.01)。Cu 与Cd、Pb、As、Hg、过氧化氢酶之间呈极显著正相关(P<0.01);Cu 与Zn 之间呈显著正相关(P<0.05);Zn 与Cd 之间呈极显著正相关(P<0.01),与Pb 之间呈显著正相关(P<0.05);Cd 与Pb、As、Hg、过氧化氢酶之间呈极显著正相关(P<0.01),与细菌呈显著正相关关系(P<0.05);Pb 与Hg、真菌、放线菌之间呈极显著正相关(P<0.01),与碱性磷酸酶之间呈显著正相关关系(P<0.05);As与Hg、过氧化氢酶之间呈显著正相关(P<0.05);放线菌与真菌、脲酶、碱性磷酸酶之间呈极显著正相关(P<0.01);真菌与脲酶、碱性磷酸酶之间呈极显著正相关(P<0.01);脲酶与碱性磷酸酶之间呈极显著正相关(P<0.01);其余指标之间差异均不显著。
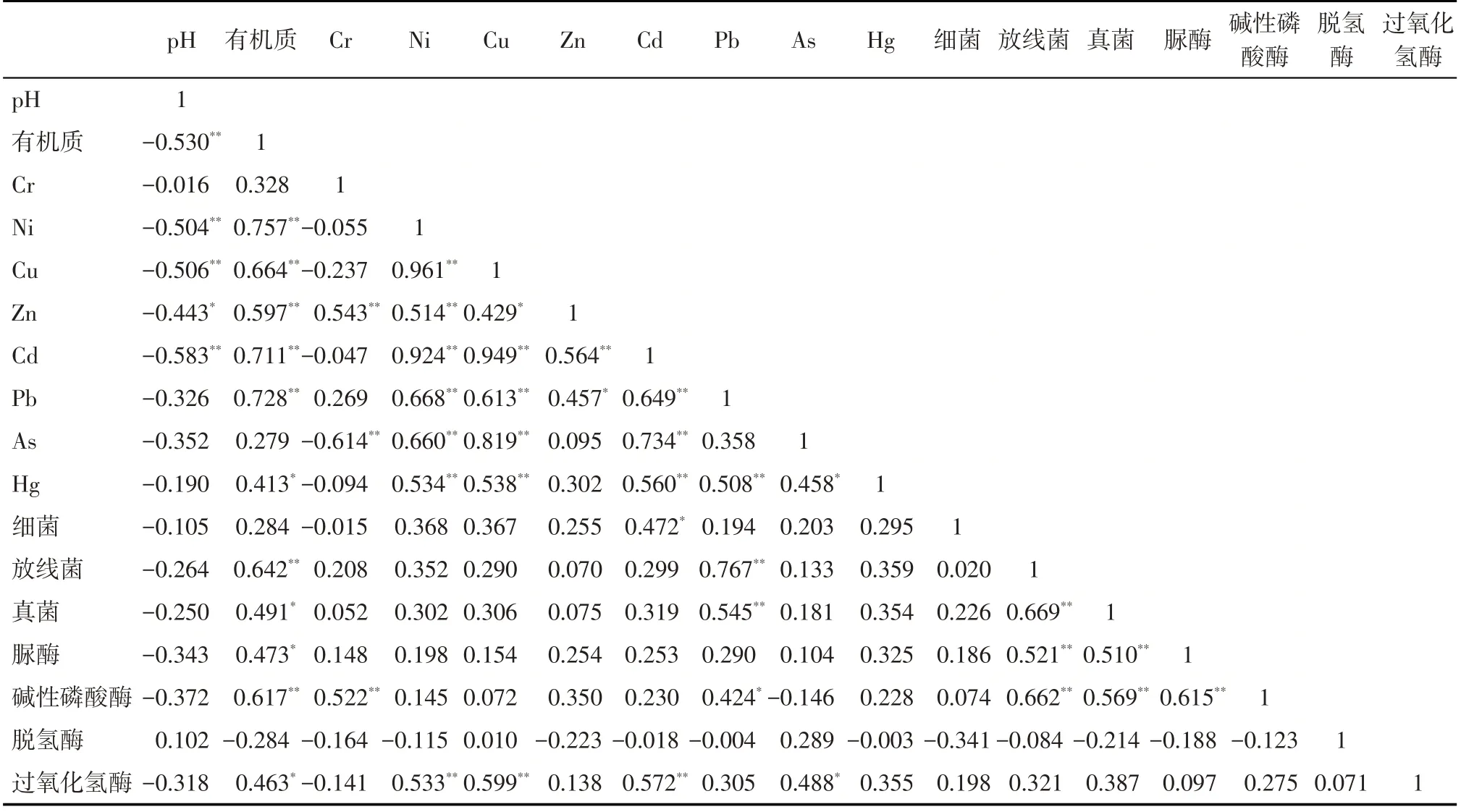
表3 土壤化学、生物性状及重金属含量之间的相关性分析Tab.3 Correlations coefficients between soil chemical and biological properties and the content of heavy metals
2.4 土壤生物学性状和土壤重金属含量之间的典范对应分析
为了进一步了解土壤中的重金属含量对土壤生物学性状的影响,对土壤生物学性状和土壤重金属含量之间的关系进行典范对应分析(图3)。结果表明:CCA1 和CCA2 分别解释总变异的58.38%和0.53%。Pb、Hg、Ni、Cu、Cd、As与细菌、脲酶、碱性磷酸酶、过氧化氢酶、脱氢酶呈负相关关系。Cr 与放线菌和真菌之间呈正相关关系,Zn与细菌之间呈正相关关系,细菌与放线菌之间呈负相关关系;蒙特·卡罗检验结果表明(表4),Pb、Zn 和Cr 为主导土壤生物学性状的主要因子,其贡献率依次为72.4%,16.2%和4.9%,且Pb、Zn 差异达显著水平(P<0.05);这说明土壤中Pb 和Zn 对农田土壤生物学性状有显著影响。

图3 土壤生物学性状与土壤重金属之间的典范对应分析Fig.3 Canonical correspondence analysis for soil biology properties and soil heavy metals content
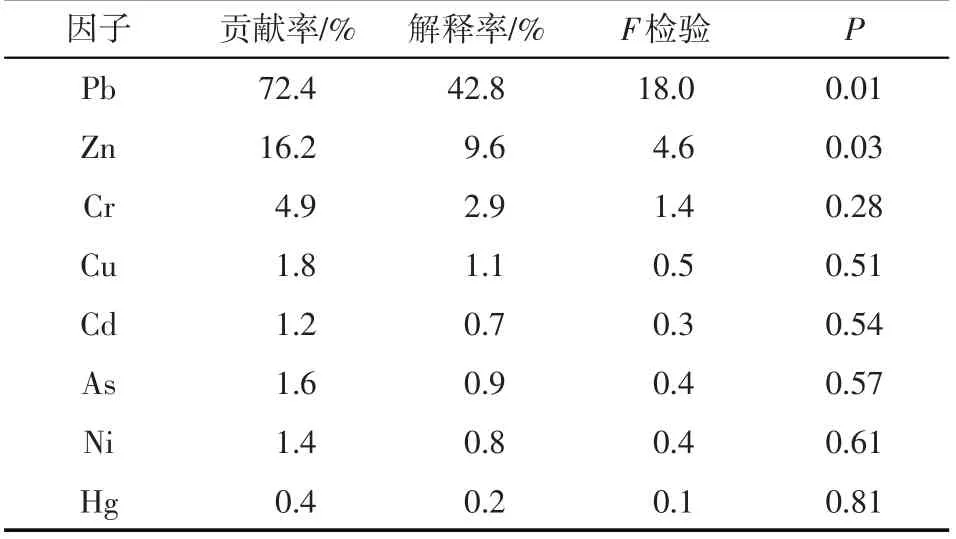
表4 典范对应分析蒙特·卡罗检验结果Tab.4 Results of Monte Carlo permutation tests from the canonical correspondence analysis
3 讨论
3.1 不同采样区重金属含量分布特征及影响因素分析
由表5 可知,Cr 含量在0~20 cm 和20~40 cm 土层均是A 区最高,其次是B 区,C 区最小,这可能是因为A 区距离矿山最近,其次是B 区,C 区最远,在长期的降雨淋溶条件下,矿山中的Cr淋溶导致不同区域Cr 的差异;Ni、Cu、Cd 和As 含量在0~20 cm 和20~40 cm 土层均是C 区最高,Hg 含量在0~20 cm 土层C 区最高,这是由于距离C 区不远的东北方向有一冶炼厂烟囱,且C区处于冶炼厂烟囱的下风向,长期排放烟尘可能导致该区域重金属含量较高;Zn含量在0~20 cm土层A区最高,其次是C区,B区最小,而在20~40 cm 土层A 区最高,其次是B 区,C 区最小,这可能是土壤本身的空间变异性所致。Pb含量在0~20 cm 和20~40 cm 土层均是B 区最高,其次是C区,A区最小;这是由于B区采样点距离公路最近,可能是由于机动车尾气污染所导致土壤Pb 含量增加。
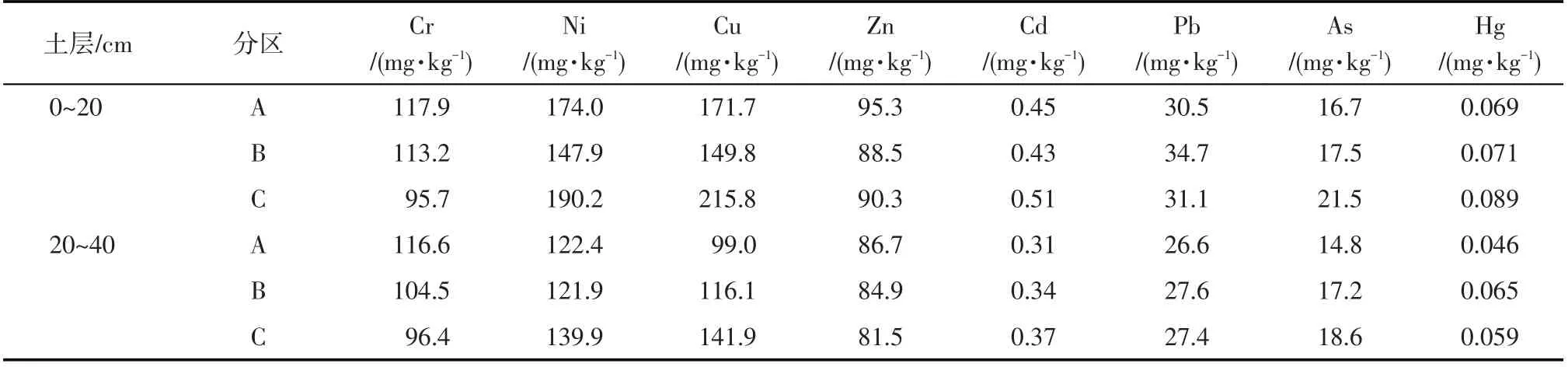
表5 不同采样区重金属含量Tab.5 Content of soil heavy metals at different sampling group
3.2 重金属复合污染对土壤微生物的影响
土壤微生物群落结构是表征土壤生态系统群落结构和稳定性的重要参数,能够较好地指示土壤环境污染状况[29]。土壤微生物一般包括细菌、放线菌和真菌等,在不同浓度范围的重金属,对土壤微生物数量增长的影响也不一定相同[27]。在大多数情况下,重金属污染能够明显影响土壤的微生物群落,如王秀丽等[30]认为,重金属Cu、Zn、Cd、Pb复合污染能够降低细菌、真菌、放线菌菌落数量,Gao等[31]指出,重金属Cd、Pb 复合污染能够降低细菌和放线菌菌落数量,而真菌对重金属污染不敏感。在本研究中,A、B、C 3个区域中,重金属Ni、Cu和As 在C区点位超标率最高,且在C 区0~20 cm 土层,细菌、真菌和放线菌菌落数量最低,这说明Ni、Cu和As复合污染能够降低细菌、真菌、放线菌菌落数量。
不同类群微生物对不同重金属的敏感程度不同,如吴春艳等[32]对水稻土研究认为,对Cd2+的敏感度为放线菌>细菌>真菌,对Cu2+的敏感度为真菌>放线菌>细菌;Pan 等[33]研究认为,细菌对重金属的敏感性高于真菌或放线菌;Zhang等[34]研究指出,重金属Cd-Cr 复合污染能够明显改变细菌群落结构,与土壤微生物量相比,其对重金属污染更为敏感;也有研究认为重金属对微生物的影响不仅与重金属总量有关,而且与其存在形态有关[35],陈任连等[36]研究指出,土壤总Pb含量与拟杆菌门和厚壁菌门呈显著正相关,而有效态Pb与放线菌门和酸杆菌门呈显著负相关。本研究发现,Cd与细菌呈显著正相关关系(P<0.05),Pb与真菌、放线菌之间呈极显著正相关(P<0.01)。本研究仅对重金属总量进行了研究,在以后的研究中应该对其存在的形态进行研究,探讨重金属形态和微生物生物量之间的关系。
3.3 重金属复合污染对土壤酶活性的影响
土壤酶不仅推动土壤中有机质的矿化分解和土壤养分C、N、P 和S 循环,而且是表征土壤质量的重要生物学指标[37],其优势在于测定简便、反应灵敏,能够较早预测重金属毒害下土壤养分和质量的变化过程[38];土壤酶活性对重金属胁迫的响应主要取决于重金属离子在土壤中的含量、价态以及土壤类型和理化性质[39-40]。例如土壤含水量的变化会改变氧化还原电位、重金属有效性和价态、微生物活性等,从而直接或间接影响重金属对土壤酶的毒性[41]。土壤有机质、黏粒、阳离子交换量、pH 是影响重金属抑制磷酸酶、脱氢酶、硝酸还原酶活性的主控因素[42-43];土壤微生物群落的特异性也会影响重金属抑制酶的活性[44],重金属对土壤酶活性存在低剂量激活和高剂量抑制现象[45]。另外,重金属老化过程对酶抑制程度,可能取决于重金属的有效性、微生物群落的抵抗力和恢复力、胞外酶的特性(例如同工酶的比例、抗性酶、土壤中酶库的大小等)[46]。在本研究中,对A、B、C 3个区域进行比较,重金属Ni、Cu 和As 在C 区点位超标率最高,且在C 区0~20 cm土层,碱性磷酸酶平均值含量最低,而过氧化氢酶和脱氢酶含量最高,这说明Ni、Cu和As复合污染能够降低土壤碱性磷酸酶含量,提高土壤过氧化氢酶和脱氢酶含量。
在本研究中还发现,土壤有机质与碱性磷酸酶、脲酶、过氧化氢酶之间呈显著正相关关系,这是因为土壤有机质含量越高,土壤对酶的保护和对重金属毒性的缓冲作用越强[41]。典范分析结果表明,土壤重金属Pb、Hg、Ni、Cu、Cd、As与细菌生物量、脲酶、碱性磷酸酶、过氧化氢酶、脱氢酶呈负相关关系,这与王盼盼等[47]报道土壤脲酶和过氧化氢酶活性随着Pb、Cd 含量的增加有明显的降低结果相一致;与闫文德等[19]研究土壤过氧化氢酶与Zn、Mn、Pb 呈正相关,与Ni 呈负相关不完全一致。
4 结论
通过对甘肃省金昌市金川区宁远堡镇白家咀村典型农田土壤重金属含量与土壤微生物和酶活性之间的关系分析,得出以下结论:
(1)研究区土壤在0~20 cm 土层,Ni、Cu 和As点位超标率依次为15.4%、30.8%和38.5%;在20~40 cm土层,Ni、Cu和As点位超标率均为7.7%。因此,冶炼厂生产活动已引起周围农田局域深层土壤重金属污染的问题。
(2)Pb、Hg、Ni、Cu、Cd、As与细菌、脲酶、碱性磷酸酶、过氧化氢酶、脱氢酶呈负相关关系。Cr 与放线菌和真菌生物量之间呈正相关关系,Zn与细菌生物量之间呈正相关关系,细菌生物量与放线菌生物量之间呈负相关关系。在铜镍砷复合污染区,过氧化氢酶活性对重金属Cu、Ni、Cd、As 较为敏感,可作为该区土壤质量评价的有效指标。
(3)在Pb、Zn、Hg、Ni、Cu、Cd、Cr、As 8种重金属中,研究发现Pb、Zn和Cr为主导土壤生物学性状的主要因子,其贡献率依次为72.4%、16.2%和4.9%,且Pb、Zn差异达显著水平。

