前列腺癌自适应放疗中基于深度学习的CBCT临床靶区及危及器官自动勾画
【作 者】 宋新宇,张翔宇,李京,梁兰,杨阳,李光俊,柏森
1 四川大学华西医院 放疗科,成都市,610041
2 武汉大学 物理科学与技术学院,武汉市,430072
0 引言
外照射放射治疗是前列腺癌的主要治疗手段,对前列腺癌死亡率、转移率、临床进展、治疗失败和并发症等终点进行大规模比较研究表明放射治疗与手术的效果相当[1]。有报告指出,随着前列腺癌放疗的分次剂量递增,肿瘤控制率不断提升[2],但相应增加了直肠、膀胱等危及器官(organ at risk,OAR)的副反应风险。在线自适应放射治疗(adaptive radiation therapy,ART)能根据临床靶区(clinical target volume,CTV)和OAR的轮廓修改计划,减少OAR的受照剂量和体积,降低不良事件发生率[3]。医用直线加速器的机载锥形束CT(cone-beam CT,CBCT)能获取患者解剖信息,在ART中发挥着重要作用[4-5]。
实现快速的ART计划设计的核心在于对CBCT 图像中CTV和OAR的快速准确勾画[6]。CBCT能够显示CTV和OAR在分次间的解剖学变化,多次勾画能通过评估分次间的平均轮廓来生成个性化的CTV外扩范围[7],辅助多叶准直器叶片运动优化和计划设计。目前,CBCT上的勾画多通过与计划 CT图像形变配准完成[8-9],如MIN[10]和 RayStation等[11]软件。但盆腔器官受充盈状态等影响存在较大的解剖差异,前列腺位置也受到肠道气体影响[12],基于强度的图像配准难以满足临床要求。此外,图像伪影和靶区形态改变也将破坏计划CT与CBCT的全局对应关系。为了消除图像配准带来的误差,有必要开发一种仅依赖CBCT图像的快速、自动的多器官勾画方法。
基于CBCT勾画的CTV和OAR的前列腺癌放疗计划设计的可行性评估结果表明:相比基于CT和MRI的计划,基于CBCT的计划呈现出更大的观察者间差异,采用自动勾画模型能够提高勾画结果的鲁棒性。为了规避CBCT图像软组织对比度差的劣势,提高勾画精度,许多课题组使用超声图像来辅助CBCT图像勾画,或使用CBCT生成伪MRI、伪CT图像作为模型输入[6,13-14],均实现了勾画精度的提升。在本研究中,我们使用基于U-Net网络的深度学习模型,在仅使用CBCT图像作为输入的情况下完成CTV、膀胱、直肠、股骨头的精确自动勾画。
1 材料与方法
1.1 基于U-Net的图像勾画
U-Net结构包括主干特征提取、加强特征提取和预测网络,其高分辨率的浅层信息用于像素定位,低分辨率的深层信息用于像素分类,具有所需数据体量小、精确度高、速度快等优点[15],广泛应用于医学图像勾画任务。我们改进了U-Net网络的拓扑结构,在主干特征提取网络中,使用VGG16网络架构,前2个模块包含2个卷积层和 1个最大池化层,后3个包含3个卷积层和1个最大池化层,在进行两次卷积后都进行批归一化(batch normalization,BN),使上下层参数分布保持一致,减少参数初始化影响,提高网络的泛化性能和收敛速度,再执行最大池化。在加强特征提取网络中,为方便网络构建,提高通用性,在每个模块先进行两倍逆卷积再进行特征融合,同样进行批归一化后执行两次卷积,使最终获得的图像和输入图像大小相同。最后,利用一个1×1卷积进行最终特征层的通道数调整,采用Concatenate层连接对应层数的主干特征提取模块与加强特征提取模块。激活函数为ReLU,我们设计的自动勾画模型框架,如图1所示。基于此结构添加2D网络层,得到最终模型。基于TensorFlow3深度学习框架在Python中完成搭建,在Linux操作系统工作站上使用 GPU进行模型训练。
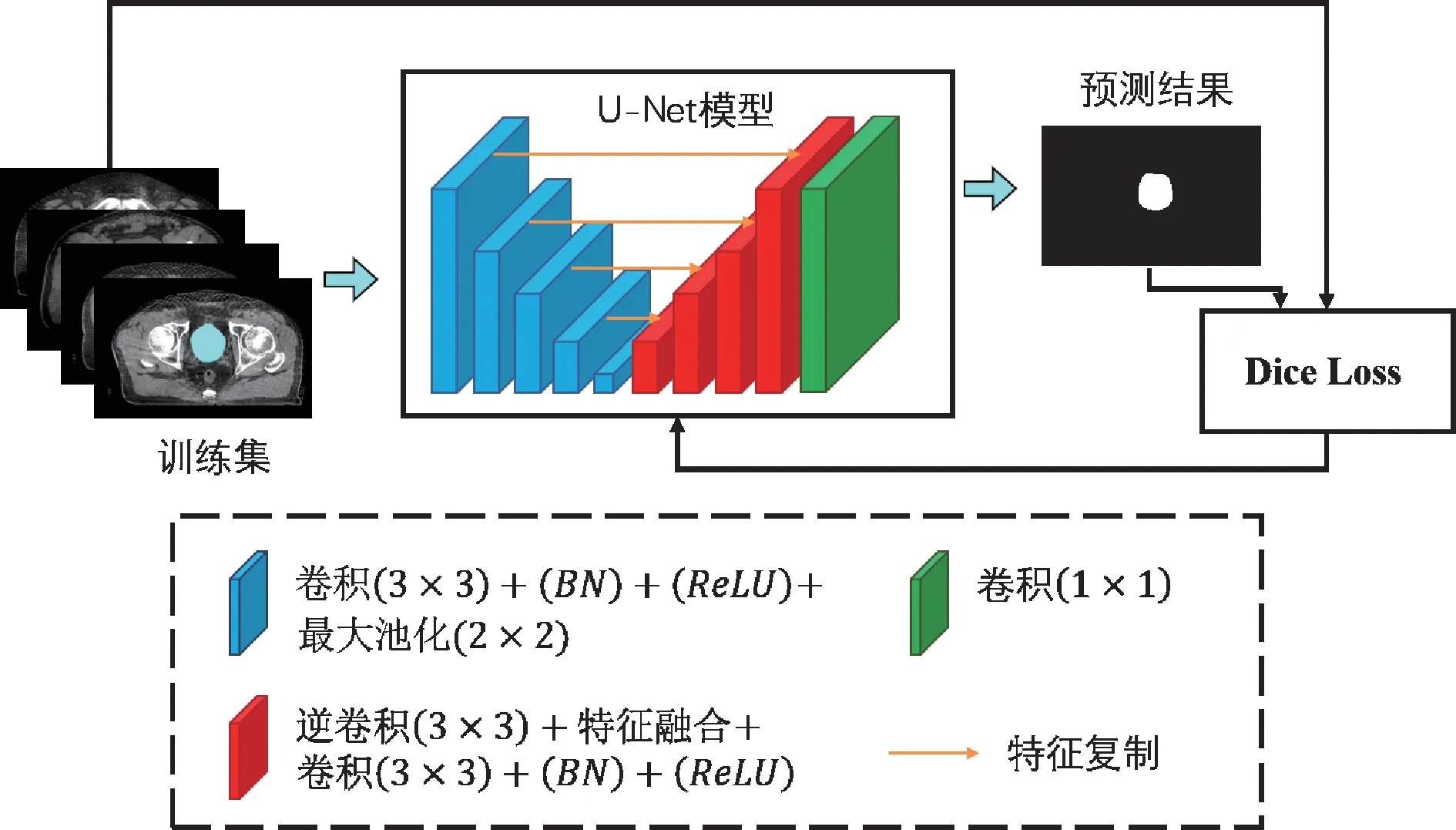
图1 自动勾画模型框架Fig.1 Proposed schematic workflow for prostate automatic delineation
1.2 数据集
本研究纳入2018年3月—2021年3月在四川大学华西医院放疗科Edge加速器放射治疗的40例前列腺癌患者,收集治疗期间的Varian On-Board Imager(OBI)CBCT全弧图像数据,图像分辨率为0.908 mm×0.908 mm×2.0 mm。本研究已获得机构审查委员会批准,使用放疗专用热塑膜将患者固定在仰卧位,在治疗位置进行计划CT扫描,并以3 mm的层厚和0.9 mm×0.9 mm的分辨率重建图像。每个患者的CTV和OAR轮廓首先由单个放疗医生手动描绘,然后经过审查、评估,最后由负责的放疗医生批准。OAR包括膀胱、股骨头和直肠。使用Raystation计划软件的图像配准功能将轮廓传播到CBCT,经医生细化修改和批准后,从RS文件中提取每张CBCT图像上CTV和OAR对应的掩模图,用于模型的训练和测试。
1.3 模型训练和测试
随机选取28例患者的CBCT与对应掩模图数据作为训练集,6例作为验证集,6例作为测试集。在将CBCT图像和对应的掩模图像输入模型前,对CBCT图像进行图像增强及标准化处理以提高轮廓清晰度,统一图像尺寸为512像素×512像素。采用Dice损失函数将模型输出的预测结果与输入的掩膜图像进行损失计算并反向传播,具体流程如图1所示。
使用翻转、旋转、缩放等数据增强方法扩大训练数据集,模型训练的批尺寸(batch_size)为8,神经网络的学习率范围通常为(10-6,1)我们通过试验确定使用学习率为 2×10-4的Adam优化器,进行60个epoch的训练,大约需要15 h。训练完成后,模型能在40 s内完成一个CBCT层面上的轮廓勾画。
1.4 评估指标
本研究采用Dice系数(dice similarity coefficient,DSC)及Housedorf距离(HD)指标来评估预测精度。DSC是一种集合相似度度量指标,用于计算手动勾画X和模型预测轮廓Y之间的体积重叠率,完全一致时DSC值为1,可由式(1)得出:

HD量化了手动勾画轮廓X和模型预测轮廓Y中点之间最大距离的95%百分位数,计算式为:
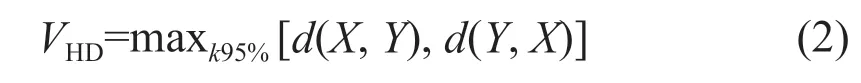
2 结果
自动勾画模型对CTV的勾画效果较好,训练集和验证集自动勾画模型的DSC值和HD值均基本一致,自动勾画方法的准确度的评估参数见表1,DSC为0.828,HD为3.822 mm,但在边界模糊区域仍存在一定的误差,6例测试例患者在CBCT上的CTV勾画,如图2所示,其中红色为预测模型,绿色为手动勾画轮廓,蓝色箭头所示区域误差较大。
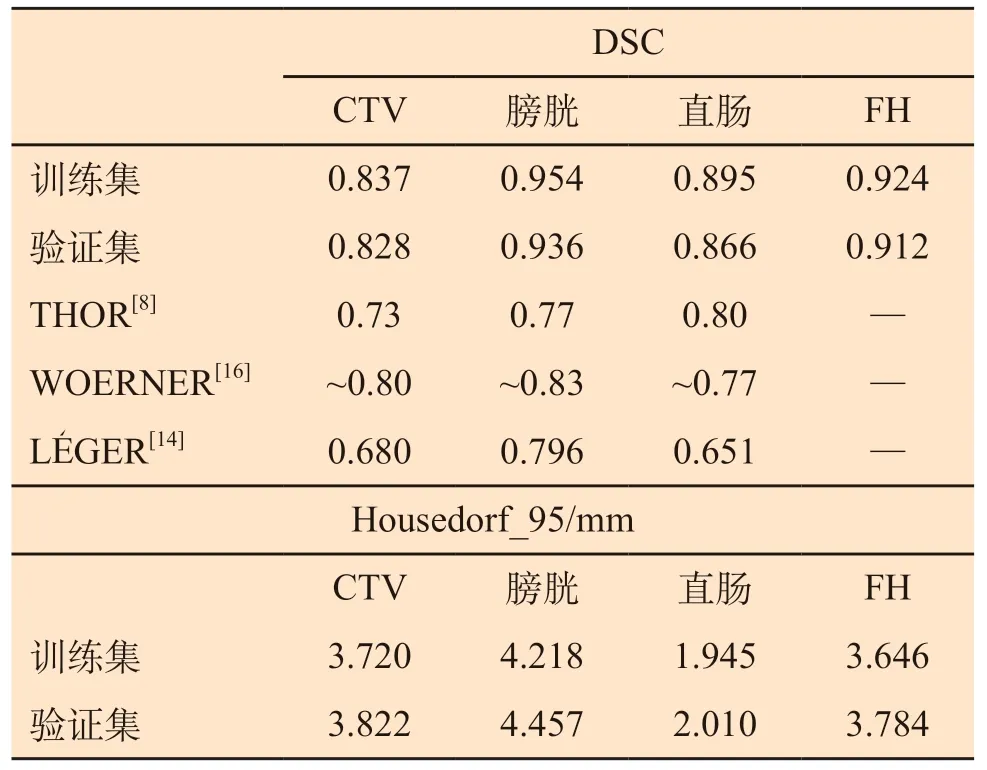
表1 自动勾画方法的准确度的评估参数Tab.1 Evaluation parameters for accuracy of automatic sketching method
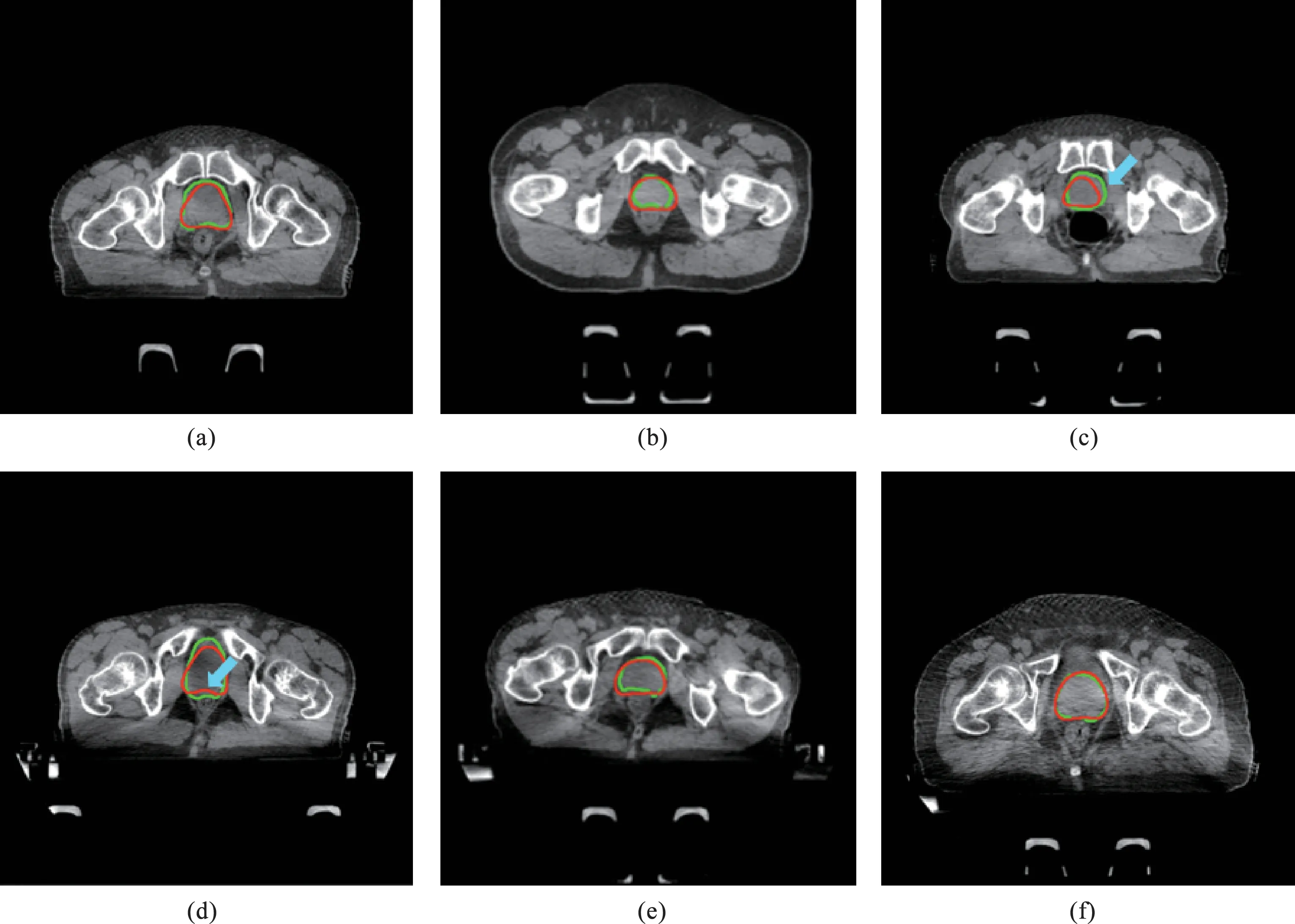
图2 6例测试例患者在CBCT上的CTV勾画Fig.2 Clinical target volume (CTV) contouring on CBCT for 6 test cases
模型对OAR的勾画效果优于CTV,膀胱、股骨头的DSC值均大于0.9,验证集中直肠的DSC值为0.866(见表1)。6例测试例患者在CBCT上的OAR勾画,如图3所示,绿色为手动勾画,红色为预测模型,图3表明自动模型所勾画的轮廓与手动勾画基本一致,在膀胱与前列腺交界区域的存在勾画误差,如蓝色箭头所示,表明U-Net网络对边界模糊的ROI性能有待提高,而对骨结构的分割性能更好。
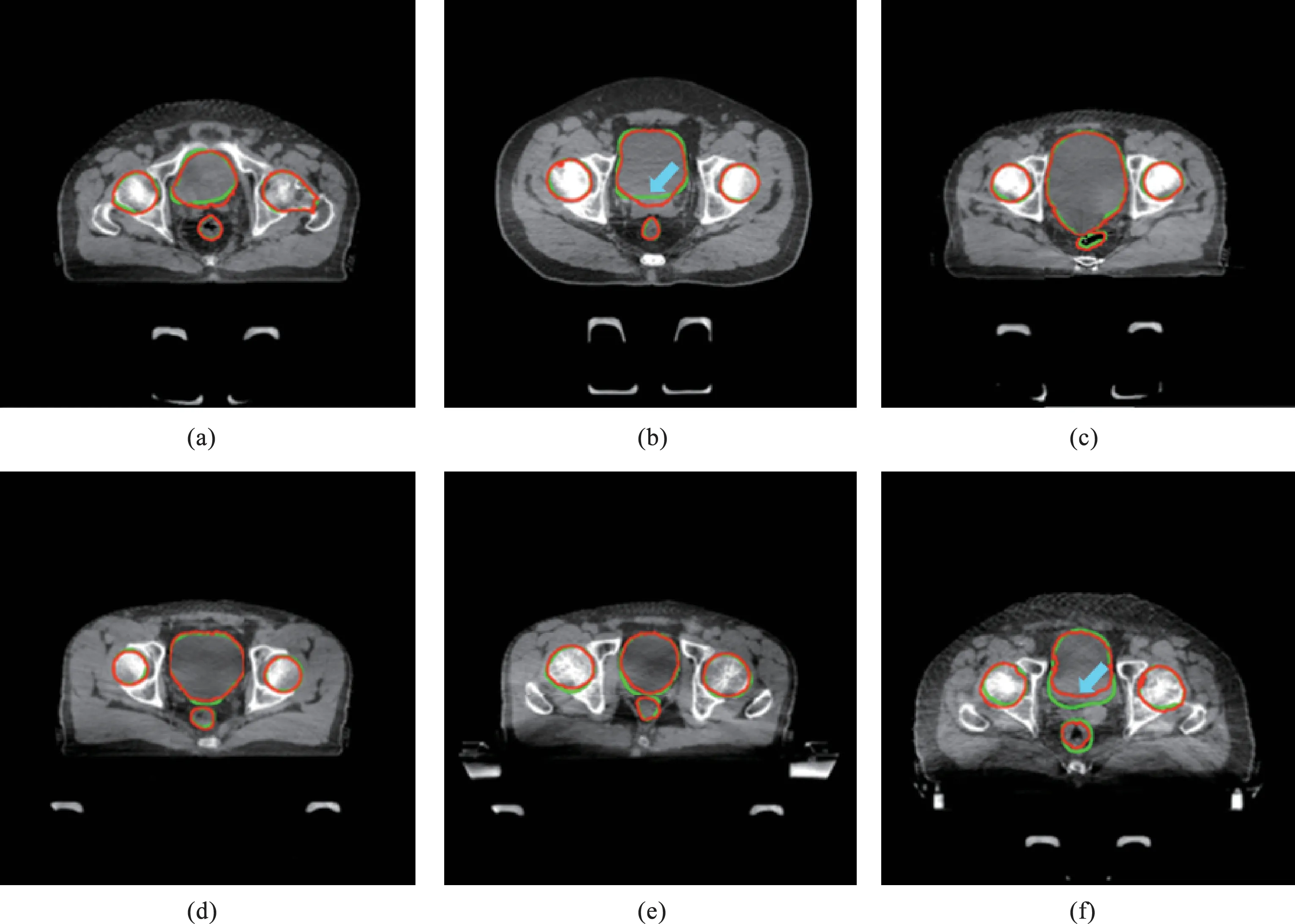
图3 6例测试例患者在CBCT上的OAR勾画Fig.3 Organ at risk (OAR) contouring on CBCT for 6 test case
3 讨论
CTV和OAR的勾画是放疗计划的基本任务,勾画精度会影响计划的适形性和剂量分布,但在CBCT图像上进行手动勾画耗时耗力,因此,开发一种在CBCT图像上快速准确地勾画多个器官的自动方法十分必要,这将简化ART流程,促进ART发展。我们提出了一种基于U-Net网络的CBCT图像CTV和OAR的自动勾画方法。
本方法在CTV和主要OAR上的勾画精度较高,膀胱的平均DSC值为0.936,验证集中CTV的DSC值为0.828,直肠的DSC值为0.866,股骨头的DSC值为0.912,精度高于BRION等[14]结果,而利用Raystation形变图像配准的CTV勾画DSC值仅为0.74[17]。在已发表的结果中,都采用了CBCT与CT、伪CT、MRI等影像结合的方法提高勾画精度,我们仅使用CBCT图像得到了精度更高的预测效果,证明对网络结构做出的改进能够提升网络性能。其中,最重要的改进为将主干特征提取网络替换为VGG16,并使用VGG16网络的预训练权重作为初始训练,提供了更优的模型初始化[18]。同时,本研究所用CBCT图像来自Varian OBI系统,OBI成像虽然在均匀性和低对比度分辨率上劣于计划CT,但成像的对比度、噪声比、空间分辨率与计划CT无异,不同患者间的CBCT图像一致性很高[19],保证了数据集的一致性,有益于模型预测精度的提升。OBI 系统的全弧成像几乎不需要校正即可用于ART[19],保证了本研究的临床应用价值。
本方法在膀胱和股骨头的勾画任务中取得了更好的效果,这是由于U-Net网络善于处理视觉和几何边缘信息,在处理边界清晰的勾画任务时具备优势,对边界相对模糊的部分较为劣势,考虑到直肠、前列腺的体积较小,得出的DSC值相应较低也可以接受。此外,我们观察到在器官的起始和结束附近的CT层面勾画效果相对较差,这可能源于患者间的轻微差异和放疗医生对起始和结束位置的不同定义,导致这些CT层面有特征偏差,削弱了模型的识别能力[20]。
本研究得到的模型在CBCT自动勾画中取得了较好的效果,但还存在一些限制。首先,由于软组织对比度低,在CBCT上进行手动勾画比较困难,存在较大的观察者偏倚。我们纳入的40个病例的轮廓细化修改是由一名医生完成的,这可能受到医生勾画习惯的影响,为了解决这个问题,需对CBCT上的手动勾画进行观察者间一致性评估,以便从数据集中排除观察者间差异较大的患者,扩大观察者间的共识轮廓数量能够提高手动勾画轮廓的可靠性。我们也会继续扩大数据集,获取更多的训练图像,进一步提高模型性能。其次,在常规的前列腺癌治疗中,还需要评估精囊、淋巴管、小肠等OAR剂量,以实现基于CBCT的自适应放射治疗。在下一步工作中,我们将研究CBCT勾画精度的剂量学效应,以评估其对前列腺放疗计划质量的影响。
4 结论
本研究团队开发了一种用于前列腺放疗的CBCT图像勾画方法,能快速自动勾画CTV和OAR,具有较高的精确度,可以减少手动勾画时间,简化自适应放疗的计划流程,具有一定的临床应用价值。

