苯并[a]芘降解菌在不同土壤无机胶体表面的吸附研究
甘信宏,滕 应,牟婷婷,刘国强,徐 建①,骆永明
〔1.生态环境部南京环境科学研究所/ 国家环境保护土壤环境管理与污染控制重点实验室,江苏 南京 210042;2.中国科学院土壤环境与污染修复重点实验室(中国科学院南京土壤研究所),江苏 南京 210008;3.中国科学院大学,北京 100049〕
由于微生物降解具有成本低、非二次污染等特点,已成为农田多环芳烃(PAHs)污染土壤修复的主要技术手段之一[1-2]。微生物修复的关键在于高效降解微生物的筛选与开发[3]。笔者课题组从长期重PAHs污染场地土壤中筛选出一株能够以高分子多环芳烃苯并[a]芘(BaP)为唯一碳源的高效降解菌——噬氨副球菌(ParacoccusaminovoransHPD-2),将菌株HPD-2接种到含有3.0 mg·L-1BaP的无机盐培养基中,5 d后BaP降解率可达89.7%,然而接种到污染土壤中,14 d降解率只有26.0%[4]。这是因为外加降解微生物于土壤后,多环芳烃的生物降解受到土壤组分、环境因素和营养条件等多种因素的制约[5]。土壤组分对微生物降解的影响已成为微生物修复污染土壤研究领域的核心内容之一[6]。
作为土壤中最活跃的组分,土壤胶体构成了土壤功能的基础,其中,无机胶体构成了土壤胶体的骨架,在土壤污染物迁移转化过程中起着重要作用。为研究不同无机胶体对微生物降解的影响,首先要了解无机胶体与降解微生物之间的界面作用机制。为此,以噬氨副球菌(ParacoccusaminovoransHPD-2,革兰阴性菌)和性质差异大的赤铁矿、高岭石和蒙脱石3种典型土壤无机胶体为研究对象,采用传统物理化学和微生物学方法,综合运用比表面仪、Zeta电位仪、动态光散射仪、X射线衍射、接触角仪和红外光谱等仪器,在系统表征菌株HPD-2细胞和无机矿物胶体表面性质(比表面积、Zeta电位、疏水性和等效粒径)的基础上,通过批处理实验研究降解菌HPD-2细胞在不同无机矿物胶体表面的吸附特征,采用Ex-DLVO理论探究菌株HPD-2与无机矿物胶体颗粒间的吸附作用力和相互作用能,分析菌株HPD-2在不同无机矿物胶体表面吸附的主要作用力,比较菌株HPD-2细胞在不同无机矿物胶体上的吸附特征,并对其内在机理分别进行讨论,进而阐明菌株HPD-2细胞在无机矿物胶体表面的内在吸附机制,为研究无机矿物对降解微生物活性和微生物在矿物表面定殖的影响机制提供理论依据。
1 材料与方法
1.1 噬氨副球菌HPD-2的培养与活化
菌株HPD-2分离自江苏省无锡市某长期受高浓度PAHs污染场地土壤[4]。菌株保存于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号为CGMCC No. 2568[7]。将保存的菌液管放入冰盒中缓慢融化后,吸取少许菌液接种于10 mL液体LB培养基[8](成分为5.0 g酵母提取物、10.0 g蛋白胨和10.0 g NaCl混匀于1 L水中)中进行复壮培养,培养12 h(避光,30 ℃,150 r·min-1)后按1∶10接入150 mL液体LB中培养24 h。将菌液在相对离心力(RCF)为8 000条件下离心5 min,弃去上清液,并用0.2 mol·L-1PBS缓冲液(磷酸盐缓冲液,pH=7.4)清洗2次后悬浮于0.1 mmol·L-1KNO3溶液中,利用酶标仪(BioTekμQuant,美国)测定细胞悬液在波长为600 nm的D600值,并将D600值调至1.0,细胞浓度约为2.8×108CFU·mL-1。
1.2 无机胶体的制备与表征
根据SCHWERTMANN等[9]的制备方法,在实验室中合成赤铁矿。合成方法简要说明:在90 ℃恒温条件下,将300 mL 1.0 mol·L-1KOH溶液缓缓滴加入500 mL含40 g Fe(NO3)3·9H2O的溶液中,转移到密闭烧瓶内,随后加入50 mL 1.0 mol·L-1NaHCO3溶液。经90 ℃老化48 h后,将混合液以RCF为5 000离心20 min后弃去上清液备用。
高岭石和蒙脱石(AR)购自上海国药试剂有限公司。利用沉降虹吸法[10],将制备的赤铁矿同购买的黏土矿物中粒径<2 μm的组分分离出来,得到粒径<2 μm的无机胶体组分。将得到的无机胶体用超纯水洗至上清液电导率<20 μS·cm-1,最后将沉淀用体积分数为95%的乙醇清洗去除少量有机物,置于110 ℃烘箱中烘干12 h后,研磨过0.15 mm孔径筛,备用。
将得到的3种无机胶体分别用X射线衍射仪(XRD,Ultima IV,Rigaku Corporation,日本)进行分析鉴定[11]。采用V-Sorb 2800P analyzer(Gold APP Instrument Co.,中国)对无机胶体外比表面积进行Brunauer-Emmett-Teller(BET-N2)测定[12]。细菌比表面积测定则采用亚甲基蓝吸附测定法[13],Zeta电位(ζ, mV)和等效粒径(De, μm)采用Zeta电位仪(ZetaPlus 90,Brookhaven Instruments Corporation,美国)在pH为7.0的0.1 mmol·L-1KNO3电解质溶液条件下测定[14]。接触角测量采用静态液滴接触角法[15]。
1.3 无机胶体对噬氨副球菌的等温吸附实验
根据蒋代华[16]研究的细菌和无机胶体的等温吸附方法进行改进。简要说明:将0.25~10 mL细菌悬液分别加到含有200 mg无机胶体的50 mL三角瓶中,以1 mmol·L-1KNO3溶液为背景电解质溶液,控制pH为7.0,补充去离子水至总体积为20 mL。将混合体系置于摇床中,在25 ℃条件下以200 r·min-1振荡240 min至吸附平衡。采用密度梯度离心法分离游离态和矿物结合态细菌。吸取10 mL悬液于20 mL离心管中,用5 mL移液枪小心地向管底加入5.0 mL质量分数为60%的蔗糖溶液(在离心管底形成蔗糖层)。再将离心管在RCF为3 000低速条件下离心20 min,然后小心地将游离细菌和上层清液(10 mL)转移到洁净离心管中(切勿扰动或吸取底部矿物)。用旋涡振荡仪充分分散游离菌体悬液,在600 nm波长下测定其吸光度D600值,根据“吸光度-细胞浓度”标准曲线计算游离菌浓度。细菌吸附量为细菌加入量减去游离菌量,即为单位质量无机胶体吸附菌体的鲜重,单位为mg·kg-1。将加入同等体积KNO3背景电解质溶液(0.25~10 mL)代替菌液作为对照。
1.4 傅里叶红外光谱与场发射电子扫描显微镜
将1.3节等温吸附实验中离心得到的沉淀冷冻干燥后,采用傅里叶变换红外光谱仪(FTIR,Thermo Nicolet Company,美国)进行分析[17],采用OMNIC软件进行数据处理和分析。利用场发射电子扫描显微镜(FE-SEM)观察细菌在无机胶体上的分布及形貌。将无机胶体(200 mg)与2 mL细胞悬液(D600=1)在pH为7.0的0.1 mmol·L-1KNO3溶液(体系最终体积为20 mL)中振荡240 min(避光,150 r·min-1,25 ℃)。然后将样品离心分离,用0.1 mmol·L-1KNO3溶液洗2次,利用体积分数为2.5%戊二醛溶液进行固定2 h以上,然后用0.1 mmol·L-1KNO3进行清洗,再分别用体积分数为30%、50%、75%和100%的乙醇清洗,最后将样品固定在硅晶片上脱水。经冷冻干燥后,利用场发射电子扫描显微镜(FE-SEM)观察细菌在无机胶体上的分布及其形貌[18]。
1.5 扩展DLVO理论
DLVO理论是一种关于胶体稳定性的理论,是带电胶体溶液理论的经典描述分析。在经典DLVO理论的基础上,VAN OSS[19]提出了扩展DLVO(Ex-DLVO)理论,即总位能(GTot)等于范德华力(GLW)、疏水作用力(GAB)和静电力(GEL)等作用力之和[20],计算公式为
GTot(d)=GLW(d)+GEL(d)+GAB(d)。
(1)
式(1)中,G为作用能,J;d为两粒子间距,nm。
各作用力计算公式[21-22]为
(2)
(3)
(4)
式(2)~(4)中,1表示细菌,2表示无机胶体颗粒,w表示水;r1为细菌等效粒径,m;λ为水衰减长度,通常为0.5 nm;d0为最小平衡距离,为0.157 nm;ε为水的介电常数,为6.96×10-10V-2·m-1;A1w2为水中细菌与无机胶体的联合Hamaker常数,J;ΔGAB(d0)为细菌矿物间距最小(d0)时的Lewis酸碱作用能,J·m-2;ψ01和ψ02分别为细菌和无机胶体表面电位,V;κ为Debye长度的倒数,m-1。
A1w2由表面张力参数中的范德华力组分计算得到,其计算公式[22]为
(5)
ΔGAB(d0)计算公式为
(6)
式(5)~(6)中,γ为无机胶体表面张力参数,其中,γ+和γ-分别为电子受体和供体组分的表面张力参数。
ψ01和ψ02计算公式为
(7)
式(7)中,ζ为颗粒的Zeta电位,mV;r为相互作用的粒子半径,m;z为胶体表面到滑动面间的距离,取0.5 nm[22]。κ与溶液离子强度有关[23],计算公式[24]为
(8)
式(8)中,kB为波尔兹曼常数,取3.81×10-23J·K-1;T为温度,取298 K;e为电子电量,取1.602×10-19C;NA为阿伏伽德罗常数,6.02×1023mol-l;I为离子强度,mol·m-3。
γ2+和γ2-一般通过测定固体(无机胶体)与3种供试液体的接触角求解得到[25]。该研究供试液体为水(H2O)、甲酰胺(CH3NO)和二碘甲烷(CH2I2),分别测得相应接触角,进而求得固体(无机胶体)表面张力参数。参照MICHALSKI等[26]的研究,3种液体表面张力参数见表1。
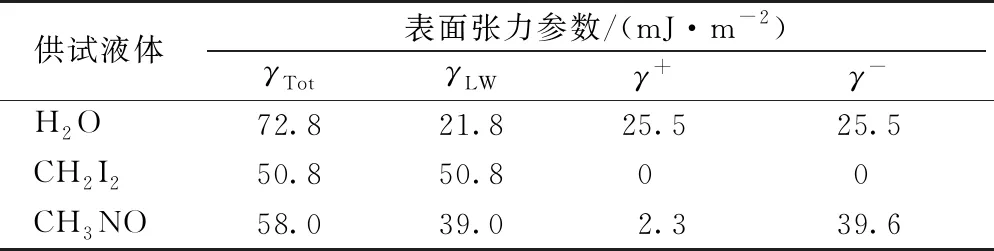
表1 测定接触角的供试液体表面张力参数
1.6 数据统计分析
采用Microsoft Excel 2011软件进行数据统计与表格制作;采用Origin 8.5软件进行图件绘制;采用SPSS 15软件对数据进行LSD差异显著性检验。
2 结果与讨论
2.1 无机胶体与噬氨副球菌的特性表征
选取高岭石、蒙脱石和赤铁矿3种无机胶体XRD图谱中3个特有衍射峰,将测得的衍射数据与国际衍射数据中心数据进行对比,得到理论上为100%无机胶体组分。菌株HPD-2和3种无机胶体的等效粒径(De)、外比表面积(SESA)、Zeta电位和不同液体接触角结果见表2。

表2 无机胶体和菌株HPD-2细菌的特征
由表2可知,赤铁矿粒径最小,高岭石次之;相应地,赤铁矿比表面积最大。而蒙脱石比表面积大于高岭石,这可能与这两种黏土矿物的结构有关。在Zeta电位方面,赤铁矿表面带正电,而高岭石与蒙脱石表面带负电荷,且高岭石电负性高于蒙脱石。由于噬氨副球菌为革兰阴性菌,其细胞表面含有大量羟基、羧基等官能团,使得菌株HPD-2表面也带负电荷[27]。界面与水的接触角越大,表明疏水性越强,通过接触角的比较得到疏水强弱的顺序为菌株HPD-2>蒙脱石>高岭石>赤铁矿。
2.2 噬氨副球菌菌株HPD-2的吸附等温线
根据240 min后上清液中细胞平衡浓度(CE),采用差减法计算得到无机胶体吸附菌量(Q),并以CE为横坐标,以Q为纵坐标绘制等温吸附散点图。采用3种经典吸附模型对得到的散点数据进行模拟,得到相关参数(表3)。

表3 3种无机胶体对菌株HPD-2的吸附等温线参数
由表3可知,采用Freundlich和线性方程拟合得到的决定系数R2均非常小,表明两类吸附模型不适用于该吸附过程。而对于Langmuir吸附模型,3种无机胶体吸附常数k由大到小排序为赤铁矿>>高岭石>蒙脱石。结合表2各样品性质来看,推测可能是由于各胶体电负性和表面疏水性差异造成的,且表面电荷起主导作用,使得胶体与菌株相互结合的作用力不一样,进而表现出不同的吸附强度。比较3种模型R2发现,3种无机胶体Langmuir方程R2均高于Freundlich方程和线性方程,且均大于0.86,由此可见,矿物对菌株的吸附比较符合Langmuir模型。进而采用Langmuir方程分别拟合各种无机胶体对菌株HPD-2的吸附等温线(图1)。
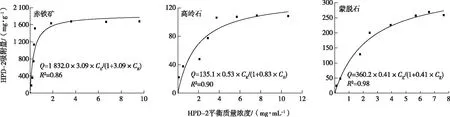
Q为无机胶体吸附菌量,CE为细胞平衡浓度。
拟合后,3种无机胶体对菌株理论最大吸附量(Qm)由大到小依次为赤铁矿>>蒙脱石>高岭石。这可能是由于赤铁矿表面带正电,能与带负电的细菌异电相吸,且赤铁矿比表面积也大于其他2种黏土矿物,有更多吸附位点暴露给菌株HPD-2细胞。同理,由于比表面积的差异,蒙脱石吸附菌量高于高岭石。
2.3 无机胶体与噬氨副球菌HPD-2之间的作用力
根据Ex-DLVO理论计算得到单个菌株与单个矿物胶体之间的总相互作用能(GTot)随颗粒间距的变化(图2)。由图2可知,当颗粒间距d>50 nm时,两粒子之间的相互作用能几乎为0,当d不断减小时,赤铁矿GTot出现负值,表明赤铁矿对菌株HPD-2菌具有吸引力。而高岭石和蒙脱石GTot为正值,即对菌株HPD-2细胞表现为斥力;当d减小为约4 nm时,两粒子间作用能达到最大值,即能障值[28];当d继续减小时,斥力随之骤然减少,当d小于约1 nm时表现为引力。赤铁矿对菌株HPD-2菌的吸附是自发的,而高岭石和蒙脱石则必须跨越能障才能与菌株HPD-2菌产生吸附,且高岭石需要跨越的能障值大于蒙脱石。上述结果很好地解释了图1中3种无机胶体等温吸附的差异。
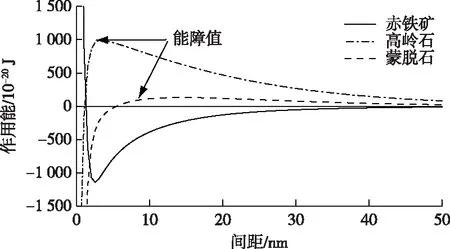
图2 利用Ex-DLVO理论求得的无机胶体对菌株HPD-2的总相互作用能
菌株HPD-2细胞与3种无机胶体的相互作用能见图3。
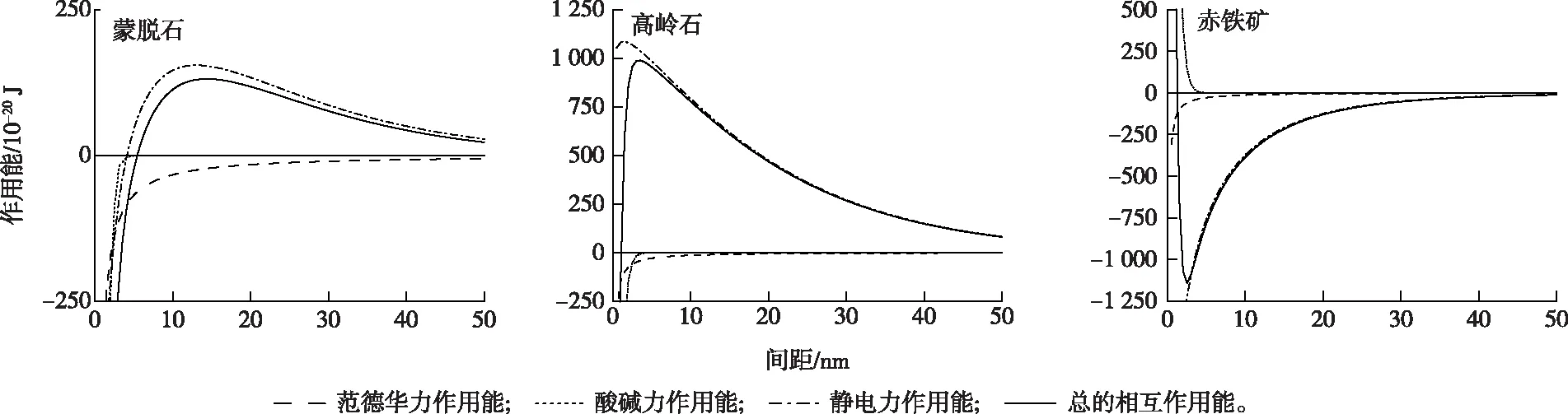
图3 基于Ex-DLVO理论的无机胶体对菌株HPD-2的各类相互作用能
由图3可知,细胞与黏土矿物(高岭石和蒙脱石)之间的能障主要由静电斥力决定,而间距很小时的极小能则主要取决于疏水作用力。这是由于在供试溶液条件下,静电力和疏水作用力的作用范围不一样,前者为长程作用力(0~50 nm),而后者只在间距很小(0~5 nm)时才发挥作用。范德华力带来的作用能始终为负值,对于吸附是有利的,但远远低于静电力和酸碱作用力带来的作用。蒙脱石和高岭石只有跨越能障才能与菌株HPD-2细胞发生相互吸附,且高岭石的能障值大于蒙脱石,这是由于不同无机胶体静电力不同造成的,蒙脱石表面电位负电性小于高岭石,进而静电斥力小于高岭石。当两粒子间距d<5 nm时,疏水作用力逐渐发挥主导作用,使得两粒子间斥力不断减小,甚至在d为1 nm时表现为引力。赤铁矿与菌株HPD-2菌发生吸附时没有产生能障,是一种自发行为。但当d<1 nm时,由于酸碱作用力,赤铁矿与菌株HPD-2细胞表现出相斥作用,这可能是由于赤铁矿表面亲水基团使得赤铁矿表现为亲水性,进而赤铁矿与菌株HPD-2细胞近距离接触时表现出排斥作用。
2.4 无机胶体对噬氨副球菌HPD-2吸附作用机制
根据等温吸附和DLVO理论计算得到,3种矿物对菌株HPD-2细胞的吸附强度由高到低依次为赤铁矿>蒙脱石>高岭石。选取高岭石、蒙脱石和赤铁矿分别与菌株HPD-2细胞作用240 min后的样品,经体积分数为2.5%的戊二醛固定并冷冻干燥后,采用FE-SEM进行观察(图4)。

A为高岭石,B为蒙脱石,C为赤铁矿。
由图4可知,赤铁矿颗粒粒径最小,此与粒径测定结果一致,高岭石则呈现出其特有的片层结构,蒙脱石在吸水膨胀后结晶程度减弱。在相同视野中,可以看到赤铁矿对菌株HPD-2的吸附量大于蒙脱石,蒙脱石大于高岭石。高岭石对菌株HPD-2的吸附面较小,细菌表面大部分裸露出来;而赤铁矿则紧紧包裹菌株HPD-2细胞,菌株只有很小一部分表面裸露;对于蒙脱石,细菌可吸附在大的颗粒表面,且细菌与颗粒的接触面积大于高岭石。综上,赤铁矿颗粒与菌株HPD-2细胞的接触面积远大于蒙脱石,蒙脱石则大于高岭石。

由图5可知,蒙脱石的最强吸收来自1 087 cm-1处Si—O非面内伸缩振动和1 032 cm-1处Si—O面内伸缩振动,3 340 cm-1处表面羟基O—H弯曲振动和1 635 cm-1处O—H弯曲振动等水的特征峰吸收也比较强;除此以外,还包括911 cm-1处Al—Al—OH弯曲振动、837 cm-1处Al—Mg—OH弯曲振动和837 cm-1处Si—O面外弯曲振动等蒙脱石的特征吸收峰。与高岭石类似,蒙脱石吸附菌株HPD-2细胞后,细菌表面酰胺Ⅰ基由1 635 cm-1红移到1 631 cm-1处,以及在1 010 cm-1处出现酰胺Ⅱ吸收峰。与高岭石一样,蒙脱石与菌株HPD-2细胞的作用主要为细胞表面蛋白作用。

图5 无机胶体与菌株HPD-2相互作用的FTIR图谱
从赤铁矿红外光谱可以看到,赤铁矿基团在水中时相对简单,3 279 cm-1处伸缩振动吸收被强且宽的水吸收峰所掩盖,1 645 cm-1处亦出现水羟基弯曲振动吸收。赤铁矿中Fe—O位于3 193 cm-1处的伸缩振动吸收被强且宽的水吸收峰所掩盖,1 640 cm-1处亦出现水羟基的弯曲振动吸收,888和790 cm-1处尖锐吸收峰分别来自表面Fe—O面内和面外的弯曲振动。对于赤铁矿吸附菌株HPD-2后的红外光谱,除1 645和1 642 cm-12处酰胺基振动发生变化外,还监测到增加的1 372 cm-1处—COOH振动和1 068 cm-1处PO2—较强吸收峰,说明除了蛋白质结构变化参与作用外,还有较强的P—OFe化学键的参与[31]。相较于高岭石和蒙脱石而言,赤铁矿与菌株HPD-2形成了作用能远强于其他胶体的化学键。菌株HPD-2细胞在蒙脱石和高岭石上的胶粒属于松散吸附,而在赤铁矿胶粒上的吸附属于紧密吸附,该结果再一次验证了前文中赤铁矿与菌株HPD-2菌的相互作用远高于高岭石和蒙脱石的结论。
3 结论
(1)相较于黏土矿物(高岭石和蒙脱石),赤铁矿对菌株HPD-2细胞的吸附能力更强,理论最大吸附量可以达到1 800 mg·g-1,且3者等温吸附均较好地符合Langmuir模型(R2均在0.86以上)。
(2)EX-DLVO理论说明赤铁矿对菌株HPD-2细胞的吸附不需要突破能障,是自发的过程,在颗粒间距d>3.6 nm时主要是静电引力产生作用,而当小于这个间距时,疏水作用力迅速上升,表现出排斥的倾向。而黏土矿物需要突破一定能障才能发生吸附,高岭石能障值大于蒙脱石。
(3)FTIR谱图分析结果表明,除氢键和细胞表面蛋白作用外,赤铁矿与菌株HPD-2发生吸附的作用力还包括作用力较强的P—OFe化学键。而高岭石和蒙脱石对菌株HPD-2菌的作用力主要为细胞表面蛋白质构型的变化,相互作用较弱。

