香豆素类化合物结构修饰合成及抑菌活性测定
高冬梅,杜振亭
(1.杨凌职业技术学院,陕西 杨凌 712100;2.西北农林科技大学 化学与药学院,陕西 杨凌 712100)
香豆素类化合物具有α-苯并吡喃酮结构[1],广泛存存在于植物、动物、微生物及其次生代谢物中。目前已分离得到的1300多种香豆素类化合物及其衍生物,根据环上取代基种类及位置不同,将香豆素类化合物分为简单香豆素、吡喃香豆素、呋喃香豆素及其他香豆素[2]4大类。
由于香豆素类化合物苯并吡喃环共轭体系及特殊取代基的存在,使该类化合物具有丰富的结构和多样的用途,如抗凝血[3-5]、抗菌[6-7]、抗肿瘤[8-9]、抗病毒[10]、抗氧化[11]、抗炎[12]、杀虫[13-14]等生物活性,还可作为荧光增白剂、荧光燃料[15]、检测阴阳离子[16-17]和中性分子[18]的生物荧光探针等材料使用。虽然香豆素类化合物用途广泛,但是从植物中提取该类化合物,产量低,分离难度大等缺陷极大的限制了其大规模开发与利用,因此,对该类化合物结构修饰与化学合成方法的研究受到极大的关注。目前应用最广泛的香豆素衍生物制备方法是Knoevenagel缩合反应[19]、Wittig反应[18]、Claisen重排反应、Heck反应、Pechmann缩合反应[20]。除此之外,还出现了一些合成香豆素衍生物的新型反应,如无溶剂有机反应、光催化反应、微波辅助反应等。
本文借助合成手段将香豆素母核与新颖模式酰胺基团通过活性亚结构拼接途径连接,得到一系列香豆素衍生物并评价其抑菌活性,旨在寻找结构优良、高效、环保的抑菌剂先导化合物并通过探索其构效关系为后续化合物的设计与合成奠定理论基础。
1 实验部分
1.1 仪器与试剂
Bruker AVANCEШ 核磁共振仪(德国Bruker公司,500 MHz);DFY-5/80低温恒温反应浴(郑州凯鹏实验仪器有限公司);BC-R206旋转蒸发仪(上海贝凯生物化工设备有限公司);IKA C-MAG HS7磁力搅拌器(德国IKA公司);SB25-12DT超声波清洗机(宁波新芝生物科技股份有限公司);MP420全自动视频熔点仪(济南海能仪器股份有限公司vasinfectum);WFH-203三用紫外分析仪(上海精密科学仪器有限公司)。
取代水杨醛、4-二甲氨基吡啶、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐均为市售分析纯;无水乙醇、冰乙酸、乙酰乙酸乙酯、哌啶、丙酮、甲苯、二氯甲烷、N,N-二甲基甲酰胺(DMF)等为天津博迪化工分析纯试剂。
1.2 目标化合物合成
系列目标化合物以取代水杨醛和丙二酸二乙酯为原料,首先得到中间体1(3-甲酸乙酯-香豆素衍生物),然后进行酯的碱性水解反应酸化得到反应中间体2(3-甲酸-香豆素衍生物),在此基础上使用羧酸酰基化催化剂4-二甲氨基吡啶(DMAP),1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)催化活化,进行一系列酰基化取代获得a(a1~a9)、b(b1~b9)、c(c1~c2)、d(d1~d3)、e(e1~e3)5类共26个目标化合物。目标化合物合成路线如图1所示;系列目标化合物结构如表1所示。
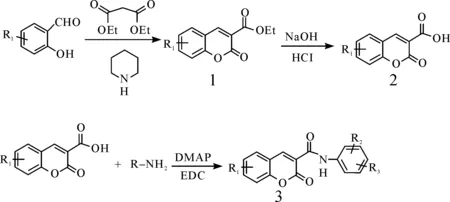
图1 目标化合物合成路线Fig.1 The synthetic route of the target compound
中间产物1的合成:在50 mL圆底烧瓶中分别加入丙二酸二乙酯(3.4 mL),各类取代水杨醛(2.1 mL)、六氢吡啶(哌啶0.3 mL)、无水乙醇(15 mL)、冰醋酸(0.5 mL),磁力搅拌下加热回流2 h,然后放置至室温(薄层色谱TLC全程跟踪实验反应进程),温度降低后加入20 mL水,后冰浴冷却1 h,待结晶后,减压抽滤,无水乙醇洗涤2~3次,得到白色晶体(熔点90-93 ℃)。
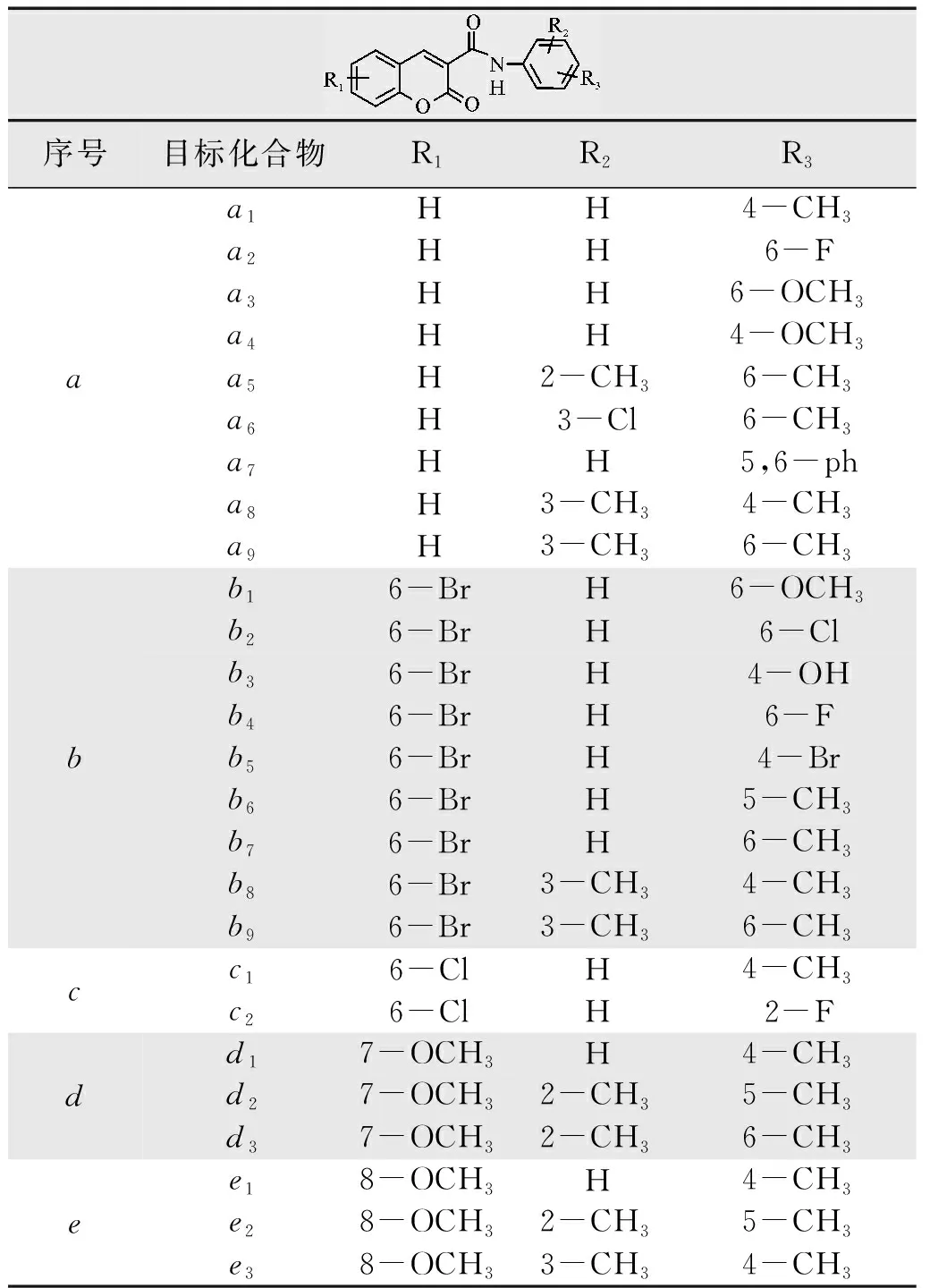
表1 目标化合物结构Tab.1 Structure of the target compound
中间产物 2的合成:将中间产物1(2 g)置入50 mL圆底烧瓶中,依次分别加入NaOH(1.5 g)、体积分数95%乙醇(10 mL)、水(5 mL),在温度65 ℃条件下磁力搅拌加热回流1 h,放置降温至室温(薄层色谱TLC全程跟踪实验反应进程);然后转入烧杯中,加入5 mL浓盐酸、25 mL水,冰浴加速结晶,后抽滤,用冰水洗涤2次干燥即可(熔点188 ℃)。
目标化合物3的合成:将中间产物2(2 g)加入50 mL圆底烧瓶中,依次分别加入DMAP(0.1 g)、EDC(0.1 g),各类苯胺(4 g),溶剂DMF25 mL,磁力搅拌下在温度85 ℃加热回流2.5 h,静置至室温(薄层色谱TLC全程跟踪实验反应进程),然后将反应体系一同转入大烧杯中,加入水50 mL水洗涤2~3次后减压抽滤,干燥后,采用硅胶柱层析、重结晶等方法分离纯化得到系列目标化合物。
1.3 抑菌活性测定
以氨苄青霉素为阳性对照,氯仿为阴性对照,采用滤纸片法测试供试化合物对蜡状芽孢杆菌(Bacilluscereus)、枯草芽孢杆菌(Bacillussubtilis)、金黄色葡萄球菌(Staphylococcusaureus)、沙门氏菌(Salmonella)、大肠埃希氏菌(Escherichiacoli)、青枯病菌(Ralstoniasolanacearum)、猕猴桃溃疡病菌(Pseudomonassyringaepv.actinidae)、铜绿假单胞菌(Pseudomonasaeruginosa)8种供试病原菌的抑菌活性。将供试化合物配制成质量浓度为100 μg/mL 的氯仿溶液,待牛肉膏蛋白胨琼脂培养基等高压灭菌处理后,采用涂布平板法将菌种均匀涂在培养基表面;然后将含有待测药液的滤纸片(6 mm)完全贴合于带菌培养基上,一个化合物设置3组重复,一个阳性对照和阴性对照。待处理完成后将培养基转移至温度37 ℃培养箱中培养9~12 h,观察各滤纸片透明程度,采用十字交叉法测定抑菌圈大小,筛选出活性较好的化合物后,进一步测定其最小抑菌浓度MIC值。
2 结果与讨论
2.1 目标化合物物态与产率
按照图1 合成路线,合成出的a(a1~a9)、b(b1~b9)、c(c1~c2)、d(d1~d3)、e(e1~e3)5类26个目标化合物,其物态、产率结果如表2所示。
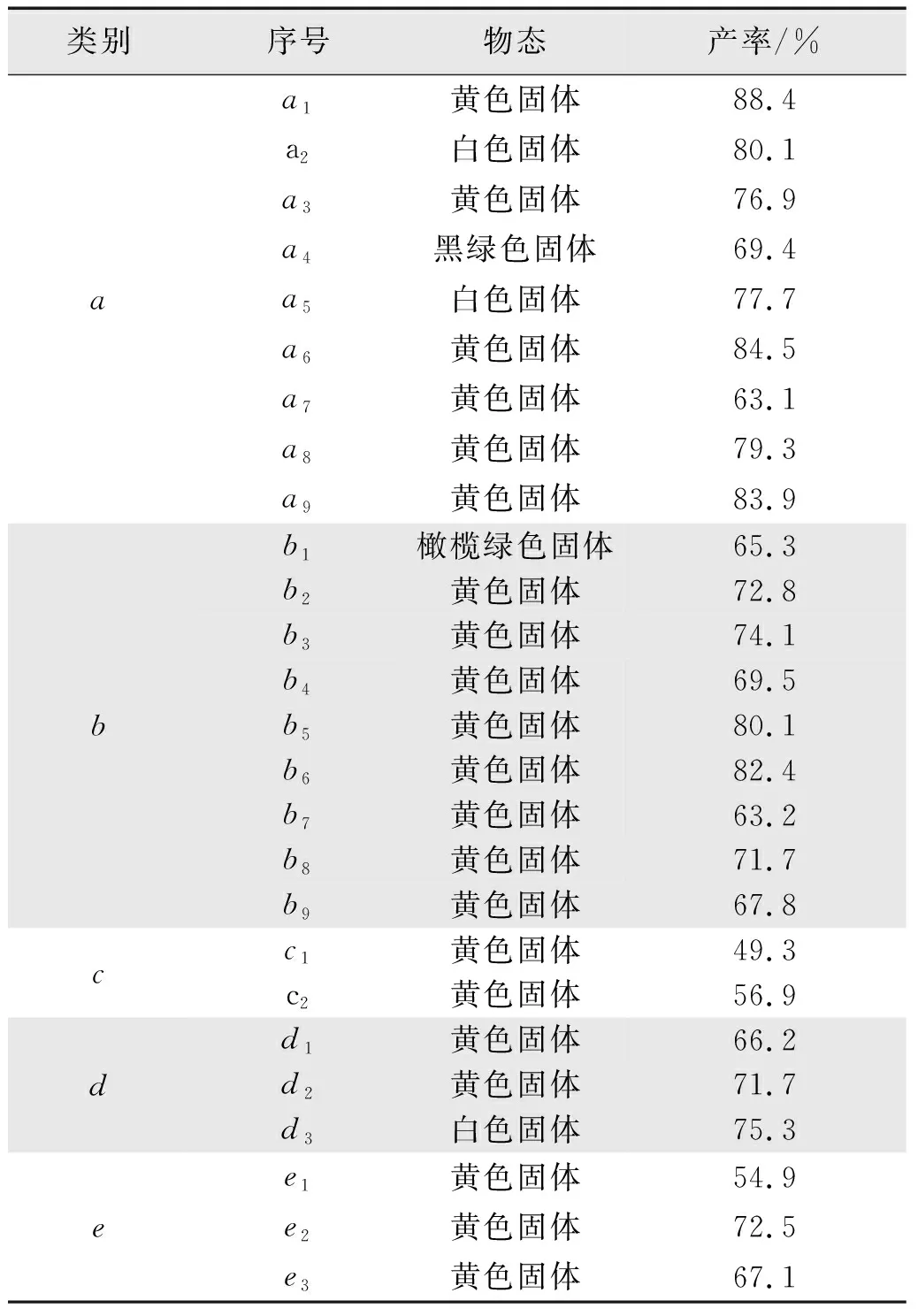
表2 目标化合物物态与产率Tab.2 State and yield of target compound
2.2 抑菌活性
目标化合物抑菌活性测定结果表明,在质量浓度为100 μg/mL条件下,该类型化合物对蜡状芽孢杆菌、金黄色葡萄球菌、沙门氏菌、铜绿假单胞菌抑制活性不佳;不同结构类型化合物对枯草芽孢杆菌、大肠埃希氏菌、烟草青枯病菌、猕猴桃溃疡病菌的抑制活性差异较大,c类化合物对这几种供试菌无抑制活性,d、e类化合物抑制活性优于a类化合物,d2、e2化合物的抑菌效果甚至接近阳性对照组;较多化合物a3、a4、a5、a6、d1、d2、d3、e1、e2、e3对枯草芽孢杆菌具有广谱抑菌性。
2.3 最小抑菌浓度(MIC)
根据目标化合物抑菌活性测试结果,筛选出部分抑菌活性较好的化合物,测定其最小抑菌浓度(MIC)值。表1中化合物d1、d2、d3、e1、e2、e3对枯草芽孢杆菌、大肠埃希氏菌、烟草青枯病菌、猕猴桃溃疡病菌有广谱抑菌效果且对枯草芽孢杆菌的MIC值低于50 μg/mL,表明抑制效果良好。表1中化合物d1对大肠埃希氏菌和枯草芽孢杆菌的抑制效果优于烟草青枯病菌和猕猴桃溃疡病菌;化合物e1对大肠埃希氏菌和猕猴桃溃疡病菌的活性相对于枯草芽孢杆菌和烟草青枯病菌较弱。
3 结语
(1)本文通过简便、快捷的方法合成了香豆素类衍生物26个,其中多数为文献未报到的新化合物,并采用核磁、红外等方法对其结构进行表征确认。所采用的合成方法路线便捷、产率高,为该类化合物的合成研究提供了参考;
(2)以氨苄青霉素为对照,测试26个目标化合物对枯草芽孢杆菌、大肠埃希氏菌、烟草青枯病菌、猕猴桃溃疡病菌、蜡状芽孢杆等8种供试病原菌的活性,以及部分抑菌活性较好化合物的MIC值,发现目标化合物结构中供电子基团所在的位置不同,其抑菌活性差别较大,该结论为香豆素类化合物结构修饰合成研究提供了理论基础。

