基于STEAM理念的项目式化学教学
庞嵩










摘要:钢铁的锈蚀及其防护是对金属性质与应用的拓展和实践。文章以“第一艘国产航母”为项目背景,将“如何对航空母舰防锈”作为驱动性问题,细分为钢铁锈蚀的原因、锈蚀速率的影响因素和防护方法三个项目式任务进行研究,融合化学、科学、军事、数学、信息技术、食品加工等学科,尝试进行跨学科实践活动,以此激发学生学习兴趣,增强动手能力。
关键词:STEAM理念;项目式学习;跨学科融合;核心素养
文章编号:1008-0546(2023)09-0028-07
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j .issn.1008-0546.2023.09.006
STEAM教育作为一种超越传统的教育模式,采用跨学科的方法在基于现实问题情境中教授科学、技术、工程、艺术和数学等方面的知识,引导学生适应不断更新的专业知识和快速变化的社会生活,提高学生未来社会竞争力。作为STEAM教育的一种呈现形式,项目化学习是让学生在一段时间内对真实有意义的问题进行持续探究,创造性地解决问题,形成公开成果,达到对核心知识的再建构与思维迁移。
为应对创新型社会挑战,促进素质教育的有效实施,培养新时代所需的综合型、实践型、创新型人才,本节课基于STEAM理念进行项目式化学教学新尝试。
一、教材分析
钢铁的锈蚀及其防护属于沪教版初中化学九年级上册第5章第3节“金属防护和废金属回收”中的内容。《义务教育化学课程标准(2022年版)》对“金属与金属矿物”的学习提出的教学要求是:“知道金属有一些共同的物理性质,通过实验探究等活动认识常见金属的主要化学性质及金属活动性顺序。以铁生锈为例,了解金属腐蚀的常用方法。了解废弃金属对环境的影响及金属回收再利用的价值”。[1]本节课以“我国第一艘国产航空母舰——山东号”为项目背景,将“如何对航空母舰防锈”作为驱动性问题,最终达成“知道钢铁锈蚀的条件并学会对其防护”的核心目标。教学过程中采用学生自评、组内互评、教师点评等多样化的评价方式,给学生提供较为全面的认知。
二、教学目标及重、难点
1.通过对比实验和U型管改进实验的设计和分析,探究钢铁生锈的条件以及影响因素,并以此发展科学思维,提高创新意识。
2.通过船体镶嵌金属的探究,学会钢铁锈蚀的防护方法,初步形成有关“物质性质决定用途”的化学观念,解决实际问题。
教学重点:钢铁生锈的条件和影响凶素。
教学难点:根据锈蚀条件探究钢铁锈蚀的防护措施。
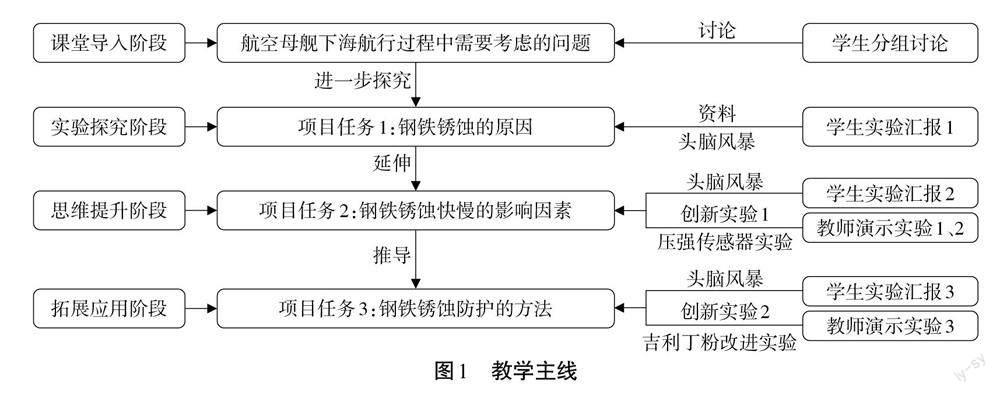
三、教学主线
见图1。
四、教学过程
项目背景:2019年12月17日下午,山东舰作为我国第一艘国产航空母舰在海南三亚某军港交付海军。山东舰下海航行过程中主要考虑哪些问题?
设计意图:航空母舰作为国之重器,备受人们关注。建造航母需要大量钢材,为了能让航母能长时间在海上航行,防锈问题尤为重要。因此用我国第一艘国产航母作为项目背景,不仅与化学教学贴合紧密,而且对学生有深刻的爱国和军事教育意义。
项目式任务1:钢铁锈蚀的原因
【资料1】
取一块废旧铁丝网,将铁丝网剪成几小片,用稀盐酸除去铁锈后,放人锥形瓶中,如图2所示。在锥形瓶中加入3~4 mL浓食盐水,塞紧带导管的单孔塞后,将导管的另一端伸人滴有红墨水的水中,过一段时间后观察并记录实验现象。
在家用铁锅中放人少量水,静置一夜后观察并记录实验现象。如图3所示。
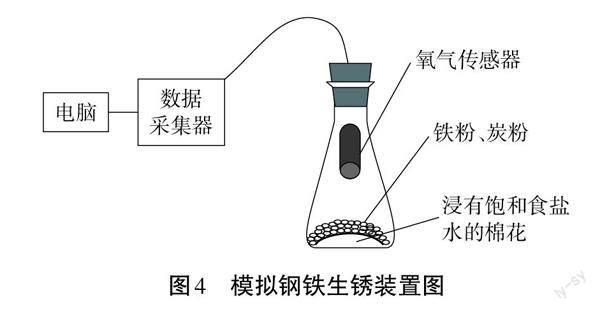
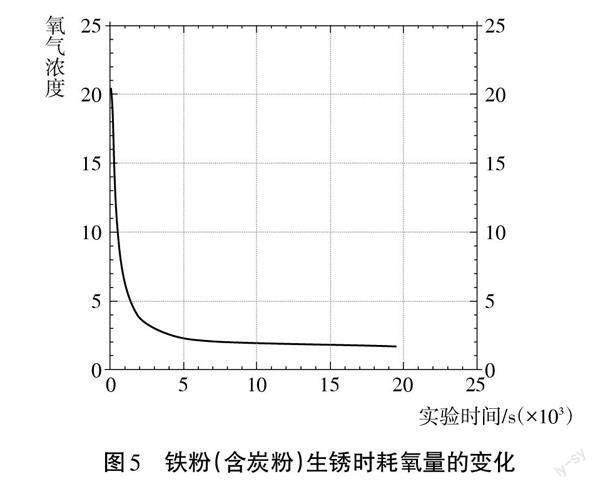
将铁粉和木炭粉混合均匀后放人浸有饱和食盐水的棉花中,如图4所示,并用氧气传感器测出锥形瓶内氧气浓度随实验时间变化的曲线,如图5所示。
请 学们根据上述信息猜想铁生锈的条件并设计实验进行验证。
设计意图:图2是沪教版初中化学九年级上册第1章的实验,学生通过此实验已经知晓铁生锈需要氧气和水的共同作用,但教师更多的是给出结论,并没有严格地设计对比实验进行验证,现在给出此图是为了激活学生记忆,为下面的猜想做铺垫。图3通过生活中的常见现象让学生推导铁生锈需要水的参与。图4.5通过演示实验,直观地展现铁生锈需要氧气参与。
学生分组采用“头脑风暴法”研讨实验设计并进行展示,教师引导筛选。学生利用提供的实验器材搭建实验装置,连续7天观察并记录现象,一周后分组进行汇报。
【学生实验汇报1】
取3枚洁净无锈的铁钉,分别放人3支试管中。在试管①中加入少量干燥剂(生石灰或无水氯化钙),再放一团干棉球,把铁钉放在干棉球上,塞紧橡皮塞。在试管②中注满迅速冷却的沸水,使铁钉完全浸没,塞紧橡皮塞。在试管③中加入少量蒸馏水,使铁钉的一半浸没在水中。进行实验,记录观察到的实验现象。
实验现象:如图6所示①中铁钉不生锈;②中铁钉第一天和第三天不生锈,第七天底部有些许锈迹;③中铁钉生锈,且在空气与水接触位置锈蚀最严重。
实验结论:铁在空气中锈蚀,实际上是铁跟氧气、水等物质作用,发生一系列复杂的化学反应,转化为铁的化合物的过程。
异常现象及问题:②中铁钉底部为什么有些许锈迹?
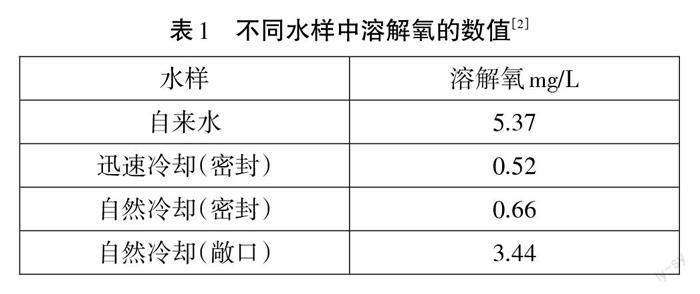
【资料2】用溶解氧传感器测定不同水样中的含氧量,见图7、表1。引导学生分析,得出结论。
实验结论:迅速冷却的沸水中依然含有少量氧气,②中铁钉长时间浸没在水中与水中溶解的少量氧气反应依然会生锈。
设计意图:引导学生控制水和氧气两大变量,设计类似书本的对比实验,通过持续观察7天时间内铁钉的锈蚀情况,推导铁生锈条件。同时试管②中的异常现象也從反面证明铁生锈是氧气和水共同作用的结果。只有知晓铁生锈的条件,才能为航母防锈提供理论支持。
项目任务2:钢铁锈蚀快慢的影响因素
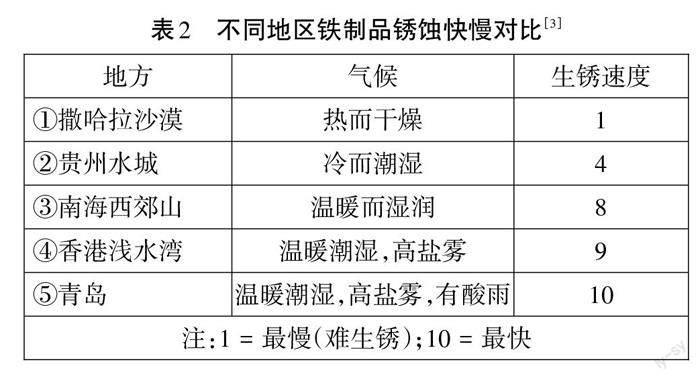
【资料3】盐雾是指大气中由含盐微小液滴所构成的弥散系统。
由表2猜想:钢铁锈蚀快慢主要受周围环境影响,在盐雾和酸性环境下铁锈蚀速率加快。学生分组采用“头脑风暴法”研讨实验设计并进行展示,教师引导筛选。学生利用提供的实验器材搭建实验装置,连续7天观察并记录现象,一周后分组进行汇报。
【学生实验汇报2】
取3枚洁净无锈的铁钉,分别放人3支试管中。在试管③中加入少量蒸馏水,使铁钉的一半浸没在水中。在试管④中加入稀硫酸或醋酸溶液,浸没铁钉后,倒去溶液。在试管⑤中加入少量氯化钠溶液,使铁钉的一半浸没在溶液中,进行实验。 实验现象:7天后试管内铁钉锈蚀情况如图8所示,④、⑤中的铁钉比③中铁钉生锈更快,锈蚀更严重。
实验结论:稀硫酸、醋酸溶液和氯化钠溶液等物质存在时会加快铁的锈蚀。
过渡:为了将实验现象数据化,便于定量分析生锈过程中的氧气和水的变化,教师用压强传感器改进实验。
【教师演示实验1】
如图9所示,三个装有压强传感器的试管中分别放人铁粉、铁粉与水、铁粉与食盐水,同时测定试管中压强的变化,并以曲线形式展示结果。
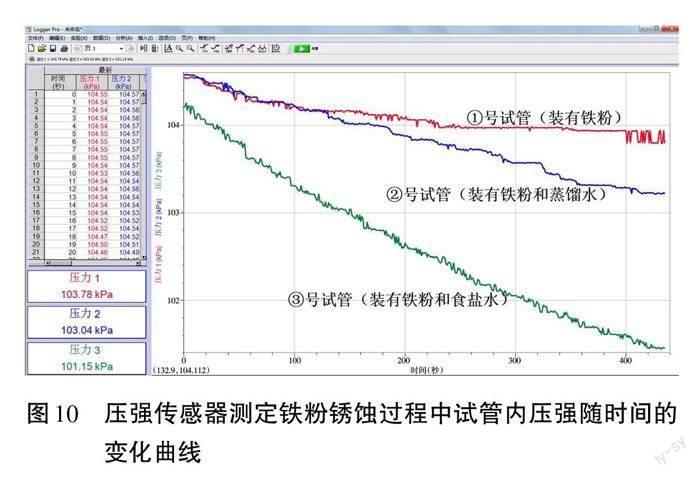
实验现象:①号试管(装有铁粉)中的压强随时间的推移变化不大;②号试管(装有铁粉和蒸馏水)中压强随时间的推移慢慢变小;③号试管(装有铁粉和食盐水)中压强随时间的推移快速变小,见图10。
实验结论:在其他条件相同时,在盐溶液中钢铁更容易生锈,生锈速率更快。
过渡:除此以外,钢铁锈蚀速率还受到哪些因素影响?
【教师演示实验2】
按照图1 1组装三套实验装置,一天后观察现象。
备注:教师提前一天做好实验,将三只U型管带到教室,让学生观察,结果见图1 2。
实现象及结论:
1.红色圈画处铁钉表面有少量铁锈,钢丝棉表面有大量铁锈,粘在壁上的铁粉表面有大量铁锈,说明在其他条件不变时,钢铁与氧气的接触面积越大,锈蚀速率越快。
2.黄色圈画处均不生锈,证明钢铁锈蚀需要水的参与。
3.蓝色圈画处铁钉和铁粉的生锈痕迹很不明显,证明钢铁锈蚀需要氧气参与。钢丝棉两侧有较明显锈迹,证明蒸馏水中有少量氧气,同时与其余两者对比也能证明在其他条件不变时,钢铁与氧气的接触面积越大,锈蚀速率越快。
设计意图:项目任务2是在任务1的基础上研究钢铁锈蚀速率问题,是对钢铁锈蚀认识的提升。本项任务的完成包含了1个学生对比实验、2个教师改进实验并进行了资料整合。既有现象的定性分析也有数字传感器的定量展现,数形结合,意在将铁锈蚀的问题研究透彻。文中钢丝棉易生锈,而水中铁粉不易生锈,说明是钢铁与氧气的接触面积影响锈蚀速率而不是钢铁本身的表面积,两者是有区别的,同时也证明化学反应需要物质之间相互接触才能发生。盐雾、盐溶液、酸性环境都是海上极为常见的自然环境,通过本项目任务的学习,让学生深刻意识到航母所处环境的恶劣,防锈刻不容缓。
项目任务3:钢铁锈蚀防护的方法
学生分组采用“头脑风暴法”研讨以下三个问题:
问题1:根据生锈的条件,可以采用什么样的原理防止钢铁锈蚀?
隔绝氧气和水。
问题2:航母可以用哪些方法防锈?
涂油喷漆、部分部位制成不锈钢。
问题3:航空母舰的外壳镶嵌一种金属达到防锈的目的,猜想这种金属是什么?
教师引导学生设计实验方案,学生利用提供的实验器材搭建实验装置,连续24 h观察并记录现象,一天后分组进行汇报。
【学生实验汇报3】
如图1 3所示,将铁钉、裹铝片的铁钉、裹锌片的铁钉、裹铜片的铁钉放在滴有酚酞的食盐水中,观察并记录实验现象。
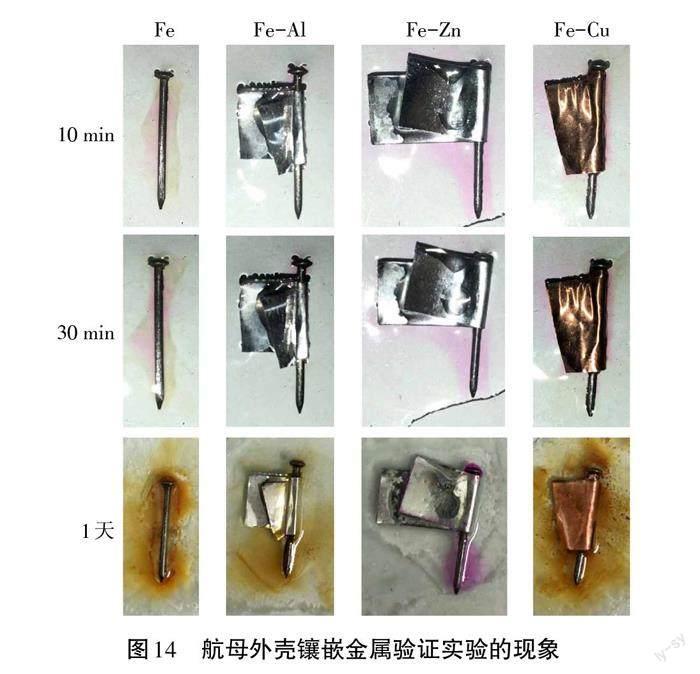
如图14所示,10 min和30 min现象类似:铁钉表面出现锈斑,溶液变红,周围伴有锈迹;裹铝片的铁钉表面无明显锈迹,铁钉头部附近的溶液变红;裹锌片的铁钉表面无明显锈迹,铁钉头部和尾部附近的溶液变红;裹铜片的铁钉头部和尾部出现锈斑,铜片附近溶液变红。
1天以后,除裹锌片的铁钉表面无明显锈迹外,其余铁钉全部锈蚀。锈蚀程度由高到低分别是:裹铜片的铁钉>铁钉>裹铝片的铁钉。
实验结论:航空母舰的外壳镶嵌锌块达到防锈的目的。
设计意图:学生通过模拟航母外壳镶嵌金属实验,用事实证明镶嵌的金属是锌块。实验不仅趣味性十足而且锻炼学生的动手能力、创新能力。裹铝片的铁钉还是会让铁钉生锈的原因可能是铝表面快速生成致密的氧化铝膜进行了自我保护,但无法阻止铁钉锈蚀。溶液变红的原因是铁锈蚀过程中产生了大量的氢氧根离子。设计意图是让学生根据变红区域区分生锈部位,但是氢氧根离子在溶液中均匀分散,致使显色区分不明显,甚至部分区域的红色被锈迹完全覆盖,效果较差。
过渡:由于这些反应都是在溶液中进行的,尤其对于显色反应而言,溶液的轻微晃动就会导致显色区域的破坏。有没有什么方法能让显色区域固定不受晃动干扰?
【教师演示实验3】
利用吉利丁粉[明胶(99%)、卡拉胶(1%)]改进实验。
将吉利丁粉溶解在冷水中,水浴加热至80℃,加入适量食盐水和酚酞,倒人模具中备用。将裹铝片的铁钉,裹锌片的铁钉,裹铜片的铁钉放在凝胶中,观察现象。
实验现象:如图15所示,显色区域固定不受晃动干扰,红色区域显色非常明显,区分度很高。裹铝片的铁钉和裹锌片的铁钉表面无明显锈迹,铁钉的头部和尾部附近凝胶变红;裹铜片的铁钉头部和尾部明顯生锈,铜片附近凝胶变红。
实验结论:航空母舰的外壳镶嵌锌块达到防锈的目的。
设计意图:将溶液中进行的铁钉锈蚀反应转入凝胶中进行,能够非常有效地标示出金属腐蚀过程中形成的“微电池”的阴、阳极位置,反应过程的图像稳定,不容易因碰撞或者溶液扩散而被快速破坏,可以让学生观察到更多反应过程的细节,提高学习的兴趣。[4]
实验反思:为什么锌块能起到防锈目的?
【资料4】
钢铁在接近中性的潮湿空气中的腐蚀属于吸氧腐蚀,其电极反应如下:
正极:O2+ 2H2O+4e==40H-
负极:2Fe - 4e==2Fe2+
总反应:2Fe+O2+2H2O==2Fe(OH)2
后续反应:4Fe(OH)2+O2+2H2O==4Fe(OH)3
铁锈蚀的本质是铁失去电子变成亚铁离子的过程,只要有金属能代替铁失去电子就可以起到保护作用,所以需要找比铁活泼的金属,例如:Zn和Al。
红色区域说明周围有大量的氢氧根离子,这是电源的正极,附近的大量的电子起到保护作用,所以红色区域“非常安全”,由此也可以看出金属锌的保护作用,銅的加速锈蚀作用。
设计意图:此环节是想借助电极反应解释为什么航母外壳镶嵌金属锌可以起到保护作用,并由此引发学生思考。根据该原理,还有哪些金属可以镶嵌在航母外壳上?理论上可以,为什么实际不可以?这也为后续的项目任务做铺垫。这样的项目式教学才能不断驱动学生深入研究,教学才能焕发生机与活力。
【板书设计】
意义解读:钢铁锈蚀需要氧气、水的共同作用,条件缺一不可。在铁的周围覆盖一圈电子可以对铁起到保护作用。
五、教学反思
本节课以“我国第一艘国产航空母舰一山东号”为项目背景,将“如何对航空母舰防锈”作为驱动性问题,分三个项目任务:钢铁锈蚀的原凶、钢铁锈蚀快慢的影响因素、钢铁锈蚀防护的方法,用三个课时的时间让学生通过实验探究了解钢铁锈蚀的条件并学会对其防护。项目式教学实施过程中一直渗透STEAM教学理念,将跨学科实践活动融人教学,最终取得了理想的效果。
节课利用吉利丁粉改进实验也可以用于金属活动性的研究。具体来看只要将铁钉与不同金属连接,便能够清晰地显示不同金属的活动性顺序。整个实验过程简单、安全、廉价,其实验设计思路可以发展到其他实验体系中,以可视化的形式表现置换反应、氧化还原反应、原电池以及金属腐蚀等研究课题,适合初中、高中学生进行课堂实验或创新拓展活动,对学生的素质培养有积极的帮助作用。[4]
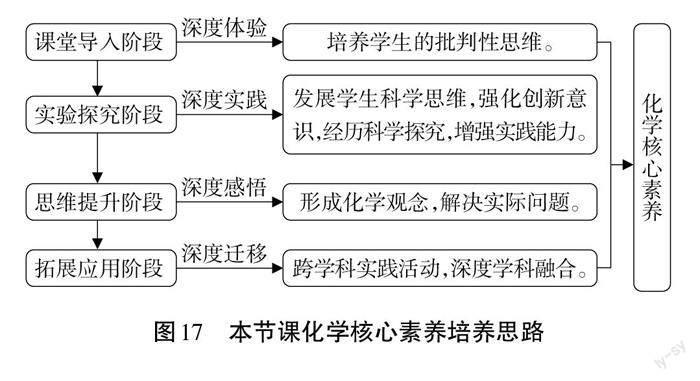
本节课的思维导图——化学核心素养的培养,见图17。
参考文献
[1] 中华人民共和国教育部.义务教育化学课程标准(2022年版)[S].北京:北京师范大学出版社,2022:19-20.
[2] 杨砚宁.基于证据推理的科学探究:实验、评价及反思——以“铁钉锈蚀实验”为例[J].化学教与学,2017(02):13-15.
[3] 顾丹丹.“境脉式教学”在初中化学新授课中的应用探究——以“金属的腐蚀与防护”为例[J].名师在线,2021(18):28-29.
[4] 许骋艺,王德明,吴梅芬.铁钉锈蚀实验的新观察[J].化学育(中英文),2017,38(17):47-49.

