青铜器粉状锈空气传播过程新探
龚钰轩,杨旭鹏,周光昭,黄永冲,杜文跃
[1. 江苏科技大学科学技术史研究所(马克思主义学院),江苏镇江 212100;2. 中国科学技术大学文物保护科学基础研究中心,安徽合肥 230026]
0 引 言
青铜“粉状锈”是一种有害锈,又称“青铜病”[1],由于其对青铜基体腐蚀严重,根治困难,且不断恶性膨胀,导致一件完好的青铜器在短时间内完全酥粉,又被形象的称为青铜“癌症”。早在1826年Davy就在古墓葬出土的青铜钉中分析发现了铜的氯化物[2]。最早认识到粉状锈生成反应的是Berthelot,他在1895年已经意识到粉状锈的腐蚀产物是碱式氯化铜,并将其分子式列为3CuO·CuCl2·4H2O,这与今天公认的碱式氯化铜分子式已经十分接近[3]。根据Berthelot的解释,青铜会发生以下腐蚀过程:

Cu2Cl2·2NaCl+3Cu2O+4H2O
(1)

3CuO·CuCl2·4H2O+2CuCl2+2NaCl
(2)

3CuO·CuCl2·4H2O
(3)
Berthelot指出在水分和氧气作用下,上述反应不断循环是青铜病爆发的原因所在。在今天来看,这个结论在本质上是正确的,但很多细节解释并不完善。Organ在1963年提出青铜病发生的主要原因是氯化亚铜水解生成氧化亚铜[4],反应生成的HCl会导致更多氯化亚铜产生,推测反应过程如下:

(4)

(5)
虽然在今天看来,第二个反应理论上是行不通的。但在当时来说,这一推测也表明了前人对青铜锈蚀过程中,粉状锈是“循环产生”的认识正逐步深化,这也为现今粉状锈生成机理的研究奠定了一定基础。
同时Organ还指出,氯化亚铜层位于青铜基体和铜盐之间,而氧化亚铜位于腐蚀产物的表面,如果氯化亚铜已经完全转化,那么此处就会变得稳定。实际上氯化亚铜在水和氧气参与反应时,并不会生成氧化亚铜,而会生成碱式氯化铜。Lucy于1972年通过实验观察了铜的点腐蚀过程和氯化亚铜的生长过程,提出了点腐蚀的“孔膜”理论,认为点腐蚀孔可以起到电化学电池的作用,孔内表面发生阳极反应,而孔外表面发生阴极反应,水中溶解的氧气可以使铜氧化成铜离子,一部分会流失到土壤当中,另一部分会回到膜表面以亚铜离子的形式存在[5],具体反应如下:

(6)

(7)

(8)
Lucy指出上述反应式的平衡是产生沉淀的原因。Taylor和Macleod在1985年时从金相结构的角度分析了青铜腐蚀过程,认为该反应发生时,锡会被最先腐蚀掉,在海水的含氧环境下,富铜的α相受到腐蚀,而在氧较少的情况下,富锡的三角区域则会受到腐蚀。因此,腐蚀产物中可能形成的锡化合物或铜化合物的浓度将受到这种选择性腐蚀现象的强烈影响[6]。我国学者宋曼等在1984年指出了青铜的内部结构由α固溶体和(α+δ)共析体组成,青铜在铸造中会出现偏析现象,晶间处最先发生腐蚀,潮湿环境下氧化亚铜容易与氯化物反应生成氯铜矿,膨胀成疱,进而呈粉状脱落[1]。赵晋保等在1985年提出青铜锈层内起泡的原因是氯化铜反应生成氯化亚铜致使氢气放出[7]。
程德润等在1989年提出了青铜表面不均匀理论,并绘制出青铜组织结构分布图,认为青铜粉状锈腐蚀反应首先生成氧化膜,同时指出了循环发生的电池反应[9]。国内对于粉状锈研究内容最多、研究范围最广的应属中国科学技术大学物理化学系的范崇正教授,他从20世纪90年代就开始研究粉状锈的生成机理问题。1992年5月,范崇正等对氯化亚铜氧化反应的化学动力学过程进行了探究,证明了氯化亚铜在酸性环境中能够反应生成铜离子[9]。在1994年他又与日本学者铃木稔等人合作研究了青铜生锈过程中铜元素的扩散,指出了氯化亚铜在粉状锈生长过程中所起的作用,对患“青铜病”文物出土后毁坏速度远大于埋藏环境中的损毁速度的原因做出了解释[10]。2004年,张瑛等对青铜器粉状锈结构特征和反应动力模型研究时,证明了氯化亚铜随氯离子浓度变化的线性关系[11]。2009年王蕙贞等对青铜器的生成机理提出了不同的观点,认为青铜器不是先与氯化物反应生成氯化亚铜,而应该是先与氧气反应生成氧化亚铜[12]。冯丽婷等于2010年利用多孔电极模拟实验测试证明了氯化亚铜的催化会加剧青铜腐蚀,碱式氯化铜为腐蚀的最终产物[13]。
随着一个多世纪关于粉状锈不断深入的研究,从反应产物的组成到反应的具体过程,其研究成果不断推进。在青铜粉状锈腐蚀机理的研究方面基本形成了一些共识:即粉状锈的最终产物为碱式氯化铜,化学式为Cu2(OH)3Cl,由氯铜矿、副氯铜矿、斜氯铜矿等同分异构体矿物混合而成。世界范围内,“青铜病”的研究历史已有150年之久,但研究资料与报道主要集中在锈腐蚀机理与反应过程、腐蚀发生条件、腐蚀产物检测方法及青铜制品的锈蚀预防处理等方面,而粉状锈的传染问题鲜有涉及。
中国学者范崇正[14]在1992年提出了粉状锈颗粒能够摆脱重力场影响随空气传播的观点,这也是国内学者关于粉状锈传播过程的最早报道。但文中只提及粉状锈会通过空气传播,并未做出详细的分析与实验。因此,本研究在对国内外粉状锈生成机理研究做了梳理的基础上,通过模拟实验对粉状锈生成过程进行了验证,并对粉状锈生长过程做了观察和记录。进而通过对粉状锈生长微环境气溶胶成分的检测,确定了粉状锈传播传染途径,串联起粉状锈从感染,到生长再到成为“传染源”,由量变到质变的全过程,对锈蚀破裂过程做出了详细的解释。
综上所述,本研究对粉状锈的传染问题进行了开创性实验研究,为粉状锈利用空气动力进行传播提供了依据,并能够为青铜器粉状锈的预防提供有益借鉴,为锈蚀产物鉴定提供更多数据支撑,同时也能为减缓粉状锈的生长和传染提供可行的方法。
1 样品与方法
1.1 样品制取
本研究中粉状锈样品由仿古浇铸青铜片(含Cu 79.23%、Sn 12.24%、Pb 6.42%)经电化学腐蚀方法制取。将规格为20 mm×20 mm×5 mm的青铜样块用不同目数砂纸打磨,去除青铜样品表面氧化层及杂质后用去离子水洗净。在3%的NaCl水溶液中逐滴加入盐酸溶液[15],将溶液pH值调至5左右。将青铜样块与稳压电源正极连接,负极连接一根纯铜丝,将二者置于盛有上述溶液的烧杯里,在水浴锅中于28 ℃[16]隔水加热。电压调至1.5 V,持续通电24 h,将生成粉状锈的青铜样品标记为S1。
1.2 自制样品实验观察箱
为满足实验需求,笔者自制一文物样品实验观察箱(图1~2)。试验箱包括箱体、箱盖、若干文物样品放置托盘,以及摄像装置适配单元。箱体中设有隔层,用于将箱体分为上层样品放置空间和下层螺杆操作空间;若干文物样品放置托盘分布在所述隔层上,包括与隔层螺接的螺杆和设置在螺杆顶部的托盘;箱盖包括盖体、嵌设在盖体两侧的两抬杆,以及在两抬杆之间设置的摄像装置适配单元;摄像装置适配单元包括丝杆、滑块、导杆以及手柄。其中,所述滑块与丝杆呈丝杆螺母运动副配合,能够沿箱体横向移动,以对不同托盘上文物样品进行无接触拍摄。该实验箱可实现无接触调节样品拍摄角度和焦距,避免了对实验样品的污染和实验过程的干扰。
实验箱四角可置一盛有250 mL饱和溴化钠溶液的烧杯以控制箱内相对湿度。饱和溴化钠溶液在室温(25 ℃)状态下,可使微环境相对湿度达到60%左右,这一数值既能够满足青铜粉状锈生成湿度需要,同时也可以控制反应速度,避免反应过快,便于对锈蚀生长过程做观察和记录。此外,常规实验室能满足此温度要求,上述温度也可模拟馆藏青铜器存放环境的实际温度。溴化钠易溶于水,且溶解后水溶液呈中性,对实验结果影响可忽略不计。将4个盛有配置好的250 mL饱和溴化钠溶液的烧杯,分别置于实验箱四角,关闭样品放置口,观察实验箱内温湿度计读数,待湿度数值停止变化且长期稳定在60%后即可将样品放入开始观察实验。
经观察与测试,该观察箱能形成有效封闭环境,具有良好的气密性。同时箱体内相对湿度在饱和溴化钠溶液调控下也能持续保持在60%。
1.3 试验方法
将样品S1放入实验观察箱内,温度保持在25 ℃,相对湿度保持在60%(±2%)左右。样品放置前用紫外线杀菌灯进行灭菌处理,实验中每隔8 h对样品进行1次灭菌处理,每次时长1 h,以确保实验环境与结果不受微生物影响。持续观察一段时间,拍照记录并对锈蚀产物取样进而做表征。
样品放入一周后,将与真空抽气装置连接的采样滤头放入实验箱内对气溶胶进行采样,滤头内置直径30 mm、孔径0.45 μm的石英滤膜,采样时间为48 h[17],样品标记为Q1。另于实验箱外采集空白对照样,标记为Q0。将采好样的滤膜置于5 mL硝酸中捣碎,超声震荡2 h,加热至沸腾,用去离子水定容至15 mL,取过滤澄清溶液10 mL,采用电感耦合等离子体质谱仪(ICP-MS)对铜离子进行测定。
利用电感耦合等离子体质谱仪测定铜离子的目的和意义在于,明确含铜离子的细颗粒物会在空气中利用气溶胶进行传播。但其所测定的铜离子含量为总含量,无法区分其价态。在粉状锈生长过程中,中间产物氯化亚铜中的铜为一价铜,最终产物碱式氯化铜中的铜为二价铜。而利用紫外-可见分光光度计测量样品溶液的吸光度可以区分其中铜离子的价态。用以进一步证明粉状锈可以利用气溶胶进行传播。
配制浓度为5 mg/L的铜标准溶液[18]、10%(M/V)盐酸羟胺溶液、37.5%(M/V)柠檬酸钠溶液和0.2%(M/V)新亚铜灵溶液。用移液管分别准确吸取0.00、0.50、1.00、2.00、3.00、5.00 mL铜标准溶液(5 mg/L)于25 mL容量瓶中,加入去离子水10 mL、盐酸羟胺溶液1.5 mL、柠檬酸钠溶液3 mL、乙酸钠-乙酸缓冲液3 mL,再用移液管准确吸取新亚铜灵溶液1.50 mL,用去离子水定容,充分混匀后静置。以水为空白样,用紫外-可见分光光度计于波长457 nm(测试范围370~600 nm)处测定吸光度,绘制标准曲线[19]。以与采集Q1相同的方式再次采集气溶胶样品,并标记为Q2。将滤膜置于10 mL去离子水中捣碎后过滤,加入柠檬酸钠溶液3 mL、乙酸钠-乙酸缓冲液3 mL(pH值约为5.7)、新亚铜灵溶液1.50 mL,用去离子水定容至25 mL,摇匀,测定吸光度。
为佐证上述实验结果,采集实验箱内气溶胶30日,每日时长24 h,取出采样滤头内石英滤膜,剪取采样口附近深色部位标记为样品K1,用显微拉曼光谱法测定其成分组成。
相关实验方法与仪器参数如下:
1) 扫描电子显微镜分析。
实验仪器:肖特基场发射扫描电子显微镜能谱仪(Sirion200型,日本电子公司JEOL)。
实验方法:取样品经过喷铂处理后,使用扫描电子显微镜能谱仪观察样品剖面与表面。样品在200倍与500倍条件下可见基体部分与锈蚀层。在10 000倍与20 000倍条件下可对表面锈蚀物进行观察。
2) X射线衍射分析。
实验仪器:样品水平型大功率X射线粉末衍射仪(Rigaku,TTR-Ⅲ)。
实验方法:取样品表层锈蚀产物研磨后利用X射线衍射分析其物相结构。
3) 拉曼光谱分析。
实验仪器:激光拉曼光谱仪(LabRAM HR Evolution)。
实验方法:利用显微激光拉曼光谱仪分析滤膜处细微颗粒物的物相结构。
4) 电感耦合等离子体质谱分析。
实验仪器:电感耦合等离子体质谱仪(Thermo Fisher iCAP RQ)
实验方法:利用电感耦合等离子体质谱仪对测定制备样品中的铜离子含量。
5) 吸光度分析。
实验仪器:紫外-可见-近红外分光光度计(UV-Vis-NIF Spectrometer)
实验方法:紫外-可见-近红外分光光度计分析制备样品吸光度,以确定铜离子价态及含量。
2 实验结果
2.1 粉状锈生长情况与产物表征结果
持续观察样品S1 9 d,粉状锈生长变化情况如图3(左)所示。随着时间推移,锈蚀产物堆积增多,并出现锈层开裂、剥离、破裂、掉落(图3右)等现象。

图3 粉状锈泡锈生长变化图(左)和粉状锈泡锈破裂后掉落瞬间图(右)Fig.3 Images of growth and variation of powdery rust bubbles (left) and rusty powder dropping after bubble rupture (right)
为了进一步了解粉状锈的生长情况,在对样品进行切割后,观察剖面的形貌,表征结果如图4所示。
分别对样品S1表层绿色锈蚀与底层白色锈蚀进行表征,分析结果如图5~7。

图5 表层绿色锈蚀扫描电镜图(左)与底层白色锈蚀扫描电镜图(右)Fig.5 SEM images of surface green rust (left) and bottom white rust (right)
从图4的剖面扫描电镜图可以清晰观察到青铜样品的基体和锈蚀层,青铜基体内部结构仍然致密,而越接近外部锈蚀层,结构越发酥松,且锈蚀颗粒呈逐步增大的趋势。
根据图5的扫描电镜图片可以观察到,锈蚀整体由无数细颗粒堆积聚集而成,颗粒之间有疏松孔隙。绿色锈蚀粒径大都在1 μm左右,而白色锈蚀颗粒更为细小,在100 nm左右。
从图6~7的S1样品X射线衍射图谱可以看出,绿色锈蚀主要由两种矿物组成,其中2θ=16.2°、18.9°、30.9°、32.6°、39.3°、53.5°的峰归属于斜氯铜矿,其为碱式氯化铜的一种不稳定同分异构体;2θ=16.2°、31.8°、39.3°、50.0°、53.5°、62.3°的峰归属于碱式氯化铜。白色锈蚀由氯化亚铜组成,2θ=28.5°、33.0°、47.4°、56.3°、69.3°、76.6°、88.3°为其主要衍射峰。
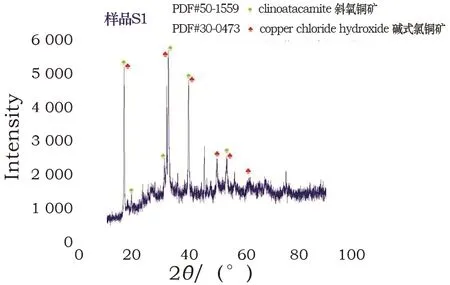
图6 表层绿色锈蚀X射线衍射图谱Fig.6 XRD pattern of surface green rust

图7 底层白色锈蚀X射线衍射图谱Fig.7 XRD pattern of bottom white rust

图8 粉状锈生长与腐蚀过程示意图Fig.8 Schematic diagram of the growth and corrosion process of powdery rust
由此可见,在使用电化学法模拟粉状锈生长过程实验中,利用观察箱可以观察到完整的锈蚀过程,而对锈蚀产物的分析可以明确其成分。粉状锈对青铜基体的腐蚀是由表及里的过程,青铜块表面部分先形成氯化亚铜,然后在潮湿空气中形成碱式氯化铜并逐渐向外部堆积、膨胀,最后脱落。同时氯化亚铜也会继续向内层腐蚀,并重复生成碱式氯化铜的过程。因此,粉状锈对基体的腐蚀是由表及里的,而粉状锈自身的生长,是由内向外的。
2.2 实验箱内气溶胶颗粒物成分分析结果
表1是实验箱内外气溶胶中(总)铜离子含量的ICP-MS检测结果。结果显示,相同时间内实验箱里气溶胶中铜离子含量约为实验箱外的4倍左右,实验箱内的(总)铜离子含量的异常值表明气溶胶颗粒物中含有Cu的化合物。为明确其铜离子价态,特利用紫外-可见分光光度计测量样品溶液的吸光度。图9为Cu+离子标准溶液吸光度曲线图。

表1 实验箱气溶胶颗粒物中(总)铜离子ICP-MS含量检测结果Table 1 ICP-MS results of the total copper ion contained in aerosol of the inspection box

图9 铜标准溶液吸光度曲线图Fig.9 Absorbance curves of the standard solutions of copper
将吸光度数值散点图利用最小二乘法进行函数线性拟合,结果如图10所示。

图10 铜标准溶液吸光度散点图Fig.10 Absorbance scatter diagram of the standard solutions of copper
样品Q2的吸光度如图11所示。在457 nm处同样有吸收峰出现,说明原溶液中有Cu+存在。

图11 样品Q2吸光度曲线图Fig.11 Absorbance curve of Sample Q2
根据朗伯-比尔定律,得出公式:
(9)
式中,A为样品吸光度值,测定三次取平均值;A0为空白吸光值;a为回归方程截距;b为回归方程斜率;V为样品体积,单位为mL。
将各数据代入计算得,样品CCu+=0.257 mg/L。
结合Q1的结果,样品CCu2+=1.336 mg/L。
通过对样品溶液吸光度的测定,可以证明样品溶液或者说滤膜中至少存在两种含铜化合物。其后利用激光拉曼测定其物相结构。
采用细激光束分别对K1样品石英滤膜上两种显微可见细颗粒物进行对焦检测,拉曼分析结果如图12~13所示,部分锈蚀颗粒物在368 cm-1、513 cm-1、823 cm-1、912 cm-1、979 cm-1有极强的衍射峰,符合氯铜矿的特征;而另一部分锈蚀颗粒在63 cm-1、111 cm-1、128 cm-1、155 cm-1处有较强衍射峰位,与氯化亚铜的特征峰较为一致。因此,该样品应为氯化亚铜和氯铜矿的混合颗粒。其中氯化亚铜中铜为一价,氯铜矿中铜为二价。结果与紫外-可见分光光度计测量结果一致。

图12 样品K1的拉曼图谱(200~1 000 cm-1)Fig.12 Raman spectrum of Sample K1 (200~1 000 cm-1)
3 结论与建议
基于上述模拟实验与检测分析,得出主要结论如下:
1) 碱式氯化铜为粉状锈的主要组成成分,也是粉状锈生成反应的最终产物。氯化亚铜为反应的中间产物,其在氧气和潮湿环境下会转化为碱式氯化铜。
2) 粉状锈的生长过程是一个由内而外的过程,内部反应会使反应产物膨胀,并不断向外生长扩大,直至出现裂隙或者炸裂。
粉状锈对青铜基体的腐蚀是由表及里的,表层青铜基质完全反应后会成为碱式氯化铜,质地疏松且易脱落的同时也方便外界氧气与水分进入,进而继续向里层反应,在环境条件适宜的情况下,这种反应会持续进行,直至青铜合金被完全反应掉。
3) 粉状锈产物主要由氯化亚铜与碱式氯化铜混合而成,多为粒径2.5 μm以下的疏松、细小的颗粒状物质。粉状锈细小颗粒受泡锈分裂破裂作用力影响,随气流变成完全不规则的悬浮态物质,落到周围环境中,当接触到其他青铜器时,便会在氧气和水的作用下令其“感染”粉状锈。
基于以上结论,在此对青铜文物的保存和展示提供一些建议:
首先,青铜文物保存环境中需减少空气的流动,切断粉状锈传播途径,尤其在有大量青铜器展览陈列的条形大展柜和青铜器存放的库房中,更应重视展柜和库房中空气的流量和流向,避免内部空气与多件青铜器交叉接触。条件允许的情况下建议有粉状锈的青铜器,在库房或展陈中单独密封存放。不具备单独密封存放条件的,也应尽可能避免置于空气流通较好的地方,如空调口或风扇上风处等等。
此外,还应加强青铜器存放环境中颗粒物的定时监测,当颗粒物浓度达到一定警戒丰度时,要即时进行清洁除尘作业,避免粉状锈气溶胶浓度过高引起同一件器物多部位被传染和不同器物之间的相互传染现象。对于布展、出入库房等过程中掉落的锈蚀粉末也应及时清理,即使是无害锈粉末通过悬浮、沉降等过程降落到文物器表也会增加局部吸湿效果,从而加剧青铜器的电化学反应。
其次,对患有青铜病的文物进行保护修复时,要严格按照“特器特办”的原则,应单独设置有害锈文物保护修复区域,配备单独的修复工具,对采用物理方法清理出来的粉状锈粉末颗粒,应随时回收,统一做好后续处理,严格控制修复室内空气交叉流动,设置新风口。在对一件器物进行去除粉状锈操作时,应最大限度避免取下的粉状锈与器物其他部位接触,减少其他部位被二次“感染”的可能性。另外,应确保粉状锈被完全去除干净后,再采用去离子水冲洗器物,避免未除尽的粉状锈残点在高湿环境中二次生长。同时,在文物保护修复过程中,应重视“泡状”锈蚀的处理,避免在保存过程中泡状锈蚀破裂,产生有害颗粒物在空气中的迁移。

