免疫亲和柱净化柱后光化学衍生高效液相色谱-荧光检测法同时测定制马肾中4种黄曲霉毒素
孙艳杰 赵磊 李正刚 王路宏

【摘 要】 目的:建立免疫亲和柱净化柱后光化学衍生高效液相色谱-荧光检测法同时测定制马肾中黄曲霉毒素B1、B2、G1、G2的含量。方法:样品采用70%甲醇作为提取溶剂,经免疫亲和柱净化、高效液相色谱分离、光化学柱后衍生后,通过荧光检测器测定其中黄曲霉毒素的含量。结果:黄曲霉毒素B1的线性范围为0.0104~0.0520 ng(r=0.999 9)、黄曲霉毒素B2的线性范围为0.0038~0.0190 ng(r=0.999 8)、黄曲霉毒素G1的线性范围为0.0108~0.0540 ng(r=0.999 8)、黄曲霉毒素G2的线性范围为0.0038~0.0190 ng(r=0.9998),线性关系良好,回收率在89.68%~101.44%之间,RSD≤3.5%。结论:该方法操作简便,灵敏度高、重复性好、结果准确,可用于制马肾中黄曲霉毒素的测定。
【关键词】 制马肾;免疫亲和柱;光化学衍生;高效液相色谱-荧光检测器;黄曲霉毒素
【中图分类号】R284.1 【文献标志码】 A【文章编号】1007-8517(2023)23-0019-04
DOI:10.3969/j.issn.1007-8517.2023.23.zgmzmjyyzz202323005
Simultaneous Determination of Content of Four Aflatoxins in EQUI PENIS ET TESTIVULUS by Mmunoaffinity Column Clean-up and HPLC-FLD with Post-column Photochemical Derivatization
SUN Yanjie ZHAO Lei LI Zhenggang WANG Luhong*
Siping Institute for Food and Drug Control,Siping 13600,China
Abstract:Objective To establish the contamination method of aflatoxin B1,B2,G1 and G2 in EQUI PENIS ET TESTIVULUS by immunoaffinity column clean-up and HPLC-FLD with post-column photochemical derivatization.Methods After extraction with 70% Methanol and purification by immunoaffinity columns,aflatoxin B1,B2,G1 and G2 in samples were anlyzed by HPLC-FLD with post-column photochemical derivatization.Results The linearity of Aflatoxin B1 was at 0.0104-0.0520 ng(r=0.9999), Aflatoxin B2 was at 0.0038-0.0190 ng(r=0.9998), Aflatoxin G1 was at 0.0108-0.0540 ng(r=0.9998), Aflatoxin G2 was at 0.0038~0.0190 ng(r=0.9998), The average recoveries were within 89.68%-101.44% with RSD≤3.5%. Conclusion The above method has demonstrated convenient operation,good repeatability,highsensitity and accuracy.This method is suitable for the determination of AF in Renshenguipi pills.
Keywords:Equi Penis Et Testivulus;Immunoaffinity Column;Photochemical Derivation;HPLC-FLD;Aflatoxi
馬肾药材标准收载在《吉林省中药材标准》第二册2019版[1],为马科动物成年马Equus caballus Linnaeus雄性的干燥阴茎及睾丸。制马肾为马肾经过滑石粉炒,祛除其腥味,便于保存和临床应用[2]。黄曲霉素(aflatoxins,AF)属真菌毒素,是黄曲霉和寄生曲霉产生的双呋喃环类毒素的次级代谢产物,以AF B1、B2、G1、G2较常见。AF的强致癌性,特别是AFB1,其毒性比氰化物、砷化物和有机农药等的毒性更大,已被世界卫生组织癌症研究机构列为Ⅰ类致癌物质[3-7]。黄曲霉性喜湿热,中药材及饮片潮湿季节,保存不当,容易造成黄曲霉毒素污染,特别是含蛋白质,油脂类的动物类药材更容易黄曲霉毒素超标。《中国药典》2020版一部中有较多动物类药材和饮片品种进行了AF的限量控制,如地龙、蜂房、土鳖虫等[8-10]。经查阅文献,未发现有关于马肾相关真菌毒素的研究报道。为保证制马肾的用药安全,本次研究采用检测灵敏度较高的免疫亲和柱,柱后光化学衍生,高效液相色谱-荧光检测法同时测定制马肾中AF B1、B2、G1、G2的含量,并进行了方法考察研究,验证测定方法的可靠性,为临床用药安全提供参考。
1 仪器与材料
1.1 仪器 BT125D型电子天平(北京赛多利斯仪器天平有限公司),Agilent LC 1260型高效液相色谱仪(配Agilent LC1260II型荧光检测器,安捷伦科技有限公司),KRC-25型光化学柱后衍生器(青岛普瑞邦生物工程有限公司),TDL-5-A型离心机(上海安亭科学仪器厂)。
1.2 试验材料 黄曲霉混合对照品溶液(AF B1、B2、G1、G2标示浓度分别为(1.04 μg/mL、0.38 μg/mL、1.08 μg/mL、0.38 μg/mL,批号:610001-202006,中国食品药品检定研究院)。10批制马肾来源于炮制中式样品。免疫亲和柱(青岛普瑞邦生物工程有限公司)。甲醇和乙腈(Flsher Scientific,色谱纯),纯化水为自制,其他试剂为分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 黄曲霉混合对照品工作溶液的制备 精密量取黄曲霉混合对照品溶液0.5 mL,置10 mL量瓶中,用70%甲醇稀释至刻度,作为贮备溶液。精密量取贮备溶液1 mL,置25 mL量瓶中,用70%甲醇稀释至刻度,即得黄曲霉混合对照品工作溶液。
2.1.2 供试品溶液的制备 取供试品约15 g(剪碎),精密称定,置于均质瓶中,加入氯化钠3 g,精密加入70%甲醇溶液75 mL,12000 r/min高速搅拌2 min,4500 r/min离心5 min,精密量取上清液15 mL,置50 mL量瓶中,用水稀释至刻度,摇匀,4500 r/min离心10 min,精密量取续滤液10.0 mL,通过免疫亲合柱,流速每分钟3 mL,用水20 mL洗脱,洗脱液弃去,使空气进入,将水挤出免疫亲合柱,再用适量甲醇洗脱,收集洗脱液,置2 mL量瓶中,加甲醇稀释至刻度,摇匀,用微孔滤膜(0.22 μm)滤过,取续滤液,即得。
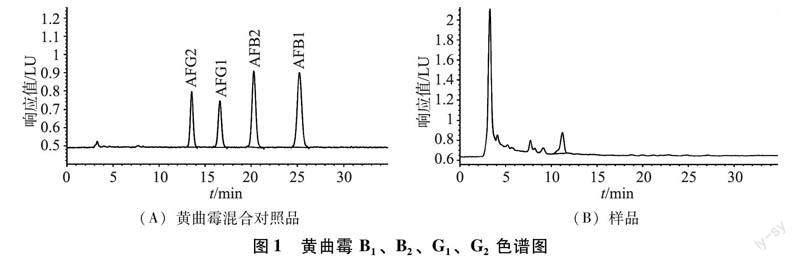
2.2 色谱条件及测定方法 采用Agilent ZORBAX SB-C18,5 μm,250 mm×4.6 mm;流动相为:甲醇-乙腈-水(40∶18∶42);流速为1.0 mL/min;柱温为25 ℃;采用柱后光化学衍生法(254 nm),以荧光检测器检测,激发波长λex = 360 nm,发射波长λex = 450 nm。分别精密吸取“2.1.1”项下黄曲霉混合对照品工作溶液5 μL、10 μL、15 μL、20 μL、25 μL,注入液相色谱仪,测定峰面积,以进样量为横坐标,峰面积为纵坐标,绘制标准曲线。另精密吸取“2.1.2”项下供试品溶液20 μL,注入液相色谱仪,測定峰面积,从标准曲线上读出供试品中AF B1、B2、G1、G2的量,进行计算。AF B1、B2、G1、G2的色谱峰与相邻色谱峰的分离度均大于1.5,且无杂质干扰峰。结果如图1所示。
2.3 线性范围和检出限 分别精密吸取“2.1.1”项下混合对照品溶液5 μL、10 μL、15 μL、20 μL、25 μL,注入液相色谱仪,测定峰面积,以进样量(ng)为横坐标,峰面积为纵坐标,绘制标准曲线。结果见表1。
取不含黄曲霉的样品15g,加入适当稀释的黄曲霉混合对照品溶液,同供试品溶液制备、测定,以信噪比(S/N)为3作为4种黄曲霉毒素的检出限(limit of detection,LOD)。结果见表1。
2.4 精密度考察 取黄曲霉混合对照品工作溶液20 μL,注入液相色谱仪,按“2.2”项下色谱条件连续进样6次,分别计算黄曲霉B1、B2、G1、G2峰面积的RSD(n=6)分别为1.15%、1.08%、1.07%、1.31%。结果表明仪器精密度良好。
2.5 稳定性试验 取“2.6”项下供试品溶液,分别于0 h、4 h、8 h、16 h、18 h、24 h,按“2.2”色谱条件,进样20 μL,记录所测各组分峰面积,黄曲霉 B1、B2、G1、G2峰面积的RSD(n=6)分别为1.82%、2.01%、1.91%、1.93%,结果表明对照品溶液在24 h内稳定。
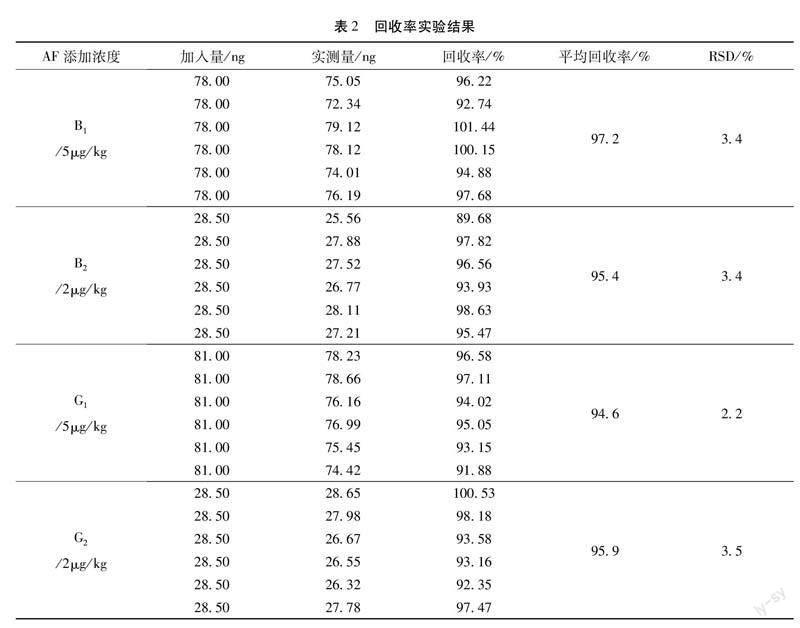
2.6 重复性试验及回收率试验 经考察10批制马肾中均未检出黄曲霉B1、B2、G1、G2,故本次实验重复性在加样回收的6个平行试验的同时进行考察。取不含黄曲霉的供试品粉末约15 g,各6份,精密称定,分别置于均质瓶中,精密加入黄曲霉混合对照品储备液75 μL,按“2.1.2”项下操作,按“2.2”项下色谱条件测定,计算回收率。测定结果见表2。结果表明方法的重复性良好,准确度达到方法要求。
2.7 样品测定 取10批次制马肾样品,按照“2.1.2”项下方法制备供试品溶液,按“2.2”项下条件进样测定,结果均未检出AF B1、B2、G1、G2。
3 讨论
3.1 样品提取方法考察 本实验分别采用匀质法和超声提取法进行了制马肾样品中黄曲毒素的提取处理,结果匀质提取法AF B1、B2、G1、G2平均回收率分别为96.1%、95.2%、93.8%、94.4%,超声提取法AF B1、B2、G1、G2平均回收率分别为90.5%、89.1%、91.1%、90.6%。回收率匀质法优于超声提取法。且样品的提取采用匀质法,12000 r/min 高速搅拌2 min即可完成操作,而超声提取法需要超声30 min,提取效率较匀质法低。故本次采用匀质法进行制马肾样品中黄曲霉毒素的提取。
3.2 色谱条件的考察 以甲醇-乙腈-水(40∶18∶42);流速为1.0 mL/min-1;柱温为25 ℃为色谱条件,分别考察了Agilent ZORBAX SB-C18(4.6 mm×250 mm,5 μm)、YMC-Hydrosphere-C18(4.6 mm×250 mm,5 μm)、Diamonsil C18(4.6 mm×250 mm,5 μm),3个不同品牌的色谱柱的测定效果。结果,AF B1、B2、G1、G2的分离度均达到2.0以上,塔板数均高于8000,表明方法的适用性较好。
3.3 黄曲霉检测方法选择 黄曲霉毒素有多种检测分析方法,包括酶联免疫吸附法、高效液相色谱-荧光法、胶体金快速定量法、实时荧光PCR方法、高效液相色谱-串联质谱法等[11-13]。其中高效液相色谱-荧光法检测应用最为广泛。在4种黄曲霉毒素中,AF B1和G1遇水荧光猝灭,需要先进行柱后衍生化,来提高AF B1和G1的荧光强度,增强其灵敏度。柱后衍生法有碘衍生法和光化学衍生法两种。碘衍生化法需要配制碘饱和溶液,且衍生剂有一定的腐蚀作用,也会造成基线的漂移,设备成本高。而光化学衍生操作简便、不需要衍生剂与衍生温度,延长检测器寿命,购置成本低,仪器配制简单,并且可以通过开关光化学衍生器,AF B1和G1的信号响应值变化来鉴别AF B1和G1假阳性反应,适用性更好。
本研究進行了免疫亲和柱净化柱后光化学衍生高效液相色谱-荧光检测法同时测定中药饮片制马肾中AF B1、B2、G1、G2 4种黄曲霉毒素含量,并进行了方法学各项指标验证,均满足分析测定的要求。由于本次仅收集了10个批次样品,虽然均未检测出黄曲霉毒素,但马肾为动物类药,蛋白质含量高,湿热环境下非常容易感染黄曲霉毒素,存储温度控制不好,会存在非常大的安全风险,故对其进行AF的更多批次样本和持续监控检测仍然具有非常大的意义[14-16]。
参考文献
[1]吉林省药品监督管理局.吉林省中药材标准(第二册)[S].长春:吉林科学技术出版社,2020:21.
[2]卫生部药品标准·中药成方制剂·第十三册[S].1991:9.
[3]黄晓静,王少敏,毛丹,等.曲霉属真菌毒素的毒性研究进展[J].食品安全质量检测学报,2017,8(5):1679-1687.
[4]罗自生,秦雨,徐艳群,等.黄曲霉毒素的生物合成、代谢和毒性研究进展[J].食品科学,2015,36(3):250-257.
[5]陈宗良,周玲娜,赵静芳,等.自动固相萃取-HPLC-在线柱后光化学衍生法测定藿香正气水中黄曲霉毒素[J].中国现代应用药学,2021,38(10):1218-1221.
[6]谭静玲,丁晓萍,姜涛,等.安神益脑丸中黄曲霉毒素残留量测定及LC-QQQ/MS确证[J].中国医院药学杂志,2021,41(7):687-691.
[7]张玮玮,张志鹏,董雪,等.远志产地初加工过程中黄曲霉污染调查及病发规律研究[J].时珍国医国药,2021,32(3):603-606.
[8]国家药典委员会.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2020:127.
[9]国家药典委员会.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2020:373.
[10]许晓辉,李晨曦.QuEChERS-分散固相萃取-液质联用法快速测定地龙中黄曲霉毒素[J].分析测试技术与仪器,2021,27(1):18-23.
[11]于鹏浩,张磊.免疫亲和柱净化光化学衍生高效液相色谱-荧光检测法同时测定土鳖虫中黄曲霉毒素B1、B2、G1、G2、M1、M2[J].中国中药杂志,2019,44(23):5083-5087.
[12]袁京磊.黄曲霉毒素检测方法的研究进展[J].现代食品,2022,28(1):14.
[13]戴煌,黄周梅,李占明,等.免疫法在食品黄曲霉毒素检测中的应用[J].中国食品学报,2021,21(10):287.
[14]范妙璇,傅欣彤,陈奕菲,等.三线定量胶体金免疫亲和试纸法定量中药饮片中黄曲霉毒素B1及B1、B2、G1、G2总量的研究[J].中草药,2021,52(17):5275.
[15]叶萍,张慧娥,李光,等.质谱技术在黄曲霉毒素检测中的研究进展[J].食品与机械,2021,37(10):227.
[16]赵晓野,王儒,王婷,等.黄曲霉毒素的危害及检测方法研究进展[J].食品安全导刊,2022(3):155.
[17]王振峰,王文萍,夏小明.黄曲霉毒素检测方法及其应用[J].食品安全导刊,2021(3):163.
(收稿日期:2023-03-02 编辑:刘 斌)
基金项目:吉林省地方中药炮制规范项目(JLPZGF-2020-066)。
作者简介:孙艳杰(1980—),女,汉族,学士,副主任药师,研究方向为药品质量检验。E-mail:383816269@qq.com
通信作者:王路宏(1965—),女,汉族,学士,主任药师,研究方向为药品质量检验。E-mail:517677231@qq.com

