HAN 基液体发射药高压热物理性质的估算
潘玉竹,余永刚,周彦煌,陆 欣
(南京理工大学能源与动力工程学院,江苏 南京210094)
引 言
液体发射药的热物理性质通常包括热力学性质和输运性质两大类,热物理性质的选取对理论计算结果的准确性影响较大。但是目前有关HAN 基液体发射药在高压下的实验数据较少,因此在理论研究中迫切需要估算其高压热物理性质。
庄逢辰[1]在建立液滴的高压蒸发理论时,采用经验公式估算了计算中所需要的热物性参数。Hsieh[2]、李玉琦[3]在确定多组分液滴的高压热物理性质时,先估算出每一组分的热物理性质随压力和温度的变化关系,然后再按照一定的混合规则进行平均。针对HAN 基液体发射药的热物理性质,国内外学者开展过一系列的基础研究。Klein[4]、Decker[5]在进行相关实验之后,对HAN 基液体发射药及其组元的物理性质进行了理论预测,并与实验结果进行对比,验证了其理论的正确性;张续柱[6]整理了国内外有关HAN 基液体发射药的文献,对其物理性能给出了较为系统的预测,但未详细探讨其在高压下的热物理性质。
本研究把HAN 基液体发射药看作是极性物质,在估算出HAN 基液体发射药的临界参数之后,将其看作是一种具有临界性质的液体化合物,对其高压热物性进行估算,绘制并分析了LP1845液体发射药热物性参数随温度及压力的变化关系曲线。
1 临界性质的估算
对于液体燃料来说,临界性质的估算对其蒸发潜热、摩尔相变热、比热容、导热系数及扩散系数的预测有着非常重要的影响。而临界温度、临界压力和临界体积是反映临界性质最常用的基本参数,估算这3个参数的方法有很多种[7],对于纯物质最常用的是Joback法、Constantinou-Gani法和Wilson-Jasperson法等;对于混合物最常用的是Chueh-Prausnitz法、Li法以及Liu法等。
Spencer[7]通过计算发现,Chueh-Prausnitz法的估算值与实验值之间的偏差相对较小,认为此法是有效可行的。本研究借助Chueh-Prausnitz法[7]估算HAN 基液体发射药LP1845、LP1846的临界温度Tc、临界压力pc及临界体积Vc,结果如表1所示,与Kounalakis和Faeth[8]估算结果接近。除上述3个基本参数之外,还有一个常见的临界参数是偏心因子ω。偏心因子的估算方法最常用的是根据Lee-Kesler蒸气压方程和偏心因子定义式导出的偏心因子关联式[9],利用此法估算LP1845、LP1846的偏心因子值,结果见表1。
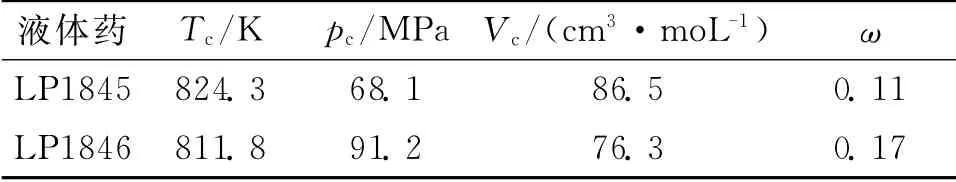
表1 HAN 基液体发射药的临界参数Table 1 Critical parameters of HAN-based liquid propellants
2 热力学性质的估算
2.1 密 度
2.1.1 气体密度
HAN 基液体发射药蒸气密度可借助状态方程计算,由气体状态方程计算出给定温度和压力下气体的体积,则气体密度可表示为:

式中:ρ为密度,g/cm3;V为体积,cm3/mol;M为平均摩尔质量,g/mol。
考虑到高压条件下真实气体不能当作理想气体看待,因此必须选择合适的实际气体状态方程。由于SRK 状态方程形式简单、计算精确且适用于极性物质,本研究选用SRK 状态方程,其形式如下:
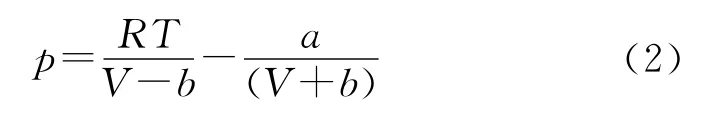
式中:p为压力,MPa;T为温度,K;R为通用 气体常数,J·mol-1·K-1;a、b为SRK 状态方程参数,可由临界参数计算得到。
2.1.2 液体密度
液体发射药密度是温度、压力的函数。Murad[6]根据状态方程推导出了HAN 基液体发射药密度与压力、温度的综合关系式,本研究采用Murad式来计算液体发射药密度,其形式如下:
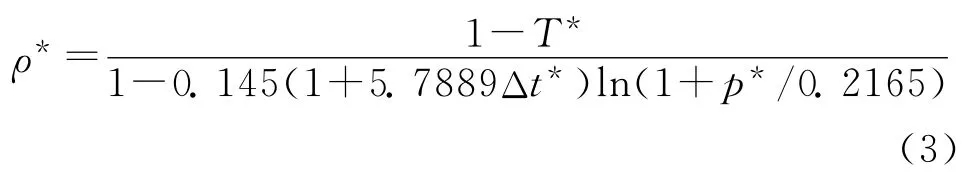
式中:ρ*=ρ×α3;T*=T/β;p*=pα3/β;Δt*=(T-298.15)/β;对于LP1845发射药:α=0.843 912,β=2 337。
根据式(3),计算了LP1845液体密度与温度和压力之间的关系曲线,如图1所示。
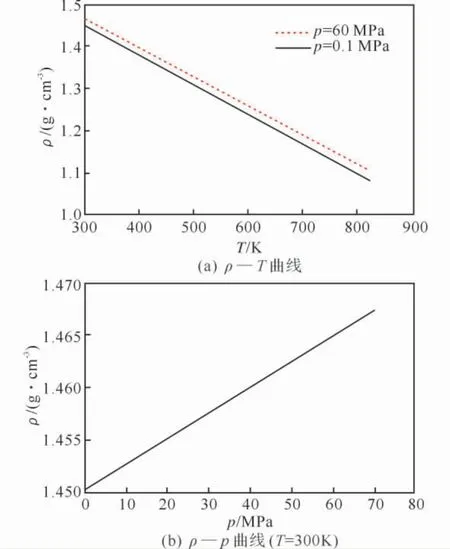
图1 LP1845液体密度与温度和压力之间的关系曲线Fig.1 Liquid density curves of LP1845versus temperature and pressure
当T=300K,p=0.1MPa时,LP1845的密度估算值为1.4503g/cm3。由图1(a)可知,对于LP1845,在300~800K 且压力保持恒定的情况下,随着温度的增加,液体密度显著减小。从图1(b)中可以看出,当温度为300K,0.1~70MPa时,随着压力的增大,液体密度只增加了1.17%。因此,温度对密度的影响大于压力的影响。
2.2 定压比热容
2.2.1 气体定压比热容
在相同的温度条件下,实际气体的定压比热容可以表示为理想气体定压比热容与剩余比热容之和。即:

其中,理想气体定压比热容可由经验公式确定,而剩余比热容ΔCp由通用的修正比热的关系式确定。Decker[5]采用式(5)确定HAN 基液体发射药蒸气的,即:
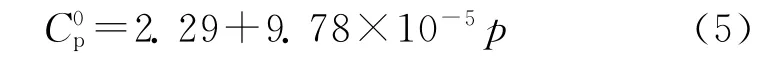
式中:为理想气体定压比热,J·g-1·K-1。
本研究采用Lee-Kesler通用修正关系式[10]来求取剩余比热容ΔCp,其形式为:
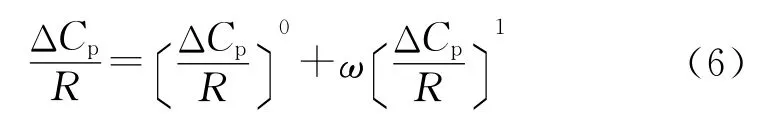
式中:(ΔCp/R)0、(ΔCp/R)1在文献[10]中以对比压力pr、对比温度Tr的CSP表格形式给出。此方法的适用范围是:0<pr<10,0.3<Tr<4。
根据上述方法计算不同压力下LP1845蒸气的实际定压比热容随温度的变化情况,如图2所示。
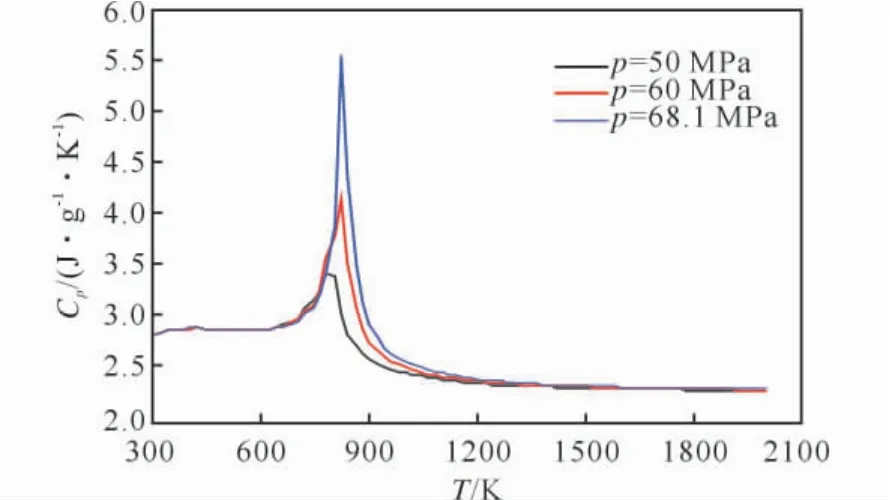
2 LP1845蒸气定压比热容随温度和压力的变化曲线Fig.2 Specific heat curves of LP1845vapour versus temperature and pressure
由图2可知,在相同的压力条件下,温度为300~600K 时,定压比热容基本不受温度的影响;之后,随着温度的上升,比热容略有增大;当达到某一温度时,比热容迅速增大,达到峰值;随后,定压比热容随着温度的增大而急剧下降;当温度超过1 400K 以后,温度对比热容基本无影响。从图2中还可以看到,当压力达到LP1845 的临界压力(68.1MPa)时,定压比热容峰值最大。
2.2.2 液体定压比热容
对于液体定压比热容的估算,常用的方法有基团贡献法和对比态法两种。考虑到研究的温度较高,采用Sternling-Brown经验公式[9]估算液体定压比热容Cpl。Sternling-Brown公式的实质是使用饱和压力下的液体定压比热容来代替所有压力下的定压比热容,即认为液体定压比热容仅为温度的函数,其形式如下:
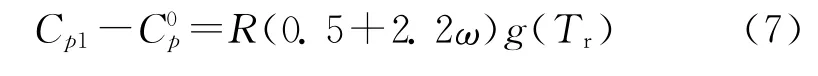
式中:
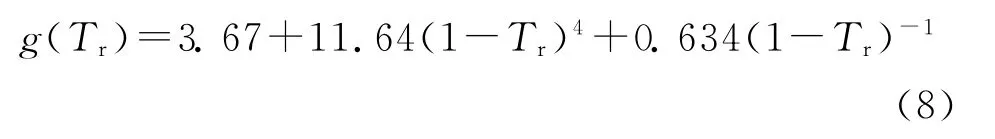
式中:Tr为对比温度,Tr=T/Tc。
图3给出50MPa压力下LP1845的液体定压比热容随温度的变化关系。由图3可见,在近临界温度区域附近,液体定压比热容出现了突变。在其临界温度824.3K 附近,液体定压比热容从2.98J·g-1·K-1迅速上升至15.30J·g-1·K-1,之后又迅速下降。而在远临界温度区域,液体定压比热容基本不受温度的影响。
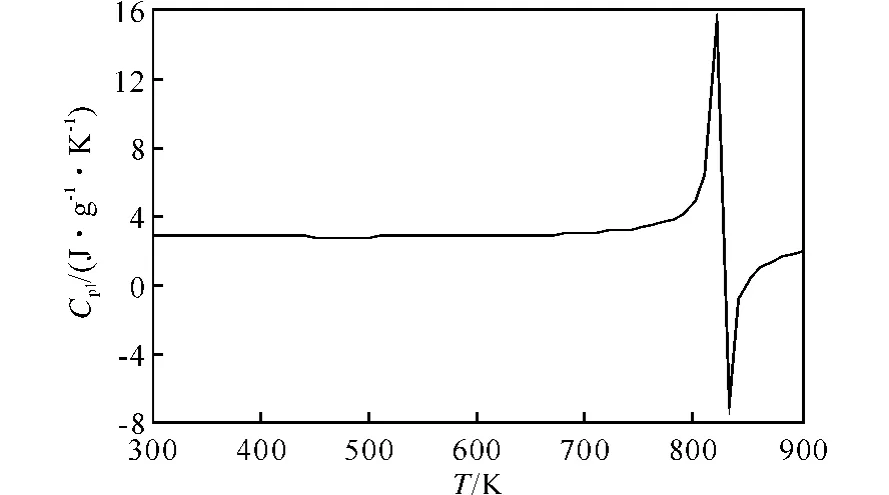
图3 LP1845液体比热容随温度的变化曲线Fig.3 Liquid specific heat curves of LP1845 versus temperature
2.3 饱和蒸气压
由于HAN 基液体发射药为均相液体,其饱和蒸气压可由Clapeyron方程来描述,即:
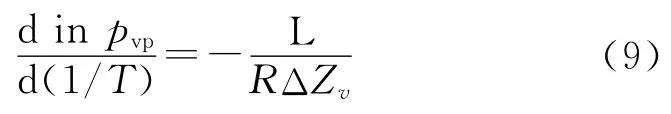
式中:pvp为饱和蒸气压,MPa;L为蒸发潜热,kJ/mol;ΔZv为饱和蒸气与饱和液体之间的压缩因子差。
Decker[5]借助实验手段测量了一定温度范围内LP1845、LP1846的蒸气压数据。本研究通过把实验数据代入上述Clapeyron方程中,从理论上推出LP1845、LP1846 在标准大气压下的沸点分别为399.9、396.7K。
另外,假设L/ΔZv为常数,且与温度无关。积分方程(9)可得:
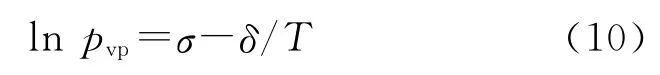
式中:σ为积分常数;δ=L/(RΔZv)。
式(10)也称为Clausius-Clapeyron 方程,在小温度区间内是一个比较理想的蒸气压近似关联式。
基于Clausius-Clapeyron方程,结合Decker测量的实验数据,本研究拟合出LP1845饱和蒸气压与温度的关系式为:
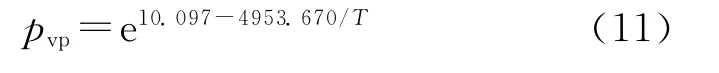
2.4 蒸发潜热和摩尔相变热
蒸发潜热是饱和蒸气与饱和液体之间的焓差;摩尔相变热是指在一定的温度和压力条件下,液体转变成蒸气时所吸收的热量。两者之间的差值称为等温焓差,即在温度保持不变时,压力变化到饱和压力时摩尔焓的变化。三者之间的关系可以表示为:
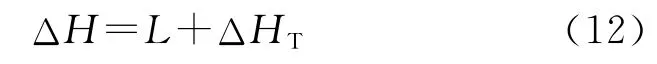
式中:ΔH为摩尔相变热,kJ/mol;ΔHT为等温焓差,kJ/mol。
由于饱和压力仅随温度而变化,蒸发潜热仅为温度的单值函数。蒸发潜热L用Pitzer偏心因子关系式[7]进行计算:
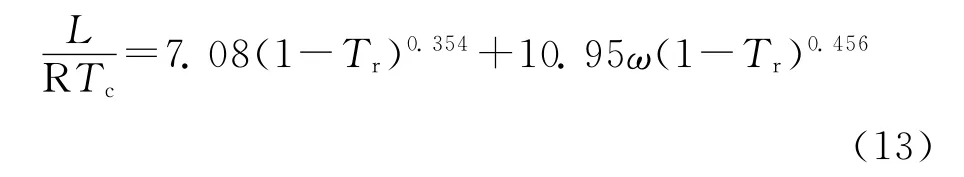
由化工热力学知识,等温焓差可以表示为[11]:
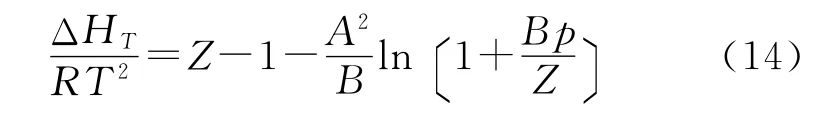
式中:Z为压缩因子,可由SRK 状态方程求得;A=a0.5/RT,B=b/RT,a、b含义同方程(2)。
用式(13)、(14)计算了LP1845 的蒸发潜热及摩尔相变热随温度的变化关系曲线,如图4所示。

4 LP1845蒸发潜热及摩尔相变热随温度的变化曲线Fig.4 Curves of evaporation latent heat and molar transformation heat of LP1845versus temperature
由图4可知,随着温度的升高,蒸发潜热逐渐降低。当温度接近LP1845 的临界温度824.3K 时,蒸发潜热趋近于零。摩尔相变热为压力和温度的二元函数,在一定的压力下,随着温度的升高,摩尔相变热减小。温度一定时,压力越大,摩尔相变热越小。在研究的压力范围内,当温度接近LP1845的临界温度824.3K 时,摩尔相变热趋于零。
3 输运性质的估算
3.1 黏 度
采用Murad半经验关系式[5]确定HAN 基液体发射药的黏度,其公式可表示为:
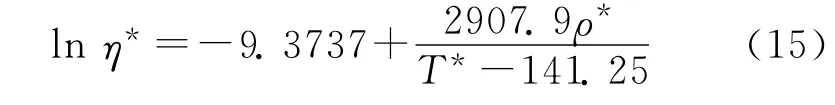
式中:η*=ηα/(Mβ)3,η为动力学黏度,Pa·s;T*=T/β;ρ*依照式(3)计算。对于LP1845:α=1.8141,β=1.1684。
根据式(15)计算了温度为300K 时LP1845的动力黏度随压力的变化情况,如图5所示。

图5 LP1845液体黏度随压力的变化曲线(T=300K)Fig.5 Liquid viscosity curves of LP1845versus pressure(T=300K)
由图5可见,T=300K 时,在0.1~70MPa,随着压力的升高,液体黏度基本呈线性增大,拟合公式为:
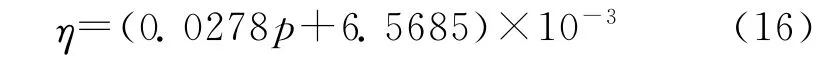
3.2 导热系数
在标准大气压下,液体物质的导热系数可以根据Latini方法[7]来计算。而HAN 基液体发射药LP1845作为一种液体燃料,也可以采用此法来计算其在大气压下的导热系数。Latini方法可表述为:
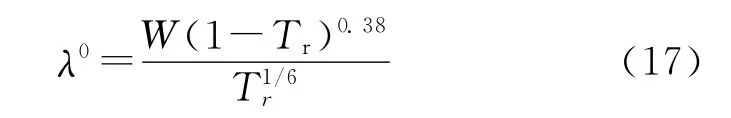
式中:λ0为低压导热系数,W·m-1·K-1。
W针对不同种类化合物有不同的表达式。对于HAN 基液体发射药,通过查表[7]可得:

在高压下,液体物质的导热系数与大气压下导热系数之间的关系可以通过Missenard关系式[7]求得。本研究采用此法对液体发射药LP1845导热系数进行修正。Missenard关系式的表达形式为:
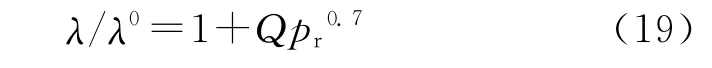
式中:

用式(19)、(20)计算了LP1845 液体药导热系数随温度和压力的变化曲线,如图6所示。由图6(a)可见,在压力相同的条件下,随着温度的升高,导热系数减小。当温度从300K 上升到LP1845的临界温度时,导热系数减小到原来的10%左右。从图6(a)中还可以看出,压力对LP1845导热系数的影响较小。由图6(b)可见,在温度为300K 时,压力从0.1MPa增加到70MPa时,液体导热系数只相对增加了1.12%。
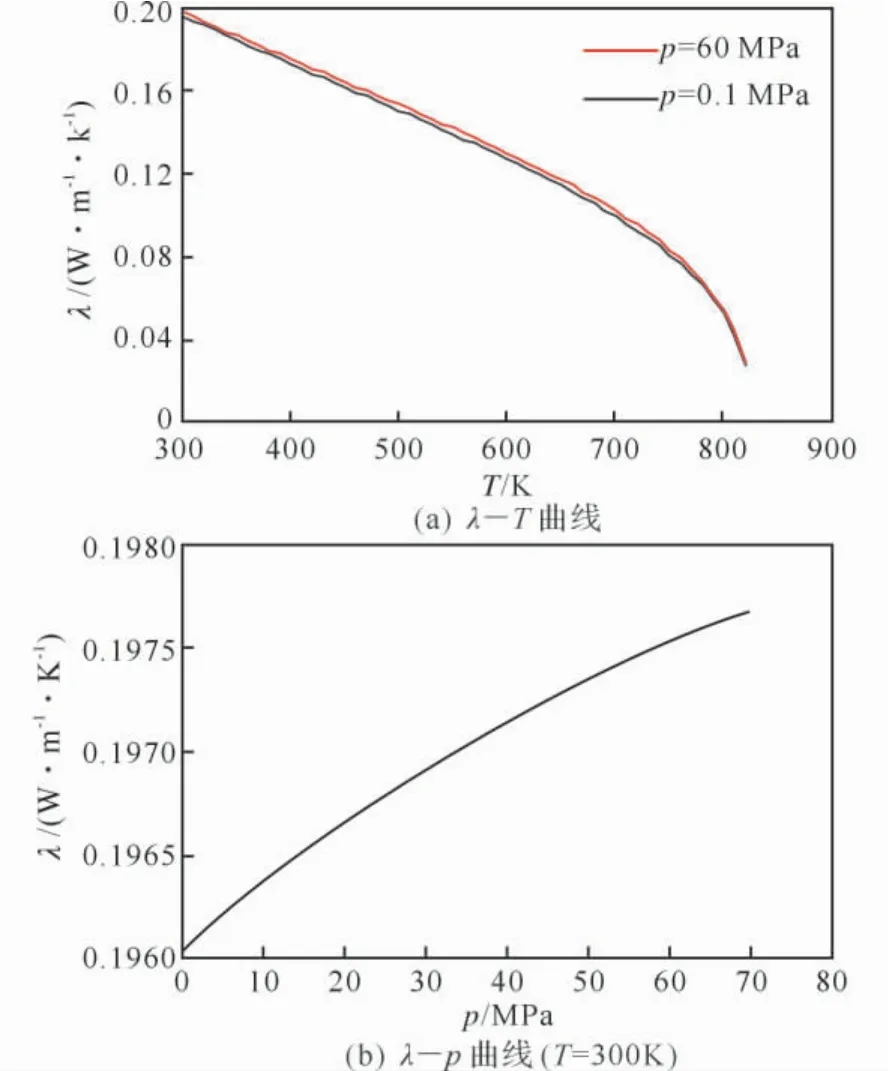
图6 LP1845液体导热系数随温度和压力的变化曲线Fig.6 Liquid thermal conductivity curves of LP1845 versus temperature and pressure
3.3 扩散系数
标准大气压下气体二元扩散系数的估算方法很多,Fuller等的方法[12]产生的平均误差最小,应用广泛且已被证明相当可靠,其形式为:
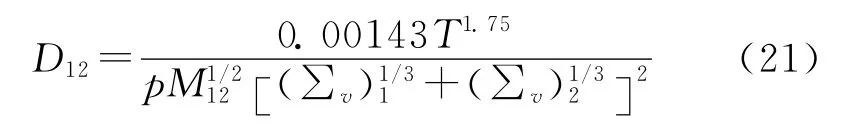
式中:D12为扩散系数,cm2/s;M12=2(1/M1+1/M2)-1;∑v为分子扩散体积,由原子扩散体积相加得到,常见的原子扩散体积及简单分子扩散体积见文献[12]。
为了研究压力对扩散系数的影响,Takahashi[13]提出对比态方法,其关联式为:
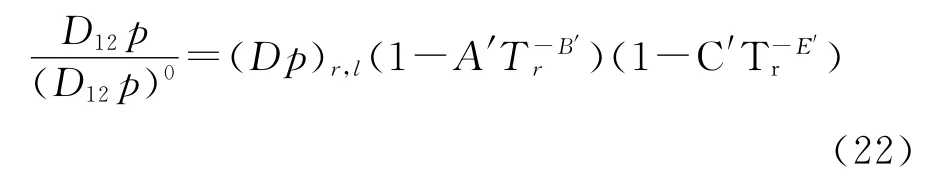
式中:(D12p)0表示大气压下的扩散系数与压力的乘积;(Dp)r,l、A′、B′、C′、E′随pr的变化而取不同的值。此高压修正式的适用范围是:0<pr<5,0.9<Tr<5。式(22)中的对比压力pr和对比温度Tr由Kay混合规则确定,即:
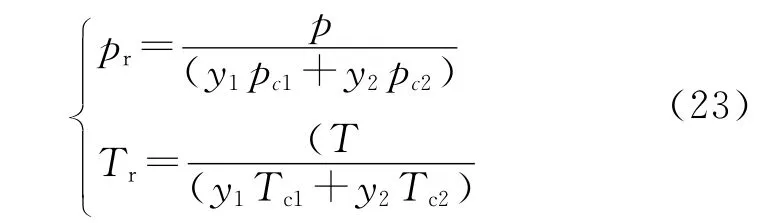
式中:y为摩尔分数;下标1、2分别代表两种相互扩散的气体,文中指燃料蒸气和氮气。
气相混合物(10%的LP1845燃料蒸气和90%的N2组成)在不同的温度和压力下扩散系数的变化曲线见图7。
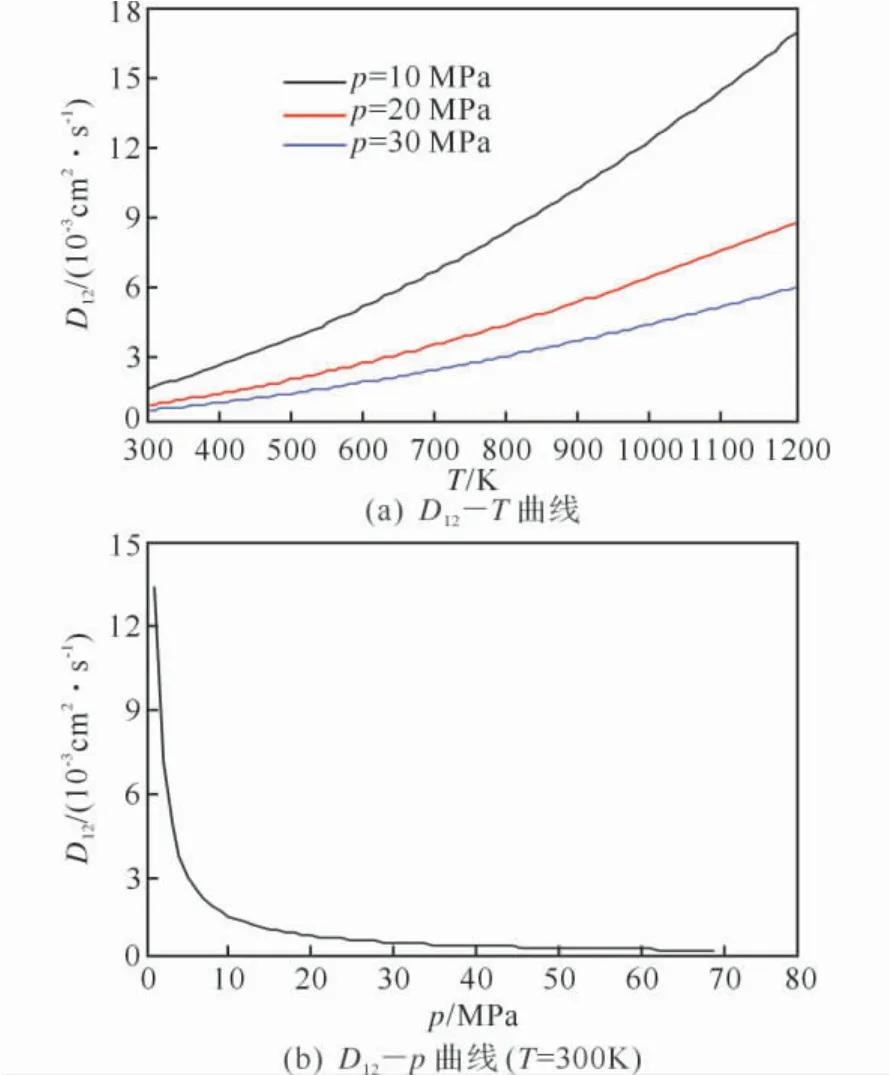
图7 LP1845-N2 气相混合物的扩散系数与温度和压力之间的关系曲线Fig.7 Diffusivity curves of LP1845-N2gas mixture versus temperature and pressure
由图7(a)可知,在压力保持不变时,气体混合物的扩散系数随着温度的增加而增大。因为温度越高,分子间运动越剧烈,有利于扩散过程的进行。从图7(b)可以看出,在0.1~10MPa下,扩散系数随着压力的增大迅速减小;10~70MPa下,随着压力的增大,扩散系数只是略有减小。
4 结 论
(1)利用通用理论或经验公式,计算出HAN 基液体发射药LP1845 的高压热物理性质参数,为HAN 基液体发射药高压燃烧推进理论计算提供了部分基础数据。
(2)根据合适的经验公式估算出HAN 基液体发射药LP1845 和LP1846 的临界压力分别为68.1、91.2MPa,临界温度分别为824.3、811.8K。
[1]庄逢辰,陈新华.燃料液滴高压蒸发理论[J].工程热物理学报,1982,3(3):276-283.
ZHUANG Feng-chen,CHEN Xin-hua.Theoretical investigation of fuel droplet vaporization at high pressures[J].Journal of Engineering Thermophysics,1982,3(3):276-283.
[2]Hsieh K C,Shuen J S,Yang V.Droplet vaporization in high-pressure environments I:near critical conditions[J].Combustion Science and Technology,1991,76(1):111-132.
[3]李玉琦.二甲醚、生物柴油及其混合燃料物性估算和缸内工作过程模拟研究[D].北京:北京交通大学,2008.
LI Yu-qi.Properties estimation and in-cylinder working process simulation of DME,biodiesel and the blend[D].Beijing:Beijing Jiaotong University,2008.
[4]Klein N.Liquid propellants for use in guns-a review,ADA153051[R].Springfield:NTIS,1985.
[5]Decker M M,Klein N,Freedman E,et al.HANbased liquid gun propellants:physical properties,ADA195246[R].Springfield:NTIS,1987.
[6]张续柱,肖忠良.液体发射药[M].北京:中国科学技术出版社,1993.
[7]Poling B E,Prausnitz J M,O'connell J P.The properties of gases and liquids[M].5th ed.New York:McGraw-Hill Book Company,2001.
[8]Kounalakis M E,Faeth G M.Combustion of HANbased liquid monopropellants near the thermodynamic critical point[J].Combustion and Flame,1988,74(2):179-192.
[9]童景山,李敬.流体的热物理性质[M].北京:中国石化出版社,1996.
[10]Lee B I,Kesler M G.A generalized thermodynamic correlation based on three-parameter corresponding states[J].AIChE Journal,1975,21(3):510-527.
[11]童景山,高光华,刘欲品.化工热力学[M].北京:清华大学出版社,1995.
[12]Fuller E N,Ensley K,Giddings J C.Diffusion of halogenated hydrocarbons in helium.the effect of structure on collision cross sections[J].The Journal of Physical Chemistry,1969,73(11):3679-3685.
[13]Takahashi S.Preparation of a generalized chart for the diffusion coefficients of gases at high pressures[J].Journal of Chemical Engineering of Japan,1974,7(6):417-420.

