粒细胞集落刺激因子治疗糖尿病足感染的系统评价
喻朝宁,何继东,刘莉
(1.四川省邛崃市医疗中心医院内二科,四川邛崃611500;2.四川省雅安市第二人民医院内分泌科,四川雅安625000)
粒细胞集落刺激因子治疗糖尿病足感染的系统评价
喻朝宁1,何继东2,刘莉2
(1.四川省邛崃市医疗中心医院内二科,四川邛崃611500;2.四川省雅安市第二人民医院内分泌科,四川雅安625000)
目的系统评价粒细胞集落刺激因子(Granulocyte Colony-Stimulating Factors,G-CSF)治疗糖尿病足感染(diabetic foot infections,DFI)的有效性和安全性。方法制定严格纳入和排除标准进行文献检索,计算机检索Cochrane图书馆临床对照试验数据库(2011年第4期)、Medline、PubMed(1978~2011年)、Embase(1978~2011年)、OVID数据库(1978~2011年)、中国生物医学文献数据库(CBMDisc)(1978~2011年)、维普中文期刊数据库(1989~2011年)、中国期刊全文数据库(1979~2011年)、万方学位论文数据库(1978~2011年),并手工检索相关会议论文集及查阅检索到的所有文献的参考文献,收集G-CSF治疗DFI的随机对照试验。按照国际Cochrane协作网推荐的方法进行系统评价。结果共纳入8个试验包括197例患者。Meta分析结果显示:①DFI截肢率:G-CSF治疗优于安慰剂/空白组(P=0.004);②Wanger分级下降情况:GCSF治疗优于安慰剂/空白组(P=0.001);③抗生素使用时间和住院时间:G-CSF与安慰剂/空白组比较,差异均无统计学意义(P=0.61,P=0.07);④副作用及并发症发生率:G-CSF治疗组无明显治疗相关副作用及并发症的发生,与安慰剂/空白组比较,差异均无统计学意义(P>0.05)。结论目前的证据表明:G-CSF辅助治疗DFI可减少截肢率,且有较好安全性。但仍需大量循证医学证据的进一步积累,从而指导临床实践。
粒细胞集落刺激因子;糖尿病;足感染;系统评价;Meta分析
糖尿病患者常常伴有神经病变、血管病变以及中性粒细胞功能减退,故尤其容易引起足部感染。糖尿病足感染(diabetic foot infections,DFI)是最常见的糖尿病慢性并发症之一,流行病学资料显示,25%的糖尿病患者合并糖尿病足,其中35%~50%最终需截肢[1]。在美国,所有非创伤性截肢患者中,50%患者的截肢原因是DFI控制不佳。DFI可增加住院的频率、时间,以及下肢截肢的风险[2~4]。我国资料显示[5],全国14家三甲医院糖尿病足患者人均住院费用14 906元,平均住院日是26天,呈逐年上升趋势,且合并感染及缺血的足病患者住院天数及住院费用均明显增加。目前,尽管多种方法用于DFI的治疗,但是如何选择更好的方法治疗DFI仍然是临床的一大难题。
粒细胞集落刺激因子(Granulocyte Colony-Stimulating Factors,G-CSF)是一种多胎链的细胞生长因子,可特异性调节粒系细胞的增殖与分化,并能增强成熟粒细胞的趋化性,吞噬作用及杀菌能力;还作为伤口愈合的启动子,参与加速伤口愈合所必需的一系列机制如参与血管生成,而血管生成的介质是源于炎症细胞的血管内皮生长因子、促进单核细胞和巨噬细胞在局部征募和增生,进而增加局部调节愈合过程的细胞因子,如白介素-1、肿瘤坏死因子、巨噬细胞集落刺激因子的产生,促进溃疡愈合,同时对机体应激防御系统有重要意义[6,7]。研究显示,在糖尿病及DFI患者,G-CSF尤其能增强粒细胞功能[8]。目前国内外关于G-CSF辅助治疗DFI的临床研究已有报道,但研究结论并不一致,且大部分研究的样本量较小,不能提供足够的检验效能。本研究采用国际Cochrane协作网推荐的方法对G-CSF治疗DFI的有效性和安全性进行系统评价,以期为临床实践提供循证医学的最佳证据,并为今后的进一步临床研究指出方向和思路。
1 资料与方法
1.1 纳入标准
1.1.1 研究类型不分文种,凡是有关G-CSF治疗DFI的临床随机对照试验(RCT)的全文及摘要均予纳入。
1.1.2 研究对象纳入标准为临床试验纳入患者的条件,即年龄≥18岁;患有DFI。排除有以下情况之一的患者:①癌性溃疡或溃疡恶变。②未经治疗的骨髓炎。③难以控制的高血糖(糖化血红蛋白HbA1c>12%)。④正在接受皮质激素、免疫抑制剂及化疗治疗者。⑤正在接受或过去1个月内接受过生长因子、高压氧、热疗及真空辅助闭合技术疗法治疗。⑥糖尿病酮症酸中毒及糖尿病高渗综合征。⑦严重心肺疾病。⑧怀孕或哺乳者。
1.1.3 干预措施G-CSF治疗开始的时间、疗程不限。对照组可采用空白或其他治疗方法。试验组和对照组可同时接受相同剂量、疗程的其他治疗。
1.1.4 疗效评价指标①主要指标:DFI缓解时间、DFI截肢率、副作用及并发症发生率;②次要指标:Wanger分级下降情况、抗生素使用时间、住院时间。
1.2 文献检索计算机检索Cochrane图书馆临床对照试验、Medline、Embase、OVID数据库、CBMDisc、VIP、CNKI数据库。手工检索美国糖尿病学会会议论文集;查阅检索到所有文献的参考文献索引,手工检索相关文献。
1.3 方法学质量评价和资料提取由两位研究者独立进行文献质量评价并按设计好的表格提取资料。方法学质量评价采用Cochrane协作网推荐的方法进行,质量评价包括以下内容:①随机分配方法;②分配方案的隐藏;③盲法;④是否描述了失访、退出的发生情况;⑤是否进行了意向性分析(Intention to treat,ITT)[9]。
1.4 统计分析采用Cochrane协作网提供的Revman 4.2.软件进行Meta分析。各试验结果的异质性检验采用卡方检验,若无统计学异质性(P>0.10),Meta分析选择固定效应模型,否则在解释异质性可能的原因后选择随机效应模型。若有足够试验可进行敏感性分析。计数资料计算OR值及其95%CI。对于计量资料,当各临床试验对同一疗效指标采用相同的测量工具进行测量时,计算加权均数差值(weighted mean difference,WMD)及其95%可信区间,否则计算标化均数差值(standardized mean difference,SMD)及其95%可信区间。各个疗效判定指标的分析均采用ITT分析。当纳入足够多研究时,则进行漏斗图分析观察是否存在发表偏倚。若各临床试验提供的数据不能进行Meta分析,则只对其进行描述性的定性分析。
2 结果
2.1 纳入试验的特点及方法学质量最初检索到相关文献76篇,其中计算机检索73篇,手工检出3篇。阅读题目及摘要后,排除综述类文章及信件,筛选得到治疗性临床试验类文章16篇,其中可能符合纳入标准的文章10篇。仔细查阅全文后,2篇试验由于研究目的不同被排除,最终纳入8个试验[10~17],包括197例患者。其中5个试验为国外研究[10~14],样本量最大包括40例患者[10,11],最小的仅为10例[15~17]。8个试验均有明确的纳入及排除标准。4个试验采用盲法[10,11,13,14],8个试验均明确指出两组基线情况具有可比性。8个试验均报告了退出失访的情况,所有试验均未对疗效指标采用ITT分析[10~17],详见表1。
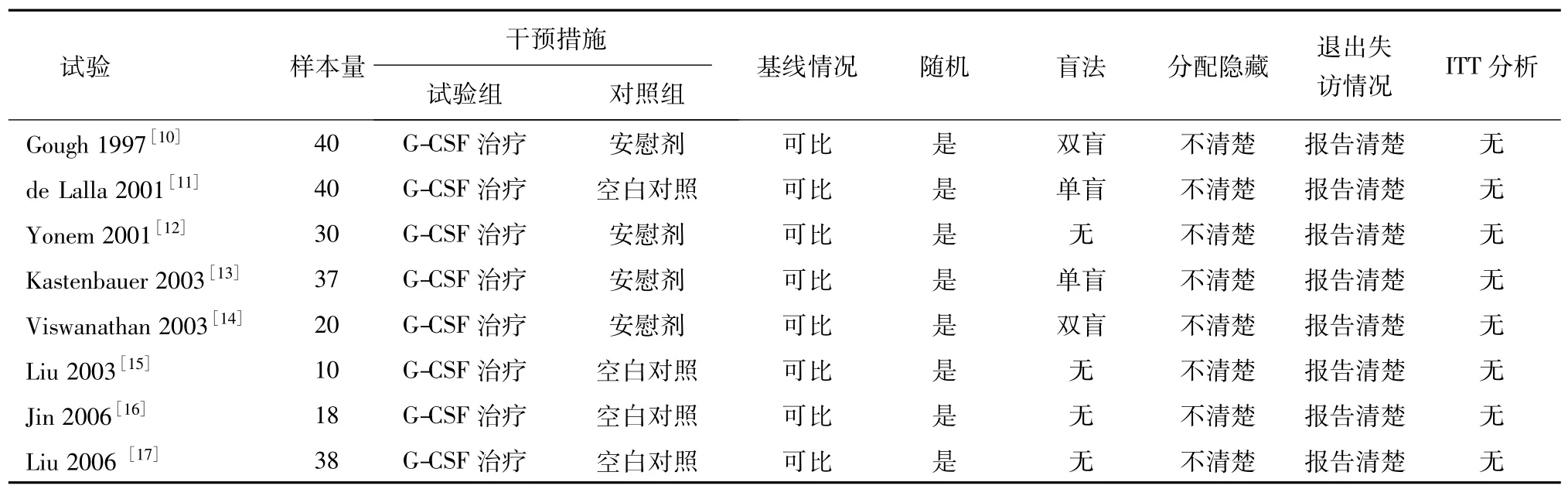
表1 纳入试验的质量评估及研究特点
2.2 Meta分析结果
2.2.1 DFI缓解时间有2个试验[10,12](包括70例患者)提供了DFI缓解率的资料。Yonem等纳入30例患者的RCT结果显示,G-CSF组与对照组比较,感染缓解时间分别为(23.6±1.8)天和(22.3±1.7)天,差异有统计学意义(P<0.05);Gough等纳入40例患者的RCT结果显示,G-CSF组与安慰剂组比较,蜂窝组织炎缓解时间分别为5~20天和5~93天(平均12天),差异有统计学意义(P=0.03)。
2.2.2 DFI截肢率有5个试验[10~14](包括167例患者)提供了DFI截肢率的资料。其中2个试验[10,14]采用双盲,2个采用单盲[11,13]。5个试验均报告失访退出的情况。Meta分析结果显示试验间无异质性(P=0.68,I=0%),故采用固定效应模型。DFI治疗组DFI截肢率为7%,对照组为24.39%,两组间差异有统计学意义[OR:0.26,95%CI(0.10~0.65);P=0.004],见图1。漏斗图分析提示无发表偏倚(图2)。
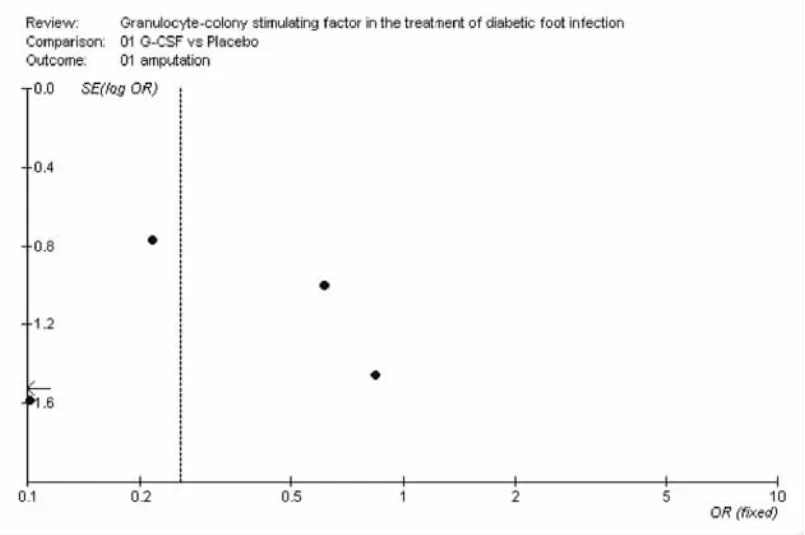
图2 漏斗图
2.2.3 Wanger分级下降情况有3个试验[15~17](包括30例患者)提供了Wanger分级下降情况的资料。其中3个试验均未采用盲法,3个试验均报告失访退出的情况。Meta分析结果显示试验间无异质性(P=0.80,I=0%),故采用固定效应模型。DFI治疗组Wanger分级下降为100%,对照组为46.67%,两组间差异有统计学意义[OR:12.29,95%CI(1.81~83.36);P=0.001],见图3。
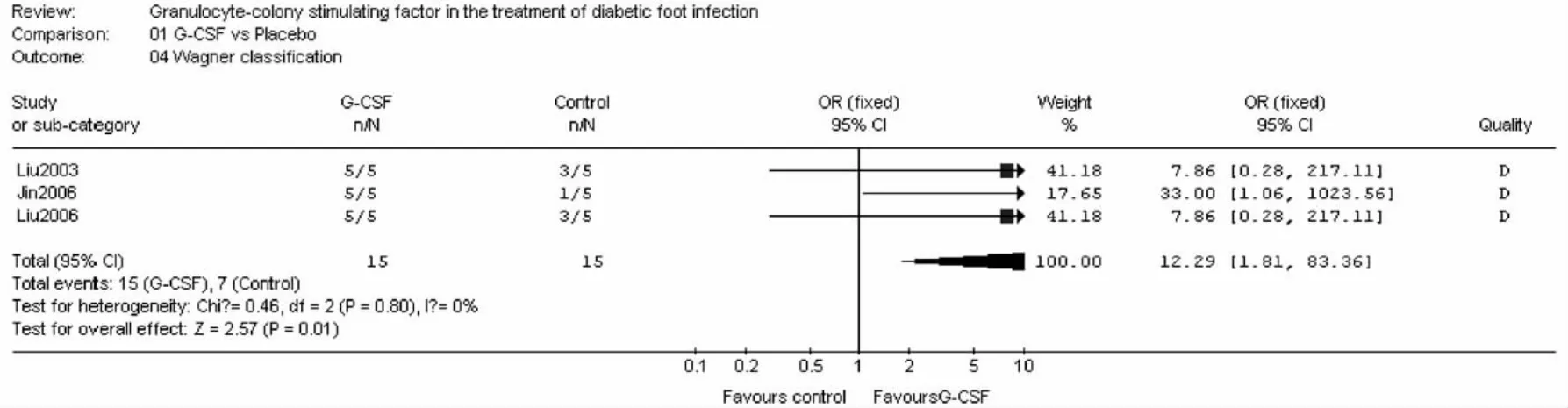
图3 DFI治疗VS对照组治疗对Wanger分级下降情况影响的Meta分析
2.2.3 抗生素使用时间有4个试验[10~13](包括147例患者)提供了抗生素使用时间的资料。其中1个试验采用双盲[10],2个采用单盲[11,13],4个试验均报告失访退出的情况。Meta分析结果显示各试验间无异质性(P=0.45,I=0%),故采用固定效应模型。DFI治疗组抗生素使用时间与对照组间差异无统计学意义[WMD:-0.27,95%CI(-1.30~0.77);P=0.61],见图4。

图4 DFI治疗VS对照组治疗对抗生素使用时间影响的Meta分析
2.2.4 住院时间有3个试验[10,12,14](包括90例患者)提供了住院时间的资料。其中2个试验采用双盲[10,12],3个试验均报告失访退出的情况。Meta分析结果显示各试验间有异质性(P<0.00001,I=0%),故采用随机效应模型。DFI治疗组住院时间与对照组差异无统计学意义[WMD:-3.14,95%CI(-7.10~0.27);P=0.07],见图5。
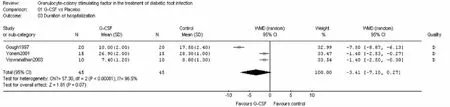
图5 DFI治疗VS对照组治疗对住院时间情况影响的Meta分析
2.2.5 副作用及并发症发生率纳入各试验均无严重治疗相关副作用及并发症发生。
3 讨论
糖尿病足的严重感染会造成截肢,在糖尿病足的各项处理中,首要的是解决好感染的问题,它是创面修复、血管重建等其他治疗的基础。目前DFI的治疗方法主要包括外科手术、抗感染以及新近出现的高压氧治疗(HBOT)、真空负压封闭(VAC)、GCSF治疗等,在DFI的治疗中显示了一定的疗效。
G-CSF可通过增加白细胞内超氧化物的产生而增强白细胞作用,并介导中性粒细胞超氧阴离子的产生及抗体依赖的细胞杀伤性作用[18]。国内外有报道局部表面应用G-CSF,能促进糖尿病脂质渐进性坏死伴反复下肢溃疡者溃疡愈合并减少溃疡复发[19~21]。几个RCT研究亦显示G-CSF辅助治疗DFI取得较好的疗效,但样本量均较小,我们采用循证医学的方法,以期为G-CSF辅助治疗DFI的临床实践提供循证医学的证据。
本系统评价中,2个试验结果显示,G-CSF辅助治疗可以缩短DFI缓解时间,由于纳入患者及疗效指标不一致,无法进行Meta分析,仅作描述性评价,且纳入2个试验样本量均较小,结果解释应谨慎。纳入的5个试验的Meta分析结果显示,G-CSF治疗在截肢率上优于安慰剂/空白对照。纳入5个研究中,2个采用单盲,2个试验采用双盲。漏斗图提示无发表偏倚。但纳入研究最大样本量仅40例患者,且各研究纳入标准仍存在差异,需谨慎对待结果。纳入3个随机对照试验的Meta分析结果显示,GCSF治疗减少Wanger分级,纳入3个试验均未采用盲法,且样本量小。说明结果仍存在一定的局限性。纳入4个试验的Meta分析结果显示,G-CSF治疗在抗生素使用时间上与安慰剂/空白对照差异无统计学意义。1个试验采用双盲,2个报告采用单盲,但2个试验纳入研究样本量较小,结果应谨慎对待。3个试验的Meta分析结果显示,G-CSF治疗在住院时间上与安慰剂/空白对照差异无统计学意义,其中2个试验采用盲法,但纳入研究样本量均较小,需谨慎对待结果,有待大样本RCT及系统评价的证据。纳入各试验均无严重治疗相关副作用及并发症的报道,说明G-CSF治疗具有较好的安全性。
总之,因所发表的临床研究方法学质量良莠不齐,存在多种方法学局限性,故应谨慎看待以上结果。目前仅能对G-CSF治疗DFI的有效性及安全性做出推论。今后有必要进行高质量、大样本的设计严格的RCT予以证实。今后开展的临床研究应充分考虑到现有研究的局限性,特别是在设计方案上要尽量改进研究的方法学缺陷,尽量减少偏倚,必要时结合经济学评价,以为临床应用提供更多的证据。
[1]Jude EB,Oyibo SO,Chalmer N,et al.Peripheral arterial disease in diabetic and nondiabetic patients:A comparison of severiry outcome[J].Diabetes Care,2001,24(8):1433-1437.
[2]Pinzur MS,Slovenkai MP,Trepman E,et al.Guidelines for diabetic foot care:recommendations endorsed by the Diabetes Committee of the American Orthopaedic Foot and Ankle Society[J].Foot Ankle Int,2005,26(1):113-119.
[3]Lipsky BA.A report from the international consensus on diagnosing and treating the infected diabetic foot[J].Diabetes Metab Res Rev,2004,20(Supp11):68-77.
[4]Lavery LA,Armstrong DG,Wunderlich RP,et al.Risk factors for foot infections in individuals with diabetes[J].Diabetes Care,2006,29(6):1288-1293.
[5]王爱红,赵浞,李强,等.糖尿病足患者医疗费用分析[J].中华内科杂志,2007,46(6):471-474.
[6]Cianfarani F,Tommasi R,Failla CM,et al.Granulocyte/macrophage colony-stimulating factor treatment of human chronic ulcers promotes angiogenesis associated with de novo vascular endothelial growth factor transcription in the ulcer bed[J].Br J Dermatol,2006,154(1):34-41.
[7]Stagno F,Guglielmo P,Consoli U,et al.Successful heal ing of hydroxyurea-related leg ulcers with topical granulocyte-macrophage colony-stimulating factor[J].Blood,1999,94(4):1479-1480.
[8]Sato N,Kashima K,Tanaka Y,et al.Effect of granulocyte-colony stimulating factor on generation of oxygen-derived free radicals and myeloperoxidase activity in neutrophils from poorly controlled NIDDM patients[J].Diabetes,1997,46:133-137.
[9]Higgins JPT,Green S.Cochrane Handbook for Systematic Reviews of Interventions 4.2.4[S].The Cochrane Library,2005.
[10]Gough A,Clapperton M,Rolando N,et al.Randomised placebo-controlled trial of granulocyte-colony stimulating factor in diabetic foot infection[J].Lancet,1997,350:855-859.
[11]de Lalla F,Pellizzer G,Strazzabosco M,et al.Randomized prospective controlled trial of recombinant granulocyte colony-stimulating factor as adjunctive therapy for limb-threatening diabetic foot infection[J].Antimicrob Agents Chemother,2001,45:1094-1098.
[12]Yonem A,Cakir B,Guler S,et al.Effects of granulocyte-colony stimulating factor in the treatment of diabetic foot infection[J].Diabetes Obes Metab,2001,3:332-337.
[13]Kastenbauer T,Hornlein B,Sokol G,et al.Evaluation of granulocytecolony stimulating factor(filgrastim)in infected diabetic foot ulcers[J].Diabetologia,2003,46:27-30.
[14]Viswanathan V,Mahesh U,Jayaraman M,et al.Beneficial role of granulocyte colony stimulating factor in foot infection in diabetic patients[J].J Assoc Physicians India,2003,51:90-91,
[15]刘媛,冒咏震,姚春莉.粒细胞集落刺激因子治疗糖尿病足感染的初步探讨[J].辽宁实用糖尿病杂志,2003,11(3):33-34.
[16]金进,关秀军.粒细胞集落刺激因子治疗糖尿病足临床观察[J].中国医师杂志,2006:299-300.
[17]刘媛,冒咏震,姚春莉.粒细胞集落刺激因子治疗糖尿病足感染的初步探讨[J].中国现代实用医学杂志,2006,12(5):49-50.
[18]常宝成,潘从清,曾淑范.糖尿病足的诊断和治疗[J].国外医学内分泌学分册,2002,22(1):27.
[19]王维萍,袁南兵,王椿,等.一例糖尿病性类脂质渐进性坏死左小腿皮肤溃疡患者的循证治疗[J].中国循证医学杂志,2007,7(11):830-835.
[20]Remes K,Rönnemaa T.Heal ing of chronic leg ulcers in diabetic necrobiosis lipoidica with local granulocyte-macrophage colony stimulating factor treatment[J].J Diabetes Complications,1999,13(2):115-118.
[21]Evans AV,Atherton DJ.Recalcitrant ulcers in necrobiosis lipoidica diabeticorum healed by topical granulocyte-macrophage colonystimulating factor[J].Br J Dermatol,2002,147(5):1023-1025.
A systematic review of granulocyte-colony stimulating factor in the treatment of diabetic footinfection
YU Chao-lin1,HE Ji-dong2,LIU Li2(1.The second Department of Internal Medicine,Qionglai City Medical Center Hospital,Qionglai 611500,China;2.Department of Endocrinology,The Second People's Hospital of Yaan,Yaan,625000,China)
ObjectiveTo review the effectiveness and safety of Granulocyte-Colony Stimulating Factor(G-CSF)therapy in the management of Diabetic Foot Infections(DFI).MethodsWe collected all randomized controlled trials of G-CSF for DFI by searching Cochrane Central Register of Controlled Trails(CENTRAL,vol 4,2011),MEDLINE or PUBMED(1978~2011),EMBASE(1978~2011),OVID Database(1978~2011),Chinese Biological Medicine database(CBMDisc)(1978~2011),CNKI(1978~2011),Chinese VIP Database(1989~2011)and WANFANG database(1978~2011),and hand searching the bibliographies of retrieved articles and correlated proceedings as well.Then,a systematic review was conducted using the method recommended by The Cochrane Collaboration.ResultsEight trials involving 197 patients were included in the systematic review.Meta analysis showed that G-CSF therapy was superior to placebo in diabetic foot amputation rate and Wanger Classification reduction(P=0.004 and 0.001,respectively).However,there were no differences between G-CSF therapy and placebo in duration of antibiotic use,duration in hospital,rates of sideeffect and complications(P=0.61,0.07 and>0.05,respectively).ConclusionsThe current evidence suggested that G-CSF therapy may be safe and effective in the reduction of amputation rate for patients with DFI.
Granulocyte-Colony Stimulating Factor Therapy;Diabetes mellitu;Diabetic foot infections;Systematic review;Meta-analysis
R587.29;R392.114
A
1672-6170(2012)05-0210-05
2012-03-14;
2012-07-17)

