国内外超级细菌的研究进展及防控措施
郑 璇 郑育洪
(广东出入境检验检疫局,广州 510623)
超级细菌(superbugs)是一类细菌的统称,这一类细菌的共性是对大部分抗生素都有强大的耐药性。就是能对抗生素有强大的抵抗作用,能逃避被杀灭的危险。目前引起特别关注的超级细菌主要有:耐甲氧西林(甲氧苯青霉素)金黄色葡萄球菌(MRSA)、万古霉素肠球菌(VRE)、耐多药肺炎链球菌(MDRSP)、多重耐药性结核杆菌(MDR-TB)、最近新发现的携带有NDM-1基因的大肠杆菌和肺炎克雷伯氏菌以及多重耐药鲍曼不动杆菌(MRAB)等等。超级细菌并非新事物,它们一直存在并且随着人类滥用抗生素而进化出强大耐药性。由于大部分抗生素对其不起作用,超级细菌对人类健康已造成极大的危害。其中,MRSA已成为全球发生率最高的医院内感染病原菌之一,MRSA感染被列为世界3大最难解决的感染性疾病首位,而携带有NDM-1基因的大肠杆菌和肺炎克雷伯氏菌的出现更是给人类社会造成了极大的恐慌。超级细菌可以在人类、动物和环境中转移,目前的动物滥用抗生素状况与人感染耐药菌联系紧密,特别是具有耐药性的人畜共患病原细菌,食源性动物感染之后,会经过食物链或皮肤接触传染给人,长期食用含耐药性细菌或抗生素残留的肉类会增加人体内细菌的耐药性。现就超级细菌的基本情况,耐药机制及相关的研究进展,食源性动物的抗生素使用与超级细菌的联系,各国的应对措施等进行综述,并对我国食源性动物的超级细菌防控工作提出有针对性的意见和建议。
1 超级细菌基本情况
1.1 发现史
20世纪60年代,产生了耐甲氧西林的金黄色葡萄球菌(MRSA),MRSA取代链球菌成为医院感染的主要菌种。耐青霉素的肺炎链球菌同时出现。20世纪90年代,发现可耐万古霉素的肠球菌、耐链霉素的“食肉链球菌”。
进入21世纪,发现泛耐药绿脓杆菌对氨苄西林、阿莫西林、西力欣等8种抗生素的耐药性达100%;以及发现碳青霉烯酶肺炎克雷伯菌对西力欣、复达欣等16种高档抗生素的耐药性高达52%~100%。
现了携带有NDM-1基因的大肠杆菌和肺炎克雷伯氏菌,对除替加环素和多黏菌素之外的所有抗生素都产生耐药性。2010年,发现了多重耐药鲍曼不动杆菌(MRAB)。
随着更强效的新型抗生素的研发和应用,更强大的超级细菌也不断产生。
1.2 耐甲氧西林金黄色葡萄球菌
超级细菌中最著名的是耐甲氧西林金黄葡萄球菌(Methicillin-Resistant Staphylococcus Aureus,MRSA)。MRSA现在极其常见,可引起皮肤、肺部、血液和关节的感染。MRSA的耐药性发展非常迅速,在1959年西方科学家用一种半合成青霉素(即甲氧西林)杀死耐药的金黄色葡萄球菌之后,196年在英国就首次发现了耐甲氧西林金黄色葡萄球菌,并以惊人的速度在世界范围内蔓延,而到了上世纪80年代后期,MRSA已经成为全球发生率最高的医院内感染病原菌之一(也被列为世界3大最难解决的感染性疾病首位)。MRSA在许多国家发生日益严重,1974年葡萄球菌感染病例中只有2%感染的是MRSA,而到了2003年,这一数字达到了64%。在2003~2004年间,在英格兰和威尔士由MRSA造成的死亡病例上升了22%。仅2005年,英国就有3 800人死于MRSA。在美国,在2006年共有19 000例感染MRSA的死亡病例和105 000感染致病病例。2007年,美国《美国医学会杂志》周刊刊登1份政府调查报告说,每年预计有超过9万人严重感染MRSA。荷兰国家公共卫生及环境研究所指出,全球可能有多达5300万人带有致命的超级病菌MRSA(该研究结果发表在英国医学杂志《柳叶刀》上)。
图1 MRSA病毒
MRSA包括医院获得(hospital-acquired,HA)感染的HA.MRSA和社区获得(community-acquired,CA)感染的CA.MRSA 2大类型。近50年来,HA.MRSA在全世界流行。20世纪90年代,出现了以潘顿-瓦伦丁杀白细胞素(Panton-Valentine leukocidin,PVL)为特征的强毒力的CA.MRSA。CA.MRSA多引起坏死性肺炎和严重的皮肤感染,已发现的主要有5个克隆谱系[1]:STl,ST30,ST80,ST59,ST8(即usA300),其地理分布特点和所携带SCCmee(葡萄球菌染色体mecA)型与传统的HA.MRSA不同。由于2者都能通过mecA基因对所有的β-内酰胺类抗生素均耐药[2],但前者不断地获得更强大的耐药性,还对β-内酰胺类抗生素以外的多种抗生素耐药,甚至万古霉素;后者目前仅发现对β-内酰胺类抗生素耐药。两者均具有强致病性,可引起死亡。MRSA以其高致病性和多重耐药性成为人类健康的巨大威胁[3]。
1.3 耐万古霉素肠球菌
1987年在英国首次发现耐万古霉素肠球菌(vancomycin resistant enterococus,VRE),随后纽约发现北美第1例VRE感染,此后VRE感染迅速波及世界各地。肠球菌属感染作为一种引起医院感染的主要致病菌已经引起医学界的广泛关注,美国全国医院感染监测与控制系统将其列为医院感染的第2大病原菌。近年来由于抗生素的广泛使用,使原本就对部分抗菌药物具有内在耐药性的肠球菌耐药性进一步扩大,特别是VRE危害性逐年增加,已成为临床治疗棘手的问题。VRE感染以60岁以上患者居多,感染性疾病治疗时间越长,越容易发生VRE感染,可以发生在社区,也可以发生于医院,医院感染较社区感染高。VRE感染多发生于癌症、肝硬化、慢性肾炎尿毒症、脑梗死等重症住院患者,主要造成肺部、腹腔感染。其次,为血液、手术伤口、泌尿道感染。值得注意的是,一部分病例在感染VRE前就出现了耐药葡萄球菌生长。专家由此推测,有可能是葡萄球菌把其耐药质粒基因传播给肠球菌,从而产生VRE。另一方面,VRE又成为更新的“超级细菌”——耐万古霉素金葡菌(VRSA)的“中介”。VRE致死率最高达到73%。
1.4 携带有NDM-1基因的大肠杆菌和肺炎克雷伯氏菌
NDM-1(New Delhi metallo-β-lactamase 1,新德里金属β内酰胺酶-1)不同于上述2种“超级细菌”,它实际上是“超级细菌”携带的一种耐药性基因。NDM-1能够进入大多数细菌的DNA线粒体中,从而使细菌产生呈现相似症状的广泛耐药性。只要细菌体内拥有这个基因并通过它指导合成相应的酶,就可以对除替加环素和多黏菌素之外的所有抗生素都产生耐药性,其中有些“超级细菌”甚至对现在所有抗生素都有耐药性。更可怕的是,NDM-1基因并不只存在于细菌的染色体上,还可以存在于一种名叫质粒的独立于染色体外的遗传物质中。质粒不但能垂直地遗传给子代,也具有在不同种类细菌细胞间转移的能力,这种基因结构可以在同种甚至异种细菌之间“轻松”复制。目前,研究人员多在大肠杆菌和肺炎克雷伯氏菌等耐碳青霉烯革兰阴性肠杆菌科细菌内发现NDM-1基因,也就是说目前携带有NDM-1基因的大肠杆菌和肺炎克雷伯氏菌才是真正意义上的“超级细菌”。

图2 日本新潟大学教授山本达男日前通过电子显微镜拍摄到的NDM-1“超级”大肠杆菌照片
携带NDM-1耐药基因超级细菌的复制能力很强,传播速度快且容易出现基因突变,在现在滥用抗生素的情况下,是非常危险的一种超级细菌。2009年,英国卡迪夫大学、英国健康保护署和印度马德拉斯大学的医学研究机构在一些曾去印度接受过外科手术的病人身上发现NDM-1大肠杆菌,根据研究者发表在医学专业杂志《柳叶刀》上的文章指出,被携带NDM-1的大肠杆菌感染,会导致许多病人出现尿路感染和血液中毒。截至2010年11月,NDM-1耐药基因超级细菌感染病例在4大洲、超过20个国家发生,其中,2010年10月26日,中国疾病控制中心通报了中国大陆有3例感染NDM-1耐药基因超级细菌的病例。据不完全统计,日本、巴西、英国已分别因它致死27人、18人、5人。
由于含这种基因的新型超级细菌对几乎所有抗生素具有免疫力,就连“杀伤性较强的”碳青霉烯类抗生素也对这类细菌束手无策,而且传播力强并能跨种类转移耐药性。欧洲临床微生物和感染疾病学会声称,预计至少10年内没有抗生素可以“消灭”含NDM-1基因的细菌。
1.5 多重耐药鲍曼不动杆菌
日本2010年发现另外一种超级细菌。这种细菌被命名为“多重耐药鲍曼不动杆菌”(MRAB),东京帝京大学附属医院2010年9月11日通报,自去年起,这家医院共有58名住院患者感染耐药性不动杆菌,其中32人死亡,死亡率高达55%。
目前,超级细菌已引起国际社会的广泛重视,法国将所有曾在国外住院的病人进行超级细菌的检测;中国卫生部要求对超级细菌检测呈阳性的结果必须在12 h内报告;世卫组织将抗击耐药性细菌作为2011年世界卫生日的主题。
2 超级细菌耐药机制及研究进展
2.1 耐药性分类
2.1.1 固有耐药性(intrinsic resistance) 又称为天然耐药性或内源性耐药性,它是指自然界中细菌的某些属种、株或1个株内的个别细菌对某些抗生素天然不敏感,具有细菌的遗传特征,一般不会改变,主要由染色体基因介导的耐药,它决定抗菌药物的抗菌谱。如肠道阴性杆菌对青霉素,绿脓杆菌对氨苄西林,链球菌对庆大霉素等类型的耐药性。
2.1.2 获得性耐药(acquired resistance) 是指细菌在接触抗生素后,改变代谢途径,使自身获得不被抗菌药物杀灭的抵抗力。这种耐药菌可通过耐药基因的传代、转移、传播、扩散、变异形成高度和多重耐药。细菌除通过基因突变获得耐药性外,还可通过携带可转移遗传因子包括质粒、转座子和噬菌体等使耐药性扩散传播。这些基因元件自身携带一种或多种抗性基因,通过基因水平转移(HGT)的方式在沙门氏菌种内或细菌种间传播,导致细菌耐药谱不断增宽,耐药性增强。如MRSA对甲氧西林等抗生素的耐药性。
2.2 耐药性机制分类
2.2.1 细菌产生灭活酶或钝化酶,破坏抗生素的结构,使其失去活性 目前,细菌产生的灭活酶或钝化酶主要是β-内酰胺酶、氨基糖苷类抗菌药物钝化酶、氯霉素乙酰转移酶、MLS(大环内酯类-林克霉素类-链球菌素类)类抗菌药物钝化酶。
2.2.2 改变抗生素作用的靶位蛋白结构和数量,使细菌对抗生素不再敏感 如万古霉素和革兰氏阳性菌的细胞壁肽聚糖前体五肽中的D-丙氨酸-D-丙氨酸末端(D-ala-D-ala)结合,抑制细菌细胞壁蛋白合成。但因为临床上万古霉素的大量使用及其在使用中的不合理现象,导致了耐万古霉素肠球菌(VRE)的出现。VRE可通过DNA获得质粒或转座子以及突变株的发生,而产生耐药性。
2.2.3 细菌细胞膜渗透性改变,使抗生素不能进入菌体内部细菌细胞膜是一种具有高度选择性的渗透性屏障,某些细菌由于膜孔蛋白较少或蛋白通道较小,使某些抗菌药物不能进入菌体内部,属原有性耐药。如铜绿假单胞菌的细胞外膜上没有大多数革兰氏阴性细菌所具有的典型的高渗透性孔蛋白,它的孔蛋白通道对小分子物质的渗透速度仅为典型孔蛋白通道的1/100。
2.2.4 细菌主动药物外排泵作用,将抗生素排出菌体 细菌主动药物转运系统根据其超分子结构、机理和顺序的同源性等可以将其分为4类:(1)主要易化(MF)家族;(2)耐药小节分裂(RND)家族,它也包括转运钙离子、钴离子和镍离子的转运器;(3)链霉素耐药或葡萄球菌多重耐药家族,它假定由4种转膜螺旋组成的小转运器;(4)ABC(ATP-bindingcassette,ATP结合盒)转运器,它由2个转膜蛋白和2个ATP结合亚基或结构域组成。前3类主动泵出系统运行所需能量由氢离子药物反转运体逆转H+,形成H+浓度差而产生的势能所提供,而第4类利用ATP水解所释放的自由能排出细胞内有毒物质。实际上是因为细菌的生理结构影响,抗生素只是因为具有某一种特殊结构而成为外排泵作用的对象并诱导外排泵的表达[4]。
2.2.5 细菌生物被膜的形成,降低抗生素作用 细菌生物被膜是指细菌粘附于固体或有机腔道表面,形成微菌落,并分泌细胞外多糖蛋白复合物将自身包裹其中而形成的膜状物[5]。常见的形成细菌生物被膜的临床致病菌有铜绿假单胞菌、表皮葡萄球菌、大肠埃希菌等。细菌形成生物被膜后,往往对抗菌药物产生耐药性。其原因有:(1)细菌生物被膜可减少抗菌药物渗透。(2)吸附抗菌药物钝化酶,促进抗菌药物水解。(3)细菌生物被膜下细菌代谢低下,对抗菌药物不敏感。(4)生物被膜的存在阻止了机体对细菌的免疫力,产生免疫逃逸现象,减弱机体免疫力与抗菌药物的协同杀菌作用。在细菌引发的感染中,直接与机体免疫系统接触的生物被膜成分主要是胞外基质和由细菌释放出来的各种抗原性物质,由于它们的强抗原性,刺激机体产生大量特异性抗体[6]。但是,生物被膜包裹在细菌外起到物理屏障作用,使免疫系统因难以接触到细菌本体而发挥不了作用。而大量的抗体与相应的可溶性抗原形成免疫复合物沉积在感染病灶周围,吸引较多的中性粒细胞浸润。中性粒细胞释放的蛋白水解酶因不能够穿透生物被膜而对细菌损伤不大,而使宿主组织遭到严重破坏[7]。这是形成生物被膜的细菌引发耐药性的免疫机制,同时,也是临床上久治不愈的慢性感染的重要原因。
部分已知抗生素对应的主要耐药性发生机理详见表1。

表1 部分已知抗生素对应耐药性机理示例简表
2.3 抗生素压力与耐药性
耐药机制的产生是细菌长期进化的结果,是部分细菌为获取生存优势的手段,说明与抗生素接触(抗生素压力)是细菌产生获得性耐药性的主要源动力。
1985年,著名学者McGowan指出了与医院内细菌耐药性的出现相关的7个方面:(1)引起医院感染的微生物的耐药性比引起社会感染的微生物的耐药性更多见;(2)医院中耐药菌株感染者使用的抗菌药物比敏感株感染或定植者使用的抗菌药物多;(3)抗菌药物使用情况的变化会引起细菌耐药情况的变化,如投入或停用某种抗菌药物常与其耐药性的消长有关;(4)抗菌药物使用愈多的区域耐药菌分布愈多;(5)抗菌药物应用时间越长耐药菌定植的可能性越大;(6)抗菌药物剂量越大耐药菌定植或感染的机会更多;(7)抗菌药物对自身菌群有影响并有利于耐药菌生长。
1998年,Stuart BLevy在《新英格兰医学杂志》上发表题为《多重耐药——一个时代的标志》的文章,认为(1)抗菌药物只要使用了足够时间,就会出现细菌耐药性,如使用青霉素25年后出现耐青霉素肺炎球菌、氟喹诺酮使用10年后出现了肠杆菌耐药;(2)耐药性是不断进化的,随着抗菌药物的应用,耐药也从低度耐药向中度、高度耐药转化;(3)对一种抗菌药物耐药的微生物可能对其他抗菌药物也耐药;(4)细菌耐药性的消亡很慢;(5)使用抗菌药物治疗后,患者容易携带耐药菌。
可见,细菌耐药属于一种自然现象,然而,抗生素的使用加速了细菌耐药性的产生,使细菌在生长繁殖过程中更容易产生耐药性基因的突变。抗生素在细菌耐药的过程中间起到诱导和选择的作用,抗生素用得少一点的时候对细菌诱导和选择的能力就差,用得越多,让整个环境中抗体存在大量残余,细菌就会接触,自然就会产生耐药的能力。
最新的抗生素压力与耐药性机制的研究中,Henry H.Lee等人利用暴露于浓度不断增大的氟喹诺酮抗菌药“诺氟沙星”的一个大肠杆菌连续培养物所做实验表明,少数自然出现的抗药变体能保护其种群的绝大部分。这些具有高度耐药性的分离菌种产生信号作用分子“吲哚”,它能激发易感皮肤中的药物外排泵和其他保护机制。这种利他行为使较弱的成分能够存活,并有机会进行有益的突变[8]。
2.4 超级细菌耐药机制和传播途径的研究进展
2.4.1 形成超级细菌的环境影响因素 国立爱尔兰大学研究人员发现,消毒剂还会“训练”细菌,使其对抗生素药物也产生耐药性,从而形成“超级病菌”。他们在实验过程中向绿脓杆菌的培养液中添加消毒剂,并且不断增加消毒剂的用量。结果发现,这种细菌会努力适应消毒剂并存活下去。而当他们把对消毒剂产生抵抗力的绿脓杆菌置于临床常用抗生素“环丙沙星”环境中时,绿脓杆菌竟然有了耐药性。也就是说,在之前未接触过抗生素的情况下,绿脓杆菌在消毒剂的“训练”下就可以产生耐药性。研究人员认为,细菌本身可以不断适应有消毒剂的环境,变得能更有效地把细菌细胞内的抗菌物质排出。这时细菌的遗传物质DNA(脱氧核糖核酸)已经发生了一定改变,使其对某种抗生素产生特定耐药性。研究结果对于研究如何更加有效地控制医院内细菌感染非常重要,而且也有助于进一步理解细菌产生耐药性的环境影响因素[9]。
2.4.2 控制超级细菌致病能力的化合物 加拿大麦克马斯特大学的研究人员发现,以MRSA为代表的超级病菌内部存在着控制其致病能力的“中央处理器”。所谓的“中央处理器”,其实是一种小化合物。研究人员发现,这种化合物由MRSA以其耐药性的形式产生,由它决定了这种病菌的传染强度和传染能力。主持该项研究工作的内森·马加维副教授表示,他们发现在MRSA里的这些小化合物停止发挥作用时,MRSA就会丧失功能并失去传染性。

图3 绿脓杆菌
麦克马斯特大学研究人员使用了先进的化学探测手段,在细菌内部分辨出这些科学家称之为“细菌小分子中央处理器”的小化合物,从而发现了与其形成有关的分子间联系。其后,为分析该化合物的功能,科学家关闭了它的合成。关闭其合成的结果显示,这种致命的细菌得到制服,丧失了攻击红血球的能力[10]。
2.4.3 超级细菌MRSA产生致命蛋白攻击人体免疫系统 美国国立过敏和传染病研究所(NIAID)的微生物学家Michael Otto和同事发现,MRSA可以产生一类酚可溶性蛋白(PSMs),这赋予了它们强大的威力。Otto的小组在实验室中培育出了一些PSM分子,并且将其应用于人类嗜中性粒细胞(neutrophil,一种人类免疫细胞,人体抵御葡萄球菌的第1道防线)。结果发现,数分钟后,这些免疫细胞开始变平,1 h后,许多免疫细胞都遭到破坏。研究人员还对医院和社区获得性MRSA菌系进行了对比研究。尽管后者比前者抵抗的药物种类略少,但却更加强大,往往在数天内就能致人于死地。研究结果表明,几种社区获得性MRSA菌系能够制造更多的PSM,而大多数的医院菌系并不制造该蛋白。研究人员认为,这可能就是社区获得性MRSA威力更加强大的原因,进一步的研究证实了这一观点。当研究人员移除与编码PSM相关的基因后,社区获得性MRSA对小鼠的威胁程度降低,同时在小鼠皮肤上留下的脓肿块也较少。Otto的小组正致力于创造PSM抗血清,并在小鼠身上进行试验[11]。
2.4.4 超级细菌MRSA的传播途径 英国研究人员利用新一代基因检测技术,对细菌基因组进行完整的分析,绘制出超级细菌MRSA在各大洲间的传播路线图,并根据基因变异情况得出各地细菌间的家族谱系图。Simon Harris等人应用一种新的方法来绘制许多不同MRSA菌株基因组中的各个点。在这些点的DNA序列的差别仅仅为几个“字母”,甚或只是一个字母的差异。科研人员用这种方法来检验属于“ST239”世系的63株MRSA,它们具有对抗生素的抵抗力,并占了全世界与医疗有关的MRSA感染中的大部分。这些样本中大约有2/3来自1982~2003年间在全世界采集到的样本,从而为人们提供了一个有关全球ST239种群的独立观察;有1/3的样本来自在一个为期7个月的时间段内的泰国某一医院的患者。通过分析样本间的遗传变异量,科研人员组建了一个“系谱图”,该系谱图显示了ST239克隆是如何扩散到世界的不同区域的,以及他们在不同国家通过进一步的演化而产生出成簇的在遗传学上相似的菌株。
研究人员发现,1997年葡萄牙暴发的耐甲氧西林金黄色葡萄球菌疫情是从巴西传播过来的。研究人员还分析了泰国一家医院里耐甲氧西林金黄色葡萄球菌的传染情况,结果显示,通过基因检测得出的不同患者体内细菌间的关系,与这些患者所处病房的位置有关,说明这种方法同样适用于分析人际间的细菌传播路线。这一方法可以帮助卫生部门了解细菌在人与人之间、医院与医院之间、国家与国家之间的传播特点,有助于查明在控制感染的策略中有关预防传播的方面究竟有哪些不足之处,以制定有效的防疫措施[12]。
3 食源性动物与超级细菌
3.1 抗生素滥用导致超级细菌大量出现
细菌在接触抗生素之前,就已存在具有耐药性的突变株。而抗生素的滥用,导致对细菌产生巨大的选择压力(selective pressure),实际上是对细菌进行了一次强制选择,在绝大多数普通细菌被杀死后,消灭了竞争性细菌,原先只占极小比例、具有耐药性的“超级细菌”(10-6~10-9,自发突变频率)存留下来开始大量繁衍,并占据主导地位,使得抗生素使用剂量越来越大,失效的抗生素也越来越多。
凡超时、超量、不对症使用或未严格规范使用抗生素,都属于抗生素滥用。抗生素的滥用主要有2个来源:(1)在人类疾病治疗过程中滥用抗生素;(2)动物饲料添加抗生素的问题。2010年引起全球轰动的超级细菌NDM-1在大多数国家都是输入性的。但在印度、巴基斯坦还有中国,它是内源性的,也就是说,这些国家本土有滋生超级细菌NDM-1的土壤,而这几个国家正好是抗生素滥用大国。
在上世纪50~60年代,全世界每年死于感染性疾病的人数约700万,而现在这个数字上升到了2 000万。死于败血症的人数上升了89%,大部分人死于超级细菌带来的用药困难。特别是在中国,世界卫生组织WHO调查显示,目前我国已经成为世界上滥用抗生素最为严重的国家之一。住院患者的抗生素使用率高达80%,外科手术则高达95%,而世界卫生组织推荐的抗生素院内使用率为30%,欧美发达国家的使用率仅为22%~25%。中国使用量、销售量列前15位的药品,有10种是抗生素,每年有数万人直接或间接死于滥用抗生素。卫生部部长陈竺2010年8月20日曾表示,NDM-1的出现,实际上是由于不恰当、过度地使用抗生素所产生的细菌耐药性。
而抗生素的使用在全世界的养殖业都是较为普遍的,在动物疾病防治、提高饲料利用率、促进畜禽生长等方面发挥了重要作用。但随着抗生素的不科学地滥用,特别是在饲料中添加亚治疗剂量的抗生素,导致动物细菌对抗生素产生耐药性,并通过食物链将耐药性转移给危害人类。1970年美国FDA进行了动物饲料中抗生素使用的调查,认为使用亚治疗剂量的抗生素易引起耐药性细菌的形成,并首次证实动物多种耐药性细菌的产生与抗生素的使用有关。用作饲料添加剂的抗生素,虽然经过慎重选择,而且使用剂量远远低于临床治疗用量,但饲用抗生素的长期使用特别是滥用可能是导致多重耐药菌甚至超级细菌增加的主要原因。食源性动物细菌耐药性问题日益突出,也作为一个重要的公共卫生和食品安全问题应引起世界各国政府及业内人士的高度重视。
3.2 食源性动物的抗生素使用史
抗生素在食源性动物的应用已经有60多年的历史,1935年人工合成抗生素磺胺和1940年应用于医学临床的青霉素,到20世纪40年代中期已在兽医临床开始使用,1946年Moore等已报道磺胺、链霉素添加于饲料中有促生长作用。至50年代初,在欧、美等发达国家,青霉素、磺胺、链霉素、金霉素等已作为促生长添加剂用于牛、猪和鸡的饲料。以后随着许多新抗生素的出现,除了兽医临床使用抗生素防治畜禽疾病外,还大量使用抗生素作为饲料添加剂,以预防动物生病,提高动物生产性能,改善饲料转化效率,获取更高经济收益等作用。抗生素使养殖场能够限制牲畜的饲养空间和活动,同时保持动物处于最佳健康状态。如果没有抗生素,集约化畜牧系统可能不会成为利润丰厚的生产模式。
3.3 国外食源性动物抗生素滥用与超级细菌的发生
长期以来,全球兽用抗生素用量远远超过了动物治疗疾病的需要量,国家细菌耐药性监测中心副主任马越研究员曾指出:滥用抗生素的现象远比人们想象的要严重,全球每年消耗的抗生素大多数被用在食用动物身上,且其中90%都只是为了提高饲料转化率而作为饲料添加剂来使用。20世纪60年代,西方国家曾将生产抗生素的废渣用作饲料喂猪,可使猪或其他动物长得更快。后来,又将抗生素发酵残渣都用作家禽、家畜的饲料添加剂。表2是美国2009年度食源性动物中获批的抗菌药种类及销售情况统计。在美国,大约70%的抗生素被用作鸡、猪和牛饲料添加剂。这种做法使食源性动物和动物源性食品中发生超级细菌和抗生素残留的几率就大大增加了。
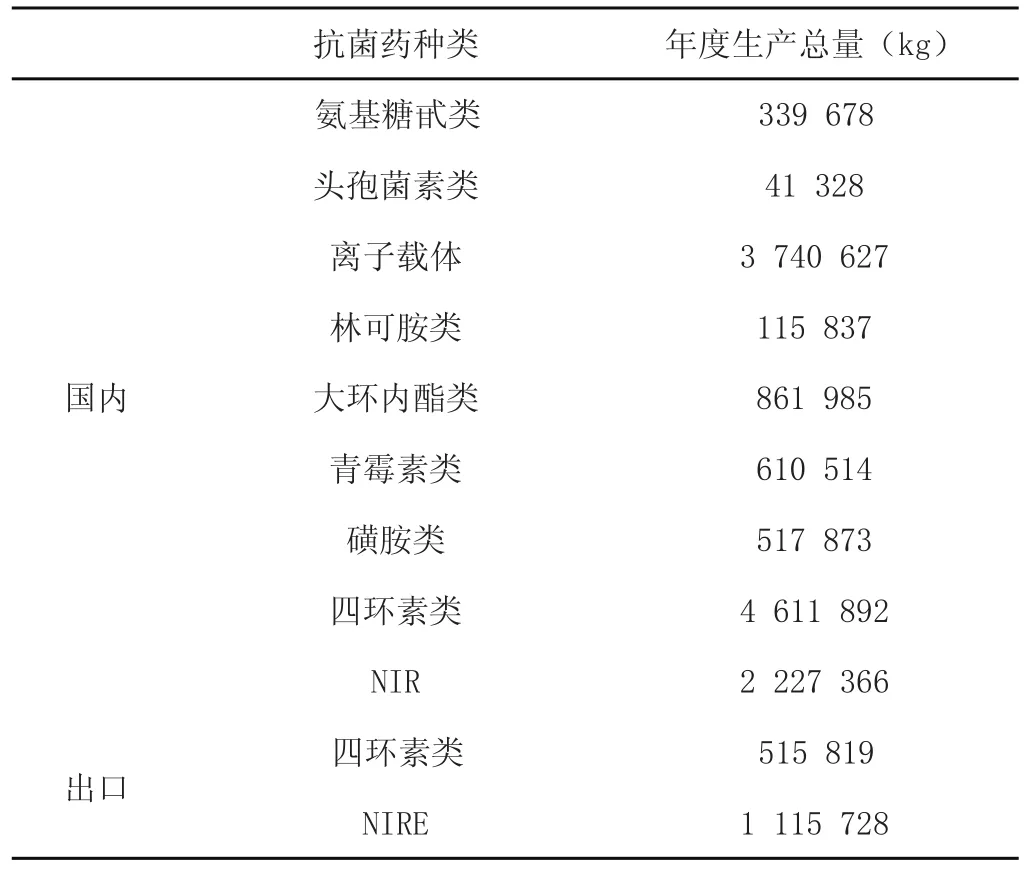
表2 美国食源性动物中批准使用的抗菌药物2009年销售数据表
由于抗生素的长期使用,2006年荷兰在9个屠宰场进行的有关MRSA检测发现,有39%的生猪呈阳性。官方进一步检测发现,有20%的猪肉、21%的鸡肉和3%的牛肉携带了这种病菌。而荷兰是畜产品出口大国,每年向邻国出口的生猪就多达600万头。更令人忧虑的是,由于食源性动物是MRSA的宿主,大大增加人感染MRSA的风险,在荷兰几乎有一半的养猪农户携带了这种新型MRSA,是荷兰全部人口携菌率的1 500倍。如在一个主要的养猪地区,80%患者的感染源都是农场中携带病菌的牲畜。此外,尽管MRSA ST398是2003年才在荷兰第1次发现,但到2007年,40%的以及50%的荷兰猪场都携带ST398,且正在进一步蔓延。在荷兰医院里每3例MRSA病例中就有1例是由该菌株引起的。
2008年德国官方宣布在莱茵河北威斯特伐利亚州,40家猪场中有28家发现畜养猪只感染MRSA,70%的猪体内都发现了这种病菌,这些猪原本都是健康的。据推测,猪农才是真正的携带者,因为据信这种病原是先从人传给猪,然后才在猪群当中传播开来。
2009年,欧洲食品安全局(EFSA)、欧洲疾病控制中心(ECDC)和欧洲药品管理局(EMEA)关于家畜、宠物和食品当中的抗甲氧西林金黄色葡萄球菌(MRSA)发表了一篇联合科研报告。应欧洲委员会的要求,EFSA的生物危险专业委员会和ECDC研究并得出结论,食用家畜,包括猪、小肥牛和肉仔鸡常常携带CC398菌株的MRSA而不表现症状。所以,食品可能遭MRSA污染,与携带CC398菌株MRSA动物接触的人可能会面临感染的风险。报告得出结论,由于动物互相之间以及动物与人类之间的接触活动有可能是MRSA传播的重要途径,因此在畜场水平实施控制措施是最有效的。近年来发现动物当中的MRSA与人类MRSA感染有关。在发现食用动物当中存在MRSA的欧盟地区内,与这些动物接触的人,例如农场主、兽医及其家人,都面临着遭受MRSA感染的风险。鉴于有些MRSA感染的严重性,ECDC支持采取措施确保食用动物抗生素使用的谨慎。
2009年,欧盟食品安全机构(EFSA)公布了欧盟全境种猪群首次MRSA普查的结果。结果显示,在欧盟一些成员国的种猪设施里,MRSA普遍存在。这次普查在24个成员国当中进行,17个成员国的种猪设施当中发现了某种类型的MRSA,7个成员国未发现任何MRSA。整体来看,欧盟平均每4家种猪场当中就有一个有MRSA,但普查结果还显示,不同成员国之间情况差异很大。欧盟种猪设施中见报最多的MRSA类型是MRSA ST398。MRSA ST398这个类型,在有些家畜身上已经分离到,对农场工作人员、兽医及其家属构成了职业性的健康风险,因为这些人有可能通过直接接触动物而感染上这种病原。
2007年,加拿大研究人员在Ontario的猪和农场主身上发现2个MRSA细菌变种,这是第一次关于MRSA报道是在北美的动物上。科学家很快强调加拿大猪肉仍然很安全,因为一般蒸煮很快会杀死细菌。但是从发现结果来看猪场应该是MRSA的感染源。
英国首席医疗官,Sir Liam Donaldson 说:“动物上形成的耐药性细菌可能威胁人类健康。抗生素在农业体系中必须适度使用且只在对动物福利必要时方可使用。”
3.4 中国食源性动物抗生素滥用情况
化学工业学会和制药工业学会2005年统计数据显示,我国每年抗生素原料生产量约为21万t,其中有9.7万t(占年总产量的46.1%)用于畜牧养殖业。抗生素的滥用在全世界的养殖业都是非常普遍的,但在中国显得更为严重。(1)加大抗生素使用剂量和长期使用现象普遍存在;(2)使用禁用抗生素现象时而发生,虽然2000年以来国家陆续公布了一些在畜禽生产中禁用的药物,但在兽药监督检查或养殖场中时而能够看到,其使用依然禁而不止;(3)人药兽用现象依然存在,虽然《兽药管理条例》明令禁止人药兽用。但由于兽药抗生素的品种较少,或人们担心兽药的质量,使用人药情况时有发生;(4)兽用原料药直接使用情况屡禁不止,近年来,在兽医临床上或自配饲料直接使用兽药原粉(即原料药)的现象比较普遍;(5)不按规定休药期使用。
由于国内对食源性动物MRSA等超级细菌的监测机制不健全,无法获得相关数据。
3.5 食源性动物超级细菌与食品安全
鉴于全球每年消耗的抗生素大多数被用于食源性动物等养殖业,耐药性微生物不可避免地产生,尤其是人畜共患病的耐药性病原菌株种类多、增长快;耐药基因又可随细菌繁殖垂直传代;也可通过携带可转移遗传因子包括质粒、转座子和噬菌体等使耐药性扩散传播,特别是超级细菌更可通过接触、环境、饲料、肥料和食品等环节在动物、微生物和人之间传播。进入食物链和流通环节的超级细菌,将使消费者承担更大的食品安全和生命健康风险。
例如美国伊利诺伊大学的科学家发现,土壤和农田地下水中的细菌从来自猪的肠道菌那里获得了耐受四环素的耐药基因。耐药基因长期存在于土壤和水生细菌中,而且可能传播到那些毒性很强的细菌从而形成超级细菌。如果人饮用这样的水,就会被超级细菌感染。而人类消费排泄的富含抗生素残留的废物如果污染环境和食物链,自然环境中的细菌接触到各种各样的大量抗生素,由此产生了耐药性,细菌耐药性扩散的链条由此形成。
因为抗生素的滥用,食源性动物很可能是一个蓄积耐药细菌,并向人体传递耐药细菌的储蓄库。我们吃的动物源性食品可能含有抗生素残留和耐药菌,而且能把人体变成了一个培养超级细菌的小环境。一旦发生细菌感染,即使从来没有使用过抗生素药物的人,同样可能面临抗生素治疗束手无策的局面。中国、美国、英国和德国也相继出现“耐药宝宝”,这些被称为“耐药宝宝”的婴儿对7种抗生素都有耐药性,婴儿耐药性是因母亲吃抗生素残留肉禽时,摄入过量抗生素残留,继而传给胎儿,产生耐药菌。
4 预防超级细菌
4.1 国际组织
为加强对兽用抗生素耐药性的管理,各国际组织都成立了相应的耐药性特设工作组,召开相关会议和制定相关文件。
1999年5月OIE成立了抗生素耐药性特设工作组(0IE ad hoc group on antimicrobial resistance),并限定了其职权范围,包括控制并减少耐药性产生的方法(抗生素合理使用);对动物及公共卫生相关的危险性进行风险评估和管理;监测计划及实验室方法间的调和;改善对全世界抗生素耐药性知识的认识(数据收集)。
2006年7月食品法典委员会(codex alimentarius commission,CAC)第29届会议设立了政府间抗生素耐药性特设工作组,该工作组和食品卫生法典委员会、食品兽药残留法典委员会有交叉联系,旨在提供以科学为依据的指导,评估食品和饲料中存在的(通过食品及饲料传递的)耐药微生物及耐药基因给人体健康带来的危险性,并提供适当的危险管理咨询,从2007年起,在4年内完成该项工作。
兽药注册技术要求国际协调会(international cooperation on harmonization of technical requirements for the registration of veterinary medicinal,VICH)是一个由OIE帮助成立的协调兽用药品注册要求的三边(欧盟-美国-日本)机构。VICH下设9个专家工作组,其中包括抗生素耐药性专家工作组(antimicrobial resistance expert working groups),该工作组负责针对耐药性问题提出建议,制定国际公认的管理和技术标准。
各国际组织间还不断的进行交流和合作,尤其是WHO、OIE和FAO等涉及公共卫生和食品安全的重要组织,先后召开了多次国际联合专家咨询会来讨论非人类用抗生素耐药性的有关问题,并制定了一系列管理策略。1997年,在柏林召开的世界卫生组织会议倡议在动物饲料中谨慎使用抗生素,以减少病原菌抗药性的扩散。同年3月,国际粮农组织在巴黎召开会议,会议确定通过“风险分析、风险处理、慎用抗生素和抗药性检测”来控制饲料中使用抗生素对公众健康的威胁。会议提议成立欧洲细菌抗药性检测体系,以发现对抗生素具有抗药性的病原菌。耐药性问题是一个多因素问题,需要多方位和多机构联合采取措施加以解决。因此,WH0和FA0、0IE共同考虑关于非人类用抗生素耐药性问题,于2003年和2004年在瑞士日内瓦召开了关于“非人类用抗生素使用与耐药性”2次研讨会,专家普遍认为非人类用抗生素的使用导致动物性食品中耐药菌的产生,通过食源性途径和其他途径耐药菌株最终可以从动物转移到人。非人类用抗生素使用和耐药性相关风险应该作为人类安全评估的一部分;应考虑建立每种抗生素-动物-病原体耐药临界值;WHO负责制定“人医上极重要的抗生素目录”,OIE负责制定“兽医上重要的抗生素目录”等。
4.2 欧盟
1986年,瑞典成为首个在动物饲料中部分禁用AGP(抗生素生长促进剂)的国家。1991年,法国政府规定,进口的鸭、鹅产品必须具备无抗生素残留证明。1998年底,欧盟委员会颁布了杆菌肽锌、螺旋霉素、维吉尼亚霉素和泰乐菌素4种抗生素在畜禽饲料中作为生长促进剂使用的禁令,禁令自1999年7月1日起生效。这4种抗生素占动物抗生素市场总份额的80%。同时欧盟关于一些抗球虫药的使用许可在1999年到期后将不再延期。除了几种广泛使用的抗球虫药,允许在饲料中继续使用的抗生素促生长剂只有莫能霉素、盐霉素、黄霉素和卑霉素4种。欧盟认为,这4种药在当前的人药体系中不重要,不会导致人类致病菌产生抗药性。从2006年1月1日起,欧盟全面禁止食品动物使用抗生素促生长饲料添加剂,抗生素只能用于治疗目的。
在欧盟成员国中,在食源性动物抗生素使用管理方面走在最前列的是出口猪肉大国-丹麦。1998年4月,丹麦猪肉行业宣布35公斤以上生猪自愿停止使用一切抗生素饲料;同年,丹麦政府开始对使用抗生素的猪收税(每头猪2美元)。2000年,丹麦政府下令,所有动物,不论大小,一律禁用抗生素饲料。禁用当年,猪出现大量病患,动物医用抗生素使用量比1999年多了20多t。不过,另一数据更值得关注:动物抗生素(包含抗生素饲料和动物医用抗生素)的年使用量,从1995年的210 t,降至2000年的96 t。此后,丹麦养殖业者通过改善饲料、打造环境舒适的猪舍等措施,最终使动物医用抗生素的使用量也降低了。禁用抗生素饲料不仅让丹麦食用肉更安全,还让丹麦人感染耐药性肠球菌的数量不断减少。
从《英国抗生素应用以及若干人畜病原耐药性的概况:2007》获悉,从2004~2007年,英国平均每吨用于生产食品的屠宰动物活重所分摊的抗生素销售量从80g降低到60g。
4.3 美国
美国是世界最大的畜禽产品出口国之一,在制定抗生素促生长剂和治疗用药物的使用标准方面具有举足轻重的地位。美国所考虑的措施集中于使用风险评估策略来保护人类健康,同时承认饲用抗生素对改善人类健康,提供大量和廉价的肉蛋奶方面都是很重要的。但在超级细菌等耐药性病菌发展的情况下,美国生产商和动物药物管理部门与公众加强了抗生素促生长剂的安全性方面的沟通。美国对抗生素的安全性评估和耐药性监测很严格,如果发现耐药菌特别是超级细菌产生,便采取相应的措施,包括收回药物使用许可证。1996年由美国FDA、疾病控制和预防中心、农业部协作成立了国家抗生素耐药性检控体系。该机构已开始实施一系列研究项目,包括饲料中通过食物链传播的病原菌的检测新方法,以及这些病菌获得耐药性的机理。现在慎用抗生素原则与流行病学和微生物学检控一道构成了美国防止抗生素促生长剂引起耐药性的首要防线。2002年,美国政府也出台了针对养殖业促生长目的抗生素安全性评估的专门指导方针。
2008年兽药用户收费修正案(ADUFA)第105章修正了美国食品、药物与化妆品法案第512章,要求应用含有抗生素活性成分新兽药的申请商向美国食品药品监督管理局(FDA)递交年度报告,报告需要包括食源性动物用药中每种成分的用量及销售情况,还要包括产品经销商的信息。制定该项立法以帮助FDA分析人类和食源性动物用药的持续相互作用(包括耐药性)、功效和安全性。ADUFA第105章将FDA年度汇总报告的信息公开化。
4.4 发达国家
一些发达国家针对耐药性问题都采取了一系列措施,包括成立耐药性管理工作组、制定相关文件指南和召开相关会议、进行耐药性风险分析、建立耐药性监测系统、对抗生素进行分级、慎用抗生素等,但是各个国家又不尽相同。例如加拿大和澳大利亚管理上有很多相似点,都是首先由抗生素相关的委员会递交食品动物抗生素使用与耐药性产生的相关报告,然后联邦政府根据递交的报告进行考察商讨,发布回应文件,召开研讨会,最后提出建议和措施。
4.5 中国
2005年10月28日,中国农业部发布的“兽药地方标准废止目录”中禁止万古霉素、头孢哌酮、头孢噻肟等人用抗生素用于食品动物,原因是会产生耐药性问题,影响动物疫病控制、食品安全和人类健康(农业部公告第560号)。在2007年4月12日农业部发布的“关于淘汰兽药品种及兽药安全评价品种目录”中指出,对甲磺酸培氟沙星、盐酸洛美沙星、氧氟沙星进行安全评价,2010年前组织完成风险评估和安全评价工作,并根据评价结果公布淘汰品种(农业部公告第839号),防止兽用产生耐药性可能导致人类疾病治疗失败,这表明中国已经开始关注兽用抗生素耐药性问题[13]。但相比发达国家而言,我国还存在很大的差距:没有专门的工作组来进行耐药性的管理;虽然制定了《中华人民共和国兽药管理条例》、《饲料和饲料添加剂管理条例》、《兽药注册办法》,而且也涉及到耐药性问题,但对其并没有专门的规定和指南;没有完善的管理制度,抗生素滥用、误用很严重;也没有建立兽用抗生素耐药性监测系统和耐药性风险评估体系;没有对抗生素进行分级;教育和培训工作也做得不够到位。
5 未来展望
食源性动物的超级细菌防控问题是一个涉及全球的复杂问题,需要国际组织及各国的协调一致,需要国际社会共同努力,在防控现有超级细菌的同时,减少因滥用抗生素而产生新的超级细菌的可能。中国这方面才刚刚起步,相关部门应该积极学习欧盟等发达国家的先进做法,加大管理力度,各行各业相关人员都要积极参与进来,共同降低兽用抗生素耐药性的产生和蔓延,保护动物和人类健康和食品安全。
为此,建议采取以下措施:(1)农业部及有关部门应该成立专门的耐药性小组来负责解决耐药性相关问题;加强对兽用抗生素的全程管理,控制抗生素的生产和使用规模;(2)建立覆盖全国的大型食源性动物细菌耐药监测网络,定期发行耐药监测公报,做好抗生素耐药性监测和抗生素使用量监测及耐药性产生后的应对措施;(3)制定全面实施执业兽医制度与兽药处方制度,加强基层兽医培训,加强养殖户的教育和引导,改善饲养管理,增强动物的抗病力,搞好预防接种,减少抗生素的使用;(4)科学合理使用抗生素,在规定的使用对象、剂量、期限等范围内使用,遵守休药期,决不能高等级的人用抗生素兽用;(5)加强进口肉类和活食源性动物的检验检疫,防止外源性超级细菌入侵国内;(6)依法严惩滥用抗生素的养殖者和销售药物残留超标动物产品的违法行为;(7)加强研究中草药等抗生素替代药物。(8)加强国际上的交流和合作,参照国际上的标准和规定,根据中国的具体情况制定正确合理的措施予以实施。
[1]Binh An Diep and Michael Otto.The role of vinllelR3e determinants in conmmnity-associated MRSA pathogenesis[J].Trends in Microbiology,2008,z6(8),361.
[2]Jevons MP Celbenin.resistant staphylococci[J].Br Med J,1961,1:124.
[3]Hujo Grundmann,MartaAircs-de-Sousa,John Boyce,et a1.Emergence and resurgece of meticillin—resistsmt StaphylococcusⅫreus as a public-health threat[J].Lancet,2006,368:874.
[4]Ploy MC,Lambert T,Couty JP,et a1.Integroes:811 antibiotic resistance gene capture and expression system[J].Clin Chem Lab Med,2000,38(6):483-487.
[5]李明,蔡锦兰,张瑞苓.科学合理的使用抗生素[J].中华临床医学研究杂志,2006,12(5):633—634.
[6]宋志军,吴红,Michael Givskov.细菌生物膜与抗生素耐药[J].自然科学进展,2003,13(10):1015.
[7]Cannichacl G.ESBLs:the next challenge in infectioneont ml[J].Lancet Infect Dis.2004,4(8):480.
[8]Henry H.Lee,Michael N.Molla,Charles R.Cantor,James J.Collins,Bacterial charity work leads to population-wide resistance,Nature doi:10.1038/nature09354
[9]Paul H.Mc Cay,Alain A.Ocampo-Sosa and Gerard T.A.Fleming,Effect of subinhibitory concentrations of benzalkonium chloride on the competitiveness of Pseudomonas aeruginosa grown in continuous culture,Microbiology 156(2010),30-38;DOI 10.1099/mic.0.029751-0
[10]Morgan A.Wyatt,Wenliang Wang,Christelle M.Roux,Federico C.Beasley,David E.Heinrichs,Paul M.Dunman,Nathan A.Magarvey,Staphylococcus aureus Nonribosomal Peptide Secondary Metabolites Regulate Virulence,Science DOI:10.1126/science.1188888
[11]Rong Wang,Michael Otto et a1.Identification of novel cytolytic peptides as key virulence determinants for community-associated MRSA,Nature Medicine 13,1510 - 1514(2007)
[12]Simon R.Harris,Edward J.Feil,et a1.Evolution of MRSA During Hospital Transmission and Intercontinental Spread,Science 22 January 2010:DOI:10.1126/science.1182395
[13]张苗苗,戴梦红 等.国内外兽用抗生素耐药性管理研究.中国畜牧兽医,2010,37(6):13-16

