高效液相色谱法测定三九胃泰颗粒中芍药苷的含量
马 英 马桂云 崔 晓
(河北省石家庄以岭药业股份有限公司质检科,石家庄 050035)
高效液相色谱法测定三九胃泰颗粒中芍药苷的含量
马 英 马桂云 崔 晓
(河北省石家庄以岭药业股份有限公司质检科,石家庄 050035)
目的 建立三九胃泰颗粒中芍药苷的含量测定方法。方法 以岛津Shim-pack ODS C18(250mm×4.6mm,5μm)为色谱柱;以乙腈-0.1%磷酸 (21∶79)为流动相;检测波长为230nm;流速为1.0ml·min-1。结果 芍药苷在0.8244μg~%2.474μg范围内与峰面积的线性关系良好,r=0.9999,平均回收率为99.45%,RSD=0.39%。结论 该法简便、准确、重现性好,可用于制剂中该成分的含量测定。
三九胃泰颗粒;芍药苷;高效液相色谱法
三九胃泰颗粒由三叉苦、黄芩、茯苓、白芍、地黄等8味药材组成,具有清热燥湿、行气活血、柔肝止痛的功能。临床主要用于湿热内蕴、气滞血瘀所致的胃痛,症见脘腹隐痛、饱胀反酸、恶心呕吐、嘈杂纳减;浅表性胃炎、糜烂性胃炎、萎缩性胃炎见上述证候者。白芍作为三九胃泰颗粒的主要组成成分之一,其性微寒,味苦酸,归肝经[1],具有养血调经、敛阴止汗、柔肝止痛、平抑肝胆之功能。芍药苷 (C23H28O11)为白芍 (Radix Paeoniae Alba.)中的有效成分之一,以芍药苷作为单一定量指标来控制白芍总苷 (total glucoside of paeony,TGP)的质量,采用HPLC法测定芍药苷已有许多报道[2-5]。为更好地控制产品中白芍的含量,本实验亦采用高效液相色谱法(HPLC)测定三九胃泰颗粒中芍药苷的含量。
1 材料与方法
1.1 仪器 高效液相色谱仪:Waters515-717-2487型,PDA检测器;AG285电子天平 (上海梅特勒托利多仪器有限公司);超声波清洗器 (KQ-500E,昆山市超声仪器有限公司)。
1.2 试剂 甲醇、乙腈均为色谱纯 (天津科密欧);水为纯净水;其余试剂均为分析纯。芍药苷对照品 (中国药品生物制品检定所提供,批号:110736-201035,纯度为96.5%)。
1.3 材料 三九胃泰颗粒系华润三九医药股份有限公司提供 (规格:每袋2.5g,批号:110601~110605)。
1.4 方法
1.4.1 色谱条件 色谱柱为岛津Shim-pack ODS C18(250mm×4.6mm,5μm);流动相为乙腈-0.1%磷酸(21∶79) (v/v);流速为1.0ml·min-1;柱温:30℃;检测波长230nm;理论塔板数不少于4000;进样量20μl。
1.4.2 对照品溶液的制备 精密称取芍药苷对照品适量(0.01056g),置100ml容量瓶中,用稀乙醇溶解制并稀释至刻度,摇匀。得到101.9μg·ml-1的对照品溶液。
1.4.3 供试品溶液的制备 取三九胃泰颗粒,研匀,精密称取2.0365g,置于100ml具塞锥形瓶中,精密加入稀乙醇50ml,称定重量,超声处理 (功率240W,频率45KHz)30min,放冷,再次称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取滤液,即得供试品溶液。
2 结果
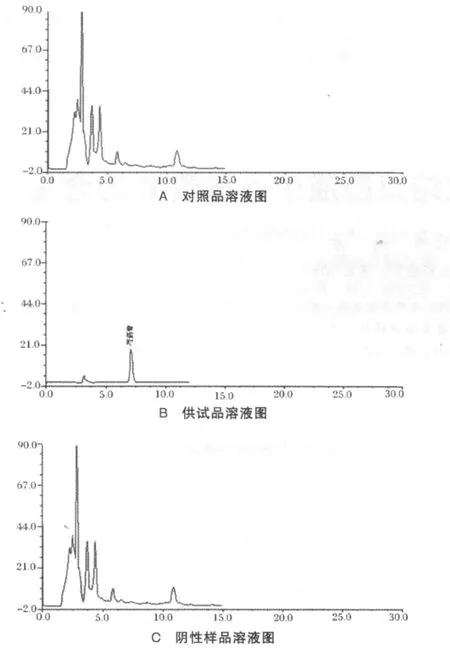
2.1 空白试验 按处方项下比例制备缺白芍的颗粒剂,同 “1.4.3”项下同法制得阴性样品溶液,备用。分别精密吸取对照品溶液、供试品溶液、阴性样品溶液各20μl注入液相色谱仪分析,记录色谱图,如图A、B、C。
2.2 标准曲线的绘制 精密称取芍药苷对照品适量(0.01068g),置50ml容量瓶中,用稀乙醇溶解制并稀释至刻度,摇匀。得到206.1μg· ml-1的对照品储备溶液。分别精密吸取芍药苷贮备液 (206.1μg·ml-1)5ml、15ml、10ml、5ml、15ml置于25ml、50ml、25ml、10ml、25ml量瓶中,加稀乙醇稀释成41.22μg·ml-1,61.83 μg·ml-1,82.44μg·ml-1,103.0μg·ml-1,123.7μg·ml-15个系列对照品溶液,分别吸取上述溶液各20μl注入液相色谱仪分析,按 “1.4.1”色谱条件测定,记录色谱图,以其色谱峰面积 (A)值为横坐标,芍药苷对照品的进样量 (C,单位μg)为纵坐标,绘制标准曲线,计算回归方程为:C=9.61×10-6A+0.067 (r=0.9999)。结果表明,芍药苷在0.8244μg~2.474μg范围内与峰面积的线性关系良好。
2.3 精密度试验 精密吸取同一份供试品溶液20μl注入液相色谱仪,按 “1.4.1”项下色谱条件测定,重复进样6次,测定其色谱峰面积分别为286773、290633、286458、288476、290454、287181,平 均 值 为 288329,RSD为0.64%。结果表明仪器精密度良好。
2.4 稳定性实验 取同一份供试品溶液,室温放置,分别在0、2、6、12、24h,按 “1.4.1”项下色谱条件测定,测定其色谱峰面积分别为252045、251949、252015、251882、251666,平均值为251911,RSD为0.06%。结果表明供试品溶液室温放置24h内稳定。
2.5 重复性试验 取同一批号样品 (110601批)6份,按 “1.4.3”项下处理后,按 “1.4.1”项下色谱条件测定,独立测定6次,测定每片样品中含芍药苷的量,RSD为0.64%。结果表明方法重复性良好。
2.6 回收率实验 (采用加样回收法) 精密称取已知含量的样品9份,每份约1.0g,然后精密加入芍药苷对照品溶液206.1μg·ml-15ml,按 “1.4.3”项下制成供试品溶液。精密吸取续滤液20μl,注入液相色谱仪,记录色谱图。将测得峰面积代入线性方程计算供试液中芍药苷的含量,并计算回收率。平均回收率为99.45%,RDS为0.39%,回收率较好。
2.7 样品含量测定及结果分析 取本品5个批号(110601~110605)的样品,按 “1.4.3”项制成供试品溶液,分别精密吸取样品溶液和对照品溶液20μl注入液相色谱仪分析,测定其中芍药苷的含量,在上述色谱条件下测得峰面积,按外标法计算含量,结果见表1。

表1 5批三九胃泰颗粒中芍药苷含量测定结果
3 讨论
3.1 流动相的选择 HPLC测定芍药苷采用乙腈和磷酸溶液的混合溶液作流动相的文献报道较多[5,6],本实验采用乙腈—0.1%磷酸溶液混合溶液 (21∶79)(v/v)作流动相,在此实验条件下,待测组分芍药苷与样品中其他组分完全分离,色谱图峰形尖锐,基线平稳。本实验前后试验并调整乙腈-0.1%磷酸溶液混合溶液 (v/v)的比例,①10∶90,②20∶80,③22∶78,④21∶79等,通过出峰时间、分离度、峰面积以及峰形等多方面综合考察,最后确定以乙腈-0.1%磷酸溶液混合溶液 (21∶79)(v/v)为最佳流动相。
3.2 检测波长的选择 根据芍药苷的理化性质,选用C18柱 (250mm×4.6mm,5μm)芍药苷与其他成分完全分离,理论塔板数不低于4000。通过紫外全波长扫描,芍药苷在230nm处有最大吸收,参考药典及文献中的最大吸收波长,确定选择230nm为检测波长。
3.3 对照品溶剂的选择 本实验曾采用甲醇和稀乙醇为溶媒配制对照品溶液,经考察选择稀乙醇为溶媒较为适宜。
3.4 供试品的处理方法的选择 ①样品的前处理是中药复方制剂分析的关键,其目的在于提取待测成分,消除其他成分的干扰,芍药苷可溶于醇及水[1],而且2010版中国药典中以芍药苷作为HPLC法测定白芍药材和含芍药苷制剂有30余种[1]。且据文献报道[3-5,7],以 HPLC 法测定白芍药材及含芍药苷制剂中芍药苷的方法稳定。②超声提取苷类成分省时,节约药材,杂质少,提取率高等优点,本实验参考2010版药典白芍药材的含测方法[1],以稀乙醇为溶剂进行超声提取,用补充损失溶媒的方法处理供试品,对于HPLC法而言最为快速、简便,而且方法的回收率和重现性均良好。③在供试品溶液的制备过程中,曾采用10、20、30、40、50min进行超声提取,分别测定其峰面积,结果表明超声提取30min后芍药苷得率趋于稳定,40min、50min反而有所下降,是否因超声时间长产热,对芍药苷有所破坏?据有关文献报道[8],芍药苷在含水溶液中会因受热而不稳定,因其结构含有苯甲酸酯键,在有水的条件下受热易分解或受其他成分的干扰,故其含量下降。但是超声过程中的产热一般≤60℃,故认为其影响很小,综合10、20、30、40、50min五个实验结果差别并不大,因此选择的表现出的10~50min提取量的不规则波动也有可能是实验误差所造成,所以最后确定超声时间为30min。
本实验建立的方法简便、准确、重现性好,空白无干扰,可用于三九胃泰颗粒的质量控制。
[1]国家药典委员会.中国药典一部[M].北京:中国医药科技出版社,2010:96.
[2]胡世林,付桂兰,冯学锋,等.不同产地和部位赤芍中芍药苷的含量测定[J].中国中药杂志,2000,25(12):714-716.
[3]吕永宁,张玉良,徐楚鸿,等.反相高效液相色谱法测定疹痒康合剂中芍药苷的含量[J].医药导报,2004,23(5):336-337.
[4]贾善学,窦忠花,陈志忠,等.高效液相色谱法测定十全大补丸中芍药苷的含量[J].医药导报,2002,21(11):735-736.
[5]熊文碧,杨龙辉,谢昵,等.高效液相色谱法测定宫炎康颗粒中芍药苷含量[J].医药导报,2003,22(1):55-56.
[6]朱伟,王学美.黄芪剂量对补阳还五汤中芍药苷、阿魏酸含量的影响[J].中国实验方剂学杂志,2006,12(3):11-13.
[7]周荔,王庆彪,刘甸杨,等.高效液相色谱法测定中药芍药苷的含量[J].海峡药学,2002,14(3):24-25.
[8]闫兴丽,张建军,李小燕,等.温度对白芍药材、白芍提取物及乾坤清颗粒成品中芍药苷含量稳定性的影响[J].中草药,2003,34(2):131.
The Determination of Content of Paeoniflorin in Sanjiuweitai Granules by HPLC
Ma Ying Ma Guiyun Cui Xiao
(Quality Testing Department of Shijiazhuang Yiling Pharmaceutical Co.,Ltd,Shijiazhuang 050035,China)
Objective An assay method was established for the determination of paeoniflorin in Sanjiuweitai granules by HPLC.Methods The chromatographic colum was Daojin Shim-pack ODS C18(250mm×4.6mm,5μm)。A mixture of acetonitrile-water(1%phosphoric acid)(21∶79)was used as the mobile phase,the detection wavelength was at 230nm and the flow rate was 1.0ml·min-1.Results The calibration curve was showed good linearity within the mass range of 0.8244~2.474μg,r=0.9999,the average recovery was 99.45%,RSD=0.39%.Conclusion The method is accurate,simple and reproducible,and can be used to control the quality of this preparation.
Sanjiuweitai;Granules;Paeoniflorin;HPLC
10.3969/j.issn.1672-2779.2013.05.110
1672-2779(2013)-05-0158-03
(本文校对:韩世辉
2013-02-06)

