南极磷虾蛋白质的分离特性及其组分分析
李芳,刘俊荣,梁姗姗,闫瑞霞
(大连海洋大学 食品科学与工程学院,辽宁 大连116023)
南极磷虾Euphausua superba是一种小型的甲壳类动物。南极磷虾资源丰富,生物总量为10 ~30亿t,年可捕捞量为0.6 ~1亿t[1]。目前国内外对南极磷虾加工利用的研究主要围绕着蛋白质、磷虾油及甲壳素等三大组分开展[2-4],此外,针对磷虾酶也有相关的研究[5]。南极磷虾蛋白质含量丰富,为完全蛋白质,富含人体所需的9种必需氨基酸(包括婴儿所需的组氨酸),其必需氨基酸含量符合1985年FAO/WHO/UNU 报告中所推荐的氨基酸摄入量[6]。Gigliotti等[2]对磷虾蛋白质品质包括消化率、生物学价值、净蛋白质利用率等的研究表明,磷虾蛋白质与酪蛋白无显著性差异。因此,磷虾蛋白质为高品质蛋白质源。海洋蛋白质作为原料可加工成鱼糜和蛋白粉或鱼粉供人类食用或用作饲料。但鱼糜的局限性在于对原料蛋白质要求苛刻,制约了一部分变性海洋蛋白质的利用[7]。利用pH调节法制备分离蛋白是近几年探讨的一种方法,该方法不需要除去水产动物的骨骼和皮等,可以回收肌浆蛋白质并提高蛋白质的回收率,能有效地去除中性脂肪和膜脂,且回收蛋白质的功能性较好[8]。本研究中,作者以冷冻南极磷虾为原料,采用pH调节法尝试南极磷虾蛋白质分离回收的可行性,旨在为磷虾资源的有效利用提供参考。
1 材料与方法
1.1 材料
冷冻南极磷虾由辽宁省大连海洋渔业集团公司提供,原料冻藏一年左右,冷冻块状运输至实验室后,立即放入冰柜(-20 ℃)中冷冻保存。
试验仪器:DS21 型高速匀浆机,为上海样品模型厂产品,电机输出功率为200 W(220 V,50 Hz);GL-21M 高速冷冻离心机,为湖南湘仪实验仪器开发有限公司产品;Sartorius 型pH 计(PB-10),为赛多利斯科学仪器(北京)有限公司产品;721 型分光光度计,为上海光谱仪器有限公司产品。
1.2 方法
1.2.1 蛋白质的溶出、分离与回收
1)南极磷虾的预处理。取南极磷虾150 g,于4 ℃下解冻,解冻后加入9 倍质量的去离子水混合,以5 000 r/min 匀浆2 min,过滤得到南极磷虾匀浆和虾壳残渣。由于南极磷虾内源蛋白酶极其活跃,整个实验过程中温度控制在4 ℃。
2)蛋白质的溶解。南极磷虾匀浆pH 设置为1.5 ~12.0,以0.5 为pH 变化梯度。将匀浆分为两份,一份用2 mol/L HCl 依次调到1.5(酸处理),一份用2 mol/L NaOH 依次调到12.0(碱处理),在4 ℃下以10 000 g 离心20 min,得到不同pH 下的溶出物和未溶出物。
3)蛋白质的回收。用2 mol/L HCl 或2 mol/L NaOH 调节南极磷虾溶出物至等电点,在4 ℃下以10 000 g 离心20 min,得到分离蛋白和未回收溶出物。
1.2.2 分析测定
1)一般化学组成的测定。采用直接干燥法(GB/T5009.3-2003)测定水分含量,采用灼烧称重法(GB/T5009.4-2003)测定粗灰分含量,采用凯氏定氮法(GB/T5009.5-2003)测定粗蛋白质含量,采用三氯乙酸沉淀法测定非蛋白态氮含量,采用索氏抽提法(GB/T5009.6-2003)测定粗脂肪含量。每种组分测定3次,取其平均值。
2)蛋白质的溶解度和回收率。采用双缩脲法[9]测定蛋白质含量,以牛血清白蛋白为标准制作标准曲线,得出不同pH 下南极磷虾蛋白质的溶解度和回收率曲线,其计算公式为
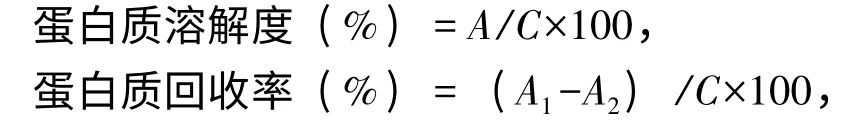
其中:A 为离心中层清液蛋白质含量(mg),A=离心中层清液蛋白质浓度(mg/mL)×离心中层清液体积(mL);A1为第一次离心中层清液蛋白质含量(mg);A2为第二次离心上清液蛋白质含量(mg);C 为总蛋白质含量(mg),C=总蛋白质浓度(mg/mL)×匀浆体积(mL)。
3)SDS-PAGE 电泳。用SDS-PAGE 电泳测定用酸碱法提取过程中不同阶段的蛋白质组成。选取pH 为1.5和12.0 两个点。分析样品包括匀浆液、溶出物、未回收溶出物及分离蛋白。样品中加入3倍体积的4×SDS 样品缓冲液,混合后加入总体积为5%的β-巯基乙醇,在95 ℃下水浴10 min。样品上样量为10 ~15 μL,用120 g/L 分离胶、50 g/L 浓缩胶配制胶板。用考马斯亮蓝R250 染色,脱色。
2 结果与讨论
2.1 冷冻南极磷虾的化学组成
经测定,冷冻南极磷虾的基本组成成分含量:水分79.37%、总脂肪3.22%、粗蛋白质11.45%、粗灰分3.03%。经分析表明,南极磷虾非蛋白态氮含量为26.7%(干基)。
2.2 分离过程中蛋白质溶解度的变化
从图1可见:当pH 为1.5 ~4.5 时,溶解度呈逐渐下降趋势;当pH 为4.5 ~12.0 时,溶解度呈逐步上升趋势。即在酸性或碱性pH 时,蛋白质带同种正电荷或负电荷,蛋白质之间的静电排斥和蛋白质与水分子的结合促使蛋白质溶解[10]。在极端pH 条件下,如pH 为1.5和pH 为12.0 时,具有强烈的静电排斥,使蛋白质分子之间难以聚合沉淀,同时,蛋白质与水分子结合,溶解度较高;当pH 为4.5(等电点)时,蛋白质净电荷为零,蛋白质分子之间缺少静电排斥,促进了蛋白质疏水作用和蛋白质聚合,蛋白质溶解度最低[11]。酸性溶液中蛋白质溶解度在pH 为1.5 时最大(61.5%),碱性溶液中蛋白质溶解度在pH 为12.0 时最大(66.1%);当pH 为4.5 时溶解度最小(15.8%)。

图1 南极磷虾蛋白质溶解度随pH 的变化曲线Fig.1 Changes in protein solubility with pH value in Antarctic krill
2.3 分离过程中蛋白质回收率的变化
从图2可见:南极磷虾蛋白质回收率的变化趋势与溶解度的变化趋势一致。当pH 为1.5 ~4.5时,回收率呈逐渐下降趋势;当pH 为4.5 ~12.0时,回收率呈逐步上升趋势。酸性溶液中蛋白质回收率在pH 为1.5 时最大(49.8%),碱性溶液中蛋白质回收率在pH 为12.0 时最大(45.7%);当pH 为4.5 时回收率最小(0.3%)。
与鱼类蛋白质回收率(60% ~80%)相比[8,12],南极磷虾蛋白质回收率相对较低。根据Chen等[13]的研究结果,用酸碱处理法只能部分回收水溶性肌浆蛋白质,而且肌浆蛋白质的回收与离子强度有关。南极磷虾含有较高浓度的肌浆蛋白质[14],本研究中原料冷冻保藏时间过长,导致自溶酶对蛋白质有一定的降解作用(图3),这就可以在一定程度上解释了南极磷虾蛋白质回收率低的原因。此外,还有一些实际操作中的影响因素,如匀浆转速、离心转速以及操作过程中对蛋白质的损失等。

图2 南极磷虾蛋白质回收率随pH 的变化曲线Fig.2 Effect of pH on recovery of Antarctic krill protein
2.4 蛋白质分子量的分布特性
图3和图4 为用酸、碱处理法回收和分离蛋白前后蛋白质分子质量的分布图谱。南极磷虾匀浆蛋白质分子质量为小分子量蛋白质,主要有4 条特征带,分布在相对分子质量为 80 000、45 000、40 000、32 000 处。
对比图3和图4可以得出:用酸处理时,可以回收大部分溶出物蛋白质组分,未回收溶出物的蛋白质相对分子质量为40 000 左右;用碱处理时,溶出物中蛋白质组分较多,但分离蛋白中蛋白质组分较少,仍有多种蛋白质组分未回收,未回收溶出物蛋白质相对分子质量分布在80 000和35 000~45 000 处。

图3 酸处理和碱处理过程中不同样品的蛋白质组成Fig.3 Protein composition of different samples in acid and alkaline treatments by SDS-PAGE
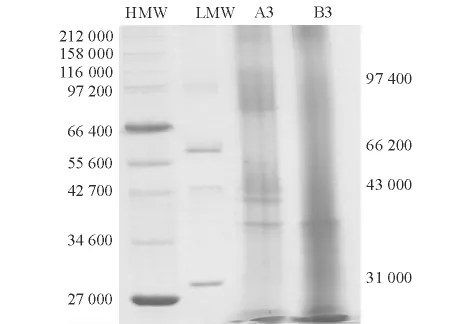
图4 酸处理和碱处理分离蛋白的蛋白质组成Fig.4 Protein composition of protein isolates from acid and alkaline solubilization process by SDS -PAGE
Kawamura等[15]研究表明,磷虾蛋白质自溶非常迅速,尤其是肌球蛋白重链的降解,24 h 后大部分蛋白质降解为低分子量物质。本研究中所用原料因长期冻藏,其自溶作用不言而喻,研究分析结果也佐证了这一点。
2.5 分离过程中蛋白质的分布特性
由于南极磷虾回收率较低,针对分离过程中南极磷虾含氮物的分布进行跟踪分析,包括南极磷虾、虾壳残渣、未溶出物、未回收溶出物及分离蛋白等五部分。
从表1可见,分离过程中南极磷虾含氮物质主要分布在未回收溶出物和分离蛋白中。其中,用酸、碱处理法回收分离的蛋白质得率分别为37.76%和37.13%;酸、碱处理中未回收溶出物中的含氮物质占很大的比例,分别为31.89%和37.13%,可解释为冷冻南极磷虾的自溶作用导致大量非蛋白态氮产生,因而无法在蛋白质等电点处絮凝回收;酸、碱处理中原料处理产生的虾壳残渣含有部分含氮物,分别占原料总氮的7.13%和9.48%;碱处理的蛋白质溶出效果要明显好于酸处理,酸、碱处理中未溶出物中粗蛋白质的含量分别为15.52%和2.57%。
由于本试验原料为冷冻南极磷虾,自溶酶降解作用已积累到一定程度。试验结果表明,利用pH调节法分离回收蛋白质的得率较低,因此,pH 调节法不适用于冷冻南极磷虾蛋白质的分离回收。

表1 分离过程中南极磷虾含氮物质的分布(干基)Tab.1 Profile of Antarctic krill nitrogenous compounds in the separation process(dry basis) w/%
[1]刘建军.加速开发南极磷虾资源打造战略性新兴产业[J].辽宁经济,2011(1):78-82.
[2]Gigliotti J C,Jaczynski J,Tou J C.Determination of the nutritional value,protein quality and safety of krill protein concentrate isolated using an isoelectric solubilization/precipitation technique[J].Food Chemistry,2008,111(1):209-214.
[3]施佳慧,吕桂善,徐同成,等.磷虾油的脂肪酸成分及其降血脂功能研究[J].营养学报,2008,30(1):115-116.
[4]姚宏亮.南极磷虾虾壳制备甲壳素/壳聚糖的工艺研究[J].水产科学,2004,23(5):34-36.
[5]孙松,严小军.南极大磷虾的生物活性物质及其用途研究进展[J].极地研究,2001(3):213-216.
[6]Chen Y C,Tou J C,Jaczynski J.Amino acid and mineral composition of protein and other components and their recovery yields from whole Antarctic krill(Euphausia superba)using isoelectric solubilization/precipitation[J].Journal of Food Science,2009,74(2):31-39.
[7]刘俊荣,汪涛,石泰,等.不同pH 条件下罗非鱼肌肉蛋白分离效果及其功能特性的研究[J].水产科学,2010,29(6):317-323.
[8]Nolsöe H,Undeland I.The acid and alkaline solubilization process for the isolation of muscle proteins:state of the art[J].Food and Bioprocess Technology,2009(2):1-27.
[9]Kristinsson H G,Liang Y.Effect of pH-shift processing and surimi processing on Atlantic croaker muscle proteins[J].Food Chemistry and Toxicology,2006,17(5):C304-C312.
[10]Palafox H,Córdova-Murueta J H,Navarrete del Toro M A,et al.Protein isolates from jumbo squid(Dosidicus gigas)by pH-shift processing[J].Process Biochemistry,2009,44(5):584-587.
[11]Kristinsson H G,Ingadottir B.Recovery and properties of muscle proteins extracted from tilapia light muscle by pH shift processing[J].Food Engineering and Physical Properties,2006,71(3):132-141.
[12]傅润泽,刘俊荣,王帅,等.采用酸碱提取法对鲢肌肉蛋白分离特性的影响[J].大连海洋大学学报,2011,26(6):539-543.
[13]Chen Y C,Jaczynski J.Protein recovery from rainbow trout(Oncorhynchus mykiss)processing by-products via isoelectric solubilization/precipitation and its gelation properties as affected by functional additives[J].Journal of Agricultural and Food Chemistry,2007,55:9079-9088.
[14]Suzuki T,Shibata N.The utilization of Antarctic krill for human food[J].Food Reviews International,1990,6(1):119-147.
[15]Kawamura Y,Nishimura K,Igarashi S,et al.Characteristics of autolysis of Antarctic krill[J].Agricultural and Biological Chemistry,1981,45(1):93-100.

