手性冠醚在手性识别中的应用研究进展
袁 碧 陈卫红 汪吴林 石 浩
(浙江工业大学,浙江 杭州 310014)
0 前言
手性是自然界最普遍的现象,目前用于临床的三千多种原料药中,有一半是合成药物,在合成药中又有40%是外消旋体。在外消旋体药物中,往往只有一种立体异构体有效,而它的对映体往往没有药效,甚至是具有相反的药效[1-2]。据统计,市场上大约60%以上的处方药物分子具有手性,而其中绝大部分是以外消旋体的形式存在。随着人们生活水平的提高,高效低毒的单一手性对映体药物越来越受到人们的青睐。因此利用有效的方法对手性药物对映体进行分离分析在新药研究开发和药品质量控制中具有十分重要的意义。
据此,本文就手性冠醚手性识别各种对映体化合物的应用进行了综述。
1 手性冠醚
冠醚是第一代超分子化合物,其具有亲水性内腔和亲脂性外壳,能与大小相当的客体分子如金属离子、含伯氨基的化合物形成稳定配合物[3]。
自从Cram等成功的合成了含1,1'-联萘基的手性冠醚并将其应用于外消旋α-氨基酸对映体及其衍生物的拆分,手性冠醚作为一种具有优秀对映体选择性的人工受体分子愈来愈受到人们的关心和重视。
手性冠醚除了具备一般冠醚的空穴和外腔,还具有手性中心这一特点。根据插入到冠醚中的手性单元,可以将手性冠醚主要分为四类:①以有机酸为基体的手性冠醚;②插入联萘单体的手性冠醚;③从糖类化合物出发的手性冠醚;④以有机醇为手性源的手性冠醚。
2 手性冠醚在手性识别中的应用
2.1 以有机酸为基体的手性冠醚
2.1.1 酒石酸
以有机酸为手性源来制备手性冠醚,酒石酸是研究最成熟的,由其制备的多种手性冠醚已投入商业化生产。
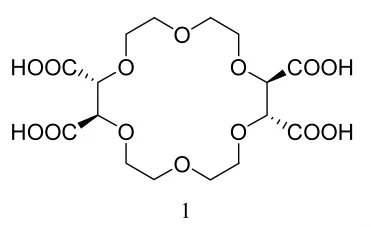
Lehn等[4]以酒石酸出发最先合成了(+)-(18-crown-6)-2,3,11,12四羧酸酯(1),并将其成功地应用于各种外消旋伯胺化合物以及外消旋非伯胺化合物的手性拆分。其识别机制为质子化的伯胺化合物插入到18-冠-6的空穴中并与其氧原子形成三个N-H键从而螯合生成具有不同稳定性的络合物。
18-冠-6的制备为手性固定相的研究发展拉开了序幕。手性固定相 (chiral stationary phase,CSP)是通过物理吸附或者化学键合的方法把手性化合物键合到固相载体如全多孔硅胶上。冠醚类手性固定相(Crown Ether CSP)是手性固定相的一种,是目前拆分外消旋伯胺化合物最有效的方法之一。
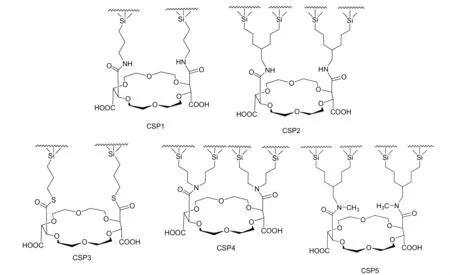
Hyun及其团队在以18-冠-6制备手性冠醚固定相方面进行了大量研究[5-9]。Hyun等将(+)-(18-crown-6)-2,3,11,12四羧酸酰氯化后经酰胺反应与氨丙基硅胶进行结合而得到手性固定相CPS1,实验发现其在分离外消旋的手性氨基化合物的同时也可以分离多种氨基醇,有机胺以及一些手性药物。
随后,为了改进和优化CSP1的手性分离能力等性能,Hyun等制备了一系列手性固定相CSP2、4、5且Cho制备了手性固定相CSP3,实验发现CSP2,3,4,5在酸性环境中的稳定性和手性拆分各种外消旋α-氨基酸,氨基醇,伯胺的分离效果都要优于CPS1。其中,CSP3分别以硫酯键取代CSP1的酰胺键,CSP5将CSP1酰胺氢原子取代,从而避免了酰胺氢原子与冠醚氧原子形成氢键即增强了其与对映体结合的稳定性。研究还发现CSP5对β-氨基酸的手性拆分能力也要稍强于 CSP1 且 CSP1、2、3、4、5 与 S 对映体结合的稳定性大于R对映体[10]。
2.1.2 其他有机酸
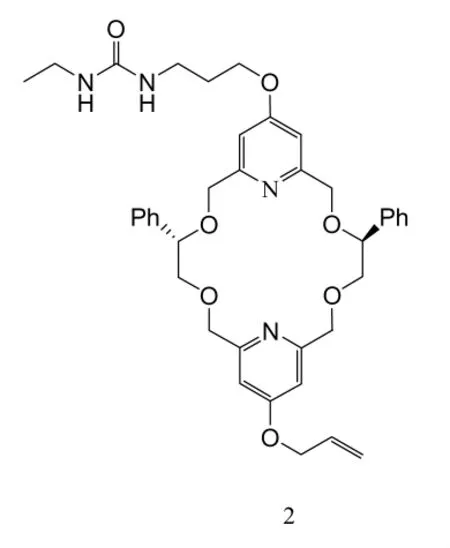
Kim J K等[11]报道了以(S)-(+)-苦杏仁酸及白屈氨酸为手性源,经十三步反应制备了一种含有尿素、二苯基、烯丙氧基基团的二吡啶并-18-冠-6手性冠醚(2)。经1H-NMR滴定法检测发现,发现该冠醚对D-和L-氨基酸甲酯盐酸盐都有一定的结合能力(结合常数 Ka=1.33×103~3.20×103),但与D-氨基酸甲酯盐酸盐结合的稳定性高于L-氨基酸甲酯盐酸盐。
2.2 插入联萘单体的手性冠醚
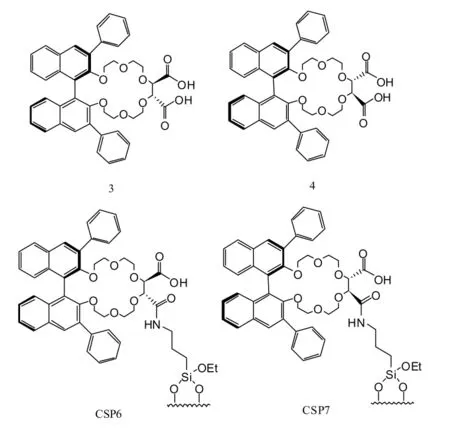
2007年,Cho Y J等[12]将两种含有 R-3,3'-二苯基-1,1'-二萘基互为立体异构体的手性冠醚3和4以共价键结合到硅胶基质上从而制备了两种手性固定相即CSP6、CSP7。发现CSP7在拆分妥卡尼类外消旋伯胺化合物拆分效果要优于CSP6,其分离因子a最高可达9.84,但CSP6和CSP7两者都不能拆分外消旋α-氨基酸化合物。
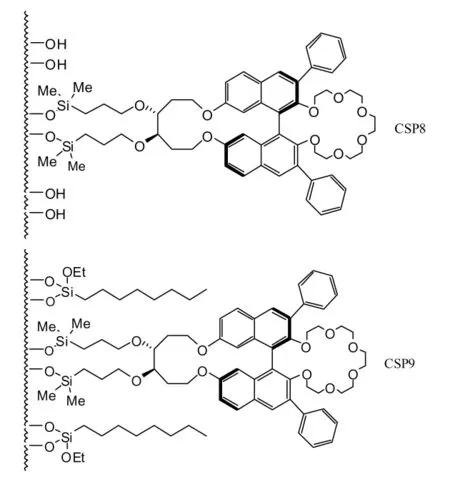
随后,Choi H J等[13]以 3,3'-二苯基-1,1'-二萘基制备了不同于CSP6、CSP7的新的手性固定相CSP8和CSP9。CSP9不同于CSP8的是在制备CSP9时用n-辛基三乙氧基硅烷基团封闭掉硅胶表面多余的羟基,这一处理提升了CSP9对α-氨基酸,伯胺,氨基醇,含芳基的氨基酮等外消旋化合物的手性识别能力。
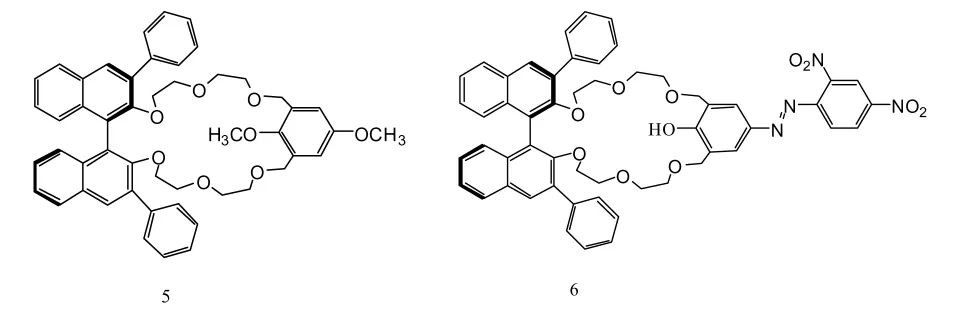
Piao M H等[14]通过(R)-(-)-2-[2-(1-{2-[2-(2-羟乙氧基)-乙氧基]-3,3'-二苯基-[1,1']-联萘-2-氧基}-乙氧基)-乙醇与1,3-二溴甲基-2,5-二甲氧基苯一锅法反应得到新型手性冠醚 (R)-(-)-3,3'-二苯基-1,1'-联萘-23-冠-6(5),并以其为基础制备了全固态对映体选择电极 (All solid-state enantioselective electrode) (ASESE)。 实 验 表 明 ,ASESE成功实现了对丙氨酸、亮氨酸、缬氨酸、苯丙氨酸、苯基甘氨酸这些氨基酸的甲酯对映异构体的拆分,其中,对苯基甘氨酸甲酯对映体拆分效果最好(K(R,S)=8.5%~7.1%)。
随后,Cho,Yinan Li等[15]在化合物5基础上,将其先后经过氧化,还原取代等反应而制备了化合物6,其对氨基醇有较好的手性分离效果,由于苯基偶氮发色团的存在使得化合物6在手性拆分对映体苯丙氨醇时显示出明显的颜色差别且KS/KR=2.51。
徐括喜、焦书燕等[16-17]以R-或S-联萘酚、2,2'-联苯酚、间苯二酚、氯腈胺为原料两步反应合成了六个手性氮杂冠醚(7~12)即 R-1,R-2,R-3和S-1,S-2,S-3。研究发现这六种化合物能高效地手性识别四种α-氨基酸阴离子对映体,且在一定浓度范围内,任意一种氨基酸阴离子的对映体能够增加手性冠醚的荧光强度五倍至六倍,而其镜像对映体则不能增加手性冠醚荧光强度。

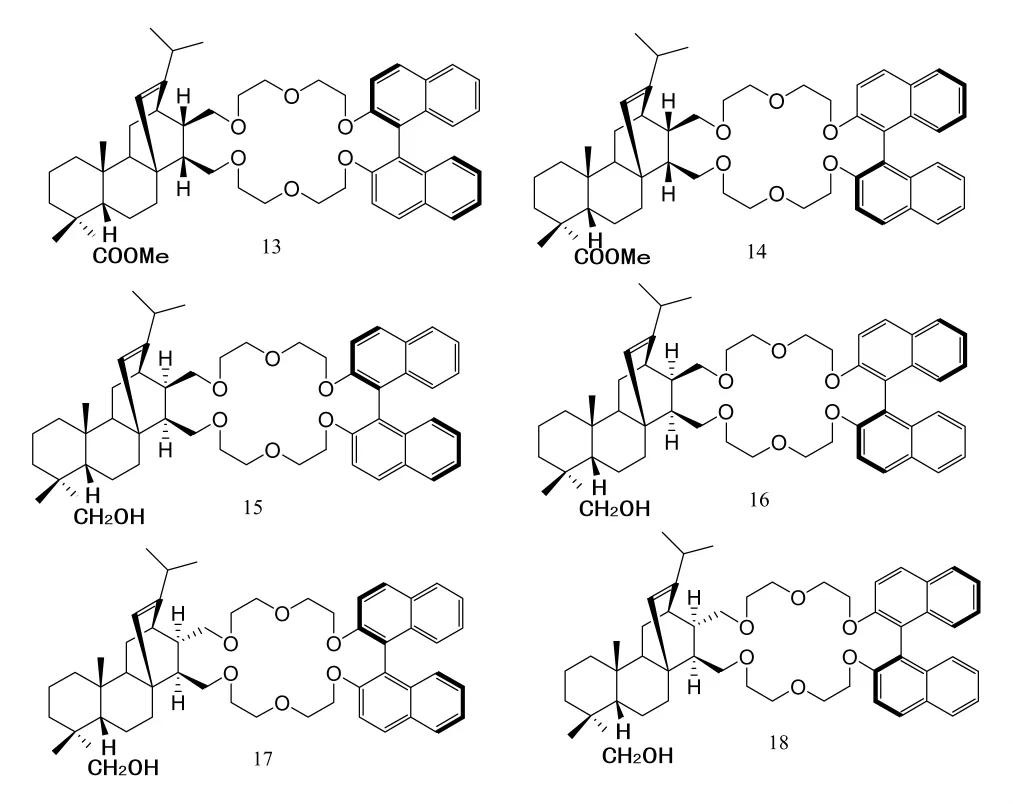
二萜类物质作为一种天然的手性池因为其具有高纯度的光学活性及稳定的骨架结构,而最近被报道用来合成一系列冠醚超分子的天然手性源。王衡山、何春欢等[18-19]将松香酸通过Diels-Alder加成反应处理后得到具有三个官能团的松香酸衍生物,再将其与一分子联萘酚为原料制备了六个具有联萘酚和贝叶烷结构的手性冠醚大环化合物,并通过紫外分光滴定法考察了这六种化合物对L/D-质子化的伯胺和L/D-氨基酸甲酯盐对映体的分离能力。在CHCl3:MeOH=2:1,25℃溶剂体系和温度条件下,化合物13~18对上述L/D对映体以高达KD/KL=6.02,DDG0=4.45 kJ/mol等表征常数而显示了其优异的手性识别能力。
2.3 含糖的手性冠醚
糖类化合物含有多个手性中心,且来源丰富,是合成手性冠醚的另一重要来源,其中以单糖D-葡萄糖、D-半乳糖和甘露醇及其衍生物为手性源的冠醚最为常见。但是,近年来,由糖类化合物衍生得到的手性冠醚主要作为相转移催化剂催化不对称反应,而作为手性分离选择剂来识别对映异构体的报道还比较少。
1977年,Stoddart等[20]以D-甘露醇出发制备了一种手性冠醚,并通过NMR共振波谱法检测了其与铵离子结合的稳定性。自此,以糖类化合物合成各种大环化合物的研究开始陆续展开。由于糖类化合物的生物相容性及可利用性,是一种非常好的天然手性源,以其出发构成的手性冠醚等大环化合物具有广阔的应用前景。
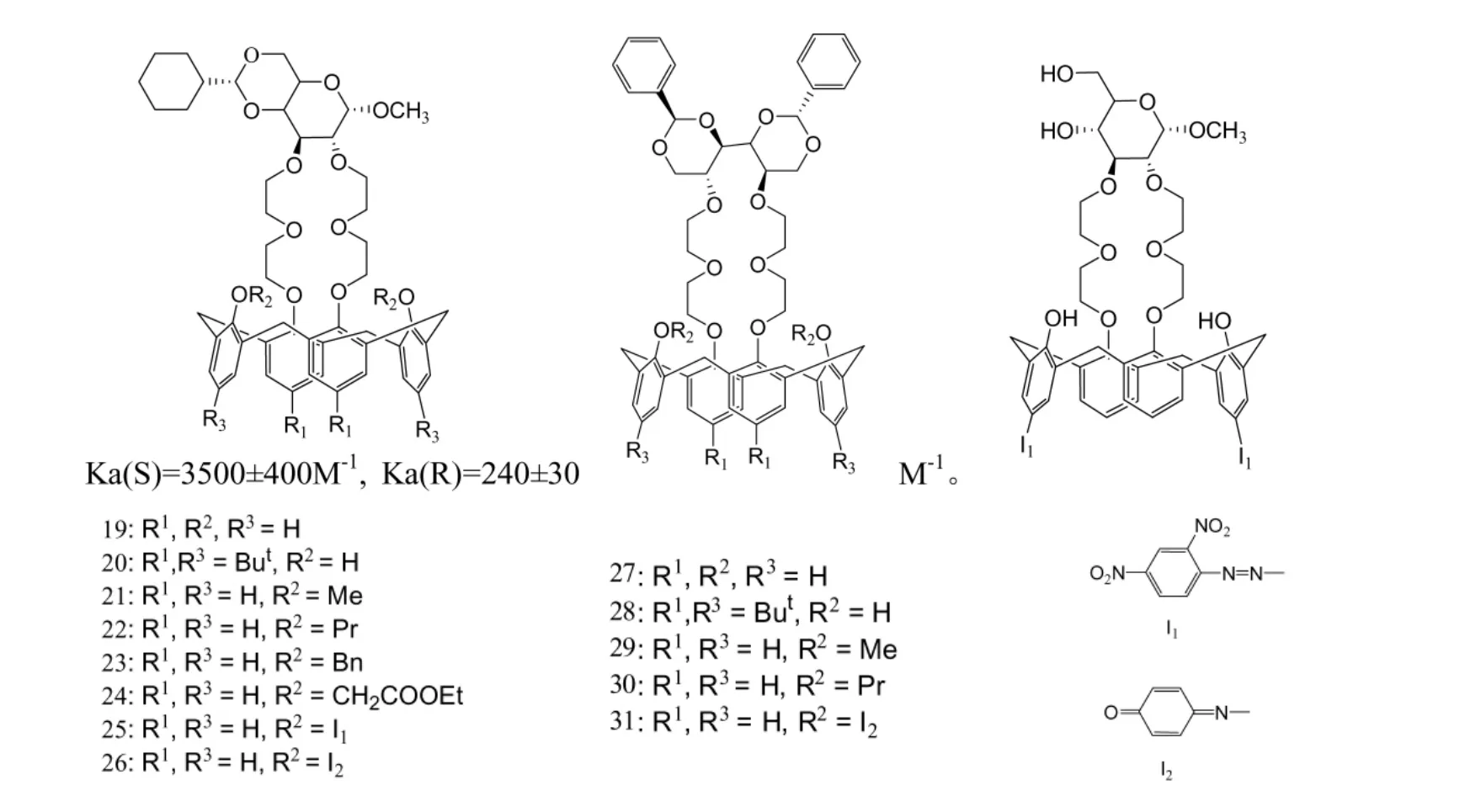
Bitter等[21]报道了以 1,1'-联萘-甲基-α-D-葡萄糖以及D-甘露醇为基础制备了三种1,3-杯[4](冠-6)醚的手性冠醚大环化合物19~31。通过紫外光谱检测表明,这几种化合物对伯胺对映体有显著地手性拆分能力,且结合常数Ka(S)=3500±400M-1,Ka(R)=240±30M-1。
Lewandowski等[22]以蔗糖为手性源,制备了五种手性冠醚32~36,并通过核磁滴定法检测了这五种冠醚对α-苯乙胺阳离子的手性拆分能力。发现:在CDCl3溶剂中,化合物33手性识别能力最强(Ka(S(-))/M-1=1244±192),化合物 35 对 α-苯乙胺对应异构体没有任何亲和作用。其可能原因之一是苯磺酸基团的吸电子作用减弱了化合物35与客体离子结合的可能性。

2.4 从手性醇出发的冠醚
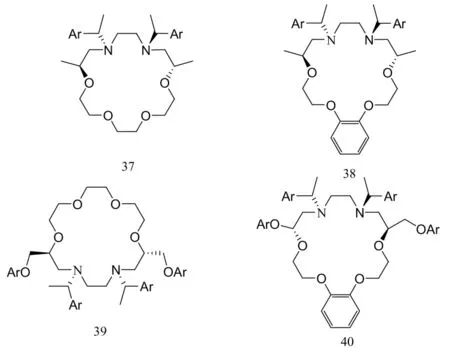
Turgut Y等[23]从(S)-3-芳氧基-1,2-丙二醇和(S)-1,2-丙二醇出发,经一系列反应得到了四种手性氮杂冠醚(37~40),通过核磁滴定法发现对氨基酸酯衍生物 (伯铵盐)有很好的拆分效果,其中对DPheAlaOMe.HCI的结合常数Ka最高且为176.93M-1。
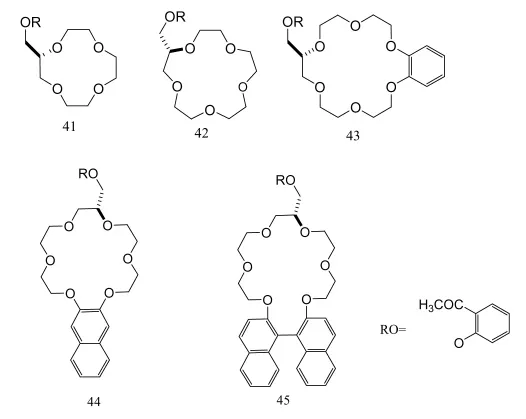
2011年Bredikhina等[24]以价格低廉及生产应用广泛的消旋3-(2-甲氧基苯氧基)丙烷-1,2-二醇即愈创木酚甘油醚为手性源,反应得到4种套索冠醚(41~45)。通过1HNMR波谱法表明,这四种化合物都不能拆分氨基盐酸盐,化合物42、43、44、45对氨基六氟磷酸盐有较好的手性识别能力,其中手性识别因子CRF(chiral recognition factor)最高可达2.5。
3 结语
手性冠醚对手性化合物有良好的识别作用,以有机酸、联萘酚、糖类、有机醇及其他天然产物作为手性源的手性冠醚能较好地拆分含伯氨基的对映体化合物。随着新类型手性冠醚在手性识别领域的不断涌现,手性冠醚的应用范围必将不断扩大,其手性识别性能也将得到提升。
[1]曾苏,王胜浩,杨波.手性药理学与手性药物分析 [M].北京:科学出版社,2009.
[2]袁黎明.手性材料的识别[M].北京:科学出版社,2010.
[3]吴成泰.冠醚化学[M].北京:科学出版社,1992.
[4]申睿,谢剑炜.手性选择剂及其在手性药物分离分析中的应用进展 [J].国外医学药学分册,2005,32(6):413-417.
[5]Lee A,Choi H J,Jin K B,Hyun M H.Liquid chromatographic resolution of 1-aryl-1,2,3,4-tetrahydroisoquino lines on a chiral stationary phase based on(+)-(18-crown-6)-2,3,11,12-tetracarboxylic acid[J].Journal of Chromatography A,2011,1218(26):4071-4076.
[6]Cho H S,Choi H J,Hyun M H.Preparation of a new crown ether-based chiral stationary phase containing thioester linkage for the liquid chromatographic separation of enantiomers[J].Journal of Chromatography A,2009,1216(44):7446-7449.
[7]Hyun M H,Cho Y J,Song Y,et al.Preparation and application of a new doubly tethered chiral stationary phase containing N-CH3 amide linkage based on(+)-(18-crown-6)-2,3,11,12-tetracarboxylic acid[J].Chirality,2007,19(1):74-81.
[8]Hyun M H,Song Y,Cho Y J,Kim D H.Preparation of a new doubly tethered chiral stationary phase based on (+)-(18-crown-6)-2,3,11,12-tetracarboxylic acid and its application[J].Journal of Chromatography A,2006,1108(2):208-217.
[9]Lee W,Yu Jin J,Baek,C S.Comparison of enantiomer separation on two chiral stationary phases derived from(+)-18-crown-6-2,3,11,12-tetracarboxylic acid of the same chiral selector[J].Microchemical Journal 2005,80(2):213-217.
[10]Hyun M H,Song Y,Cho Y J,et al.Resolution of β-amino acids on a high performance liquid chromatographic doubly tethered chiral stationary phase containing N–CH3amide linkage based on (+)-(18-crown-6)-2,3,11,12-tetracarboxylic acid[J].Chirality,2007,19(1):74-81.
[11]Kim J K,Kim J,Song S,et al.Enantiomeric Recognition of d-and l-Amino Acid Methyl Ester Hydrochlorides by New Chiral Bis-pyridino-18-crown-6 Substituted with Urea,and Diphenyl Groups[J].Journal of Inclusion Phenomena and Macrocyclic Chemistry,2006,58(1-2):187-192.
[12]Cho Y J,Choi H J,Hyun M H.Preparation of two new liquid chromatographic chiral stationary phases based on diastereomeric chiral crown ethers incorporating two different chiral units and their applications[J].Journal of Chromatography A,2008,1191(1–2):193-198.
[13]Choi H J,Jin J S,Hyun M H.Liquid chromatographic direct resolution of tocainide and its analogs on a (3,3'-diphenyl-1,1'-binaphthyl)-20-crown-6-based chiral stationary phase containing residual silanol protecting n-octyl groups[J].Chirality,2009,21(1):11-15.
[14]Piao M H,Hwang J,Won M S,et al.A Solid State Polymer-Coated Electrode Containing a Chiral Crown Ether Derivative for Enantioselective Detection of Phenylglycine Methyl Ester Isomer[J].Electroanalysis 2008,20(12):1293-1299.
[15]Cho E N,Li Y,Kim H J,et al.A colorimetric chiral sensor based on chiral crown ether for the recognition of the two enantiomers of primary amino alcohols and amines[J].Chirality,2011,23:349-353.
[16]Xu K X,Jiao S Y,Yao W Y,et al.Syntheses and highly enantioselective fluorescent recognition of α-Amino carboxylic acid anions using chiral oxacalix[2]arene[2]bisbinaphthes[J].Chirality,2012,24(8):646-651.
[17]焦书燕,姚文涌,谢恩,等.基于联萘酚的手性冠醚的合成及其晶体结构[J].化学研究,2011,22(6):1-4.
[18]Wang H S,He C H,Pan Y,et al.Synthesis and amines enantiomeric recognition ability of binaphthyl-appended 22-crown-6 ethers derived from rosin acid[J].Journal of Inclusion Phenomena and Macrocyclic Chemistry,2012,73:177-183.
[19]Wang H S,Tian X,Yang D,et al.Synthesis and enantiomeric recognition ability of 22-crown-6 ethers derived from rosin acid and binol[J].Tetrahedron:Asymmetry,2011,22(4):381-386.
[20]Bakó P,Keglevich G,Rapi Z,et al.The enantiomeric differentiation ability of chiral crown ethers based on carbohydrates[J].Current Organic Chemistry,2012,16:297-304.
[21]Lewandowski B,Jarosz S.Chiral recognition of alphaphenylethylamine by sucrose-based macrocyclic receptors[J].Chem Commun(Camb),2008,(47):6399-401.
[22]Bitter I,K觟szegi魪 G,Alajo A,et al.Synthesis of chiral 1,3-calix[4](crown-6)ethers as potential mediators for asymmetric recognition processes[J].Tetrahedron:Asymmetry,2003,14:1025-1035.
[23]Turgut Y,Aral T,Hosgoren H.Synthesis of novel C2-symmetric chiral crown ethers and investigation of their enantiomeric recognition properties[J].Tetrahedron:Asymmetry,2009,20(19):2293-2298.
[24]Bredikhina Z A,Eliseenkova R M,Fayzullin R R,et al.Synthesis and extraction properties of some lariat ethers derived from the spontaneously resolved guaifenesin,3-(2-methoxyphenoxy)propane-1,2-diol[J].Arkivoc,2011,(10):16-32.

