对甲基苯基氯化镁的合成工艺改进
严生虎,康 琳,张 跃,刘建武,沈介发
(常州大学化工设计研究院,江苏 常州 213164)
2-氰基-4'-甲基联苯(o-tolylbenzonitrile,OTBN)是最新一代沙坦类抗高血压药的关键中间体[1]。文献[2-3]报道了一些经格氏反应合成OTBN的方法,如在过渡金属Pd、Mn和Ni等催化下,以对甲苯基溴化镁与邻溴苯腈反应制备,产率较高。对氯甲苯(PCT)的价格相对低廉,就成本而言极具吸引力。但从 Ph-X 的键能(C-Cl,402 kJ/mol;C-Br,339 kJ/mol;C-I,272 kJ/mol)[4]看,氯代芳烃键能最大,反应活性最差,此外,PCT分子中,对位甲基的给电子效应使卤代烃的惰性进一步增加,反应更加困难[5],这些缺点成为PCT在该领域获得广泛应用的障碍。
格氏反应广泛应用于药物合成和精细化学品合成中[6],目前由格氏反应制备OTBN已成为主流工艺。格氏反应的常用溶剂是四氢呋喃(THF),收率一般在80%以上,但THF在使用前必须严格除水和过氧化物,给工业过程中的循环利用带来困难[7-8]。李有桂等[9]研究了在 THF-甲苯混合溶剂中引发和制备对甲基苯基氯化镁,得到 81.1%的收率;肖永鹏等[10]研究了以 THF-二氧六环混合溶剂制备格氏试剂,但该混合溶剂只能用于制备烷基氯代物的格氏试剂,对于卤代芳烃则会形成不溶性络合物而使反应淬灭[11]。用于格氏反应的醚类溶剂中只有2-甲基四氢呋喃(MeTHF)和乙醚吸水性较弱,但乙醚的沸点较低(34 ℃),在空气中能氧化成有爆炸性的过氧化物[12],很难应用于工业化生产中。市售MeTHF含水率较低,可直接用于格氏反应,简化了操作;加之MeTHF沸点较高,提高反应的安全性,且通过蒸馏即可实现更高的溶剂的回收率[13],在需要Lewis-base的有机金属反应中可以代替THF,目前在工业生产中有代替THF的趋势[11-13]。
由于原料成本、溶剂的循环套用等问题,一些文献报道的方法[2-3]很难进行中试放大研究和工业化生产。基于此,本文以价廉的PCT为原料,研究了对甲基苯基氯化镁的合成工艺,提出了一种在MeTHF-THF混合溶剂体系中制备该类格氏试剂的新方法。研究中考察了反应温度、时间、混合溶剂配比、溶剂用量等因素对产物收率的影响,优化了合成工艺条件,收率最高达 95.4%。与其它工艺方法[2-3,9]相比,该工艺的溶剂体系降低了装置无水性要求,操作简便,收率较高。该工艺为对甲基苯基氯化镁格氏试剂的生产提供了可行的技术路线,可显著降低OTBN的合成成本,提高了溶剂的回收利用率,具有良好的应用前景。
1 实验部分
1.1 仪器和试剂
IKA RCT basic 3810025型加热磁力搅拌器;WT11001R型电子天平;GC 9890A型气相色谱仪。
PCT(AR,江苏长海化工有限公司);镁粉(100~200目,上海龙昕科技发展有限公司);THF、MeTHF(AR,上海达瑞精细化学品有限公司);碘、乙酸乙酯(AR,国药集团化学试剂公司)。
1.2 反应原理
以PCT和镁为原料,在碘的引发下合成对甲苯基氯化镁,主、副反应方程式如下。
主反应
副反应

1.3 实验操作及分析方法
1.3.1 脱水预处理
THF:滴加2滴二苯甲酮于THF(300 mL)中,加入钠丝(5 g)回流直至体系变蓝色,收集66 ℃馏分,加入适量钠块密封保存待用。
MeTHF:加入适量经高温脱水活化处理过的5A分子筛,密封保存待用。
PCT:蒸馏后加入适量经高温脱水活化处理过的5A分子筛保存待用。
镁粉:用稀盐酸出去表面氧化膜,真空干燥后待用。
1.3.2 对甲基苯基氯化镁试剂的制备
将油浴加热到设定的温度后,按物料配比于N2保护下向 250 mL四颈烧瓶中加入镁粉、溶剂和PCT。保温加热,至物料开始回流时加入催化量的碘,缓慢滴加PCT,加毕继续回流,TLC监测反应至终点。反应结束时加冰水淬灭反应。
1.3.3 分析方法
淬灭后的反应液油水分离,水相以乙酸乙酯萃取(30 mL×3),合并至有机相。以气相色谱分析,氯代苯为内标物,通过相应的内标曲线计算转化率和收率。
色谱条件,RESTEK-5Ф0.25 mm×30 m玻璃毛细管柱,FID检测器;汽化、检测温度,280 ℃;柱流速,0.58 mL/min;总流速,50 mL/min;吹扫流速,5 mL/min;程序升温,70 ℃(2 min)~20 ℃/min~280 ℃(1 min) ;进样量 0.2 μL。
2 结果与讨论
2.1 THF单一溶剂体系中的合成反应
采用THF单一溶剂进行反应,在综合考察不同条件下的原料转化率及产物选择性、收率后,得到最佳反应条件为:n(镁粉)∶n(PCT)=1.2∶1,反应温度70 ℃,反应时间2.5 h,镁粉占溶剂的质量体积分数为0.04 g/mL。该条件下得到的产率为91.6%,选择性为95.0%。该最佳工艺条件与文献[9]报道结果相似,但缩短了反应时间,提高了产物的选择性和收率。
2.2 MeTHF-THF混合溶剂体系中的合成反应
2.2.1 混合溶剂不同配比的筛选
采用MeTHF-THF混合溶剂研究了对甲基苯基氯化镁的合成,固定摩尔比 nMg∶nPCT=1.2∶1,反应温度80 ℃,反应时间1.5 h,镁粉占溶剂的体积质量分数为0.04 g/mL,筛选考察了不同的溶剂配比对反应的影响,结果见表1。
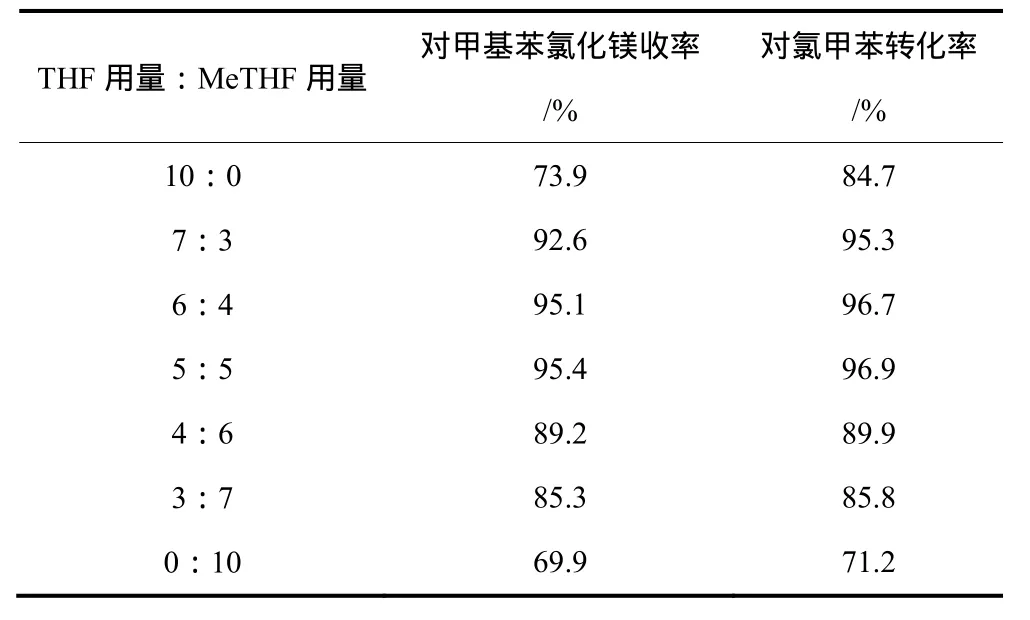
表1 混合溶剂的比例对产物收率和原料转化率的影响
从表 1可以看出,当 MeTHF的体积分数VMeTHF≤50%时,原料转化率、产物收率随着MeTHF含量的加大而上升,当 VMeTHF>50%时,原料转化率、产物收率随着MeTHF含量的加大而降低。THF和MeTHF都是环状醚,分子中氧原子较链状醚更为外露,这样氧原子较易提供孤对电子参与稳定对甲苯基氯化镁,因此反应较易引发。一方面,与MeTHF相比,THF的吸水性强,虽然用作溶剂的THF已经过脱水处理,但由于反应装置无法做到绝对严密,在反应过程中THF仍然会逐渐吸收空气中的水分,对反应活性和产物选择性产生影响;因此,当VMeTHF>50%时,原料转化率、产物收率随着THF含量的降低而上升。另一方面,与THF相比,MeTHF分子中2-位甲基存在位阻效应,且对产物的溶解性较差,本文的格氏反应底物PCT活性较低,因而当反应体系呈高含量的MeTHF溶剂时,会对反应活性和反应速率产生明显影响;因此,VMeTHF≥50%时,原料转化率、产物收率随着MeTHF含量的加大而降低。一般地,市售MeTHF含水率较低,可直接用于格氏反应,简化了操作;加之MeTHF沸点较高,可实现更高的溶剂的回收率、反应的安全性[13]。应用THF-MeTHF混合溶剂体系进行本文的格氏反应则结合了两者的优点,可同时获得良好的反应活性和产物选择性。本文兼顾反应速率和产物选择性,混合溶剂中两者的配比优选为体积比1∶1。
2.2.2 物料配比对格氏反应的影响
在反应温度80 ℃,反应时间为1.5 h,VTHF∶VMeTHF=1∶1,镁粉占溶剂的体积质量分数为 0.04 g/mL的条件下,改变PCT用量,考察了物料配比对反应的影响,结果见图1。

图1 物料配比对目标产物和副产物收率的影响
由图1可见,随着镁粉用量的增加,主产物收率上升并逐渐趋于平缓,副产物4, 4'-二甲基联苯收率下降并逐渐趋于平缓,当 n(镁粉)︰n(PCT)≥1.1∶1时,产物收率变化不大,最大值为95.6%。其可能的原因为:当PCT过量时,生成的对甲基苯基氯化镁与原料 PCT继续反应的概率增加,促进了副反应的进行,使主产物收率较低,副产物多;随着镁粉用量的增加,上述副反应的发生率逐渐降低,对甲基苯基氯化镁收率增加;当镁粉用量过量10%以上后,PCT已接近完全转化,继续增加镁粉的用量对提高主产物收率、降低副产物生成率不再有明显的改善作用。本文与传统单一THF溶剂工艺[7-8]相比,最佳物料配比相近,产物收率有显著提高。与文献报道的混合溶剂工艺的最优原料摩尔比1.2∶1,最高产物收率81.1%相比[9-10],减少了镁粉的用量,提高了产物收率。
2.2.3 反应温度对格氏反应的影响
在n(镁粉)︰n(PCT)为1.2∶1,反应时间为1.5 h,VTHF∶VMeTHF为 1∶1,镁粉占溶剂的体积质量分数为0.04 g/mL的条件下,考察了反应温度的影响,结果见图2。

图2 反应温度对目标产物和副产物收率的影响
本文采用THF-MeTHF混合溶剂,与THF单一溶剂合成工艺相比[7-8],可选择更高的反应温度。由图2可见,随着反应温度的上升,产物收率先上升后下降,在 80 ℃时收率达到最大值,主要副产物4, 4'-二甲基联苯收率逐渐上升。可能的原因为,当温度较低时,反应的动力学速率低,原料转化率成为制约产物收率上升的主要因素,此时主副产物的选择性基本稳定;随着反应温度的上升,体系中活化分子数增加,反应速率加快,原料转化率增加;当温度过高时,回流加快,混合溶剂对格氏试剂的溶剂度降低,产物稳定性降低,副反应速率增加,使主产物选择性急剧降低,产物收率降低。因此,最适宜的温度在80 ℃左右。
2.2.4 反应时间对格氏反应的影响
在 n(镁粉)︰n(PCT)为 1.2∶1,反应温度为80 ℃,VTHF∶VMeTHF为 1∶1,镁粉占溶剂的体积质量分数为0.04 g/mL的条件下,考察了反应时间的影响,结果见图3。

图3 反应时间对目标产物和副产物收率的影响
由图3可见,随着反应时间增加,对甲苯基氯化镁的收率先迅速增加,至反应1.5 h后逐渐下降,副产物4, 4'-二甲基联苯的收率逐渐增加,最佳反应时间为1.5 h。分析其原因为,反应时间过短时原料转化率低,反应不完全;因格氏试剂性质活泼,反应时间过长会增加产物与原料及产物间的接触时间,使副反应加剧,产物收率下降。适宜的反应时间应能满足PCT和镁粉充分混合和反应的需要,并尽可能减少副反应的发生。与传统单一THF溶剂工艺[7-8]相比,本文工艺的最佳反应时间较短,反应效率明显提高。
2.2.5 溶剂用量对格氏试剂制备的影响
n(镁粉)∶n(PCT)为 1.2∶1,反应温度 80 ℃,反应时间1.5 h,VTHF∶VMeTHF为1∶1,在此条件下,改变混合溶剂的用量,考察了溶剂用量对反应的影响,结果见图4。
由图4可见,溶剂用量对主副反应产物收率影响很大,随着溶剂用量的增加,主产物收率先逐步上升然后迅速下降,副反应产物收率先微微上升然后转为缓缓下降。分析其原因为,当溶剂量较小时,体系溶解性差,固液两相传质较差,格氏反应产物的进一步偶联反应加剧,原料转化率和主产物选择性均不高;当溶剂量增加到一定值时,体系溶解性显著改善,偶联反应发生率降低,原料转化率和主产物选择性均有所提高;溶剂量过大时,主产物自身偶联副反应发生率继续降低,副产物生成量进一步减少,但是反应体系的过渡稀释会导致原料分子之间碰撞概率降低,造成转化率降低,收率下降。兼顾原料转化率、主副产物选择性、溶剂成本与合成操作,本文优选混合溶剂总体积为镁粉占混合溶剂的体积质量分数为0.04 g/mL。
3 结 论

图4 混合溶剂总体积对目标产物和副产物收率的影响
(1)以镁粉和廉价的PCT为原料,在MeTHF-THF混合溶剂体系中合成了对甲基苯基氯化镁,为该格氏试剂的生产应用提供了可行的技术路线,可显著降低2-氰基-4'-甲基联苯的合成成本。
(2)研究并优化了制备对甲基苯基氯化镁的工艺条件,当镁粉PCT物质的量比为1.1∶1、反应温度80 ℃、混合溶剂中THF和MeTHF的体积比为1∶1,镁粉占溶剂的体积质量分数为0.04 g/mL,反应1.5 h时,对甲苯基氯化镁收率最高达到95.4%。与传统工艺相比,降低了原料成本,缩短了反应时间,降低了装置无水性要求,操作简便,收率较高,溶剂回收利用率高。
(3)氧气存在条件下,会产生杂质 4-甲基苯酚,通入干燥氮气作保护气并严格控制装置气密性可完全的消除该杂质。4, 4'-二甲基联苯是影响对甲基苯基氯化镁收率的主要杂质,目前的研究还不能完全消除该杂质,但可以通过在THF-MeTHF混合溶剂中调节一系列反应条件来控制其生成量,在该混合溶剂中 4,4'-二甲基联苯的产率低于在 THF单一溶剂中的产率。
[1]付春. 邻甲苯基苯甲腈的合成及其在心血管药物中的应用与前景[J]. 化工中间体,2004,1(3):17-19.
[2]Asai T,Kumai S. Preparation of biphenyl compounds:JP,08109143[P]. 1996-04-30.
[3]Kagcyama H. Method for producting an asymmetric biaryl derivative:EP,571770[P]. 1993-12-01.
[4]Matinez B V,Garcia A,Burgos C,et al. Synthesis of biaryls via intermolecular radical addition of heterarly and aryl bromides onto arenes[J]. Org. Lett.,2000,2(2):3933-3935.
[5]Grushin V V,Alper H. Transformation of ehloroarenes,catalyzed by transition-metal complexes[J]. Chem. Rev.,1994,94(4):1047-1062.
[6]Xia G M,Fang Q,Xu X G,et al. Two-photo excited fluore acence of bithiophene derivatives[J]. Chin. Chem. Lett.,2003,14(5):657-660.
[7]Todd K. The N,N-dialkyl aryl o-sulfamate as a new directed metalation group and cross-coupling partner for grignard reagents[J].Organic Letters,2005,7(13):2519-2522.
[8]Dai C,Fu G C. The first general method for palladium-catalyzed negishi cross-coupling of aryl and vinyl chlorides:Use of commercially available Vd(P(t-Bu)3)2as a catalyst[J]. J. Am.Chem. Soc.,2001,123(12):2719-2724.
[9]李有桂,吴祥瑞,何伟. 2-氰基-4'-甲基联苯的合成研究[J]. 化学研究与应用,2010,22(7):62-67.
[10]肖永鹏,何琦,陈宝珍. 制备 2-腈基联苯衍生物的方法:中国,1528740A[P]. 2004-09-15.
[11]Dietmar S. The grignard reagents[J]. Organometallics,2009,28(6):1598-1605
[12]Vittorio P,Pilar H,Laura C,et al. 2-Methyltetrahydrofura n(2-MeTHF):A biomass-derived solvent with broad applicati on in organic chemistry[J]. Chem. Sus. Chem.,2012,5(8):1369-1379.
[13]陈学玺,于航. 2-甲基四氢呋喃的回收工艺研究[J]. 精细石油化工进展,2010,11(11):30-33.

