非酒精性脂肪肝与代谢综合征组分的中西医发病机制相关性
庞晓瑜 郭卉
·综述·
非酒精性脂肪肝与代谢综合征组分的中西医发病机制相关性
庞晓瑜 郭卉
非酒精性脂肪肝(NAFLD)是21世纪全球重要的公共健康问题之一,其发病率逐年增高;并且越来越多的调查及报道显示其发病与代谢综合征(MS)相关组分关系密切。因此本文通过查找近年的相关文献,并参考出版教材,从中西医两个角度,归纳总结NAFLD的发病机制,及其与MS相关组分在发病过程中的相互联系。重点关注胰岛素抵抗(IR)所起的核心作用;寻找NAFLD与MS在发病过程中的相似点和关键环节。
非酒精性脂肪肝(NAFLD);代谢综合征(MS);胰岛素抵抗(IR);发病机制;综述
非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)是一种与胰岛素抵抗(IR)和遗传易感密切相关的代谢应激性肝脏损伤,其病理学改变与酒精性肝病(ALD)相似,但患者无过量饮酒史。疾病谱包括:非酒精性单纯性脂肪肝(NAFL)、非酒精性脂肪性肝炎(NASH)、肝硬化及其相关肝细胞癌[1,2]。
近年越来越多的流行病学报道指出,NAFLD与MS在发病中有密切关联。如汤益明等[3]提出:“非酒精性脂肪肝可视为代谢综合征的肝脏表现,90% NAFLD 至少有一种MS的组分,约1/3的NAFLD患者含所有的MS组分。” 高鑫[4]提出:“NAFLD作为MS的新组分或是胰岛素抵抗在肝脏的表现,同时存在肝脏胰岛素抵抗和周围胰岛素抵抗。开展NAFLD的早期诊断和早期筛查,对防治2型糖尿病和动脉粥样硬化性心血管疾病有着非常重要的意义。” 墨西哥Castro-Martínez MG 等[5]指出:“每10位MetS患者中就有8位发生NAFLD,该观察结果需要引起高度重视。能够降低MetS发生风险的健康措施对预防NAFLD将产生重要影响。”等等。可见NAFLD与MS各组分关系密切,因此本文将分中西医两部分阐述NAFLD与MS各组分在发病机制上的相关性。
1 NAFLD与代谢综合征组分的西医发病机制相关性
NAFLD的发病机制复杂,目前被广泛接受的机制理论为Day和James提出的“二次打击(two hits)”假说:初次打击主要指胰岛素抵抗(insulin resistance, IR)引起的肝细胞内脂质沉积;第二次打击主要为氧化应激和脂质过氧化[6]。
1.1胰岛素抵抗的形成 胰岛素抵抗(Insulin Resistance,IR)通常是指机体胰岛素作用的靶器官对胰岛素的生理作用的反应性或敏感性下降,即正常剂量的胰岛素产生低于正常生物学效应的一种状态[7]。
由于高脂饮食、酒精摄入等原因造成的热量摄入过多,以及久坐少动造成的热量消耗减少,使得机体能量过剩,脂肪在大网膜及腹腔堆积,日久形成腹型肥胖。其脂肪细胞增生、脂肪体积增大,TNF-α等细胞因子表达增多,从而促进脂肪分解,脂解速率及量明显增加,脂肪代谢紊乱,造成大量FFA入血引起高FFA血症[8]。同时,脂肪在胰岛的堆积,使β细胞功能下降,胰岛素分泌异常或分泌减少;另外,脂肪细胞肥大,使得单位面积INS受体减少,组织对INS敏感性降低,发生IR。
1.2胰岛素抵抗形成NAFLD 胰岛素对脂肪代谢的作用主要为促进脂肪合成和抑制脂肪分解。IR时胰岛素抑制脂肪分解的作用减弱,导致脂肪动员增强,释放甘油及游离脂肪酸(FFA)增多。前者在肝甘油激酶作用下,转变为3-磷酸甘油,然后脱氢生成磷酸二羟丙酮,循糖代谢途径进行分解或转变为糖[9];后者由于脂肪酸从内脏组织动员远远多于皮下脂肪,FFA可直接由门静脉入肝,形成肝细胞内FFA的堆积,经β氧化,生成过多的脂源性乙酰CoA。
乙酰CoA的增加刺激胰岛β细胞分泌INS,另外在IR状态下,INS效应低下,为了INS作用的减低,防止血糖升高,胰岛β细胞出现INS代偿性分泌增多,引发高胰岛素血症。
高胰岛素血症能增加糖降解,同时引起固醇调节元件结合蛋白-1 c过量表达而增加脂肪酸的合成,又可减少APO-B100的合成,导致脂类物质合成增多,外运障碍;加之NAFLD患者不节的饮食和生活习惯,脂肪及糖类摄入量过多,磷脂的摄入不足或合成障碍,都会导致肝脏中TG生成增多,VLDL合成与TG合成速度不相适应,造成TG在肝脏蓄积引起脂肪肝[10,11]。
1.3胰岛素抵抗与MS相关组分的发生 高胰岛素血症通过刺激交感神经兴奋,刺激α1受体,使AngⅡ水平增加,LPL降低,血浆中CM和VLDL清除减慢、HDL合成原料减少;β肾上腺素能激活脂肪组织激素敏感脂肪酶,脂肪组织动员过多而增加FFA向肝脏流向,TG产生增多;同时,高胰岛素血症时患者血清和淋巴液Apo AI浓度显著降低,LCAT活性下降,HDL成熟减慢。以上共同造成了血浆TG升高,HDL水平下降,形成高脂血症[12]。
此外,高胰岛素血症一方面增加交感神经活性,致血中儿茶酚胺水平增加;另一方面兴奋肾脏Na+转运系统 的Na+-H+逆向交换,促使近曲或远曲小管重吸收Na+增加,引起水钠潴留;同时高胰岛素血症增加内皮素释放,减少血管舒张性前列腺素的合成,影响血管舒张功能,增强血管组织和醛固酮对AngII的反应性,使血管收缩和水钠潴留的效应加强。并且,IR及及继发的高胰岛素血症改变细胞膜阳离子流量,使平滑肌细胞膜钠泵发生改变,Na+/K+ATP酶,Ca2+ATP酶和Na+/H+逆向转录加强,细胞内Na+升高,并通过逆向转运机制,使细胞内Ca2+升高,血管平滑肌细胞对儿茶酚胺和血管紧张素的敏感性增强,加强血管收缩,同时,Na+-H+逆向转运活性升高,使细胞内PH升高,细胞内碱中毒,细胞增生加速,血管平滑肌肥大,阻力增加。以上共同形成了高血压[13]。
同时,高胰岛素血症加剧了葡萄糖利用障碍,使IR进一步加重,β细胞因长期过度代偿而衰竭,INS分泌不足,产生Ⅱ型糖尿病(见图1)。
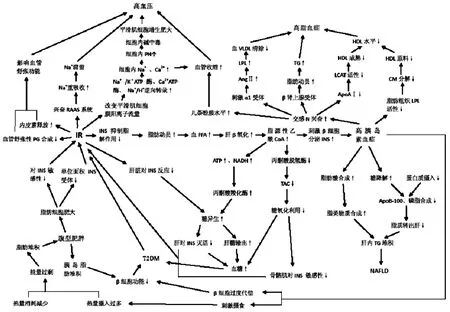
图1 NAFLD与代谢综合征组分的西医发病机制
2 NAFLD与代谢综合征组分的中医学病因病机相关性
脂肪肝在中医学中称为“肝癖”,是因肝失疏泄,脾失健运,痰浊淤积于肝,以右胁胀痛,胁下肿块为主要表现的积聚类疾病,主要分为脾虚湿阻、痰浊内蕴、肝肾阴虚、瘀血阻络等证型。究其发病根源是由于过食肥甘厚味,或劳逸失度,损伤脾胃,使得脾失健运,致痰浊内生。病位在肝、脾。
而代谢综合征(MS)在中医学中尚无统一的病名,根据其发病和临床特征,主要归属于“肥胖”、“积聚”、“消渴”、“胸痹”、“眩晕”、“头痛”、“痰饮”等范畴。其发病主要原因为饮食不节,劳逸过度,情志失调,年老体衰,禀赋不足等。病理因素以“痰湿”、“血瘀”为主。病位涉及肝、脾、肾。
可见,脂肪肝与代谢综合征在病因病机上都存在着高度一致性。二者均与饮食不节、劳逸过度等不良生活方式有关;并且在病理演变中均以脾失健运,肝失疏泄为病机核心,经过聚湿生痰、气机不利、痰阻血瘀,以及积热内蕴、气郁化火等病理变化,继而产生肥胖、食积、消渴、头痛眩晕等证,是互相影响,互为因果的。(见图2)
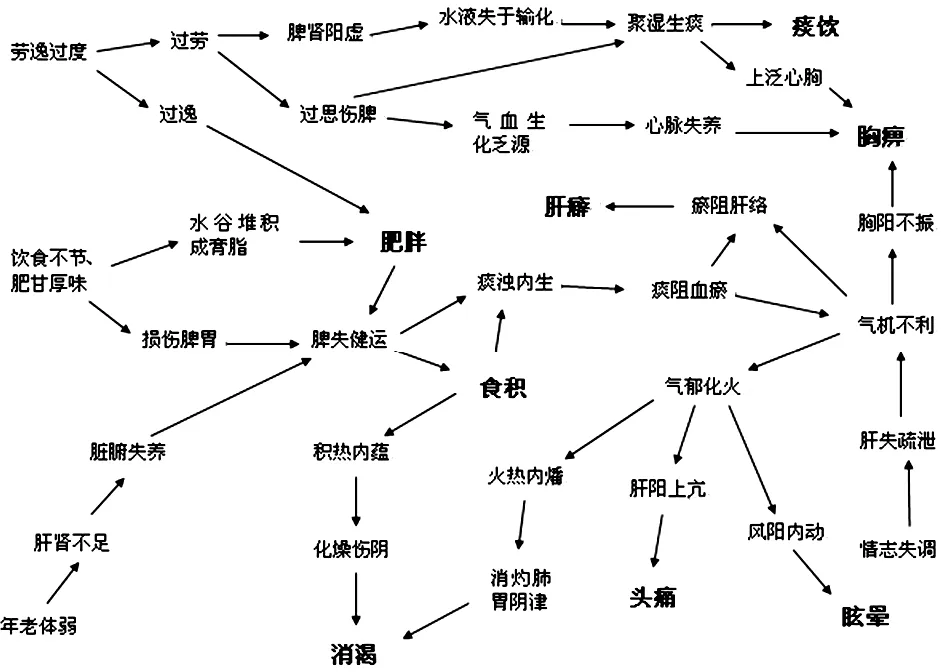
图2 NAFLD与代谢综合征组分的中医学病因病机
3 小结与展望
NAFLD是由于非过量饮酒导致的脂肪在肝细胞中过度堆积所形成的肝脏脂肪代谢障碍,是代谢综合征的重要组分,也在一定程度上预示着代谢综合征相关疾病的发病倾向。二者在中西医发病机制上均有高度相关性。
从西医学角度,NAFLD的发病机制主要包括胰岛素抵抗(IR)和脂质过氧化损伤两大方面,而IR作为NAFLD发病过程中的焦点环节以及MS的重要组分,也因此成为目前两疾病在调脂治疗中的重要关键点。2010年<<指南>>中亦指出:“治疗NAFLD的首要目标为改善IR,防治代谢综合征。”并且将调整生活方式放在了重要位置[14]。
从祖国医学的角度,在 “整体观念”的指导思想下,NAFLD与MS具有相近甚至相同的发病主因,均与不良的生活方式关系紧密,日久则使一系列病理表现相继发生,因此既要整体治疗,又要预见疾病发展的趋势,做到“上工治未病”。
[1] Farrell GC, Larter CZ. Nonalcoholic fatty liver disease: from steatosis to cirrhosis. Hepatology,2006,43(2 Suppl 1):S99-S112.
[2] de Alwis NM, Day CP. Non-alcoholic fatty liver disease: the mist gra-dually clears. J Hepatol,2008,48 Suppl 1:S104-S112.
[3] 汤益明,吴跃进,胡建平.中西医结合防治代谢综合征.实用中西医结合临床,2012,12(1):58-60.
[4] 高鑫.非酒精性脂肪性肝病与代谢综合征.中国实用内科杂志,2011,31(9):664-667.
[5] Castro-Martínez MG, Banderas-Lares DZ,Ramírez-Martínez JC,et al. Prevalence of nonalcoholic fatty liver disease in subjects with metabolic syndrome. Cirugia Y Cirujanos, 2012,80 (2):128-33.
[6] 王吉耀.内科学.第2版.北京:人民卫生出版社,2010:517.
[7] 崔常清.胰岛素抵抗的机制与临床研究进展.中国煤炭工业医学专业,2012,15(7):1119-1121.
[8] 王翔凌.游离脂肪酸与代谢综合征.中国老年保健医学,2004,2(4):42-46,48.
[9] 万福生,揭克敏.医学生物化学.第1版.北京:科学出版社,2010:183.
[10] 张玲霞,王永怡.脂肪肝与代谢综合征-防治与用药指南.第1版.北京:人民军医出版社,2010:43-47.
[11] 王继峰.生物化学.北京:中国中医药出版社,2004:176.
[12] 叶平.血脂的基础与临床.第1版.北京:人民军医出版社,2002:320.
[13] 叶平.血脂的基础与临床.第1版.北京:人民军医出版社,2002:321.
[14] 中华医学会肝病学分会脂肪肝和酒精性肝病学组. 非酒精性脂肪性肝病诊疗指南(2010年修订版). 现代医药卫生,2011,27(5):641-644.
PathogenesisrelationsbetweenNAFLDandthecomponentsofMS:fromTCMandwesternmedicineAspects
PANGXiao-yu,GUOHui.
DepartmentofclinicalpracticeteachingofTianjinUniversityofTCM,HepatologyDepartmentofFirstTeachingHospitalofTianjinUniversityofTCM,Tianjin300193,China
Nonalcoholic fatty liver disease (NAFLD) is one of the important public health problems in the world in the 21 st Century, with its incidence increasing year by year. More and more investigations and reports showed that there’s closely relationship between NAFLD and the components of metabolic syndrome (MS).Therefore,by looking up the related documents in recent years as well as referring to the materials published, from two aspects of traditional Chinese medicine and Western medicine, we summarized the pathogenesis of NAFLD and MS, and their mutual relations. Meanwhile, we focused on the core role of insulin resistance (IR)and analyzed the key links and similarities in the pathogenesis process of NAFLD and MS.
Nonalcoholic fatty liver disease (NAFLD);Metabolic syndrome (MS);Insulin resistance (IR);Pathogenesis;Review
300193 天津中医药大学临床实训教学部(庞晓瑜);天津中医药大学第一附属医院肝胆科(郭卉)
郭卉 E-mail:Guohui3105@163.com

