红土镍矿脱水机理及还原过程动力学
张建良,毛 瑞,黄冬华, ,邵久刚,李峰光
(1.北京科技大学 钢铁冶金新技术国家重点实验室,北京 100083;2.北京科技大学 期刊中心,北京 100083)
镍具有抗氧化、抗腐蚀、耐高温、延展性好、强度高等优点,被广泛用于生产不锈钢、高温合金钢、燃料电池等关键材料,是一种重要的战略性金属[1]。世界上可供开采的镍资源中有30%~40%(质量分数)是硫化镍矿,60%~70%(质量分数)是红土镍矿。目前,约有 56%(质量分数)的镍是从硫化镍矿中提取的,但是硫化镍矿资源正面临着逐渐枯竭的局面,而红土镍矿资源丰富,且采矿成本低,因此,红土镍矿将是未来镍的主要来源,加快红土镍矿的选冶研究,已成为目前国际上的重大冶金课题[2-3]。
目前,煤基直接还原工艺处理红土镍矿是红土镍矿冶炼的一个非常重要的方法,而红土镍矿的含水量很高,一般含有25%~30%(质量分数)的游离水和结晶水,使高温还原熔炼过程能耗过高,而且将导致生产过程无法顺利进行,在冶炼过程中需要对其进行干燥处理,因此,研究红土镍矿加热还原过程的反应机理对于红土镍矿冶炼工艺的改进和创新尤为重要。目前,已有很多学者在等温和非等温条件下对红土镍矿脱水机理和固体碳还原铁、镍氧化物的机理进行了研究。在红土镍矿脱水机理研究方面,谢皓等[4]对菲律宾红土镍矿进行了 XRD分析和热分析,结果表明,该原料中以含有结晶水和羟基的铁镁硅酸盐矿物为主,矿物中含有少量的铝酸盐类矿物。袁煕志等[5]研究了时间、温度对干燥和焙烧过程红土矿脱水效果的影响,发现当选取干燥温度为600 ℃、干燥时间为40 min、焙烧温度为800 ℃、焙烧时间为80 min时,红土矿中的游离水和结晶水均能被彻底脱除。刘燕等[6]对红土镍矿进行了DSC分析,将105 ℃下烘干并冷却的红土镍矿,从常温加热至1 000 ℃,质量损失为15%,其中 5.01%仍为物理水,结晶水含量低于 9.99%,结构水含量低于 2.03%。国内外学者对铁、镍氧化物的还原机理进行了大量的研究,固体碳还原铁氧化物的控速环节可能为气相扩散[7-8]、碳的气化反应[9]、界面或局部反应[10]等。SARKISYAN[11]研究了等温条件下用碳和 H2还原 Fe2O3-NiO系的动力学,发现含碳Fe2O3-NiO混合物的还原反应独立进行,无明显的交叉反应,还原产物为一系列的固溶体。CORES等[12]研究了用煤粉和H2还原NiO-Fe3O4的机理,发现还原分两步进行,第一步是NiO和NiFe2O4的还原,然后是铁氧化物的还原。ABDEL-HALIM 等[13]研究了800~1 100 ℃下固体碳还原Fe2O3-NiO纳米复合材料生成Fe-Ni合金的动力学,发现随温度和NiO含量的提高,铁氧化物的还原速率增大,在低温下还原速率由碳的气化反应控制。李博等[14]采用非等温热分析法研究了200~950 ℃下煤粉还原红土镍矿的动力学,发现还原过程分为200~500 ℃和500~950 ℃两个阶段,反应活化能分别为171.91和52.75 kJ/mol,反应速率由碳的气化反应控制。
近年来,红土镍矿冶炼镍铁工业在国内发展迅速,但对红土镍矿脱水机理和还原动力学系统的研究却不多。为此,本文作者采用热分析方法对红土镍矿的脱水机理进行分析,同时对红土镍矿的还原过程动力学进行研究,为红土镍矿火法冶炼工艺的改进提供理论参考。
1 实验
1.1 实验原料
实验所用红土镍矿来自印度尼西亚,其化学成分如表1所列。该矿石中铁、镍的含量较低,SiO2、MgO的含量较高,碱性组分CaO的含量低,S、P等有害杂质含量较低,属于硅镁型镍矿。
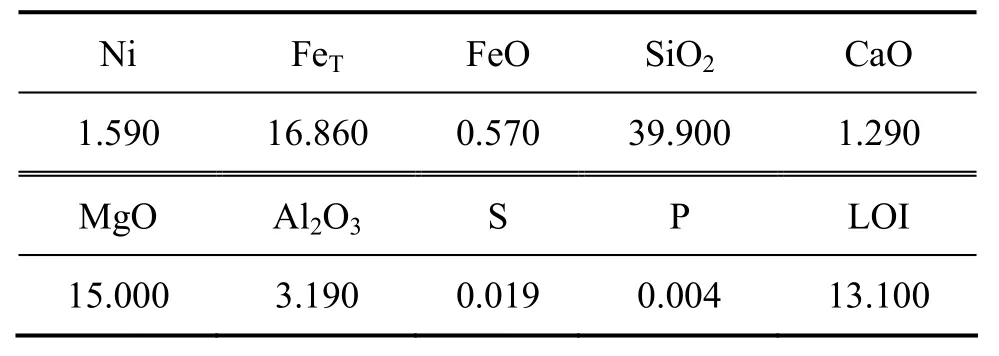
表1 红土镍矿的化学成分Table 1 Chemical composition of laterite ore (mass fraction,%)
对红土镍矿粉进行X射线衍射分析,其结果如图1所示。由图1可以看出,该红土镍矿的主要物相有斜纤蛇纹石(Mg3Si2O5(OH)4)、镍纤蛇纹石(Ni3Si2O5-(OH)4)、暗镍蛇纹石((Ni,Mg)3Si2O5(OH)4)、叶蛇纹石((Mg,Fe)3Si2O5(OH)4)、针铁矿(FeO(OH))、赤铁矿(Fe2O3)、高岭石(Al2Si2O5(OH)4)和石英(SiO2)等。研究表明,镍主要分布在硅酸盐类矿物及针铁矿中,镍在硅酸盐矿物中主要取代镁,在针铁矿中主要取代铁;铁主要分布在针铁矿、赤铁矿和硅酸盐类矿物中;脉石矿物主要有蛇纹石、高岭石和石英。由于蛇纹石和高岭石都是含水硅酸盐矿物,同时针铁矿中含有结晶水,因此,该红土镍矿中结晶水含量较高[15-16]。

图1 红土镍矿的XRD谱Fig.1 XRD pattern of laterite ore
1.2 实验设备和方法
将红土镍矿置于恒温干燥箱中在105 ℃下烘干3 h,充分脱除其中的吸附水,经密封制样机粉碎至 74 μm(占80%以上)。将红土镍矿粉和石墨粉(石墨粉粒度为178 μm占95%左右)按C与O摩尔比n(C)/n(O)为1.2(矿石中氧含量按氧化镍和铁氧化物中的氧含量计算)进行配碳,充分混匀,置于干燥箱中备用。采用TGA-SDTA 851e热重/差热同步分析仪(瑞士 Mettler Toledo公司制造)对红土镍矿和红土镍矿-石墨混合物进行热分析。为了消除脱水对还原过程的影响,同时对预焙烧红土镍矿(马弗炉中900℃下焙烧2 h)和石墨混合物进行热分析,具体实验方案如表2所列。

表2 Ar气氛下红土镍矿与石墨混合物的热分析实验方案Table 2 Thermal analysis experiment scheme of graphitelaterite ore mixture
分别称取约20 mg样品置于Al2O3坩埚中,将坩埚置于微机差热天平中,在Ar流速为30 mL/min、升温速率为10 ℃/min的条件下升温至1 300 ℃,由计算机绘制出TG、DTA和DTG曲线,再分别对各曲线进行分析和处理。
2 结果与讨论
2.1 红土镍矿脱水过程
图2所示为红土镍矿TG、DTA和DTG曲线。从图2(a)所示TG曲线可以看出,红土镍矿在升温过程中将出现4个质量损失台阶,第一个质量损失台阶的起始温度为47 ℃,DTG曲线的峰顶温度为78 ℃,伴随DTA曲线有明显的吸热,对应于红土镍矿中自由水的脱除。第二个质量损失台阶的起始温度为250 ℃,峰顶温度为272 ℃,同时伴随有吸热的发生,对应于针铁矿(FeO(OH))的分解反应,形成赤铁矿。CARLSON和SCHWERTMANN[17]报道高结晶针铁矿的脱羟基反应温度为385 ℃。细颗粒、低结晶针铁矿的分解温度通常低于粗颗粒、高结晶针铁矿的分解温度[18]。第三个质量损失台阶的起始温度为533 ℃,峰顶温度为583 ℃,对应于高岭石及蛇纹石的脱羟基反应。第四个质量损失台阶的温度区间为755~864 ℃,峰顶温度为826 ℃,对应于蛇纹石类矿物的第二段脱羟基反应[19-20]。当温度超过864 ℃后,TG曲线还表现出缓慢的质量损失,在864~1 300 ℃区间内的质量损失为1.01%。
从图2(b)可见,DTA曲线在820 ℃处有一较弱的放热峰,与镁橄榄石(蛇纹石的脱水产物)的结晶及其调整作用有关[21]。在1 058 ℃有一个明显的吸热峰,这是由于发生了镁橄榄石转变为顽火辉石的矿相转变[22]。
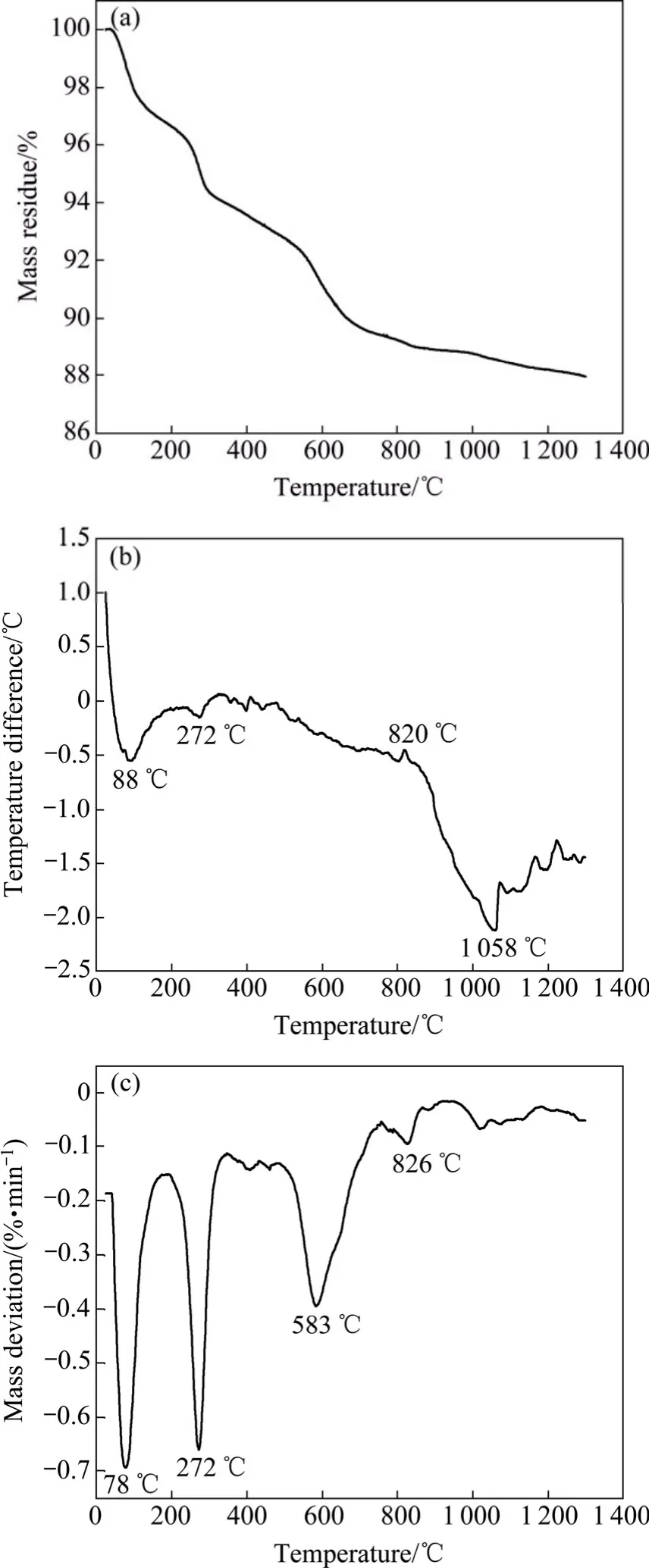
图2 红土镍矿粉的TG、DTA和DTG曲线Fig.2 TG (a), DTA (b)and DTG (c)curves of laterite nickel ore
图3所示为红土镍矿在 900 ℃下焙烧 2 h后的XRD谱。由图3分析可知,焙烧后产物的主要物相有赤铁矿(Fe2O3)、石英(SiO2)、镁橄榄石(Mg2SiO4)、顽火辉石(MgSiO3)、镍镁硅酸盐((Ni,Mg)2SiO4)和偏高岭石(Al2Si2O7),表明在此条件下,红土镍矿中的水已被全部脱除。针铁矿脱羟基后形成赤铁矿:
2FeO(OH)=Fe2O3+H2O
高岭石脱水后生成偏高岭石:

图3 红土镍矿在900 ℃焙烧2 h后的XRD谱Fig.3 XRD pattern of laterite ore calcined at 900 ℃ for 2 h
Al2Si2O5(OH)4=Al2Si2O7+2H2O
蛇纹石分解生成镁橄榄石和顽火辉石:
Mg3Si2O5(OH)4=Mg2SiO4+MgSiO3+2H2O
2.2 红土镍矿的还原过程
按表2所列的实验方案,在Ar 气氛下通过热重/差热同步分析仪对红土镍矿与石墨混合物进行热分析实验,各方案对应的 TG、DTA和 DTG曲线如图4所示。
从图4可以看出,700℃之前,红土镍矿和红土镍矿-石墨混合物的TG和DTG曲线基本吻合,说明700℃之前只发生红土镍矿的脱水反应,吸附水的脱除、针铁矿的分解、高岭石及蛇纹石的分解是最主要的反应。而对于预焙烧红土镍矿-石墨混合物,由于预焙烧温度900 ℃已高于失水温度,水分已被充分脱除,故在该过程中,质量基本上没有变化。预焙烧红土镍矿-石墨混合物和红土镍矿-石墨混合物从约700 ℃开始出现缓慢的还原,当温度高于864 ℃时,由脱羟基而引起的质量损失较小,故红土镍矿-石墨混合物与预焙烧红土镍矿-石墨混合物的 TG曲线相近。在700~864 ℃区间,红土镍矿-石墨混合物的质量损失由还原反应和脱羟基反应共同决定。综合红土镍矿的TG和DTG曲线可将红土镍矿还原过程分为3个阶段,对应的温度区间分别如表3所列。
2.3 还原过程的动力学分析
石墨还原红土镍矿的转化分数定义为

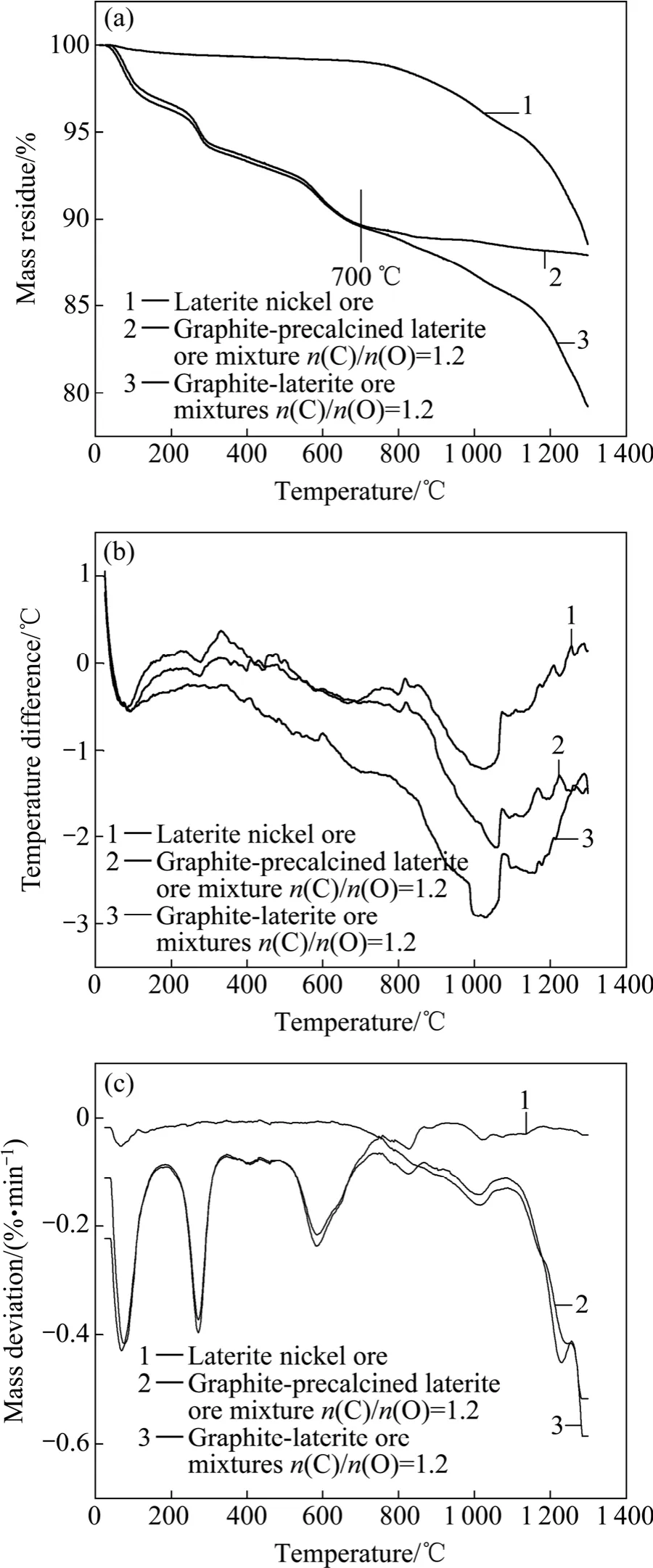
图4 红土镍矿、石墨-预焙烧红土镍矿和红土镍矿-石墨混合物的TG、DTA和DTG曲线Fig.4 TG (a), DTA (b)and DTG (c)curves of laterite nickel ore, graphite-precalcined laterite ore mixture and graphitelaterite ore mixtures
式中:m0为样品的初始质量(g),由于红土镍矿含有结晶水,升温过程中会发生脱水反应,并且由前文的分析可知,红土镍矿从700 ℃才开始发生还原反应,为了最大限度地排除脱水的影响,此处取700 ℃时样品的质量为初始质量;mt为t时刻样品的质量(g);m∞为还原终了时样品的质量(g)。

表3 红土镍矿-石墨混合物还原反应各阶段的温度区间Table 3 Temperature range of reduction reaction for graphite-laterite ore mixture
图5所示为预焙烧红土镍矿和红土镍矿被石墨还原的转化分数—温度关系。在还原反应的第一阶段,对于红土镍矿-石墨混合物,由于红土镍矿被还原过程中同时伴随着结晶水的脱除,故红土镍矿的转化分数大于预焙烧红土镍矿的转化分数。进入第二阶段后,结晶水已经基本脱除,两者的转化分数基本接近。

图5 预焙烧红土镍矿-石墨混合物和红土镍矿-石墨混合物的转化分数—温度曲线Fig.5 Conversion fraction—temperature curves of graphitelaterite ore mixture and graphite-precalcined laterite ore mixture
若非均相固体反应的动力学方程为

COATS和 REDFERN[23]用积分的方法得出非等温热重实验的表观活化能的计算公式为
当n≠ 1 时,

当n= 1时,

式中:α为固体反应物的转化分数;β为升温速率;t为反应时间;k为速率常数;n为反应的表观级数;T为反应温度;A为指前因子;E为反应的表观活化能;R为摩尔气体常数。
对于一般的反应温区和大部分E值,可近似认为上述两个表观活化能的计算公式中等号右边第一项的值为与温度无关的常数。当n≠ 1时,以对 1/T作图;当n= 1时,以对1/T作图,都能得到一条直线,其斜率为~E/R。
该法可适当推广应用于其他遵循动力学方程的非等温反应,

式中,f(α)表示速率微分式。
由Arrhenius公式得

已知升温速率为β,则

以f(α)取代由方程(2)中的(1-α)n,结合式 (6)和(7),对f(α)进行积分得

式中:g(α)是f(α)的积分函数。对式(8)两边取对数,得

式(9)中右边第一项可近似视为与温度无关的常数,则ln[g(α)/T2]与1/T呈直线关系,由其斜率可求该反应过程的表观活化能。
常用固相反应的动力学模型主要有化学反应、扩散控制、相界反应和成核与生长等,常采用的微分和积分形式的动力学机理函数见表4[24]。以 ln[g(α)/T2]对1/T作图,结果如图6和7所示。

表4 常用固相反应机理函数Table 4 Usual reaction mechanism function of solid phase

图6 预焙烧红土镍矿ln[g(α)/T 2]与1/T的关系Fig.6 Relationship between ln[g(α)/T2]and 1/T for graphiteprecalcined laterite ore mixture
按照表3所分的不同温度区间对图6和7中的曲线进行线性拟合,由于在800 ℃以下还原反应速度很慢,故第一阶段的起始温度定为800 ℃,拟合结果如表5所列。

图7 红土镍矿的ln[g(α)/T 2]与1/T的关系Fig.7 Relationship between ln[g(α)/T2]and 1/T for graphitelaterite ore mixture
由表5可知,各试样还原第一阶段都与F2的相关系数最大,动力学方程为(1-α)-1-1=kt,化学反应是过程的控速环节,反应级数为二级。
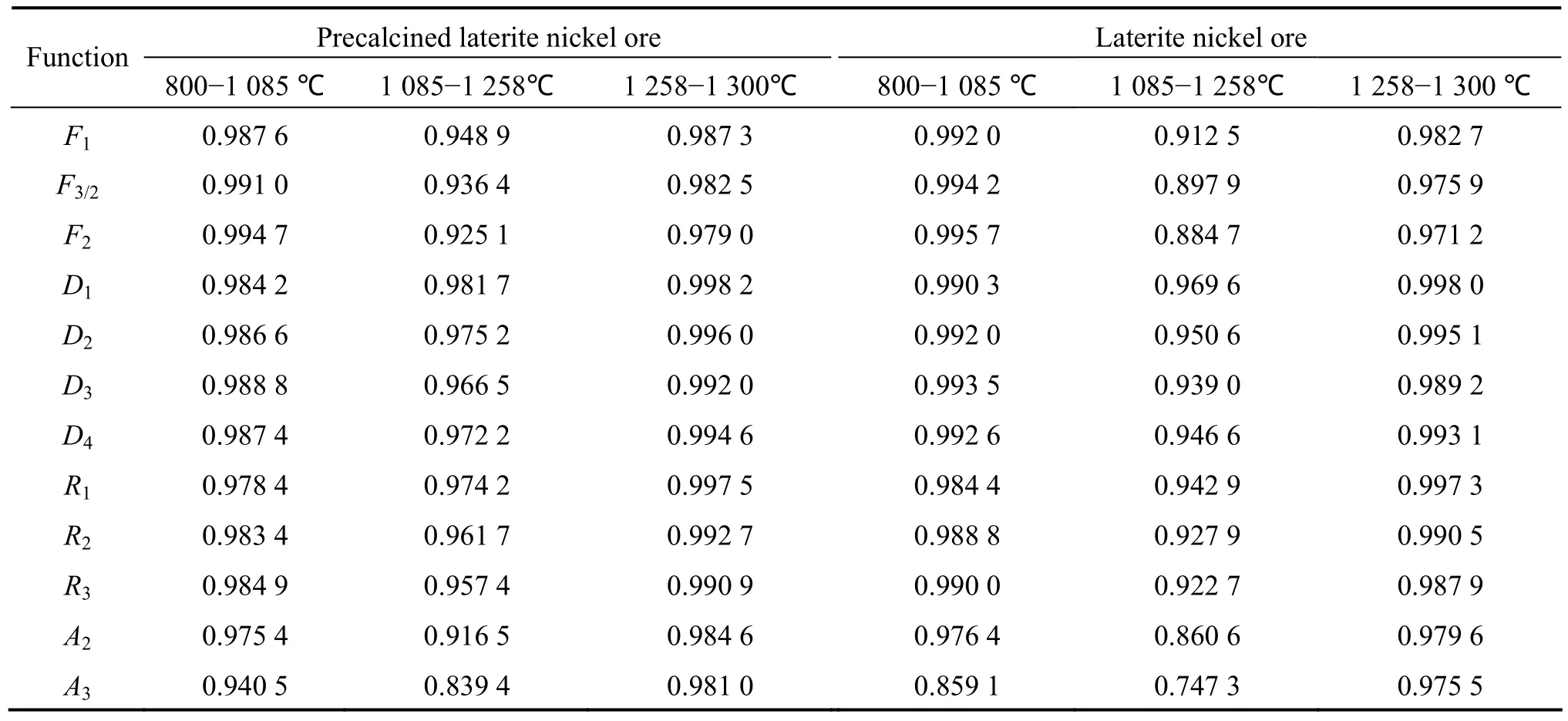
表5 红土镍矿还原过程中不同动力学机理函数的相关系数Table 5 Related coefficient of different kinetic mechanism functions for reduction process of laterite nickel ore
第二阶段和第三阶段与D1的相关系数最大,即符合一维扩散Parabolic法则,动力学方程为α2=kt,扩散是控速环节。
表6所列为还原反应各阶段的表观活化能。

表6 红土镍矿固相还原反应各阶段的表观活化能Table 6 Apparent activation energies in each stage for solid phase reduction reactions of laterite ore
表观活化能为分子从常态转变为易发生化学反应的活跃状态所需的能量,活化能越低,反应速率越快。在还原反应的第一阶段,预焙烧红土镍矿和红土镍矿的表观活化能分别为90.21和63.12 kJ/mol。预先进行焙烧的红土镍矿还原反应的活化能比未进行焙烧的红土镍矿的还原反应的活化能高27.09 kJ/mol,其原因是未焙烧的红土镍矿存在脱羟基反应,质量损失由还原反应和脱羟基反应共同决定;另一方面,蛇纹石类矿物的脱羟基反应会释放其中的镍和铁成为简单氧化物,使还原反应更易于进行。而预焙烧会造成镍、铁离子进入硅酸盐相,导致其活度下降,加大了还原的难度。预焙烧红土镍矿还原反应第二和第三阶段的活化能分别为136.42和179.58 kJ/mol,未进行焙烧的红土镍矿还原反应第二和第三阶段的活化能分别为135.23和177.53 kJ/mol,两者数值接近,表明温度达到1 085 ℃后,脱羟基反应基本上已经结束,化学反应主要为铁氧化物和镍氧化物的还原反应。
随着反应的进行,表观活化能增加较多,反应速度逐渐变慢,反应速度变慢可能有如下几个原因:对于还原反应的第一阶段,主要进行的是易还原矿物Fe2O3和NiO的还原,反应容易进行;第二阶段主要是FeO的还原,相对于Fe2O3和NiO来说,FeO较难还原,因此,其还原活化能高于第一阶段的活化能;当反应进入第三阶段后,FeO的活度将降低,且FeO会与SiO2等物质形成硅酸盐矿物,熔点较低,同时矿物表面会生成金属铁层,阻碍还原反应的进行。另外,由于碳气化反应的进行,还原剂数量逐渐减少,反应后期的还原气氛减弱,从而使反应进行得相对缓慢。
3 结论
1)所研究红土镍矿的主要物相为斜纤蛇纹石(Mg3Si2O5(OH)4)、镍纤蛇纹石(Ni3Si2O5(OH)4)、暗镍蛇纹石(Ni,Mg)3Si2O5(OH)4、叶蛇纹石(Mg,Fe)3Si2O5-(OH)4)、针铁矿(FeO(OH))、赤铁矿(Fe2O3)、高岭石(Al2Si2O5(OH)4)和石英(SiO2)等。该红土镍矿的结晶水含量较高,在900 ℃温度下焙烧2 h后,针铁矿脱羟基后形成赤铁矿,高岭石脱水后生成偏高岭石,蛇纹石分解生成镁橄榄石和顽火辉石。
2)红土镍矿在升温过程中存在 4个质量损失台阶:第一个质量损失台阶的起始温度为47 ℃,对应于红土镍矿中自由水的脱除;第二个质量损失台阶的起始温度为250 ℃,对应于针铁矿FeO(OH)的分解反应,形成赤铁矿;第三个质量损失台阶的起始温度为 533℃,对应于高岭石及蛇纹石的脱羟基反应;第四个质量损失台阶的温度区间为755~864 ℃,对应于蛇纹石类矿物的第二段脱羟基反应。
3)红土镍矿的还原过程可分为3个阶段:第一阶段(800~1 085 ℃)的动力学方程为(1-α)-1- 1 =kt,化学反应是过程的控速环节,经预先焙烧的红土镍矿还原反应的活化能比未进行焙烧的红土镍矿还原反应的活化能高;第二阶段(1 085~1 258 ℃)和第三阶段(1 258~1 300 ℃)的动力学方程为α2=kt,扩散是控速环节,反应的表观活化能逐渐增高。
[1]PATZELT N, SCHMITZ T, GRUND G.Treatment of nickel ores in rotary kilns and cyclone reactors[C]//Proceedings of International Laterite Nickel Symposium.New York, 2004:527-543.
[2]赵昌明, 翟玉春, 刘 岩, 段华美.红土镍矿在NaOH亚熔盐体系中的预脱硅[J].中国有色金属学报, 2009, 19(5): 949-954.ZHAO Chang-ming, ZHAI Yu-chun, LIU Yan, DUAN Hua-mei.Pre-desilication of laterite in NaOH sub-molten salt system[J].The Chinese Journal of Nonferrous Metals, 2009, 19(5):949-954.
[3]PICKLES C A.Microwave heating behavior of nickeliferous limonitic laterite ores[J].Mineral Engineering, 2004, 17:775-779.
[4]谢 皓, 白晨光, 邱贵宝, 吕学伟, 胡 途, 梁 栋.菲律宾红土矿烧结实验研究[J].中国稀土学报, 2008, 26(8): 170-174.XIE Hao, BAI Chen-guang, QIU Gui-bao, LÜ Xue-wei, HU Tu,LIANG Dong.Study on sintering experiment of Philippines laterite ore[J].Journal of the Chinese Society of Rare Earths,2008, 26(8): 170-174.
[5]袁煕志, 李仲恺, 刘 杰.红土镍矿干燥、焙烧工艺条件的选择[J].铁合金, 2008, 201(4): 8-13.YUAN Xi-zhi, LI Zhong-kai, LIU Jie.Choice of drying and roasting technologies on laterite ore[J].Ferro-Alloys, 2008,201(4): 8-13.
[6]刘 燕, 王永志, 陆 雷.红土镍矿干燥特性的研究[J].中国有色冶金, 2010(1): 54-56.LIU Yan, WANG Yong-zhi, LU Lei.Study on drying characteristics of nickel laterite ore[J].China Nonferrous Metallurgy, 2010(1): 54-56.
[7]CHAKRABORTY D, RANGANATHAN S, SINHA S.Investigations on the carbothermic reduction of chromite ores[J].Metallurgical and Materials Transactions B, 2005, 36(4):437-444.
[8]杨学民, 郭占成, 王大光, 谢裕生, 黄典冰, 孔令坛, 杨天钧.含碳球团还原机理研究[J].化工冶金, 1995, 16(2): 118-127.YANG Xue-min, GUO Zhan-cheng, WANG Da-guang, XIE Yu-sheng, HUANG Dian-bing, KONG Ling-tan, YANG Tian-jun.Research on the reduction mechanism of iron ore pellets containing graphite[J].The Chinese Journal of Process Engineering, 1995, 16(2): 118-127.
[9]ABRAHAM M C, GHOSH A.Kinetics of reduction of iron oxide by carbon[J].Ironmaking Steelmaking, 1979, 6(1): 14-23.
[10]丁银贵, 王静松, 曾 晖, 佘雪峰, 杨慧贤, 薛庆国.转炉尘泥含碳球团还原动力学研究[J].过程工程学报, 2010, 10(S1):303-309.DING Yin-gui, WANG Jing-song, ZENG Hui, SHE Xue-feng,YANG Hui-xian, XUE Qing-guo.Research on reduction kinetics of carbon-bearing pellets of BOF dust and sludge[J].The Chinese Journal of Process Engineering, 2010, 10(S1): 303-309.
[11]SARKISYAN L.Mechanism and kinetics of reduction of complex oxides of the NiO-Fe2O3system[J].Powder Metallurgy and Metal Ceramics, 1986, 25(10): 832-837.
[12]CORES A, FORMOSO A, LARREA M T, QRTIZ J.Kinetic regularities in joint reduction of nickel and iron oxides under non-isothermal conditions[J].Ironmaking Steelmaking, 1989,16(6): 446-449.
[13]ABDEL-HALIM K S, KHEDR M H, NASR M I,ABDEL-WAHAB M S.Carbothermic reduction kinetics of nanocrystallite Fe2O3/NiO composites for the production of Fe/Ni alloy[J].Journal of Alloys and Compounds, 2008,463(1/2): 585-590.
[14]李 博, 魏永刚, 王 华.红土镍矿的固相还原动力学[J].过程工程学报, 2011, 11(5): 767-771.LI Bo, WEI Yong-gang, WANG Hua.Solid state deoxidization kinetics of nickel laterite ore[J].The Chinese Journal of Process Engineering, 2011, 11(5): 767-771.
[15]曹志成.红土镍矿直接还原焙烧磁选回收铁镍的研究[D].北京: 北京科技大学, 2009: 28-30.CAO Zhi-cheng.The study on the recovery of iron and nickel from nickel laterite ore by direct reduction roasting and magnetic separation[D].Beijing: University of Science and Technology Beijing, 2009: 28-30.
[16]石文堂.低品位镍红土矿硫酸浸出及浸出渣综合利用理论及工艺研究[D].长沙: 中南大学, 2011: 29-37.SHI Wen-tang.Fundamental and technological study on sulfuric acid leaching of low-grade nickel laterite and comprehensive utilization of leaching residue[D].Changsha: Central South University, 2011: 29-37.
[17]CARLSON L, SCHWERTMANN U.Natural ferrihydrites in surface deposits from Finland and their association with silica[J].Geochimica et Cosmochimica Acta, 1981, 45(3): 421-425.
[18]SWAMY Y, KAR B, MOHANTY J.Physico-chemical characterization and sulphatization roasting of low-grade nickeliferous laterites[J].Hydrometallurgy, 2003, 69(1/3):89-98.
[19]VALIX M, CHEUNG W.Study of phase transformation of laterite ores at high temperature[J].Minerals Engineering, 2002,15: 607-612.
[20]BRINDLEY G W, WAN H M.Compositions, structures, and thermal behavior of nickel-containing minerals in the lizardite-nepouite series[J].The American Mineralogist, 1975,60: 863-871.
[21]TARTAJ P, CERPA A, GARCÍA-GONZÁLEZ M T, SERNA C J.Surface instability of serpentine in aqueous suspensions[J].Journal of Colloid and Interface Science, 2000, 231(1):176-181.
[22]陈国玺, 刘高魁, 王冠鑫.蛇纹石族矿物的差热曲线特征及其热转变的研究[J].矿物学报, 1983, 3: 221-228.CHEN Guo-xi, LIU Gao-kui, WANG Guan-xing.On the characteristics of DTA curves and thermo-conversion of serpentine-group minerals[J].Acta Mineralogica Sinica, 1983, 3:221-228.
[23]COATS A, REDFERN J.Kinetic parameters from thermogravimetric data[J].Nature, 1964, 201: 68-69.
[24]胡长庆, 韩伟刚, 姚少巍, 张志霞.含钛炉渣中TiO2还原动力学机理[J].钢铁研究学报, 2011, 23(9): 12-15.HU Chang-qing, HAN Wei-gang, YAO Shao-wei, ZHANG Zhi xia.Research on the kinetic mechanism of TiO2reduction in TiO2-containing slag[J].Journal of Iron and Steel Research, 2011,23(9): 12-15.

