大黄酚与甲基化-β-环糊精的超分子包合和体外释放特性研究
吴 振,李 红,陈 岗,师 萱,谭红军*
1重庆市中药研究院,重庆 400065;2 重庆市食品药品检验所,重庆 401121;3 重庆市计量质量检测研究院 重庆市食品安全工程技术中心 国家农副加工产品及调味品质量监督检验中心,重庆 401123
大黄酚(chrysophanol,Chr),是大黄、虎杖、何首乌、决明子等中药中提取的一种蒽醌类活性成分,化学名为1,8-二羟基-3-甲基蒽醌(图1),具有抗菌、缩短血液凝固时间、兴奋神经、麻痹肌肉、止咳、利尿、抗癌作用。近年来研究表明,大黄酚能延缓衰老,能清除氧自由基,增强抗氧化能力和改善学习记忆障碍等作用[1]。但大黄酚具有味苦、对胃有刺激性,难溶于水、理化性质不稳定,见光易氧化等不利因素[2],因而没有适宜的剂型供临床应用。因此,提高该类小分子生物活性成分的溶解度(增溶)对其在医药中的广泛使用和生物功能发挥具有非常重要的意义。
近年来发现,超分子包合技术是提高难溶性非极性分子药物溶解性的有效途径之一。超分子包合技术应用的包合材料主要集中在环糊精、冠醚、杯芳烃、多聚糖等[3],其中经过选择性修饰的环糊精——甲基化-β-环糊精(M-β-CD),水溶性好,在有机溶剂中也表现出良好的溶解性,因此成为提高药物溶解性的方法之一[4]。为此本实验采用电磁搅拌-喷雾干燥法(ES)制备Chr-M-β-CD 包合物制剂,旨在提高其溶解度和稳定性,掩盖不良气味,减少其对胃的刺激性,同时,对其包合过程的热力学参数和体外释放特性进行研究,为大黄酚的应用提供更好的实验基础。
1 材料与方法
1.1 材料与仪器
大黄酚标准品(Chr,HPLC≥98%,南京奥多福尼生物科技有限公司);2,6-甲基化-β-环糊精(M-β-CD,平均取代度10.12,山东滨州智源生物科技有限公司);其它化学试剂均为国产分析纯;所用水为双蒸水,所用溶液均自行配制。
高效液相色谱仪(日本Shimadzu 公司);PHS-3C 酸度计(上海虹益仪器仪表有限公司);SD-1500实验型喷雾干燥机(上海沃迪科技有限公司);R-124 旋转蒸发仪(瑞典BUCHI 公司)。
1.2 方法
1.2.1 Chr-M-β-CD 包合物和物理混合物的制备
采用电磁搅拌-喷雾干燥法(ES)制备Chr-M-β-CD 包合物,分别称取规定量的Chr 与M-β-CD 置于烧杯中,加入50%乙醇使二者溶解,置于磁力加热搅拌器上,在30 ℃下,固定转速为800 rpm,搅拌2 h后,静置。将溶液真空旋转蒸发除去乙醇,用0.45 μm 的微孔滤膜过滤以除去未被包合的大黄酚,将滤液进行喷雾干燥,得Chr-M-β-CD 包合物固体粉末。喷雾干燥的工艺参数:蠕动泵流速:1.2 mL/min,进口温度80 ℃,喷雾流量300 mL/h。
物理混合物的制备方法:准确称取适量Chr 和M-β-CD(摩尔比和使用量与超分子包合物一致),置于研钵中混合研磨,干燥,避光保存,备用。
1.2.2 相溶解度的测定
相溶解度的测定参考文献[5]的方法,精密称取M-β-CD 用蒸馏水配成质量分数为5、10、20、50、100、150 mmol/L 的系列溶液,分别吸取5 mL 置具塞试管中,均加入过量的Chr 固体粉末,超声10 min后,置于恒温振荡器(调整振荡频率为100 rpm)中分别在25、35 和45 ℃条件下,振荡5 h。使溶解达到平衡后,静置,取上清液用0.45 μm 的微孔滤膜过滤,滤液用高效液相法测定Chr 的峰面积,用标准曲线计算Chr 的浓度。以M-β-CD 浓度(mmol/L)为横坐标,Chr 浓度(mmol/L)为纵坐标,绘制平衡相溶解度图,并计算线性回归方程及包合常数,通过相溶解度的研究,分析M-β-CD 对Chr 的增溶作用。
1.2.3 等摩尔连续递变法测定包合摩尔比
采用等摩尔连续递变法(即Job’s 方法)确定化学计量比[6],在实验条件下,将所研究的Chr 和Mβ-CD 配制成一系列浓度比,而其总浓度固定不变,M-β-CD 的摩尔分数从0.1 增大至0.9。在最大吸收波长254 nm,测试体系溶液的吸光度为A1,纯Chr溶液的吸光度为A2,以吸光度变化(△A=A2-A1)对M-β-CD 的摩尔组分作图(Job’s 图),根据图中吸光度变化△A 最大处对应的M-β-CD 的摩尔组分,即可以计算出主体M-β-CD 与客体Chr 的包合比。
1.2.4 超分子包合常数和包合过程热力学参数计算
分别对不同温度的各相溶解度曲线的直线部分作线性回归,求得回归方程的斜率(SS)和截距(S0),按Higuchi-Connors 公式[7]计算超分子包合常数(Kb,L/mol)。

式中,SS为斜率;S0为截距,即各温度下Chr 在未添加M-β-CD 的水溶液中的溶解度。
根据范特霍夫方程lnKb=-△H0/RT+△S0/R,以lnKb对1/T 作线性回归,直线的斜率即为-△H0/R,截距即为△S0/R,从而求得包合反应的焓变△H0及熵变△S0;根据公式△G0=△H0-T△S0,计算不同温度下的包合反应的吉布斯自由能变化△G0。
1.2.5 Chr-M-β-CD 包合物的体外释放特性研究
参考《中国药典》2010 年版溶出度测定第一法并略作修改,测定所得体系的的体外释药特性。具体方法为:取900 mL 含0.5%十二烷基硫酸钠的pH 6.8 磷酸盐缓冲液置于溶出杯中,加热,待其温度恒定在(37 ±0.5)℃后,分别精密称取Chr 原药5 mg、Chr-M-β-CD 包合物(相当于原药5 mg)、物理混合物(摩尔比和使用量与超分子包合物一致,相当于原药5 mg)置溶出杯中,调节转速为100 rpm,分别于5~200 min 取样(同时补充等量同温溶液介质),样品经0.45 μm 滤膜过滤,采用HPLC 测定,计算各采样点时样品中的药物浓度和累积释放率。同批样品测定6 份,结果取平均值。
1.2.6 HPLC 测定Chr 含量及方法学研究
HPLC 条件:日本岛津公司LC-20A 高效液相色谱仪,色谱柱为C18Hypersil BDS(250 mm × 4.6 mm)。检测波长:254 nm;柱温:30 ℃;流动相甲醇-0.1%磷酸(65∶35);流速1.2 mL/min,进样量:20 μL,大黄酚的HPLC 色谱图具体如图1 所示。
标准曲线:精密称取Chr 标准品1.13 mg,以甲醇为溶剂溶解后定容到10 mL,摇匀得113 μg/mL Chr 对照品溶液,备用。精密吸取Chr 对照品溶液2、10、20、100、200、400、1000 μL 至2 mL 量瓶中,加甲醇稀释至刻度,摇匀,使浓度成为0.113、0.565、1.130、5.650、11.300、22.600、56.500 μg/mL 的一系列对照品溶液,进样,测定。以质量浓度对峰面积做线性回归。得回归方程Y=89977X-4833.3,R2=0.9999,线性范围为0.113~56.5 μg/mL。
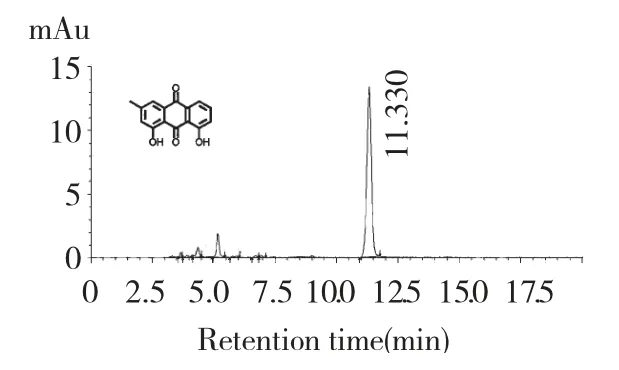
图1 大黄酚(Chr)的HPLC 色谱图(内插图为Chr 分子结构)Fig.1 HPLC chromatogram of chrysophanol (insert:molecular structure of chrysophanol)
精密度实验:制备低、中、高浓度的Chr 溶液,HPLC 测定,同日内测5 次及每天测1 次、连续测5 d。结果日内和日间的平均RSD 均<2%,表明本方法精密度好。
重复性实验:取Chr 对照品适量,共6 份,按样品处理和测定方法平行测定,计算Chr 含量,结果RSD=0.65%,表明方法重复性良好。
回收率实验:精确称取0.03 mg 大黄酚,共6份,与不同浓度的Chr-M-β-CD 样品溶液混合,HPLC测定Chr 浓度,平均加样回收率98.10%,RSD=1.28%。
2 结果与分析
2.1 Chr-M-β-CD 包合物的相溶解度分析
包合常数(Kb)和结合摩尔比是表征小分子药物与环糊精及其衍生物形成包合物的重要参数,相溶解度分析被广泛用于评价上述两个参数[8]。以CChr(mmol/L)为纵坐标,以CM-β-CD(mmol/L)为横坐标,绘制相溶解度图,分别得到25、35 和45 ℃时Mβ-CD 不同浓度对Chr 的相溶解度图,结果见图2(A)。采用线性回归拟合发现,拟合R2均>0.95。根据Higuchi 等[7]的报道,环糊精包合物的相溶解度曲线一般分为A 型和B 型。客体浓度随环糊精浓度增大而增加的为A 型,表现为增溶作用,进一步分为3个亚型:AL、AP和AN型。若环糊精对客体以物质的量之比为1∶1 进行包合,相溶解度曲线呈线性增加,表现为AL型,而AP和AN分别为线性增加的正偏差和负偏差。图2(A)显示,Chr 在不同浓度M-β-CD 作用下的相溶解度图曲线为线性AL型;随着M-β-CD 浓度的增加,Chr 的溶解度随之增加,且有较好的线性关系。图2(B)说明Chr 与M-β-CD形成了物质的量之比为1∶1 的包合物。
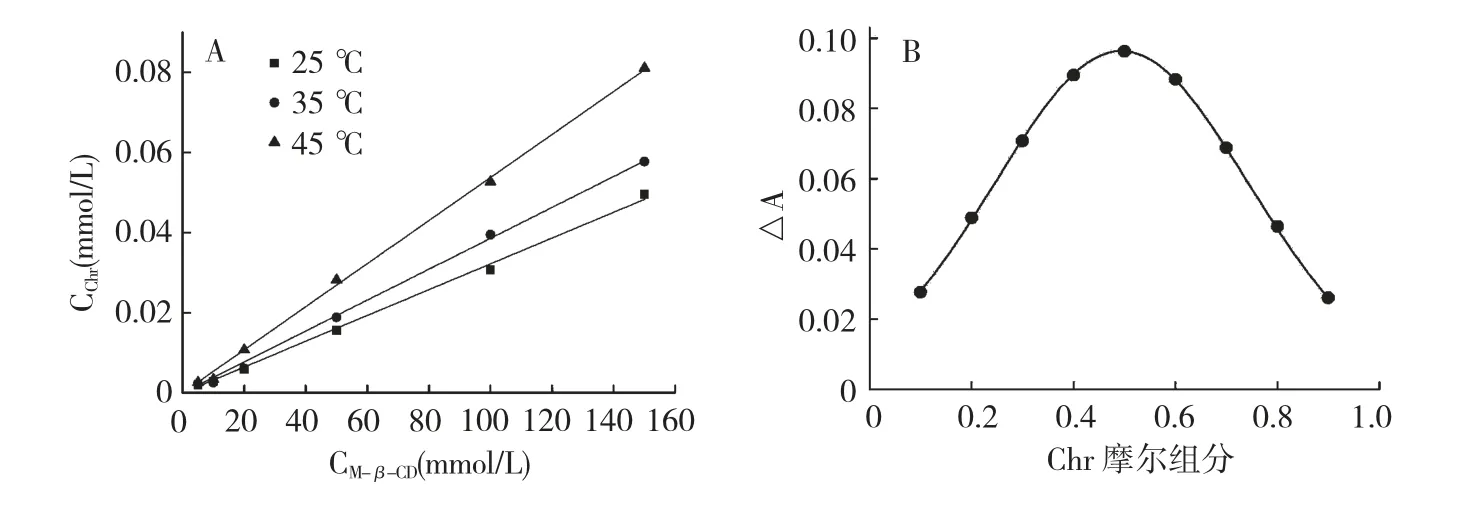
图2 Chr-M-β-CD 包合物在不同温度下的相溶解度曲线(A)和等摩尔连续递变曲线(B)(n=6)Fig.2 Phase solubility diagram (A)and continuous variation plot (B)of Chr-M-β-CD+at different temperatures
Chr-M-β-CD 超分子包合常数(Kb)是衡量包合物稳定性的重要参数,Kb越大,表明该药物与空腔分子的结合越稳定,越容易形成包合物。根据线性方程和式(1)得出包合物在25、35 和45 ℃条件下的Kb分别为:6.56 ×102、7.85 ×102、1.09 ×103L/mol。Kb随温度的升高而升高,这可能是由于分子间作用力(客体Chr 与空腔M-β-CD 间的范德华力、疏水客体与空腔问的“疏水性键力”等)的减小造成的[9]。郑晓霞等[10]研究发现,Chr-HP-β-CD 的Kb为401.19 L/mol(研究条件为:25 ℃),比较发现Mβ-CD 对Chr 的包合作用更强。Loftsson 等[11]研究发现,当环糊精及其衍生物对药物的包合常数在50 L/mol~2000 L/mol 范围内,说明二者之间有较强的相互作用。
2.2 Chr 与M-β-CD 包合过程的热力学参数分析
以lnKb对1/T 作线性回归,得线性回归方程为lnKb=– 2.416 ×103/T +14.57(R2=0.9655)。Chr 与M-β-CD 包合过程的热力学参数结果见表1。实验结果显示△G0<0,说明Chr 与M-β-CD 包合过程是一个自发过程;△H0>0,说明包合过程是一个吸热过程;△S0>0,说明包合过程是无序化增加的过程。同时实验结果说明Chr 与M-β-CD 包合过程为熵驱动过程。环糊精及其衍生物的包合增溶作用主要通过对客体小分子的包结作用实现,包合物形成是增溶的前提[12]。包合过程实质是客体分子Chr进入M-β-CD 空腔,并将其中的水分子替换出来的过程,包合的主要驱动力来自于空腔内高焓值水的释放,包合物的形成可能是Chr 与M-β-CD 间多种力相互作用的结果,如氢键、范德华力、疏水相互作用,以及M-β-CD 在包合过程中释放的环张力等。

表1 不同温度下Chr 与M-β-CD 包合过程的热力学参数Table 1 The thermodynamic parmeters of Chr-M-β-CD inclusion complex under different temperatures

图3 大黄酚及大黄酚包合物累积释放曲线(n=6)Fig.3 Dissolution profiles of Chr and its inclusion complex
2.3 Chr-M-β-CD 包合物体外释放特性分析
从图3 可知,Chr 原药在介质中的溶出行为很差,200 min 在介质中的累积释放率仅为19.9%。物理混合物中由于水溶性辅料的存在,改善了Chr的表面润湿性,对药物的溶出有所改善,但最终的累积释放率也仅为43.6%。采用电磁搅拌-喷雾干燥法(ES)制备Chr-M-β-CD 包合物,可以显著提高Chr原药的初期释放率和最终的累积释放率。ES 方法将药物溶液在热气流的作用下使雾滴中的水分迅速蒸发,直接获得疏松的干燥品,免去了后期其它加工工艺,且得到的粉末大部分为液滴经过膨胀产生的空心颗粒,有利于粉末的润湿,能更好的改善药物的累积释放率。
3 结论
经过电磁搅拌-喷雾干燥法(ES)制备的Chr-甲基化-β-环糊精(M-β-CD)包合物提高了Chr 溶解和溶出行为,不同温度下Chr 的相溶解度图均呈现出AL型特点。在25、35 和45 ℃条件下Chr 与M-β-CD 包合过程的超分子包合常数分别为6.56 ×102、7.85 ×102、1.09 ×103L/mol。包合过程的△H0为20.09 kJ/mol;△S0为121.11 J/(mol·K);△G0分别为-16.01、-17.21、-18.42 kJ/mol;M-β-CD 与Chr可自发形成质量比为1∶1 的包合物,整个包合过程体现为熵驱动过程,形成的超分子包合物均有较好的增溶作用,为Chr 的口服新剂型的设计提供新的思路。同时电磁搅拌-喷雾干燥法(ES)制备得到的Chr-M-β-CD 包合物粉末大多为液滴经膨胀产生的空心颗粒,有利于被水润湿电磁搅拌-喷雾干燥法制品较有工业化前景。
1 Li SJ(李淑娟),Li CG(李春更),Hou Y(侯勇),et al.The review on anti-aging of chrysophanol.Hebei North Univ,Med Ed(河北北方学院学报,医学版),2009,26:69-71.
2 Yan CL(严春临),Zhang J(张季),Zhang DS(张丹参),et al.Study on preparation of chrysophanol microcapsule and its in vitro release behavior.Chin J Exp Tradit Med Form(中国实验方剂学杂志),2011,3:7-10.
3 Fanga Z,Bhandaria B.Encapsulation of polyphenols-a review.Trends Food Sci Tech,2010,21:510-523.
4 Xie BT(谢伯泰),Ma XM(马晓明).Characteristics of methylated-β-cyclodextrins and their applications in pharmacy.Chin J New Drugs(中国新药杂志),2009,8:705-709.
5 He D,Deng P,Yang L,et al.Molecular encapsulation of rifampicin as an inclusion complex of hydroxypropyl-β-cyclodextrin:Design;characterization and in vitro dissolution.Colloids Surf B,2013,103:580-585.
6 Olson E,Bühlmann PJ.Getting more out of a Job’s plot:determination of reactant:product stoichiometry in cases of displacement reactions and n:n complex formation.J Org Chem,2011,76:8406-8412.
7 Higuchi T,Connors KA.Phase solubility techniques.Advances in Analytical Chemistry and Instrumentation,1965,4:117-212.
8 Villaverde J,Morillo E,Perez-Martinez JI,et al.Preparation and characterization of inclusion complex of nor?urazon and beta-cyclodextrin to improve herbicide formulations.J Agric Food Chem,2004,52:864-869.
9 Chen L(陈亮),Chao JB(钞建宾),Ma LH(马丽花).Study on preparation and properties of norfloxacin-hydroxypropyl cyclodextrin solid inclusion compounds.Chin J Magn Reson(波谱学杂志),2000,17:203-210.
10 Zheng XX(郑晓霞),Zhang DS(张丹参),Huang HN(黄红娜),et al.Chrysophanol hydroxypropyl-cyclodextrin inclusion process optimization and identification of compounds.Chin Trad Patent Med(中成药),2010,32:1518-1521.
11 Loftsson T,Hreinsdóttir D,Másson M.Evaluation of cyclodextrin solubilization of drugs.Int J Pharm,2005,302:18-28.
12 Astray G,Gonzalez-Barreiro C,Mejuto JC,et al.A review on the use of cyclodextrins in foods.Food Hydrocolloid,2009,23:1631-1640.

