丹参滴注液生产过程中的内毒素水平监控
李存玉, 支兴蕾, 李贺敏, 李红阳, 郑云枫, 彭国平*
(1. 南京中医药大学药学院,江苏 南京210023;2. 江苏省中药资源产业化过程协同创新中心,江苏 南京210023)
中药注射剂的出现给中药制剂的发展带来了新的机遇,但是由于直接进入血液,因此易引起不良反应[1-2],从而导致了安全性出现质疑的后果。而在注射剂临床使用过程中出现的热原反应,多是由于在注射剂生产、储存、运输、配液使用过程中的细菌污染所导致的,其中以生产过程最易引入污染[3],而目前对注射剂中内毒素检测仅对终产品检验作为产品质量优劣的评判,与药品生产过程实施过程分析监控的理念相悖[4]。
热原反应为最常见的中药注射剂不良反应,主要物质是内毒素,当进入体内的内毒素积量超过人体的耐受量时,便发生热原反应,临床表现为体温升高甚至高热,伴以发冷、出汗、恶心等,严重者甚至导致休克、死亡[5-6]。目前注射剂生产厂家对热原的检测主要采用家兔法和鲎试剂法[7],而家兔法在清热解毒类中药注射剂的热原检查时,由于药物的清热药效作用往往会产生假阴性结果[8]。为了降低成分对内毒素检测的干扰,本实验选用鲎试剂法进行内毒素定量测定。
为了体现过程监控的必要性,选择临床中用量较大的中药注射剂丹参滴注液作为研究对象,根据生产工艺中的关键环节进行取样,采用鲎试剂动态浊度法进行内毒素含量测定,分析生产中的易引入内毒素污染的重点环节,并对注射剂生产中的内毒素过程监控的重要性进行分析。
1 材料与方法
1.1 材料 定量检测用鲎试剂(批号1303270,最低检测限0.03 EU/mL,规格0.6 mL/Amp,湛江博康海洋生物有限公司),细菌内毒素工作对照品(批号201176,规格100 EU/Amp,中国食品药品检定研究院),细菌内毒素检查用水(批号1303120,规格5 mL/Amp,湛江博康海洋生物有限公司)。丹参滴注液(批号13042603,生产过程取样及检测在上海华源安徽锦辉制药有限公司完成)。
1.2 仪器 BET-72M 细菌内毒素测定仪(天津市天大天发科技有限公司);涡旋混合器(天津市天大天发科技有限公司);高温烘箱(HJ101-2,常州昊江电热器材制造有限公司);玻璃试管及玻璃枪头(250 ℃烘烤除内毒素2 h)。
1.3 方法
1.3.1 丹参滴注液的生产工艺 丹参药材,加纯化水煎煮3 次,煎煮液滤过,浓缩,醇沉2 次至含醇量分别为75%和85%,回收乙醇,加注射用水稀释,调节pH 至3.0,冷藏,过滤,加针用活性炭,搅拌并煮沸15 min 以上,进行脱炭过滤。取葡萄糖加入针用活性炭,搅拌并煮沸15 min以上,进行脱炭过滤,滤液与煮沸后的丹参提取液合并,调pH 为3.8 ~4.2,加注射用水及适量亚硫酸氢钠,加针用活性炭,搅拌并煮沸15 min 以上,经钛棒过滤器循环过滤,再经0.45 μm、0.22 μm 过滤器循环过滤,超滤,灌封,灭菌。
1.3.2 丹参滴注液的生产工艺中的取样环节 根据丹参滴注液生产工艺中的关键环节,确定了取样点,具体见表1。

表1 取样点及工艺步骤
1.3.3 动态浊度法检测细菌内毒素[7,9-11]
1.3.3.1 丹参滴注液内毒素限值 根据2010 年版《中国药典》附录ⅩⅢD 细菌内毒素检查法项下的规定,药品的细菌内毒素限值(L)按照下式计算:

式中,L 为供试品的细菌内毒素限值,单位为EU/mL;K为人每千克体质量每小时最大可接受的内毒素剂量,注射剂K=5.0 EU/(kg·h),M 为人用每千克体质量每小时的最大供试品剂量,以mL/(kg· h)表示,人均体质量按60 kg 计算。
丹参滴注液成人每小时最大给药剂量是500 mL,则内毒素最小限值为L =[5.0 EU/(kg·h)×1 h ×60 kg]/500 mL=0.6 EU/mL。
1.3.3.2 标准曲线的可靠性试验 取细菌内毒素工作标准品,检查用水1 mL 溶解得100 EU/mL 的内毒素母液,3 000 r/min 涡旋混匀15 min,按照稀释梯度为4 倍,配制成浓度为2.0、0.5、0.125、0.031 25 EU/mL 的内毒素溶液,各取0.1 mL 分别加到预先加有0.1 mL 鲎试剂溶液的玻璃管内,涡旋混匀,插入BET-72M 细菌内毒素定量检测仪内进行检测,其中每一浓度重复3 管,并同时做未加细菌内毒素的阴性对照3 管。按最小二乘法进行回归运算,则标准曲线为:lgT = 3.024 16 - 0.396 16lgC,r =-0.993 0。其中T 为反应时间,单位为s;C 为内毒素浓度,单位为EU/mL。反应时间在1 104 ~4 044 s 之间,内毒素浓度在2.0 ~0.031 25 EU/mL 时,阴性对照管反应时间大于标准曲线最低浓度的反应时间,且相关系数(r)的绝对值大于0.980,故标准曲线成立。
1.3.3.3 最大有效稀释倍数 最大有效稀释倍数是指在试验中供试品溶液被允许达到稀释的最大倍数(MVD),在不超过此稀释倍数的浓度下进行内毒素限值的检测,其计算公式为:
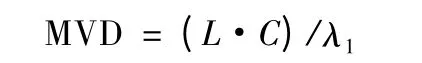
L 为丹参滴注液内毒素限值0.6 EU/mL,C 为药液质量浓度为1.0 g/mL,λ1为0.031 25 EU/mL,因此,丹参滴注液的最大有效稀释倍数为19.2 倍。
1.3.3.4 干扰试验 根据《中国药典》2010 年版附录ⅩⅢD 细菌内毒素检查法中光度法的干扰试验要求,本试验中细菌内毒素的回收率在50% ~200%之间,则认为在此试验条件下丹参滴注液不存在干扰作用。
1.3.3.5 丹参滴注液稀释倍数 为了提高检测结果的准确度,本实验选择在最大有效稀释倍数范围内,分别考察稀释2、4、8、16 倍时,以回收率为指标分析丹参滴注液对内毒素检查检查结果的干扰程度,结果见表2。
从表2 中数据可以看出,丹参滴注液在稀释倍数为8倍时,检测结果最为准确,因此本实验供试品均是以丹参滴注液成品中浓度折算稀释后,进而采用稀释8 倍进行测定。

表2 稀释倍数考察
2 结果
分析图1 中内毒素浓度的变化趋势可以看出,丹参滴注液在生产中的内毒素污染比较严重,在经过醇沉过滤后(样品1),内毒素的浓度高于100 EU/mL,这主要是由丹参药材及所用试剂和环境因素所引起的。

图1 丹参滴注液生产过程中的内毒素水平
丹参提取液在经过活性炭处理后(样品2)内毒素浓度有明显下降,但是从图1 中可以看出,由于活性炭的饱和吸附,样品2 中的内毒素浓度仍高于20 EU/mL。
丹参滴注液中所用辅料葡萄糖在配液中可以发现,葡萄糖溶液(样品3)中内毒素浓度较低,约为5 EU/mL 左右,再经过活性炭处理后浓度降至0.5 EU/mL,说明在溶液中内毒素浓度在一定范围内时,活性炭可以较好的去除内毒素,去除效果在90%以上。
但是在丹参提取液(样品2)和葡萄糖溶液(样品4)进行混合配液时(样品5),内毒素浓度出现了明显上升,远远高于二者的浓度总和,说明在配液过程中不同溶液的合并容易引起内毒素的突发污染。
合并配液后,采用活性炭处理(样品6),微孔滤膜过滤(样品7),内毒素浓度出现明显下降,但是内毒素浓度均在0.6 EU/mL 左右,与其内毒素浓度限值接近,但是在超滤处理后(样品8),内毒素浓度低于0.2 EU/mL,在灌封灭菌后(样品9)虽然出现小幅的增高,但是仍低于0.2 EU/mL,在其安全限度范围内。
3 讨论
目前中药注射剂中内毒素的检测均是以终产品的作为对象,缺乏生产保险系数。随着“药物是生产出来的,而不是检验出来的”概念提出,中药注射剂在某种程度上应当借鉴这种理念,从传统的控制成品质量上升至药品生产过程的有效监控的现代质量管理模式。
通过对丹参滴注液生产环节样品中的内毒素分析,可以发现内毒素浓度的变化水平,并根据易引起内毒素污染的关键环节进行监控,从而有效地控制丹参滴注液的内毒素的量。但是目前较灵敏的内毒素检测方法为鲎试剂动态浊度法,此方法检测准确、灵敏,但是样品的检测周期较长,且检测试剂价格偏高。由于是通过生产过程中的取样分析,取样容器和保存过程中易受外界环境的影响,无法实现在注射剂生产过程中的密闭环境中的内毒素在线监控。
目前,经文献分析发现,内毒素根据其结构特征具有类表面活性,在水溶液中呈现出团聚状态[12-13],经激光照射可呈现出散射特征[14],因此通过对内毒素本身的性质开发注射剂生产过程中的在线监控装置,通过与注射剂生产管路并联,才能真正地实现“过程监控”[15]。
[1] 李 荣,蒋英蓝,曾敬怀,等. 中药注射剂发生不良反应的相关性研究进展[J]. 中成药,2013,35 (5):1059-1061.
[2] 段为钢,张陆勇. 提高中药注射剂安全性的技术策略[J].中成药,2012,34(11):2201-2205.
[3] 吴国琳,张 力,余国友. 中药注射剂发生不良反应常见原因分析及防范对策[J]. 中国中西医结合杂志,2008,28(12):1137-1140.
[4] 马 莉,鄢 丹,曹俊岭,等. 细菌内毒素定量检测方法在中药注射剂质量控制中的应用研究[J]. 中草药,2009,40(12):2005-2008.
[5] 薛玉强,孙丽红. 控制大输液生产过程中的热原污染体会[J]. 实用医技杂志,2004,11(7):1352.
[6] 宋晓坤,李利娟. 5 种中药注射液细菌内毒素检测方法的建立[J]. 中草药,2006,37(12):1819-1821.
[7] 国家药典委员会. 中华人民共和国药典:2010 年版一部[S]. 北京:中国医药科技出版社,2010:附录ⅩⅢA,ⅩⅢD.
[8] 杨国秀,张同星,彭国平. 清热解毒类清开灵注射液中热原检测方法的比较[J]. 中药与临床,2011,2 (2):27-29.
[9] 张玉臣. 清开灵注射液细菌内毒素的检测[J]. 中成药,2008,30(2):307-308.
[10] 尹 楠,李红阳,彭国平,等. 超滤法去除中药注射液中的细菌内毒素[J]. 中国医药工业杂志,2008,39(12):927-929.
[11] 李存玉,郑云枫,李红阳,等. 细菌内毒素定量法研究活性炭与超滤法热原去除工艺[J]. 医药导报,2010,29(2):142-144.
[12] Magalhães P O,Lopes A M,Mazzola P G,et al. Methods of endotoxin removal from biological preparations:a review[J]. J Pharma Sci,2007,10(3):388-404.
[13] Li C Y,Huang X F,Xiao W,et al. Removal of bacterial endotoxin micelle from Salvia injection by composite materials ultrafiltration membrane[J]. Asi j chem,2013,25 (12):6978-6982.
[14] Santos N C,Silva A C,Castanho M A R B,et al. Evaluation of lipopolysaccharide aggregation by light scattering spectroscopy[J]. Chembiochem,2003,4(1):96-100.
[15] 彭国平,郑云枫,李红阳. 纳米粒径分析仪用于内毒素检测的方法:中国,201210196656.6[P]. 2012-06-14.

