氯化胆碱-乙二醇低共熔溶剂中电沉积纳米晶镍
李瑞乾 ,梁 军,初青伟
(1. 中国科学院 兰州化学物理研究所 固体润滑国家重点实验室,兰州 730000;2. 中国科学院大学,北京 100039)
镍金属及其合金由于具有优异的力学性能、耐腐蚀性能和电学性能而被广泛的应用于装饰、保护及电铸等表面精加工过程。国内外关于镍及其合金在水溶液中电沉积的研究已有大量报道[1-6],虽然水溶液具有价格低廉、对金属盐溶解性好、传导性高及传质速率快等优点,但是水溶液窄的电化学窗口、阴极的析氢现象、沉积过程必须采用络合剂以及废水处理等问题却严重制约了电流效率和镀层质量的提高以及工艺流程的简化。离子液体(Ionic liquid,又称室温熔盐)是指在室温及相邻温度下完全由离子组成的有机液体物质。由于离子液体具有一系列优异特性,如电化学窗口宽、熔点低、不挥发、不易燃、热稳定性好、液程范围宽、溶解能力强、性质可调等,它不仅可以沉积传统水溶液中可沉积的金属及合金,还可沉积传统水溶液中难以沉积的碱金属、碱土金属、难熔金属和半导体金属等[7],因此,离子液体被认为是电沉积金属镀层的理想溶剂。近年来,将离子液体作为电解质溶液制备镍及其合金镀层的研究已有一些报道[8-11]。例如高丽霞等[12]在2AlCl3/Et3NHCl离子液体中研究了镍及镍-铝合金的沉积机理,并探讨了沉积工艺对镍-铝合金表面形貌和电流效率的影响;王雪涛等[13]和王颖臻等[14]分别在[BMIM]PF6离子液体中成功制备出具有面心立方结构的纳米镍颗粒。但是氯化铝型离子液体对水非常敏感,并且质子或氧化物杂质的存在对离子液体的化学性质具有很大影响,因此需要在真空或惰性气体气氛保护下进行反应;而[EMIM]BF4、[EMIM]PF6类离子液体遇水或AlCl3时容易放出HF。此外,有关毒理研究表明,咪唑和吡啶类离子液体并非完全“绿色”,其毒性与传统有机溶剂的相当[15],且离子液体合成过程复杂,生产成本高,从而限制了其大规模工业化应用。
2003 年,ABBOTT等[16]首次发现了一种由季铵盐和酰胺化合物形成的新型溶剂—低共熔溶剂(Deep eutectic solvents),它不仅具有离子液体所具备的优点,而且制备容易、原料低廉、绿色无毒、可大量合成。低共熔溶剂的出现为电沉积领域的发展开辟了新的道路。YANG 等[17]在氯化胆碱-尿素低共熔溶剂中得到晶粒尺寸在4.2 nm左右、表面光亮平滑的镍镀层。GU等[18]在氯化胆碱-乙二醇低共熔溶剂中,通过改变电流类型制备得到了表面形貌分别为纳米棒、纳米片和多层花状的镍镀层。ABBOTT等[19]比较了Ni在氯化胆碱-乙二醇和氯化胆碱-尿素两种低共熔溶剂中的电沉积行为,研究光亮剂乙二胺和乙酰丙酮钠对Ni电沉积行为的影响,并首次在铝基底上制备得到Ni镀层。
在水溶液体系中,关于电流密度对电沉积金属及合金镀层的表面形貌、织构特征及性能影响的研究已有很多[2,20-24],而在离子液体体系中却鲜见报道。本文作者采用摩尔比为 1:2的氯化胆碱-乙二醇低共熔溶剂(ChCl:EG)作为电解质,考察镍在铂电极上沉积的电化学行为,并研究电流密度对电沉积镍镀层的微观形貌和织构特征的影响。
1 实验
氯化胆碱(ChCl, AR),乙二醇(EG, AR),六水合氯化镍(NiCl2·6H2O),一水合柠檬酸(C6H8O7·H2O)。将摩尔比为1:2的氯化胆碱和乙二醇混合,70 ℃下搅拌至得到无色液体,再加入0.2 mol/L NiCl2·6H2O搅拌,得到透明的亮绿色液体,最后加入 0.2 mol/L C6H8O7·H2O 搅拌溶解。
循环伏安和计时电流实验利用 RST5200电化学工作站(郑州世瑞斯),采用三电极体系,以微铂电极(2 mm×0.1 mm)作为工作电极,铂盘电极(d=1 mm)作为对电极,银线电极作为参比电极,实验前将工作电极和对电极用0.3 μm的氧化铝膏打磨抛光,并在蒸馏水中超声5 min。循环伏安实验从0 V开始,先负扫至-1 V,再反向扫至1 V,最后返回到0 V,扫速为30 mV/s。所有的电化学实验均在70 ℃下进行。
采用尺寸为30 mm×7 mm的铜片(99.5%)作为电沉积镍镀层的基底,纯镍片(99.99%)作为牺牲阳极,沉积过程保持温度(70 ℃)不变,采用频率为1000 Hz,占空比为3/4的矩形波,通过改变脉冲电流的大小,在搅拌(200 r/min)条件下沉积120 min。电镀前,铜片经砂纸打磨抛光,用蒸馏水清洗后放入丙酮中超声15 min,最后浸入质量分数为10%的盐酸中活化30 s。
采用扫描电子显微镜(SEM, JSM-5600LV)观察镍镀层的表面形貌和横截面形貌。采用X射线多晶衍射仪(D/max-2400, Cu Kα靶,γ=0.154 06 nm)分析镀层的织构特征,管压40 kV,管流60 mA,掠射角5°,扫描速度 10 (°)/min。
2 结果与讨论
2.1 Ni(Ⅱ)的电化学行为
在电沉积前,首先考察了 ChCl:2EG低共熔溶剂的电化学窗口以及镍离子在该体系的氧化还原电势。图1所示为纯ChCl:2EG低共熔溶剂及含有0.2 mol/L NiCl2·6H2O 和 0.2 mol/L C6H8O7·H2O 的 ChCl:2EG 低共熔溶剂的循环伏安曲线。如图1中插图所示,相对于 Ag/Ag+电极,氯化胆碱-乙二醇低共熔溶剂的阴极极限电位为-0.7 V,阳极极限电位为1.1 V。在-0.7 V处发生的阴极反应可归因于体系中乙二醇、氯化胆碱或微量水的还原[25]; 而1.25 V处出现的还原峰则是由于氯化胆碱发生分解,生成三甲胺[26]。由图1可知,体系加入柠檬酸后,在-0.3 V(c1)和-0.8 V(c2)处各出现一个还原峰,还原峰c1是柠檬酸的分解,而还原峰c2则属于镍的还原。REEVES等[27]利用电位分析和光谱研究了柠檬酸(H4cit)同镍离子在酸性条件下的反应,推测多齿配位的柠檬酸同镍配位的可能物种有NiHcit-,NiH2cit,NiH3cit+和 Ni(Hcit)24-。当体系中存在自由柠檬酸(即没有与镍离子形成络合物)或Ni(Hxcit)x-2(x=1,2,3)络合物时,它们都能提供H+离子,从而发生氢的还原反应,0.25 V(c3)处的氧化反应属于镍的氧化。另外,在0.1 V(c4)处出现的肩峰,则属于欠电势沉积镍的氧化峰[19]。ABBOTT等[28]在低共熔溶剂中研究Cu和Zn电沉积时,循环伏安曲线上也出现了类似的肩峰。

图1 镍在铂电极上电沉积的循环伏安曲线Fig. 1 Cyclic voltammograms of Ni(II) electrodeposited on Pt:(a) Pure ChCl:2EG at 70 ℃; (b) ChCl:2EG solution containing 0.2 mol/L NiCl2·6H2O and 0.2 mol/L C6H8O7·H2O
图2所示为铂电极在含有0.2 mol/L NiCl2·6H2O和0.2 mol/L C6H8O7·H2O的ChCl:2EG低共熔溶剂中不同电势下的计时电流曲线。初始阶段,由于电极双电层的充电导致电流迅速降低;随后由于发生镍的形核/生长过程而导致电流增加,达到最大值Im后,电流又衰减,电极表面表现为扩散控制生长。由图2可知,随电势变负,形核驰豫时间tm减小,相应的Im值逐渐增大,这说明过电位增大,导致形核速率升高,从而使得形核诱导时间减小。
金属在异质基底上的电沉积过程通常符合三维形核/生长模型,理论上可分为三维瞬时形核和三维连续形核两种方式[29]。瞬时形核是指所有的形核点同时被活化,然后匀速生长;而连续形核则指随电沉积的进行,形核点逐渐被活化,各点生长速率不同。

图2 不同电势下镍在铂电极上的计时电流曲线Fig. 2 Chronoamperograms of Pt electrode in ChCl:2EG containing 0.2 mol/L NiCl2·6H2O and 0.2 mol/L C6H8O7·H2O under different potentials at 70 ℃
SCHARIFKER和HILL[17]提出瞬时形核和连续形核的无因次公式:
瞬时形核:
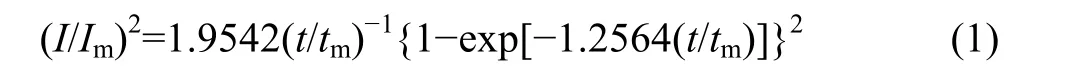
连续形核:

式中:I和Im分别表示电流和电流的最大值;t和tm分别表示时间和电流达到最大值时的时间。以(I/Im)2为纵坐标,t/tm为横坐标,将不同电位下得到的无因次(I/Im)2-t/tm曲线和经典的Scharifker-Hill模型理论数据进行拟合,如图3所示。由图3可看出,初始阶段镍的形核/生长过程符合三维连续形核机制,当t>tm后,形核方式由三维连续形核逐渐趋向于三维瞬时形核。形核机制的改变可能是由于在初始阶段,离子捕获过程贯穿电沉积过程,不断产生新的形核活性点,从而遵循三维连续形核;而随着电沉积的进行,电极表面离子覆盖趋于饱和,形核活性点在短时间内被完全占据,从而遵循三维瞬时形核[30]。

图3 不同电势下镍电沉积的无因次(I/Im)2-t/tm曲线Fig. 3 Dimensionless (I/Im)2-t/tm plots of electrode positing nickel under different potentials
2.2 电流密度对镀层表面形貌的影响
为了考察电流密度对镍镀层表面形貌及厚度的影响,本文作者选取3种不同电流密度进行镍的电沉积实验,电流密度为3、6和12 mA /dm2时电沉积镍镀层的表面形貌如图4所示。当电流密度为 3 mA/dm2时(见图4(a)),得到表面由尺寸为2~3 μm锥形颗粒堆积的镀层,且在锥形颗粒的表面均匀分布着一层细小的针状晶体;当电流密度增加到 6 mA/dm2时(见图4(b)),得到的镀层表面均匀覆盖有尺寸为1~1.5 μm的多面体形颗粒,细小的针状晶体消失;而当电流密度继续增大到12 mA/dm2时(见图4(c)),得到表面呈现圆球形突起的镀层,但镀层表面出现裂纹,这可能是由于在大的电流密度下,镍离子快速形核导致镍膜内应力升高,因此产生裂纹。

图4 不同电流密度下镍镀层表面形貌的SEM像Fig. 4 SEM images of Ni coating deposited from solution ChCl:2EG containing 0.2 mol/L NiCl2·6H2O and 0.2 mol/L C6H8O7·H2O at different current densities: (a) 3 mA/dm2; (b) 6 mA/dm2; (c) 12 mA/dm2
图5所示为不同电流密度下电沉积镍镀层的横截面背散射电子像。由图5可知,电流密度越大,镍镀层结构越致密,表面越平整。虽然图 5(a)中镀层表观厚度约为 3.71 μm,但镀层平整度较差,而且镀层出现明显的层状生长,层与层之间结合也不好。通过多处选点计算可知,当电流密度为3、6和12 mA /dm2时,镀层的平均有效厚度分别为 2.85、3.02 和 4.23 μm,即镀层厚度随电流密度的增加而增大。
2.3 电流密度对镀层织构的影响
图6所示为不同电流密度下电沉积镍镀层的XRD谱。图中44.6°、51.9°和76.5°处3个峰分别属于镍的(111)、(200)和(220)晶面的衍射峰。由XRD谱可知,随着电流密度的增大,镍的3个晶面的峰强度逐渐升高,这说明电流密度的增加提高了电沉积镍的结晶度。
根据X射线衍射理论,在晶粒尺寸小于100 nm时,随晶粒尺寸的变小衍射峰宽化变得显著, 考虑样品的吸收效应及结构对衍射线型的影响,样品晶粒尺寸可以用Debye-Scherrer公式计算[31]:

图5 不同电流密度下镍镀层截面形貌的BSE像Fig. 5 Cross-sectional BES images of Ni coating deposited from ChCl:2EG containing 0.2 mol/L NiCl2·6H2O and 0.2 mol/L C6H8O7·H2O at different current densities: (a) 3 mA/dm2;(b) 6 mA/dm2; (c) 12 mA/dm2

图6 不同脉冲电流下镍镀层的XRD谱Fig. 6 XRD patterns of Ni coating obtained at different current densities: (a) 3 mA/dm2; (b) 6 mA/dm2; (c) 12 mA/dm2

式中:Dhkl为沿垂直于晶面(hkl)方向的晶粒直径;k为Scherrer常数(通常为0.89);λ为X射线波长(Cu Kα波长为0.15406 nm);θ为布拉格衍射角(°);β为衍射峰的半高宽(rad)。
根据式(3)的计算结果,电流密度为 3、6和 12 mA/dm2时,镍晶粒的平均尺寸分别为 20.1、12.7和10.0 nm,即随电流密度的增大,晶粒尺寸减小。电流的增大意味着沉积过电位的增高,而过高的过电位有利于镍电沉积过程中晶核的形成,而晶核的生长相对受到抑制,这就必然导致晶粒尺寸的减小。
X射线扫描采用2θ扫描方式测定沉积层织构,以Tc表示晶面(hkl)的织构系数[21]:

式中:I(hkl)、I0(hkl)分别为试样镀层和标准镍片(hkl)晶面的衍射强度,Tc值越大,表明晶面择优取向程度越高。根据式(4),当电流密度为3、6和12 mA/dm2时,(111)晶面的织构系数Tc(111)分别为 91.30%、80.58% 和77.66%。这表明电流密度较小时,镍镀层更易于沿(111)晶面择优生长,而随着电流密度增加,镍镀层沿(111)晶面择优取向变弱。这一变化符合EBRAHIMI等[32]报道的随着晶粒尺寸减小,镀层的择优取向减弱。
3 结论
1) 循环伏安曲线测试结果表明,在含有C6H8O7·H2O的氯化胆碱-乙二醇低共熔溶剂中镍的电沉积过程是准可逆的。
2) 镍在铂电极上的电沉积过程遵循Scharifker-Hill三维形核模型,开始阶段符合三维连续形核,随后逐渐趋向于三维瞬时形核。
3) 电流密度对镍镀层的形貌具有显著影响,随电流密度的增大,镀层形貌先由表面覆盖有均匀针状纳米晶体的锥形颗粒转变为均匀的多面体形颗粒,最后变为圆球形突起的胞状物。
4) 随着电流密度的增大,镍镀层的厚度增加,晶粒尺寸随之减小,镍(111)晶面择优生长趋势逐渐变弱。
[1] GU Chang-dong, LIAN Jian-he, HE Jin-guo, JIANG Zhong-hao,JIANG Qing. High corrosion-resistance nanocrystalline Ni coating on AZ91D magnesium alloy[J]. Surface and Coatings Technology, 2006, 200(18/19): 5413-5418.
[2] QU Ning-song, ZHU Di, CHAN Chak-keung, LEI Wei-ning.Pulse electrodeposition of nanocrystalline nickel using ultra narrow pulse width and high peak current density[J]. Surface and Coatings Technology, 2003, 168(2/3): 123-128.
[3] BAHADORMANESH B, DOLATI A, AHMADI M R.Electrodeposition and characterization of Ni-Co/SiC nanocomposite coatings[J]. Journal of Alloys and Compounds,2011, 509(39): 9406-9412.
[4] MENG Guo-zhe, SUN Fei-long, SHAO Ya-wei, ZHANG Tao,WANG Fu-hui, DONG Chao-fang, LI Xiao-gang. Effect of phytic acid on the microstructure and corrosion resistance of Ni coating[J]. Electrochimica Acta, 2010, 55(20): 5990-5995.
[5] 杨艳玲, 申勇峰, 陈进耿, 王沿东.超声搅拌-脉冲电沉积法制备纳米镍[J].金属学报, 2007, 43(8): 883-888.YANG Yang-ling, SHEN Yong-feng, CHEN Jin-geng, WANG Yan-dong. Nanocrystalline nickel coating prepared by pulsed electrodeposition combined with ultrasonic agitation[J]. Acta Metallurgica Sinica, 2007, 43(8): 883-888.
[6] ABBOTT A P, MCKENZIE K J. Application of ionic liquids to the electrodeposition of metals[J]. Physical Chemistry Chemical Physics, 2006, 8: 4265-4279.
[7] ALLAHYARZADEH M H, ROOZBEHANI B, ASHRAFI A.Electrodeposition of high Mo content amorphous/nanocrystalline Ni-Mo alloys using 1-ethy-3-methyl- imidazolium chloride ionic liquid as an additive[J]. Electrochimica Acta, 2011, 56(27):10210-10216.
[8] LAHIRI A, DAS R. Synthesis of face centered cubic and hexagonal closed packed nickel using ionic liquids[J]. Journal of Applied Electrochemistry, 2010, 40(11): 1991-1995.
[9] GOU Shi-ping, SUN I-wen. Electrodeposition behavior of nickel and nickel-zinc alloys from the zinc chloride-1-ethyl-3-methylimidazolium chloride low temperature molten salt[J]. Electrochimica Acta, 2008, 53(5): 2538-2544.
[10] HUANG Hsin-yi, CHEN Po-yu. Voltammetric behavior of Pd(II)and Ni(II) ions and electrodeposition of PdNi bimetal in N-butyl-N-methylpyrrolidinium dicyanamide ionic liquid[J].Electrochimica Acta, 2011, 56(5): 2336-2343.
[11] ZHU Yan-li, KATAYAMA Y, MIURA T. Effects of acetone and thiourea on electrodeposition of Ni from a hydrophobic ionic liquid[J]. Electrochimica Acta, 2012, 85: 622-627.
[12] 高丽霞, 王丽娜, 齐 涛, 余 江. 从2AlCl3/Et3NHCl离子液体中电沉积制Ni和Ni-Al合金[J]. 物理化学学报, 2012, 28(1):111-120.GAO Li-xia, WANG Li-na, QI Tao, YU Jiang. Preparation of Ni and Ni-Al Alloys from 2AlCl3/Et3NHCl ionic liquid by electrodeposition[J]. Acta Physico-Chimica Sinica, 2012, 28(1):111-120.
[13] 王雪涛, 余 林, 彭兰乔, 孙 明, 许杰瑜, 余 倩, 余 坚.离子液体[bmim]PF6中制备纳米金属Ni 及其催化苯乙烯加氢的研究[J]. 功能材料, 2008, 39(3): 519-522.WANG Xue-tao, YU Lin, PANG Lan-qiao, SUN Ming, XU Jie-yu, YU Qian, YU Jian. Preparation of nano Ni catalyst in ionic liquids [BMim]PF6and its application in the styrene hydrogenation[J]. Functional Materials, 2008, 39(3): 519-522.
[14] 王颖臻, 杨明娣, 苏永庆, 李 琮, 王 宏, 蔡 英. 离子液体[BMIm]PF6介质中镍纳米粒子的制备与结构表征[J]. 中国有色冶金, 2011(1): 70-72.WANG Yin-zhen, YANG Ming-di, SU Yong-qing, LI Cong,WANG Hong, CAI Ying. Preparation and structure characterization of Ni nanoparticles in medium containing[BMIm]PF6ionic liquids[J]. China Nonferrous Metallurgy,2011(1): 70-72.
[15] 韦 露, 樊友军. 低共熔溶剂及其应用研究进展[J]. 化学通报, 2011, 74(4): 333-339.WEI Lou, FAN You-jun. Progress of deep eutectic solvents and their applications[J]. Chemistry Online, 2011, 74(4): 333-339.
[16] ABBOTT A P, CAPER G, DAVIES D L, RASHEED R K,TAMBYRAJAH V. Novel solvent properties of choline chloride/urea mixtures[J]. Chemical Communications, 2003(1):70-71.
[17] YANG Hai-yang, GUO Xin-wu, BIRBILIS N, WU Guo-hua,DING Wen-jiang. Tailoring nickel coatings via electrodeposition from a eutectic-based ionic liquid doped with nicotinic acid[J].Applied Surface Science, 2011, 257(21): 9094-9102.
[18] GU Chang-dong, TU Jiang-ping. One-step fabrication of nanostructured Ni film with lotus effect from deep eutectic solvent[J]. Langmuir, 2011, 27(16): 10132-10140.
[19] ABBOTT A P, TTAIB K E, RYDER K S, SMITH E L.Electrodeposition of nickel using eutectic based ionic liquids[J].Transactions of the Institute of Metal Finishing, 2008, 86(4):234-240.
[20] 辜 敏, 杨防祖, 黄 令, 姚士冰, 周绍民. 高择优取向铜镀层的电化学形成及其表面形貌[J]. 物理化学学报, 2002,18(11): 973-978.GU Min, YANG Fang-zu, HUANG Ling, YAO Shi-bing, ZHOU Shao-min. The formation of copper electrodeposites with highly preferred orientation and their surface morphology[J]. Acta Physico-Chimica Sinica, 2002, 18(11): 973-978.
[21] 辜 敏, 黄 令, 杨防祖, 姚士冰, 周绍民. 搅拌条件下电流密度对Cu镀层的织构和表面形貌的影响[J]. 应用化学, 2002,19(3): 280-284.GU Min, HUANG Ling, YANG Fang-zu, YAO Shi-bing, ZHOU Shao-min. Effects of current density and bath agitation on the surface morphology and texture of Cu electrodeposits[J].Chinese Journal of Applied Chemistry, 2002, 19(3): 280-284.
[22] QU Ning-song, ZHU Di, CHAN Chak-keung. Fabrication of Ni-CeO2nanocomposite by electrodeposition[J]. Scripta Materialia, 2006, 54(7): 1421-1425.
[23] 丁志敏, 冯秋元, 宋建敏, 高 宏. 电流密度对熔盐电镀铝晶粒形貌的影响[J]. 材料热处理学报, 2012, 33(9): 129-133.DING Zhi-min, FENG Qiu-yuan, SONG Jian-min, GAO Hong.Effect of current density on morphology of electrodeposition aluminum crystal from molten salts[J]. Transactions of Materials and Heat Treatment, 2012, 33(9): 129-133.
[24] LEE Y J, LEE T H, KIM D Y, NERSISYAN H H, HAN M H,KANG K S, BAE K K, SHIN Y J, LEE J H. Microstructural and corrosion characteristics of tantalum coatings prepared by molten salt electrodeposition[J]. Surface and Coatings Technology, 2013, 235: 819-826.
[25] WHITEHEAD A H, POLZLER M, GOLLAS B. Zinc electrodeposition from a deep eutectic system containing choline chloride and ethylene glycol[J]. Journal of Alloys and Compounds, 2010, 157(6): D328-D334.
[26] YUE Du-yuan, JIA Yong-zhong, YAO Ying, SUN Jin-he, JING Yan. Structure and electrochemical behavior of ionic liquid analogue based on choline chloride and urea[J]. Electrochimica Acta, 2012, 65: 30-36.
[27] BROOKS R R, LEE J, REEVES R D, JAFFRE T. Isolation and identification of a citrato-complex of nickel from nickelaccumulating plants[J]. Phytochemistry, 1977, 16(10):1503-1505.
[28] ABBOTT A P, TTAIB K E, FRISCH G, MCKENZIE K J,RYDER K S. Electrodeposition of copper composites from deep eutectic solvents based on choline chloride[J]. Physical Chemistry Chemical Physics, 2009, 11(21): 4269-4277.
[29] TSUDA T, NOHIRA T, ITO Y. Nucleation and surface morphology of aluminum-lanthanum alloy electrodepsited in a LaCl3-saturated AlCl3-EtMeImCl room temperature molten salt[J]. Electrochimica Acta, 2002, 47(17): 2817-2822.
[30] 赵旭山, 谭澄宇, 陈文敬, 刘 宇, 李劲风, 郑子樵. Ni-SiC复合镀层电结晶初期动力学分析[J]. 中国有色金属学报,2008, 18(5) : 823-828.ZHAO Xu-shan, TAN Cheng-yu, CHENG Wen-jing, LIU Yu, LI Jin-feng, ZHENG Zi-qiao. Nucleation kinetics analysis of Ni-SiC composite film during early electrocrystallization processes[J]. The Chinese Journal of Nonferrous Metals,2008,18(5): 823-828.
[31] 黄胜涛, 固体X射线[M]. 北京: 高等教育出版社, 1985: 274.HUANG Sheng-tao. The X-ray study for solid state[M]. Beijing:Higher Education Publishing House, 1985: 274.
[32] EBRAHIMI F, BOURNE G R, KELLY M S, MATTHEWS T E.Mechanical properties of nanocrystalline nickel produced by electrodeposition[J]. Nanostructured Materials, 1999, 11(3):343-350.

