Zn(II)-1,10-邻菲罗啉-曙红Y体系光谱研究及其分析应用
杨 卓, 杨学义, 刘献明, 杨红兵
(1.洛阳师范学院化学化工学院 河南洛阳471022;2.洛阳师范学院 生命科学系 河南 洛阳471022)
0 引言
锌是人体必须的微量元素之一,缺锌将导致免疫力低下、生长发育缓慢,而摄入过多又会引起急、慢性中毒,严重者会致人死亡[1].文献[2]显示我国儿童、青少年人群中缺锌现象比较普遍,且年龄越小缺锌越严重.因此,建立简便、快速、准确、灵敏的定量检测人体中锌含量的方法,给人们及时合理补锌进行一定的指导是一项非常有意义和有必要的工作.目前已报道痕量锌的测定方法主要有:分光光度法[3-4]、荧光分析法[5-6]、色谱法[7]、电化学分析法[8-9]、原子吸收法[10-11]和共振散射法[12]等.分光光度法仅限于有颜色或有颜色变化的体系,荧光分析法仅限于有荧光或有荧光变化的体系,应用受限;色谱法因其仪器和日常维护较昂贵,普及较为困难;电化学分析法因受限于电极材料而重现性和选择性有待提高;原子吸收法是国家标准认定的锌测定方法,但其存在前处理步骤繁琐、污染较大且待测锌元素易损失等缺点.共振rayleigh散射法(resonance rayleigh scattering,RRS)是一种新近发展起来的灵敏而简易的分析技术,因其对于分子间静电引力、氢键作用、疏水作用、聚集作用等弱结合力引起的相互作用十分敏锐,而备受关注[13-14].基于此,本文研究了Zn(II)-1,10-邻菲啰啉(phen)-曙红Y(EY)三元体系,结果表明:在 pH 2.8~4.5的 Britton-Robinson(BR)缓冲溶液中,1,10-phen与Zn(II)形成二价螯合阳离子后,通过静电引力和疏水作用力与EY阴离子反应形成Zn(II):phen:EY为1∶2∶2的离子缔合物,导致体系的荧光猝灭,二级散射(SOS)和倍频散射(FDS)增强,RRS显著增强,且在一定范围内Zn(II)浓度与荧光、散射强度均成线性关系.本文研究了该三元体系的荧光和散射光谱,其中RRS法具有更高的灵敏度,所以,本文以RRS法为例考察了体系的最佳反应条件、灵敏度及选择性,探讨了三元体系的反应机理及RRS增强的原因.发现:在0.1~8 μmol/L范围内Zn(II)浓度与RRS强度成正比,检出限可达0.71 ng/mL(325 nm)和0.49 ng/mL(560 nm),并且具有较好的选择性,用于人发中锌含量的测定,结果令人满意,据此发展了一种灵敏、简便、快速测定锌的RRS方法.
1 实验部分
1.1 主要仪器和试剂
Hitachi F-4500型荧光分光光度计(狭缝宽度为10 nm,光电倍增管负电压为400 V);UV-8500型紫外-可见分光光度计;PHS-3C型酸度计.
Zn(II)标准溶液:准确称取0.548 8 g二水合醋酸锌(含量>99.8%),加入适量水溶解,转移至250 mL容量瓶中,定容并摇匀,浓度为1.0 ×10-2mol/L;曙红 Y 溶液:1.0 ×10-3mol/L;1,10-邻菲罗啉溶液:1.0 ×10-3mol/L;上述溶液在使用时逐级稀释成所需浓度的工作溶液.BR缓冲溶液:0.2 mol/L的NaOH溶液与0.04 mol/L H3PO4、H3BO4和HAc的混合酸按一定比例混合,并用酸度计校正.实验用水为二次蒸馏水,所用试剂均为分析纯.
1.2 实验方法
依次准确移取一定量的Zn(II)标准溶液、1.0 ×10-4mol/L 的1,10-邻菲罗啉溶液1.5 mL、pH 3.90 的BR 缓冲溶液0.6 mL和1.0×10-4mol/L的曙红Y溶液2.0 mL于10.0 mL干燥洁净的比色管中,定容后摇匀,放置2 min后于荧光分光光度计上以λem=λex方式进行同步扫描,记录RRS光谱,然后于560 nm处测定体系的RRS强度IRRS和试剂空白的RRS强度I0RRS,且ΔIRRS=IRRS-I0RRS;以 λem=2λex和 λem=方式连续测量体系的散射强度ISOS和IFDS,绘制SOS和FDS光谱图,并分别于480 nm/240 nm和350 nm/700 nm处测量体系的散射强度ISOS和IFDS及试剂空白的散射强度I0SOS和I0FDS,ΔISOS=ISOS-I0SOS,ΔIFDS=IFDS-I0FDS;记录反应体系的荧光光谱.
2 结果与讨论
2.1 荧光光谱
图1是Zn(II)-1,10-phen-EY体系的荧光光谱,由图1可知:Zn(II)本身无荧光,1,10-phen在紫外区390 nm有弱荧光,当Zn(II)与1,10-phen共存时,其荧光特征变化不大;EY具有较强的荧光,其最大激发波长(λex)和最大发射波长(λem)分别位于544 nm和564 nm;当Zn(II)-1,10-phen-EY共存时,发生明显的荧光猝灭现象,最大λex和λem分别蓝移至519 nm和542 nm,另在542 nm处产生共振荧光峰(λex=λem=542 nm),并且荧光猝灭的程度在一定范围内与Zn(II)的浓度呈线性关系,该方法对于Zn(II)的检出限为3.04 ng/mL,故可利用该体系建立荧光猝灭法测定Zn(II)的含量.
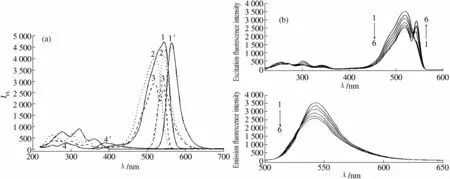
图1 Zn(II)-1,10-phen-EY体系的荧光光谱图Fig.1 Fluorescence spectra of the Zn(II)-1,10-phen-EY system
2.2 二级和倍频散射光谱
图2是体系的二级和倍频散射光谱,由图2可知:Zn(II)、1,10-phen和EY本身的SOS和FDS强度极其微弱,当Zn(II)与1,10-phen共存时,SOS和FDS仍很微弱;当Zn(II)-1,10-phen-EY共存时,体系的SOS和FDS强度明显增强,SOS和FDS散射峰(λem/λex)分别位于480 nm/240 nm,540 nm/270 nm,350 nm/700 nm,390 nm/780 nm,420 nm/840 nm,其散射强度较试剂空白分别增大 7.4,1.3,12.8,9.9,7.7 倍,因此选择 480 nm/240 nm SOS散射峰和350 nm/700 nm FDS散射峰作为测量波长,且该两波长处散射强度在一定范围内与Zn(II)浓度成线性关系,检出限分别为3.92 ng/mL和6.11 ng/mL,据此可建立SOS和FDS法测定Zn(II)的含量.

图2 Zn(II)-1,10-phen-EY体系的二级和倍频散射光谱图Fig.2 Secondary scattering and double frequency scattering spectra of the Zn(II)-1,10-phen-EY system
2.3 RRS 光谱
图3是Zn(II)-1,10-phen-EY体系的RRS光谱,可以看出:1)Zn(II)和1,10-phen单独存在时的RRS光强度极其微弱;2)当Zn(II)与1,10-phen共存时,RRS强度仍很微弱;3)EY本身在534 nm处有较强的RRS;4)当Zn(II)-1,10-phen-EY共存时,体系的RRS急剧增强,并在325 nm和560 nm出现新的RRS峰,且两波长处RRS强度的变化在一定范围内均与Zn(II)浓度成线性关系,故可利用该三元体系建立RRS法测定Zn(II)的含量;由于560 nm的线性关系较好,且灵敏度较高,检出限可达0.49 ng/mL,所以选择560 nm作为测量波长.
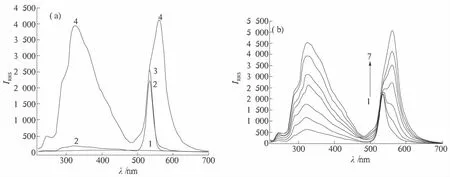
图3 Zn(II)-1,10-phen-EY体系的共振rayleigh散射光谱图Fig.3 Resonance rayleigh scattering spectra of the Zn(II)-1,10-phen-EY system
2.4 最佳的反应条件
RRS法测定Zn(II)的灵敏度高于荧光猝灭法、SOS法和FDS法,因此以RRS法为例讨论体系的反应条件、反应的机理、方法的选择性和分析应用.
2.4.1 酸度的影响 以BR缓冲溶液为酸度介质,考察了溶液酸度改变对体系RRS强度的影响(图4).随着溶液pH的增加,体系的RRS强度先增加后减小,而试剂空白的RRS强度逐渐降低,因此,体系的散射强度最大且稳定的酸度范围是pH 2.8~4.5,本实验选用pH 3.90.在最佳的酸度条件下,实验了BR缓冲溶液用量对RRS强度的影响,发现:最佳BR缓冲溶液用量为0.5~0.7 mL,本实验选用0.6 mL.
2.4.2 1,10-phen及EY用量的影响 试验中分别考察了浓度均为1.0×10-4mol/L的1,10-phen和EY用量对体系RRS强度的影响,结果如图5、6所示.随着1,10-phen或EY用量的增加,体系的RRS强度均呈现先增加后减小的趋势.当1,10-phen或EY用量较低时,反应未完全,离子缔合物的浓度较低,体系的RRS强度较低;随着1,10-phen或EY用量增大,离子缔合物的浓度增加,体系的RRS强度逐渐增大;当1,10-phen或EY用量超过一定范围时,其大的分子结构及分子间作用力阻碍离子缔合物的形成,体系的RRS强度逐渐降低.另外,随EY用量的增加,试剂空白的散射强度也逐渐增大.因此,最佳的1,10-phen用量范围为1.0~2.0 mL,本实验选用1.5 mL;最佳的 EY 用量范围为1.3 ~3.0 mL,本实验选用2.0 mL.
2.4.3 离子强度的影响 以0.1 mol/L NaCl为例考察了离子强度对RRS强度的影响,如图7所示,随着NaCl浓度的增加,溶液离子强度逐渐增大,而体系的RRS强度显著降低,由此可见:离子强度对体系的RRS强度具有明显的影响,体系的离子强度应越低越好.

图4 酸度的影响Fig.4 Effect of pH
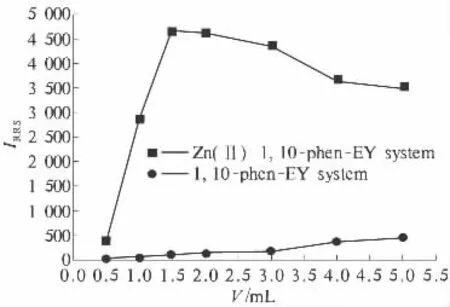
图6 曙红Y浓度的影响Fig.6 Effect of the EY concentration
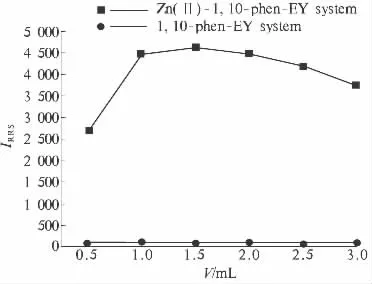
图5 1,10-phen浓度的影响Fig.5 Effect of the 1,10-phen concentration

图7 离子强度的影响Fig.7 Effect of the ionic strength
2.4.4 体系的稳定性 试验研究了体系的稳定性(图8),结果表明:1)反应温度在20~30℃时,体系较为稳定且RRS强度较大;当温度低于20℃或高于30℃时,体系的RRS强度均显著降低;2)在20~30℃的条件下该体系在2 min内反应完全,此后可稳定2 h,然后略有增加.这可能是由于放置时间过长离子缔合物聚集造成的.因此,实验均在常温下且试剂加完混匀2 min后进行测定.
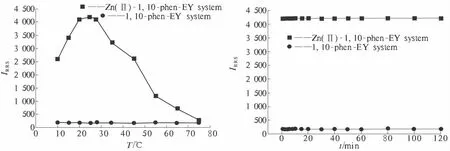
图8 体系的稳定性Fig.8 Stability of the system
3 分析应用
3.1 方法的灵敏度
在最佳的反应条件下,研究了体系的荧光、SOS、FDS和RRS法的一元线性回归方程、相关系数、线性范围和检出限,见表1.发现:1)RRS法测定Zn(II)的灵敏度高于荧光猝灭法、SOS法及FDS法;2)RRS法在560 nm处比在325 nm处具有较高的灵敏度和较好的线性.
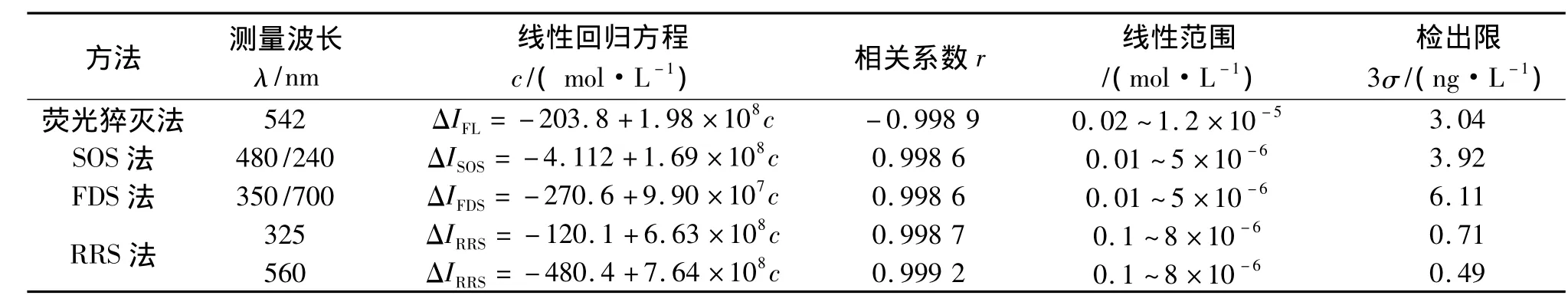
表1 标准曲线的有关参数和方法的检出限Tab.1 Analytical parameters of the calibration graphs and the detection limits
3.2 方法的选择性
在最佳的实验条件下,按RRS法考察了方法的选择性,结果表明:对于含Zn(II)5.0×10-6mol/L的测定体系,当相对误差控制在±5%范围内时,下列倍量的离子不干扰测定:人血清白蛋白、I-(20),色氨酸(22),苏氨酸(32),酪氨酸(16),Co(II)、抗坏血酸(6),葡萄糖、麦芽糖、蔗糖、乳糖(40),α-淀粉酶、Br-(100),Ba(II)(80),Ca(II)(600),K(I)、Mg(II)、SO2-4(400),CO2-4、HCO-3、NO-2、SO2-3、NH+4(200),F-(300),Cl-(1 000),Mn(II)、Cd(II)(3),Cu(II)用 5%硫脲溶液掩蔽(6.4),Fe(III)用 5%酒石酸钾钠掩蔽(4.2),Sr(II)(5),Ni(II)(2.4),pb(II)(3.2).由此可见,该体系具有较好的选择性,可用于实际样品的测定.
3.3 实际样品的测定
取健康成人发样,先后用肥皂和洗衣粉各洗涤3次,再用自来水和二次蒸馏水洗净,烘干剪碎.准确称取处理好的人发样0.2 g于小烧杯中,加入5 mL混合酸(HClO4∶HNO3=1∶5),盖上表面皿,低温加热消化并蒸发至近干.冷却后,用蒸馏水溶解过滤,调滤液pH约为4后转移入50 mL容量瓶中,用水稀释至刻度,摇匀.准确移取该溶液适量于10 mL比色管中,加入掩蔽剂,按实验方法中的RRS法测定试样中锌含量,结果见表2.

表2 实际样品的测定结果Tab.2 Determination results of practical samples
4 反应机理和共振Rayleigh散射增强的原因
4.1 离子缔合物的组成
分别用摩尔比法和等摩尔连续变化法测定了离子缔合物的组成(图9和图10),结果表明Zn(II):phen:EY=1∶2∶2.反应机理探讨如下:一个二价锌离子存在4个杂化空轨道;一个phen分子中含有两个带有孤对电子的N配位原子,当两者共存时,一个二价锌离子可以和两个phen分子配位形成较为稳定的二价阳离子螯合物.水溶液中,曙红 Y的分子结构式见图11,存在以下4种型体:H3L+、H2L、HL-和 HL2-,pKa1=-2.10、pKa2=2.85 和 pKa3=4.95[15],当溶液的 pH 在3.85 ~3.95(pKa2+1 < pH < pKa3-1)时,HL-为主要存在型体,且当溶液的pH为3.90(pH=(pKa2+pKa3)/2)时,HL-型体的量达到最大.因此,在pH 3.90的弱酸介质中,Zn(II)与phen先形成二价螯合阳离子,再进一步与一价大阴离子EY依靠静电引力和疏水作用力形成离子缔合物,其结构式如图12所示.

图9 摩尔比法Fig.9 Method of molar ratio
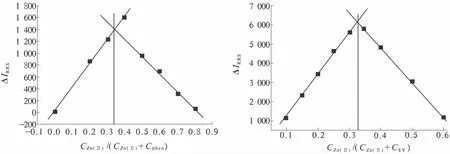
图10 等摩尔连续变化法Fig.10 Method of continuous variations of equimolar
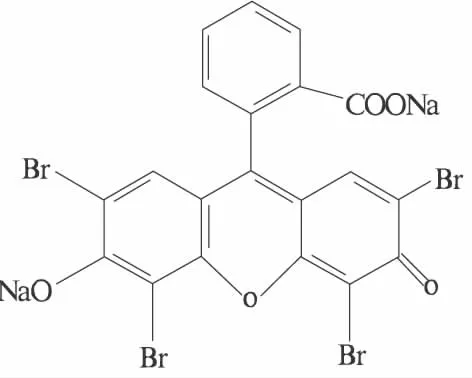
图11 水溶性曙红Y的分子结构式Fig.11 Structure of EY water soluble

图12 离子缔合物的结构式Fig.12 Structure of ion-association complex
4.2 共振Rayleigh散射增强的原因
图13是Zn(II)-1,10-phen-EY体系的共振 rayleigh散射光谱图与吸收光谱图的比较,可以看出,体系的共振rayleigh散射光谱均位于吸收带中,并且325 nm和560 nm的RRS峰分别位于吸收峰300 nm和548 nm附近,因此散射和光吸收之间发生共振而产生增强的rayleigh散射,这是散射增强的重要原因之一.
另外,根据简化的rayleigh散射公式IRRS=KMI0c可知,当测定条件(K、I0)和溶液浓度(c)一定时,散射光强度(IRRS)和粒子分子量(M)成正比,因此三元离子缔合物的形成使得分子量大幅的增加,这是导致散射增强的又一重要原因.

图13 Zn(II)-1,10-phen-EY体系的共振rayleigh散射光谱图与吸收光谱图的比较Fig.13 Comparison of the RRS spectrum and the absorption spectrum of Zn(II)-1,10-phen-EY system
[1] 林剑峰.必需微量元素锌营养研究进展[J].临床医药实践杂志,2004,13(12):887-889.
[2] 张继国,张兵,王惠君,等.1991-2009年中国九省区膳食营养素摄入状况及变化趋势[J].营养学报,2013,35(2):33-35.
[3] 龙跃,王桂红,卞立新,等.高灵敏度分光光度法测定痕量锌[J].郑州大学学报:理学版,2005,37(3):68-69.
[4] 董树国.浊点萃取—分光光度法测定茶叶中的痕量锌[J].光谱实验室,2011,28(6):3125 -3128.
[5] 张立新,刘冰,廉宁,等.流动注射浊点萃取结合荧光光谱法测定水样中的痕量锌[J].光谱实验室,2012,29(4):2144-2147.
[6] An Junmei,Yan Mihui,Yang Zhengyin,et al.A turn-on fluorescent sensor for Zn(II)based on fluorescein-coumarin conjugate[J].Dyes and Pigments,2013,99(1):1 -5.
[7] 赵永光,周永国,杨越冬.反相高效液相色谱法分离测定人发中痕量锌和铜[J].理化检验—化学分册,2001,37(9):403-404.
[8] Georgina M S Alves,Júlia M C S Magalhães,Helena M V M Soares.Voltammetric quantification of Zn and Cu,together with Hg and Pb,based on a gold microwire electrode,in a wider spectrum of surface waters[J].Electroanalysis,2013,25(2):493-502.
[9] 林洪,伍贤学,白红梅,等.锌—槲皮素—氯酸钾体系吸附催化波法测定痕量锌[J].冶金分析,2012,32(11):17-21.
[10] 何绍攀,范广宇,蒋小明,等.钨丝电热原子吸收光谱分析法测定痕量锌[J].分析化学,2010,38(8):707-710.
[11] 曾楚杰,罗济文,周能,等.浊点萃取—热喷雾火焰炉原子吸收光谱法测定水中痕量锌(II)[J].分析试验室,2011,30(3):87-89.
[12] 翟好英,张银钏,王碧.锌—硫氰酸盐—结晶紫体系共振散射法测定痕量锌[J].分析试验室,2011,30(3):94-97.
[13] Qin Mingyou,Liu Shaopu,Liu Zhongfang,et al.Resonance rayleigh scattering spectra,non-linear scattering spectra of tetracainehydro-chloride-erythrosin system and its analytical application[J].Spectrochimica Acta:Part A,2009,71(5):2063-2068.
[14] 杨晓溪,何琳,黄承志.罗曼紫复合试剂用于中药中汞残留的共振光散射光谱测定[J].中国科学:化学,2013,43(1):87-93.
[15] Fujita Y,Mori I,Toyoda M,et al.Determination of silver(I)by an association complex formation between silver-adenine and eosin[J].Analytical Sciences,1993,9(6):829 -834.

