高效液相色谱法测定土霉素片的含量
乔晓芳
(河南省安阳市食品药品检验所,河南 安阳 455000)
高效液相色谱法测定土霉素片的含量
乔晓芳
(河南省安阳市食品药品检验所,河南 安阳 455000)
目的建立土霉素片的含量测定方法。方法高效液相色谱法。采用Luna-C18色谱柱,以0.05 mol/L草酸铵溶液-二甲基甲酰胺-0.2 mol/L磷酸氢二铵(70∶25∶5)为流动相,用紫外检测器在282 nm波长处检测。结果土霉素片浓度在0.01~1 mg/mL范围内与峰面积线性关系良好(r=0.9990),平均回收率为100.1%。结论高效液相色谱法快速、简便、准确,可用于土霉素片的含量测定。
土霉素片;含量测定;高效液相色谱法;抗生素微生物检定法
土霉素为四环素类抗生素。本品为广谱抑菌剂。土霉素作用机制为药物能特异性地与细菌核糖体30S亚基的A位置结合,抑制肽链的增长和影响细菌蛋白质的合成。用于痢疾、沙眼、结膜炎、肺炎、中耳炎、皮肤化脓感染等。亦用于治疗阿米巴肠炎及肠道感染。土霉素片收载于卫生部药品标准抗生素分册,其含量测定方法是用抗生素微生物检定法二剂量法,方法步骤繁琐,培养时间长[1]。现采用HPLC法,方法简便、灵敏、准确。
1 仪器与试药
日本岛津LC-2010型高效液相色谱仪(自动进样器,四元泵,紫外检测器);抑菌圈自动测量仪CAM-III。
土霉素对照品(批号:130487-200702,含量为93.6% 中国药品生物制品检定所),土霉素片(宜昌人福药业有限责任公司,批号20130107 20121203石家庄市协和药业公司批号20130607);磷酸氢二铵、草酸铵,二甲基甲酰胺、盐酸均为分析纯,水为超纯水,空白样品(是指不含土霉素,其余辅料按制剂压片)自配。
2 方法与结果
2.1 色谱条件
WH-C18色谱柱(250 mm×4.6 mm,5 μm);流动相:0.05 mol/L草酸铵溶液-二甲基甲酰胺-0.2 mol/L磷酸氢二铵(70∶25∶5);流速:0.9 mL/min,柱温:30 ℃,检测波长:282 nm:进样量:20 μL[1]。
2.2 溶液制备
对照品溶液:精密称取土霉素对照品约25 mg置25 mL量瓶中,加0.1 mol/L盐酸溶液5 mL使溶解后,再加水至刻度,摇匀,制成每l mL含土霉素l mg的溶液,精密量取5 mL置50 mL量瓶中,再用0.01 mol/L盐酸溶液稀释至每l mL含土霉素0.1 mg的溶液。
供试品溶液:土霉素片(0.25克/片)取20片精密称定重量,精密称取适量(约相当于土霉素25 mg)置25 mL量瓶中,加0.1 mol/L盐酸溶液5 mL使溶解后,再加水,摇匀,滤过,精密量取续滤液5 mL置50 mL量瓶中,加0.01 mol/L盐酸溶液稀释至刻度,摇匀即得每l mL含土霉素0.1 mg的溶液。
2.3 系统适应性试验
精密称取土霉素对照品约25 mg置25 mL量瓶中,加0.1 mol/L盐酸溶液5 mL使溶解后,再加水至刻度,摇匀,制成每l mL含土霉素l mg的溶液,精密量取5 mL置50 mL量瓶中,再用0.01 mol/L盐酸溶液稀释至每l mL含土霉素0.1 mg的溶液,摇匀。在上述色谱条件下,取上述20 μL自动进样(图1),计算柱效为6478,分离度符合要求,连续进样5次,峰面积的RSD=0.48%。
2.4 空白干扰试验
取空白样品(是指不含土霉素,其余辅料按制剂压片)按测定方法依法操作,取20 μL自动进样,记录色谱图,未见杂质峰(图2)。
2.5 线性关系考察
取上述土霉素对照品溶液(1.0 mg/mL),分别用0.01 mol/LHCL配制成0.01、0.025、0.050 、0.075、0.10、0.50、0.75、0.25 mg/mL,共9个浓度系列对照品溶液,分别精密吸取上述对照品溶液各20 μL注入色谱仪自动进样,按拟定色谱条件测定。得各浓度峰面积,以峰面积为纵座标,浓度为横坐标绘制标准曲线,得回归方程:Y=-2.10636 ×10-3+2.0635×10-9X (r=0.9999)。结果表明,土霉素片浓度在0.01~1 mg/mL范围内与峰面积线性关系良好。
2.6 加样回收试验
分别精密量取对照品溶液(1 mg/mL)5.00、3.75、2.50 mL置50 mL量瓶中,各加入处方比例量的空白样品,用0.01 mol/L HCL稀释至刻度,摇匀,过滤,得0.1、0.075、0.05 mg/mL的溶液,按测定方法依法测定,自动进样20 μL,计算结果见表1。
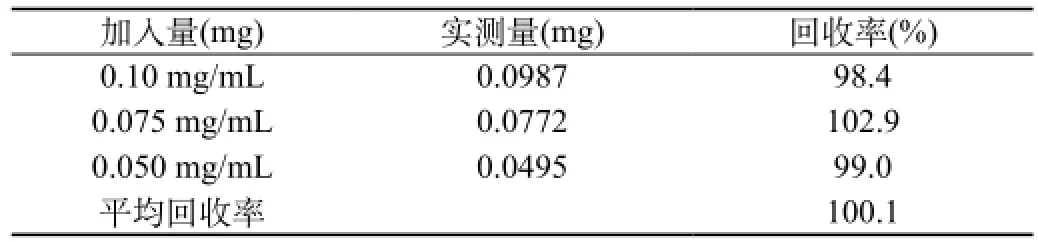
表1 HPLC法测定土霉素片回收实验结果(n=3)
图1 对照品溶液HPLC
2.7 稳定性实验
取0.1 mg/mL对照品溶液重复进样5次,每次20 μL,峰面积的RSD=0.48%。上述同一份溶液于0、2、4、6、8 h分别进样20 μL,测定土霉素峰面积,结果RSD=1.2% n=5)。
2.8 样品测定
取土霉素片按上述含量测定方法及抗生素微生物法测定法[2],结果见表2。
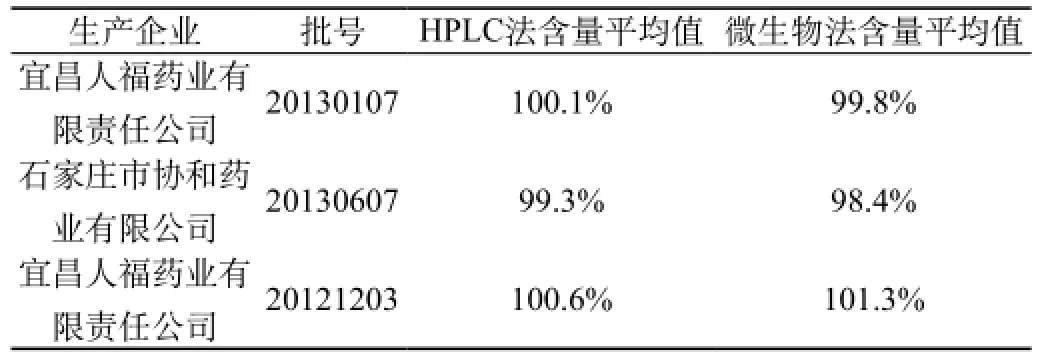
表2 样品测定HPLC法与微生物法结果比(n=3)
3 讨 论
3.1 色谱柱、流动相及检测波长,参考盐酸土霉素含量测定方法。使用C18柱和上述流动相,均有较理想的分离效果及适当的保留时间,测定波长选在282 nm也有满意的吸收值。本实验使用进口WH-C18(250 mm×4.6 mm,5 μm)柱效果更理想。
图2 辅料溶液HPLC
3.2 线性关系考察
取土霉素对照品配制的0.01~1 mg/mL的9个浓度系列的溶液,测得各点的平均峰面积,并以峰面积为纵坐标,浓度为横坐标绘制标准曲线,求得回归方程Y=-2.10636×10-3+2.0635×10-9X,相关系数r为0.9999表明土霉素在0.01~1 mg/mL的浓度范围内有良好的线性关系。
3.3 空白干扰试验:可看出空白样品在土霉素峰保留时间处(约10 min)无明显杂峰干扰。
3.4 加样回收率试验:从表1数据可说明本方法有较好的回收率100.1%。
3.5 稳定性试验,表明本法重复性较好RSD=0.48%,溶液在8h内稳定,能满足测定的要求。
3.6 高效液相色谱法与微生物法比较,从表2数据表明HPLC法与抗生素微生物法结果近似,HPLC法完全可以取代抗生素微生物检定法。用于土霉素片的含量测定[3]。
[1] 国家药典委员会.中华人民共和国药典(二部)[S].北京:化学工业出版社,2005:462-463.
[2] 中华人民共和国卫生部.药品标准(抗生素药品第一册)[S].1989.
[3] 杨开金.紫外分光光度法与抗生素微生物检定法测定土霉素含量方法比较[J].中国基层医药,2006,13(7):131.
Determination of the Content of Oxytetracycline Tablets by HPLC
QIAO Xiao-fang
(Anyang Institute for Food and Drug Control, Anyang 455000, China)
ObjectiveTo establish a method for determination of the content of Oxytetracycline tablets.MethodsHigh performance liquid chromatography. The WH-C18column, with 0.05 mol/L ammonium oxalate solution - two methyl formamide -0.2 mol/L diammonium hydrogen phosphate (70∶25∶5)as mobile phase, using a UV detector at 282 nm wavelength.ResultsOxytetracycline Tablets concentration relationship in 0.01-1 mg/mL scope with the peak area of linear(r= 0.9990), the average recovery rate was 100.1%.ConclusionThe HPLC method is rapid, simple and accurate, can be used for the content determination of Oxytetracycline tablets.
Oxytetracycline tablets; Content determination; HPLC; Microbiological method
R927.2
B
1671-8194(2014)21-0080-02

