高浓度氯化铵分解生成氨联产固体氯化钙的研究
刘润静,张振昌,胡永琪,蔡守军,侯元昇
(1.河北科技大学化学与制药工程学院,河北 石家庄 050018;2.青海盐湖工业股份有限公司,青海 格尔木 816000)
目前,我国纯碱的工业生产主要以氨碱法(索维尔法)、联碱法(侯氏制碱法)为主,分别占52.5%和40.2%。氨碱法是纯碱生产的主要方法,该过程在生产纯碱的同时,副产低浓度的氯化铵溶液,目前一般采取向10%左右的氯化铵溶液中加入石灰乳的方法,使氯化铵分解生成氯化钙和氨,然后通过蒸氨工艺将氨蒸出,氨再返回纯碱系统,实现氨循环。但此法会产生大量的浓度约为10%左右的氯化钙废液,造成了严重的环境污染和水资源浪费[1]。生产纯碱的另一个工业方法是联碱法,该方法通过冷析、盐析等过程将氯化铵从系统中以固体的形式产出,从而避免了蒸氨废液带来的污染[2-5]。固体氯化铵的主要用途是农用化肥,目前95%以上的氯化铵主要作为化肥使用。由于氯化铵是酸性含氯肥料,会造成瓜果类作物的甜度下降,口感不好,同时长期使用氯化铵化肥会造成土壤板结,因此出现了氯化铵大量过剩,造成资源的浪费[6,7]。因此本论文提出将高浓度氯化铵与粉体氢氧化钙进行反应,在实现氨循环利用的同时,直接副产固体氯化钙,其可以直接作为产品用作融雪剂和其他用途。该方法既可以避免环境污染,又可以实现资源的循环利用,从根本上解决了氨碱法所带来的环境污染问题,并且省去了蒸氨过程,降低了生产成本。对纯碱行业的发展具有重要意义。
1 实验
1.1 主要原料及仪器
氢氧化钙,工业品;氯化铵,工业级。

图1 高浓度氯化铵分解反应器图
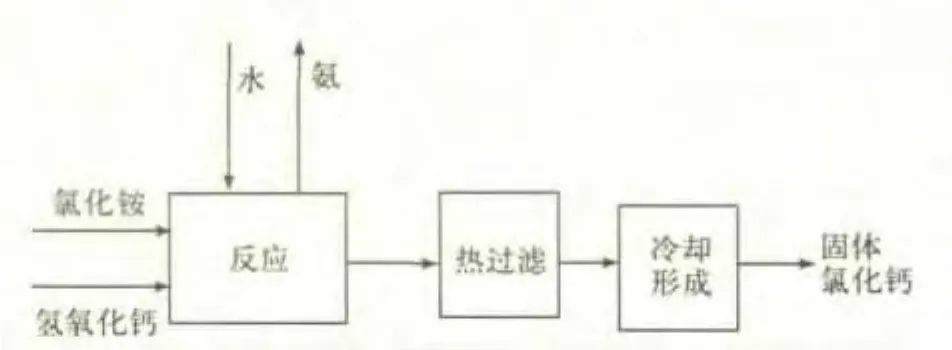
图2 高浓度氯化铵分解工艺流程图
1.2 高浓度氯化铵分解
高浓度氯化铵分解工艺流程如图2所示,将高浓度氯化铵和粉体氢氧化钙按一定比例加入反应器中,在一定温度下反应一段时间后,产物进行热过滤处理,得到的浆料进入冷却成型器,得到固体氯化钙。
本论文采用凯氏定氮法分析总氮量,再采用酸碱滴定检测游离氨含量,进而计算出氯化铵的分解率。
本论文探讨了反应温度、物料配比、反应时间、加水量对氯化铵分解率的影响,并进行了正交试验。
2 结果与讨论
2.1 单因素分析
2.1.1 加水量对氯化铵分解率的影响
取氢氧化钙与氯化铵摩尔比为1.1∶2,反应时间60min,温度115℃。考察加水量对氯化铵分解率的影响。实验结果如图3所示。
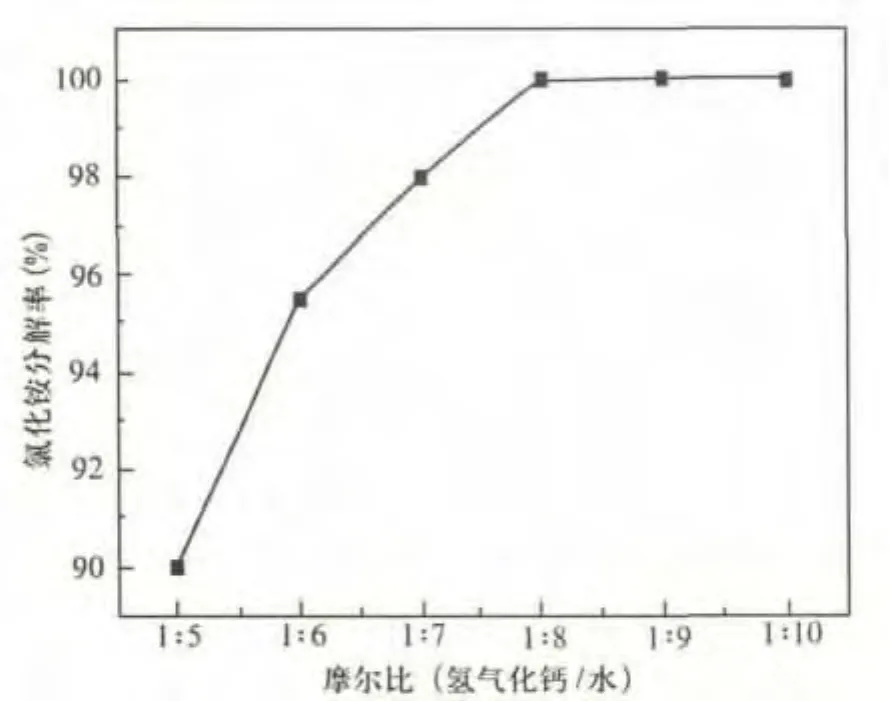
图3 加水量对氯化铵分解率的影响
由图3可知,随着水量的增加,氯化铵分解率不断提高,当氢氧化钙与水的摩尔比为1∶8时,氯化铵分解率达到100%。经分析当氢氧化钙与水的摩尔比为1∶8时,反应结束后氯化钙浓度为68%左右,这是由反应过程中水分蒸发所导致的。将浆料过滤、结晶可以得到固体氯化钙。使得氯化铵分解利用的同时,直接得到了固体氯化钙产品,从图中可以确定反应最佳加水量为氢氧化钙与水的摩尔比为1∶8。
2.1.2 温度对氯化铵分解率的影响
取氢氧化钙与氯化铵摩尔比为1.1∶2,反应时间60min,加水量为氢氧化钙与水的摩尔比为1∶8。考察温度对氯化铵分解率的影响。实验结果如图4所示。

图4 温度对氯化铵分解率的影响
由图4可以看出,随着温度的增加,氯化铵的分解率不断上升。当温度达到115℃时,氯化铵的分解率接近100%。从图中可以判定氢氧化钙湿法分解氯化铵的最佳温度是115℃。因为高浓度氯化铵的沸点在115℃左右,由于溶液的沸腾,使大量的游离氨解析,加快反应进行。
2.1.3 时间对氯化铵分解率的影响
取氢氧化钙与氯化铵摩尔比为1.1∶2,温度115℃,加水量为氢氧化钙与水的摩尔比为1∶8。考察时间对氯化铵分解率的影响。实验结果如图5所示。
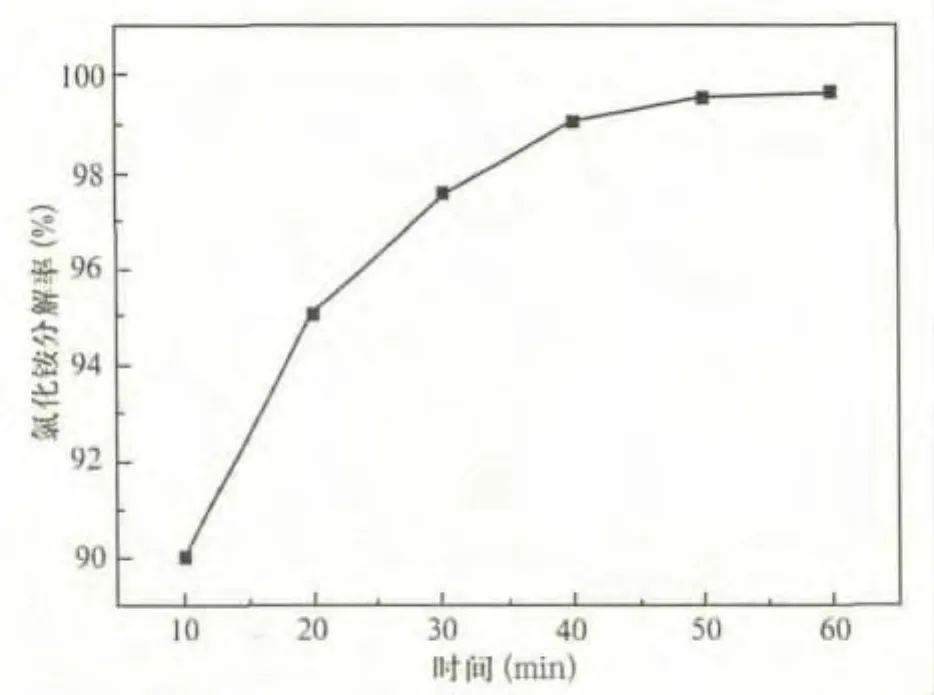
图5 时间对氯化铵分解率的影响
由图5可以看出,随着反应时间的延长,氯化铵分解不断上升。当反应时间达到50min时,氯化铵的分解率达到了最大值100%。
2.1.4 氢氧化钙与氯化铵摩尔比对氯化铵分解率的影响
取加水量为氢氧化钙与水的摩尔比为1∶8。温度115℃,时间为60min,考察氢氧化钙与氯化铵摩尔比对氯化铵分解率的影响。实验结果如图6所示。

图6 氢氧化钙与氯化铵摩尔比对氯化铵分解率的影响
从图6可以看出,随着氢氧化钙的增加,氯化铵的分解率在不断上升,当摩尔比达到氢氧化钙/氯化铵为1.15∶2时,氯化铵的分解率达到100%。氢氧化钙过量才能完成氯化铵完全分解,这是由于氢氧化钙的纯度所引起的。从图中可以判断,反应的最佳摩尔比为氢氧化钙与氯化铵的摩尔比为1.15∶2。
上述实验结果表明,适宜的反应条件为:当加水量为氢氧化钙与水的摩尔比为1∶8,温度为115℃,反应时间为50min,氢氧化钙与氯化铵的摩尔比为1.15∶2。
2.2 正交试验
2.2.1 正交试验方案
以氯化铵分解率为目标,分析前期实验数据后确定了主要影响因素为加水量、反应温度、反应时间和氢氧化钙与氯化铵的摩尔比。每个因素选择三个水平,列出了四因素三水平的正交试验因素水平表,见表1所示。按照正交试验表排列了9组实验,正交试验方案表见2所示。

表1 正交试验因素与水平表
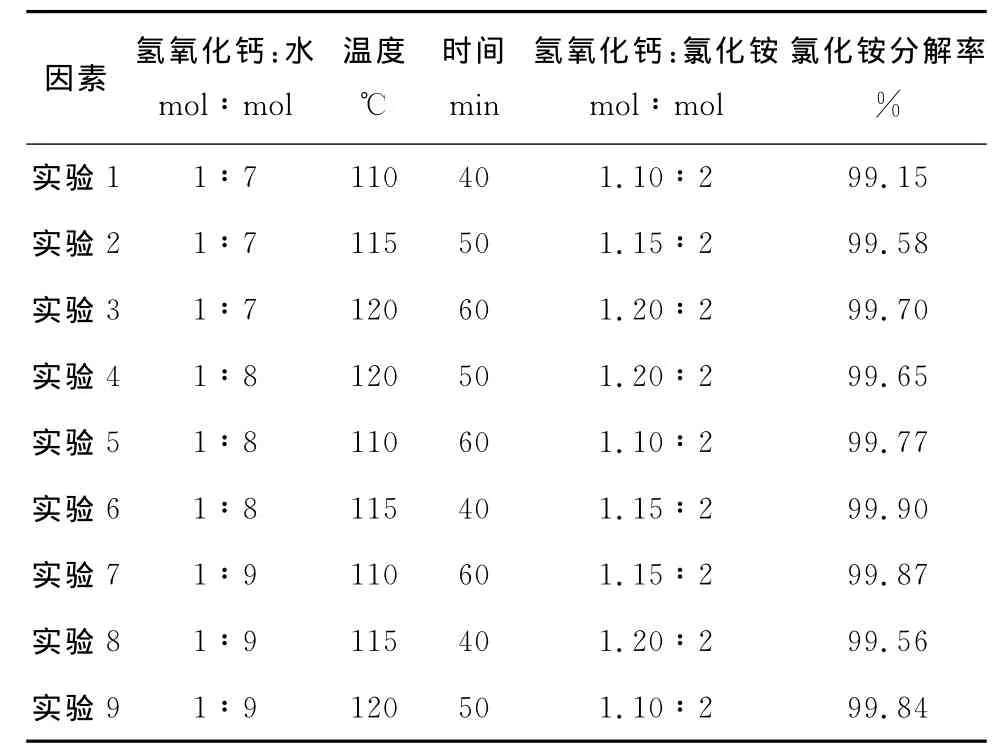
表2 正交试验方案表
2.2.2 正交试验结果分析
以氯化铵分解率为目标进行极差分析,分析结果见表3。
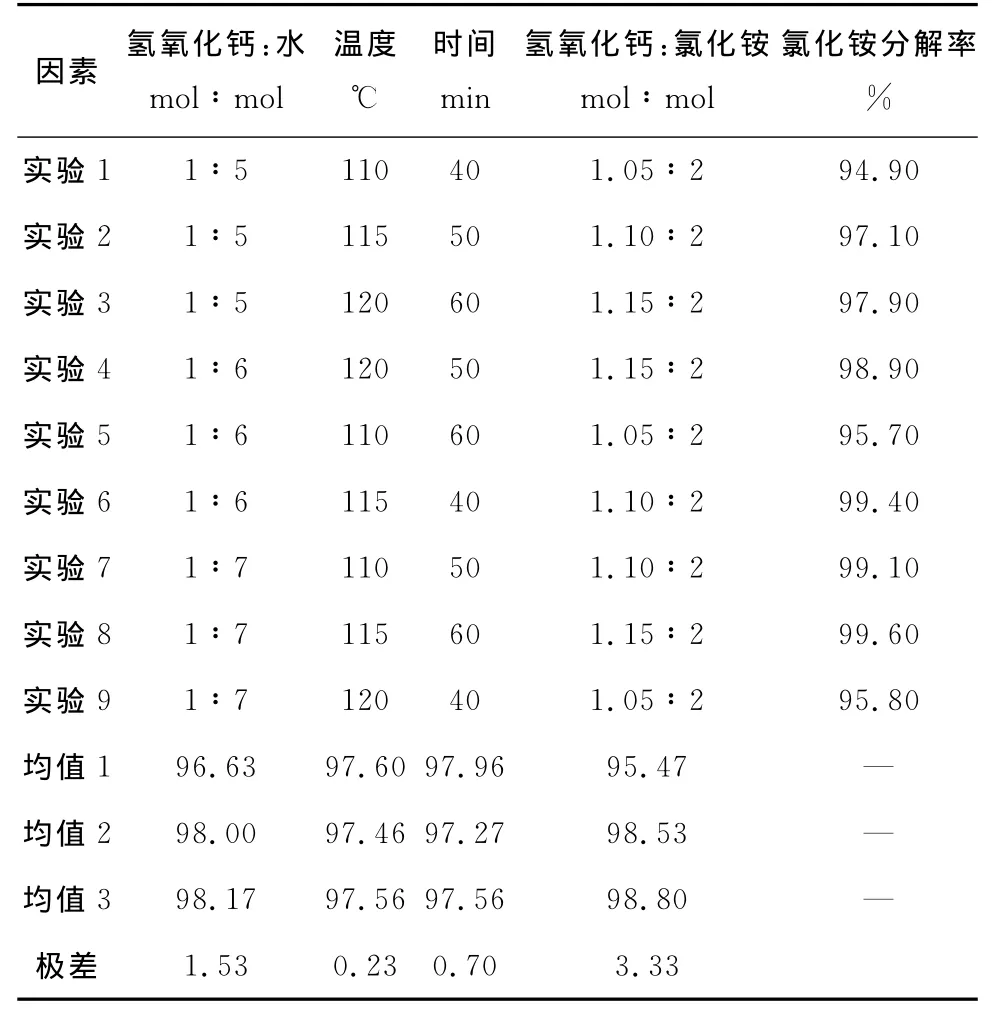
表3 氯化铵分解率极差分析表
由表2可知,第六组实验氯化铵分解率最高,氯化铵分解率为99.9%。即加水量为氢氧化钙与水的摩尔比为1∶8,温度为115℃,时间为40min,氢氧化钙与氯化铵摩尔比为1.15∶2。而从表3极差分析结果显示的较优组合为加水量为氢氧化钙与水的摩尔比为1∶7,温度为115℃,时间为60min,氢氧化钙与氯化铵摩尔比为1.15∶2。从此表3也可以看出对氯化铵分解率影响由强到弱的因素分别为加水量、氢氧化钙与氯化铵的摩尔比、温度和时间。
2.2.3 验证试验
对正交试验所得最优配方和极差分析所得最优配方进行验证试验。实验结果见表4所示。

表4 验证试验表
通过验证试验可知,由极差分析结果选出的最优组的氯化铵分解率高于实验最优组的氯化铵分解率,但两组结果相差不大。从能耗方面考虑,由极差分析结果选出的方案需要更多的能耗,不适合其工业化应用。所以最终确定方案为加水量为氢氧化钙与水的摩尔比为1∶8,温度为115℃,时间为40 min,氢氧化钙与氯化铵摩尔比为1.15∶2。
3 结 论
1)从经济和环保角度考虑,本论文采用半干法分解氯化铵是一种既经济且环保的方法:①得到经济效益高、有价值的新产品氨气和氯化钙;②避免了氯化铵大量过剩堆积造成的污染问题;③避免了10%的氯化钙废液对环境的污染问题。
2)实验确定了最佳的工艺条件:加水量为氢氧化钙与水的摩尔比为1∶8,温度为115℃,时间为40min,氢氧化钙与氯化铵摩尔比为1.15∶2。对于实现工业化打下了良好的基础。
[1] 杨燎原.浅析氨碱法环保工作面临的形势与对策[J].纯碱工业,2011(5):8-11
[2] 中国纯碱工业协会.纯碱工学[M].北京:化学工业出版社,1990
[3] 侯德榜.制碱工学[M].北京:化学工业出版社,1960
[4] 李祉川,陈歆文.侯德榜[M].天津:南开大学出版社,1990
[5] 裴正建.纯碱生产工艺综述[J].内蒙古石油化工,2011(5):38-39
[6] 毛知耘,周则芳,石孝均,等.再论氯化铵氮肥的发展前景[J].纯碱工业,2000,38(4):3-9
[7] 唐国昌,唐仁涛.氯化铵在复混肥加工中的应用[J].磷肥与复肥,2001,16(2):59-59

