灰胸竹鸡和棕胸竹鸡的线粒体基因组结构分析及比较
黄族豪, 柯坫华,柯娩娟
灰胸竹鸡和棕胸竹鸡的线粒体基因组结构分析及比较
*黄族豪, 柯坫华,柯娩娟
(井冈山大学生命科学学院,江西,吉安 343009)
竹鸡属包括灰胸竹鸡()和棕胸竹鸡()两种鸟类。两种竹鸡线粒体基因组全长为16726 bp,包含13个蛋白编码基因、22个tRNA、2个rRNA和1个控制区。基因排列顺序与红原鸡()一致,属于典型的鸟类排列顺序;碱基组成存在明显的AT偏向性。两种竹鸡线粒体基因组的13个蛋白质编码基因的序列长度和终止密码子都完全一样,但部分编码基因的起始位置以及起始密码子存在差异;两种竹鸡的线粒体基因组基因排列紧密;两种竹鸡线粒体全基因组序列之间共有1132个变异位点,其中缺失位点24个,遗传距离为0.071。
线粒体DNA;基因组;灰胸竹鸡;棕胸竹鸡;比较
随着DNA测序技术的迅猛发展,许多物种的全基因组序列得到了深入研究。线粒体基因组不含内含子[1],便于分析,已成为研究系统分类最常用的遗传标记。迄今,大量生物的线粒体全基因组被测定和分析,已测定的物种数达到了数千种。但绝大多数研究都是针对一个物种的线粒体基因组结构进行分析,或对近缘种的同源序列进行系统发生研究,但对不同物种线粒体基因组结构进行详细比较分析较少[2]。GenBank数据库为研究比较不同类群线粒体基因组结构提供了方便。
灰胸竹鸡()和棕胸竹鸡()隶属鸡形目(Galliforms)雉科(Phasianidae)竹鸡属()。灰胸竹鸡是我国特有种,主要分布于长江流域以南地区,北达陕西南部,西至四川盆地西缘,东及台湾省;棕胸竹鸡国内见于四川西南部、云南西部和南部,国外见于越南北部、缅甸和印度等地[3]。黄族豪等[4]报道了两种竹鸡线粒体DNA控制区结构比较;Shen et al[5]在研究鸡形目鸟类起源进化中测定了包括两种竹鸡在内多种雉科鸟类线粒体全基因组,但未对其结构进行比较分析。本研究根据GenBank上的序列对两种竹鸡线粒体全基因组结构进行分析并比较其异同。
1 材料与方法
1.1 序列来源
从GenBank下载灰胸竹鸡(序列号为EU165706和NC011816)[5]和棕胸竹鸡(NC020583和FJ752423)[5]各2个线粒体全基因组序列。
1.2 序列分析
用Clustal X程序[6]对DNA序列进行对位排列。用 DnaSP v5.0 软件[7]确定变异位点。用MEGA5.2[8]统计碱基组成,并用Kimura双参数模型[9]计算遗传距离。
2 结果与讨论
2.1 基因组结构与碱基组成
两种竹鸡线粒体基因组长度均为16,726 bp,包括1个非编码区(D-loop区)、13个蛋白质编码基因、22个tRNA基因和2个rRNA基因(16S rRNA和12S rRNA)。Shields & Helm-Bychowski[10]分析了3目40种鸟类线粒体基因组大小,平均为16.3~17.3 kbp。Desjardins & Morais[11]以原鸡()为材料测出第一个鸟类线粒体基因组全序列,长16,557 bp。我们统计了GenBank上31种雉科鸟类线粒体基因组平均长度为16,700 bp(16,677~16,841 bp),竹鸡的长度适中,略高于雉科鸟类的平均值。
两种竹鸡的线粒体基因排列顺序与鸟类线粒体基因典型排列顺序[12]一致,鸟类线粒体基因典型排列顺序与其它脊椎动物的不同。首先,轻链复制起始点(OL)是普通存在脊椎动物线粒体基因组tRNA-Cys和tRNA-Asn基因间的30~33 bp的非编码序列,这段序列可形成稳定的茎环结构,在脊椎动物中是比较保守的,但鸟类缺少这一结构[11];其次,哺乳动物mtDNA中Cytb和ND5基因间由tRNA-Glu和ND6隔开,而竹鸡Cyt b和ND5两个基因是连续的,并且tRNA-Glu-ND6基因紧接控制区(表1)。鹌鹑[13]、雪雁[14]、鹬类[15]和雀形目鸟类[16]线粒体基因组也均是这种排列顺序,这在鸟类中可能是一个普通现象。一些鸟类存在两个控制区,由于基因重排形成不同的基因顺序[17-18],但竹鸡属鸟类只有一个控制区。
对线粒体基因组全序列进行统计发现,两种竹鸡的碱基含量均是C>A>T>G, A+T含量高于G+C含量(表2),存在AT偏向性,与脊椎动物线粒体基因组的碱基组成相似[19]。
2.2 蛋白质编码基因
13个蛋白质编码基因分别为:细胞色素b基因、细胞色素C氧化酶3个亚基基因(COⅠ、COⅡ、COⅢ)、NADH氧化还原酶7个亚基基因(ND1、ND2、ND3、ND4、ND4L、ND5、ND6)以及2个ATPase亚基基因ATPase6和ATPase8。两种竹鸡线粒体基因组的13个蛋白质编码基因的序列长度都完全一致(表1),显示编码基因的保守性,只是ND2、ND3、ND4L、ND4、ND6的起始位置都差一个碱基(表1)。13个蛋白质编码基因序列长合计11,392 bp,占基因组全长的68.11%;其中序列最长的是ND5,达1,818 bp;最短的是ATPase8,仅为165 bp。与其它鸡形目鸟类一样,两种竹鸡的ND3基因序列174位点存在胞嘧啶的插入现象。
两种竹鸡大部分蛋白质编码基因(ND1、ND2、ND3、ND4L、ND4、ND6、Cyt b、COII、COIII、ATPase 8、ATPase 6)均使用典型的通用起始密码子ATG,但COI基因采用的是GTG。ND5基因比较特殊,在灰胸竹鸡和棕胸竹鸡中起始密码子不一样,分别是GTG和ATG,两种竹鸡的终止密码子完全一样,除COI、ND6分别以AGG、TAG作为终止密码子, COIII、ND2、ND4是不完全终止密码子T外,其余蛋白质基因的终止密码子均为TAA。两种竹鸡13个编码蛋白基因最常用的起始密码子是ATG;常用的终止密码子是TAA,这与其它鸟类相似[20]。COIII、ND2、ND4的密码子为不完全的终止密码子T,这种不完全终止密码子在鸟类中可能是一种普通现象[20],它通过在3’端添加PolyA完成转译终止[19]。柯杨等[21]统计了106种鸟类发现所有种类的COIII终止密码子均为T,推测COIII基因以不完全终止密码子T作为终止密码可能是鸟类线粒体基因组密码子进化过程中的一个共同特征,这种现象在其它的类群中并未出现,比如昆虫[22-23]、兽类[2]。两种竹鸡Cyt b基因的终止密码子是TAA,这与其他鸟类类似[24],但兽类的是AGA[2, 25](Gissi,1998;魏磊等,2011)。线粒体基因组起始密码子和终止密码子的同异性可能在系统进化研究中有特殊的意义[22].
2.3 rRNA和 tRNA
12S rRNA和16S rRNA位于tRNA-Phe和tRNA-Leu1之间,两种rRNA之间由tRNA-Val隔开。灰胸竹鸡和棕胸竹鸡的16S rRNA序列长度一样,均为975 bp;12S rRNA序列长度分别是974 bp和973 bp,相差仅一个碱基(表1)。
两种竹鸡线粒体均含有22种tRNA,基因长度在65-77 bp之间。除了tRNA-Leu和tRNA-Ser各对应2个tRNA外,其余的氨基酸均只有1个tRNA与之对应。两种竹鸡的tRNA-Phe、tRNA-Ile、tRNA-Gly、tRNA-Leu2、tRNA-Thr、tRNA-Glu等6种tRNA序列长度有1个碱基的差异,其它长度完全一致(表1)。
2.4 控制区
控制区所受进化压力较小,是线粒体基因组中碱基替换和长度变异最大的区域[26]。灰胸竹鸡和棕胸竹鸡的控制区均位于tRNA-Glu和tRNA-Phe之间,序列分别长1,146 bp、1,174 bp,相差28 bp。
对照石鸡属()鸟类控制区结构[27],分析了两种竹鸡控制区序列,确定了与终止相关序列(termination assocated sequences,TAS)和重链复制起始区(origin of H-strand replication,OH),识别了保守序列框(F-box、E-box、D-box、C-box、CSB1、CSB2、CSB3)、L-链和H-链启动子(L-strand promoter,LSP;H-strand promoter,HSP)。从图1中可以看出,两种竹鸡之间,TAS1、TAS2、F-box、E-box、D-bxo、CSB1的序列完全一样,但C-box有2个碱基的差异,CSB2/CSB3、 LSP/HSP各有 1个碱基的差异。可见,控制区保守序列框序列的保守性也是相对的。

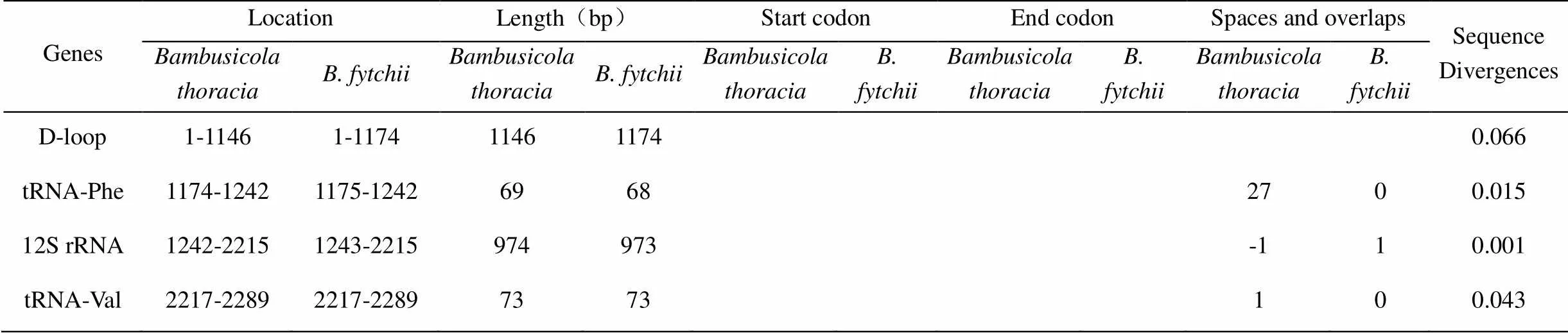
表1 灰胸竹鸡和棕胸竹鸡线粒体基因组比较
续表1 灰胸竹鸡和棕胸竹鸡线粒体基因组比较
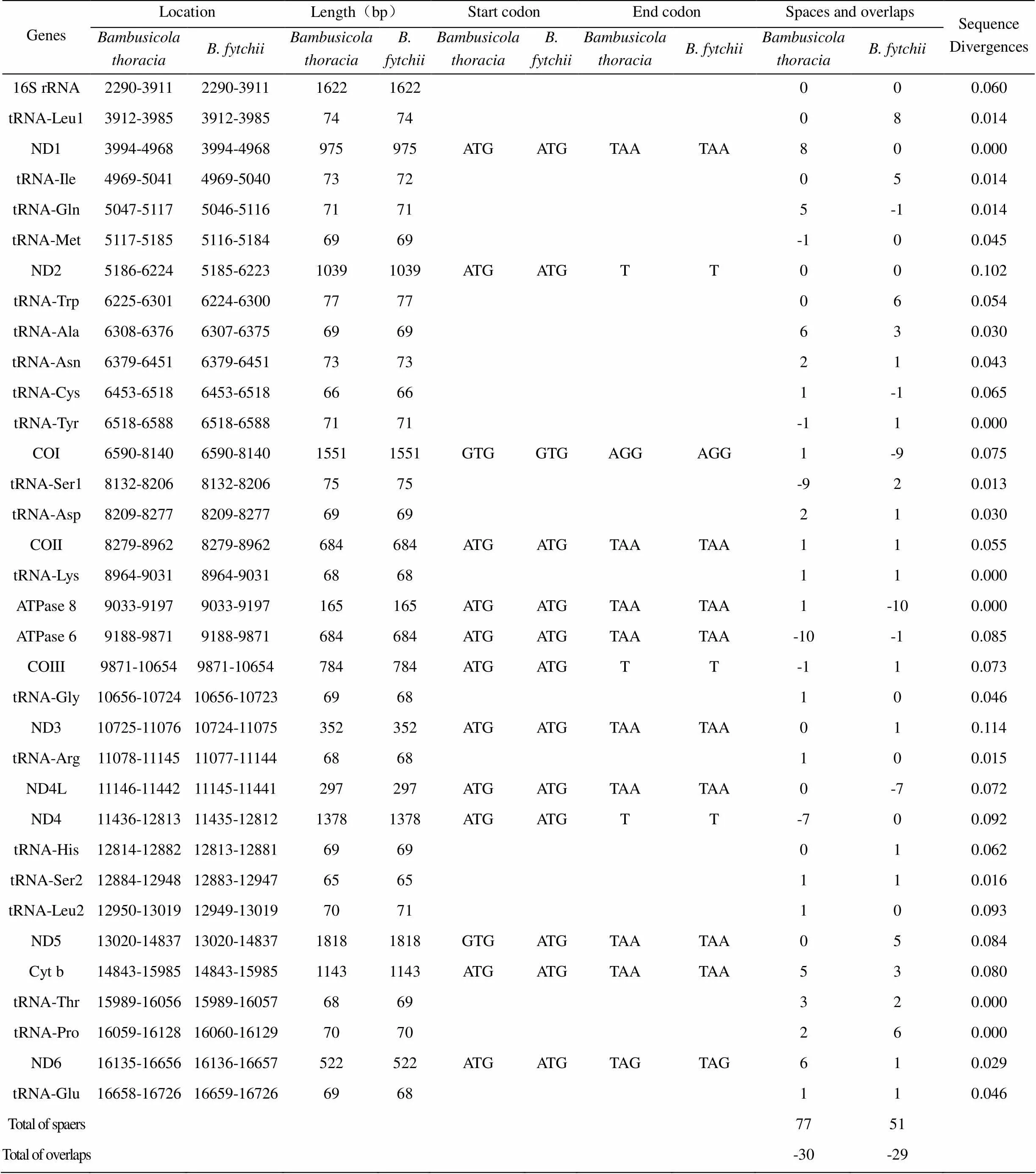
Table 1 Comparison of the mitochondrial genome between Bambusicola thoracia and B. fytchii
注:*负数代表重叠碱基数.

表2 两种竹鸡线粒体基因组碱基含量
2.5 基因重叠与间隔
动物线粒体基因之间的排列十分紧凑,一些相邻的编码基因甚至发生部分碱基的重叠;同时在一些动物线粒体基因组内,一些相邻基因之间往往存在长度不等的非编码序列,称为基因间区(intergenic spacer, IGS)。两种竹鸡的线粒体基因组基因排列紧密,重叠区长度1~10 bp不等(如表1)。灰胸竹鸡基因间区长度是77 bp,比棕胸竹鸡的长26 bp,两者主要的差异是灰胸竹鸡D-loop基因与和tRNA-Phe基因之间间区长度达到27 bp(如表1)。既没有重叠,也没有间隔的紧密排列基因均为9处(如表1)。
Haring, et al[20]统计9种鸟类线粒体基因间区,灰头阔嘴鸟()的最长,109 bp,北美潜鸭()的最短,36 bp。灰胸竹鸡和棕胸竹鸡的基因间区分别是77 bp和51 bp,位于Haring et al统计的范围之内。大多鸟类线粒体基因组重叠的碱基数在30个左右,并且ATPase 6 和ATPase 8基因之间大多都有10个碱基重叠[24],两种竹鸡也是这样,这种对紧缩容量的净化选择(purifying selection)作用是动物线粒体基因组在进化上一个特点,这对缩短整个基因组复制的时间十分有利[28]。
2.6 序列差异
对两种竹鸡线粒体全基因组序列进行对位排列后进行比较,发现两种鸟类之间共有1,132个变异位点,其中缺失位点24个,两者的遗传距离为0.071。
对所有基因分别对比分析发现,两种竹鸡的ND1、ATPase 8、tRNA-Tyr、tRNA-Lys、tRNA-Thr和tRNA-Pro等6种基因序列完全一样,序列差异最大的是ND3基因,达到0.114(如表1)。可见,ND3的变异速度比较快,是一种可用的遗传标记,已有一些研究人员用其来研究物种的系统发生[29-31]。
[1] Anderson S, Bankier A T, Barrell B G, et al. Sequence and organization of the human mitochondrial genome[J]. Nature, 1981, 290: 457-464.
[2] 魏磊,吴孝兵,诸立新,等.豹属线粒体基因组分析[J]. 中国科学: 生命科学, 2011, 54(10):917-930.
[3] 郑作新. 中国动物志鸟纲第四卷—鸡形目[M]. 北京:科学出版社,1978.
[4] 黄族豪,张姣,刘迺发.两种竹鸡线粒体DNA的遗传变异研究[J]. 动物学杂志, 2008, 43(1): 21-25.
[5] Shen Y Y, Liang L, Sun Y B, et al. A mitogenomic perspective on the ancient, rapid radiation in the Galliformes with an emphasis on the Phasianidae[J]. BMC Evolutionary Biology, 2010(1), 10:132.
[6] Thompson J D, Gibson T J, Plewniak F, et al. The Clustal X windows interface flexible strategies for multiple sequence alignment aided by quality analysis tool[J]. Nucleic Acid Research, 1997, 25(24): 4876-4882.
[7] Librado P, Rozas J. DnaSP v5. A software for comprehensive analysis of DNA polymorphism data[J]. Bioinformatics, 2009, 25(11):1451-1452.
[8] Tamura K, Peterson D, Peterson N, et al.MEGA5: Molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods [J]. Molecular Biology and Evolution, 2011, 28(10): 2731-2739.
[9] Kimura M. A simple method for estimating evolutionary rate of base substitutions though comparative studies of nucleotide sequences[J]. Journal of Molecular Evolution, 1980, 16(2):111-120.
[10] Shields G F, Helm-Bychowski K M.. Mitochondrial DNA of birds[J]. Current Ornithology, 1988(5):273-295.
[11] Desjardins P, Morais R. Sequence and gene organization of the chicken mitochondrial genome. A novel gene order in higher vertebrates[J]. Journal of Molecular Evolution, 1990, 212(4):599-634.
[12] Mindell D P, Sorenson M D, Dimcheff D E. Multiple independent origins of mitochondrial gene order in birds[J]. Proceedings of the National Academy of Sciences, 1998, 95(18):10693–10697.
[13] Desjardins P, Morais R. Nucleotide sequence and evolution of coding and noncoding regions of a quail mitochondrial genome[J]. Journal of Molecular Evolution, 1991, 32(2): 153-161.
[14] Quinn T W, Wilson A C. Sequence evolution in and around the mitochondrial control region in birds[J]. Journal of Molecular Evolution, 1993, 37(4):417-425.
[15] Wenink P W, Baker A J, Tilanus M G. Mitochondrial control region sequences in two shorebird species, the turnstone and the dunlin, and their utility in population genetic studies[J]. Molecular Biology and Evolution, 1994, 11(1): 22-31.
[16] Marshall H D, Baker A J.. Structural conservation and variation in the mitochondrial control region of fringilline finches (Fringilla spp.) and the Greenfinch (Carduelis chloris)[J]. Molecular Biology and Evolution, 1997,14(2): 173-184.
[17] Eberhard J R, Wright T F, Bermingham E. Duplication and concerted evolution of the mitochondrial control region in the parrot genus Amazona[J]. Molecular Biology and Evolution, 2001, 18(7): 1330–1342.
[18] Gibb G C, Kardailsky O, Kimball R T, et al. Mitochondrial genomes and avian phylogeny: complex characters and resolvability without explosive radiations[J]. Molecular Biology and Evolution, 2007, 24(1):269-280.
[19] Clayton D A. Replication and transcription of vertebrate mitochondrial DNA[J]. Annual Review of Cell Biology, 1991, 7(1): 453-478
[20] Haring E, Kruckenhauser L, Gamauf A, et al. The complete sequence of the mitochondrial genome of Buteo buteo(Aves, Accipitridae) indicates an early split in the phylogeny of raptors[J]. Molecular Biology and Evolution,2001, 18(10):1892-1904.
[21] 柯杨, 黄原, 雷富民. 黑尾地鸦线粒体基因组序列测定与分析[J]. 遗传, 2010, 32(9): 951-960.
[22] 曹天文, 王菊平, 宣善滨, 等. 猫蛱蝶线粒体基因组全序列分析[J]. 动物分类学报, 2013, 38(3): 468-475.
[23] 王菊平, 聂新平, 曹天文, 等. 大紫蛱蝶线粒体基因组全序列分析[J]. 动物分类学报, 2012, 37(1): 1-9.
[24] Nishibori M, Tsudzuki M, Hayashi T, et al. Complete nucleotide sequence of the Coturnix chinensis (blue-breasted quail) mitochondrial genome and a phylogenetic analysis with related species[J]. Journal of Heredity, 2002, 93(6): 439-444.
[25] Gissi C, Gullberg A, Arnason U. The Complete mitochondrial DNA sequence of the Rabbit (Oryctolagus cuniculus) [J]. Genomics, 1998, 50(2):161-169.
[26] Boore J L, Daehler L L, Brown W M. Complete sequence, gene arrangement, and genetic code of mitochondrial DNA of the cephalochordate Branchiostoma floridae (Amphioxus) [J]. Molecular Biology and Evolution, 1999, 16(3): 410-418.
[27] Randi E, Lucchini V. Organization and evolution of the mitochondrial DNA control region in the avian genus Alectoris[J]. Journal of Molecular Evolution, 1998, 47(4): 449-462.
[28] 黄族豪, 刘迺发.动物线粒体基因组变异研究进展[J]. 生命科学研究, 2010, 14(2):166-171.
[29] Docker M F, Youson J H, Beamish R J, et al. Phylogeny of the lamprey genus Lampetra inferred from mitochondrial cytochrome b and ND3 gene sequences[J]. Canadian Journal of Fisheries and Aquatic Sciences, 1999, 56(12): 2340-2349.
[30] Takacs Z, Morales J C, Geissmann T, et al. A complete species-level phylogeny of the Hylobatidae based on mitochondrialgene sequences[J]. Molecular Phylogenetics and Evolution, 2005, 36(3): 456-467.
[31] Wang W, Forstner M R J, Zhang Y, et al. A Phylogeny of Chinese leaf monkeys using mitochondrial ND3-ND4 gene sequences[J]. International Journal of Primatology, 1997, 18(3): 305-320.
THE STRUCTURE OF COMPLETE MITOCHONDRIAL GENOME AND ITS COMPARISON BETWEEN
*HUANG Zu-hao, KE Dian-hua, KE Wan-juan
(School of Life Sciences, Jinggangshan University, Ji’an, Jiangxi 343009, China)
Two species ofwere recognized asand. The entire mitochondrial genome of the two species is 16,726 bp in length, which contains 13 protein coding genes (PCGs), 22 tRNA, 2 rRAN, and one control region. The mitochondrial genomic organization and gene order are consistent with that of, belonging to typical gene order within birds, and the base composition exists obviously AT bias. The sequence length and teminator codon of the 13 PCGs of two species are just the same, but the initial position and codon of some PCGs are different. There are 1132 variable sites between the two species with 24 deletes among which, and the genetic distance between the two species is 0.071.
mitochondrial DNA; genome;;; comparison
Q959
A
10.3969/j.issn.1674-8085.2014.06.022
1674-8085(2014)06-0100-07
2014-09-09;
2014-10-19
国家自然科学基金项目(31260088);江西省主要学科学术带头人培养计划项目;江西省“赣鄱英才555工程”项目;江西省自然科学基金项目(20132BAB204022)
*黄族豪(1975-),男,湖南新宁人,教授,博士,主要从事鸟类分子生态学研究( E-mail: hzhow@163.com);
柯坫华(1972-),男,江西彭泽人,讲师,博士,主要从事鸟类学和动物行为学研究(E-mail: ssk002whu@163.com);
柯娩娟(1990-),女,湖北黄石人,井冈山大学生命科学学院生物科学专业2010级本科生(E-mail: kewanjuan@163.com).

