正交试验法优选黄芩饮片最佳切制工艺
戴衍朋,周 倩,孙立立*,曹玉华,王建刚
(1山东省中医药研究院,山东济南 250014;2山东博康中药饮片有限公司,山东济南 250014)
黄芩为唇形科植物黄芩Scutellaria baicalensis Georgi的干燥根,具有清热燥湿,泻火解毒,止血,安胎的功效[1]。黄芩临床应用广泛[2-5],为清热燥湿,泻火解毒之要药。除中医配方外,还大量用作中成药和提取黄芩素、黄芩苷的制药原料。
黄芩无论是中医处方调剂用还是制备中成药,均是以饮片为原料,黄芩饮片的制备方法,《中国药典》2010年版[1]规定为沸水煮10 min,取出,闷透或蒸0.5 h,切薄片。切制过程中蒸或煮主要是抑制酶对黄芩苷的酶解作用[6-8]。黄芩中的黄芩苷是其主要活性成分[9-13],具有抗菌、抗病毒、解热、镇痛、降压、利尿、抗肿瘤等多种药理活性,黄芩苷在酶的作用下可发生水解,生成黄芩素,易被氧化为绿色的醌类衍生物[14],影响黄芩的临床疗效。在高温处理抑制酶活性的同时,也不可避免地使有效成分流失和破坏。为更好地保证饮片质量,在灭酶的同时,需要最大程度的减少有效成分损失。因此本研究采用正交试验法对黄芩炮制工艺进行了优选,通过研究,明确了制备黄芩饮片的各项工艺参数,对于保证黄芩饮片的质量提供了重要的保障。
1 仪器和试药
Waters2695高效液相色谱仪 (Waters公司),R200D型电子天平 (Sartorius公司),DHG-9146A电热恒温鼓风干燥箱 (上海精宏实验设备有限公司),HH-4型数显恒温水浴锅 (金坛市晶玻实验仪器厂)。
甲醇为色谱纯,水为超纯水,乙醇、磷酸等其他试剂为分析纯,黄芩苷 (批号110715-201117,中国药品生物制品检定所)。黄芩药材购自亳州药材市场,经山东省中医药研究院林慧彬研究员鉴定为唇形科植物黄芩Scutellaria baicalensis Georgi的干燥根。
2 黄芩药材加热方法的考察
2.1 样品制备
2.1.1 煮法 取净黄芩药材100 g,投入沸水中,煮10 min,闷透,切薄片,干燥,即得。
2.1.2 蒸法 取净黄芩药材100 g,置已“圆气”的蒸锅内,蒸0.5 h,切薄片,干燥,即得。
2.2 外观性状 照《中国药典》2010年版黄芩饮片【炮制】项下要求对外观性状进行观察,主要包括切片形状,切面颜色和饮片完整情况。
2.3 内在质量 以黄芩中主要有效成分黄芩苷的量作为内在质量评价标准,照《中国药典》收载方法[1]进行测定。
2.3.1 色谱条件 Thermo Syncronis C18色谱柱(250 mm ×4.6 mm,5 μm),流动相为甲醇-水-磷酸 (47∶53∶0.2)。检测波长280 nm,体积流量1 mL/min,柱温25℃。
一是强化在评标阶段对虚假材料的甄别。二是坚持增加竞标活动的透明度,同时防范恶意质疑和投诉。三是统一供应商违规行为处罚政策,加大处罚力度。对虚假应标的处罚,监管部门应严格按《中华人民共和国政府采购法》第十三条、第七十七条(一)规定,处以罚款,并列入不良行为记录名单,一至三年内禁止参加政府采购活动。四是推出供应商违规行为的赔偿政策,打击供应商侥幸心理,调动政府采购各参与方追究违规供应商行为的积极性。
2.3.2 对照品溶液制备 取黄芩苷对照品适量,加甲醇适量制成每1 mL含60 μg黄芩苷对照品的溶液。
2.3.3 供试品溶液的制备 取本品粉末 (过40目筛),每份 0.3 g,精密称定,加 70%的乙醇40 mL,加热回流 3 h,放冷,滤过,滤液置100 mL量瓶中,用少量70%乙醇分次洗涤容器和残渣,洗涤液滤入同一量瓶中,加70%乙醇至刻度,摇匀,精密量取1 mL,置10 mL量瓶中用甲醇定容至刻度,经0.45 μm滤膜滤过,即得。
2.3.4 测定法 取黄芩苷对照品溶液及各黄芩供试品溶液各10 μL,注入液相色谱仪,照上述色谱条件进行测定,计算。
2.4 比较结果 黄芩饮片外观性状和内在质量结果见表1。由表1可知,两种方法制备的黄芩饮片,均未呈现绿色,表明蒸法和煮法均可杀灭黄芩药材中所含酶。但蒸法制备的黄芩饮片在切面颜色和饮片完整性方面均优于煮法,黄芩苷含量亦为蒸法较高,表明蒸的热处理方法优于煮法,更适于黄芩饮片的热处理。

表1 热处理方法对黄芩饮片质量影响Tab.1 Effects of different heating methods on the quality of Scutellaria pieces
3 “圆气”对黄芩饮片质量的影响
取净黄芩药材2份,每份100 g,置蒸锅内,分别以冷水 (不“圆气”)和沸水(“圆气”)蒸0.5 h,然后切薄片,干燥,得黄芩饮片。照“2.2”和“2.3”项下方法对二者进行外观性状和内在质量的比较,结果见表2。

表2 “圆气”对黄芩饮片质量影响Tab.2 Effects of“Yuanqi”on the quality of Scutellaria pieces
由表2可知,不“圆气”方法制备的黄芩饮片,切面略带黄绿色,表明该方法的杀酶效果较差,原因可能是冷水逐渐升温的过程中,黄芩酶尚未破坏,从而导致部分黄芩苷被酶解,进而变绿。黄芩苷含有量低于“圆气”蒸法制备的黄芩饮片。该结果提示,在蒸法处理黄芩药材时,应当在“圆气”后,加入药材处理。
4 正交试验设计优选黄芩切制工艺参数及结果
4.1 正交设计 根据预试验结果,首先确定了黄芩切制时宜采用蒸制的加热方法,在切制过程中影响黄芩饮片质量的主要因素为蒸制时间、切片厚度、烘制温度和烘制时间,因此将该四因素确定为正交试验的主要因素,每个因素分别设定三个水平,以传统质量标准 (外观性状)和内在质量标准 (黄芩苷量)为考察指标,选用L9(34)正交表进行试验。因素、水平设计见表3。
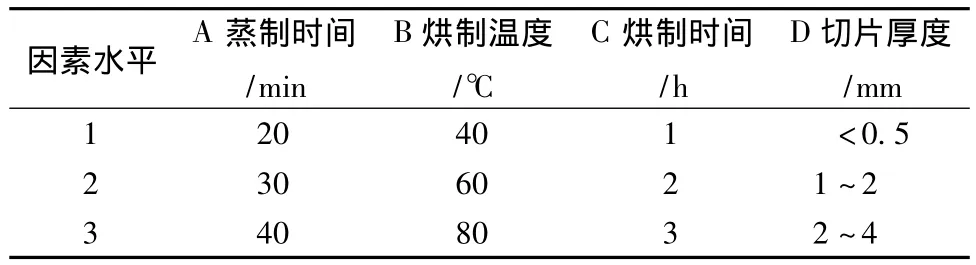
表3 因素水平Tab.3 Factors and levels
4.2 考察指标选择依据及评价标准
4.2.1 传统质量标准 参照《中国药典》2010年版黄芩【性状】项下规定 (类圆形或不规则形薄片。外表皮黄棕色或棕褐色。切面黄棕色或黄绿色,具放射状纹理。)将性状评分标准规定为:切面黄棕色4~5分,黄绿色2~3分,绿色1分,切片完整4~5分,有少量碎片2~3分,碎片多1分。评分结果见表4。
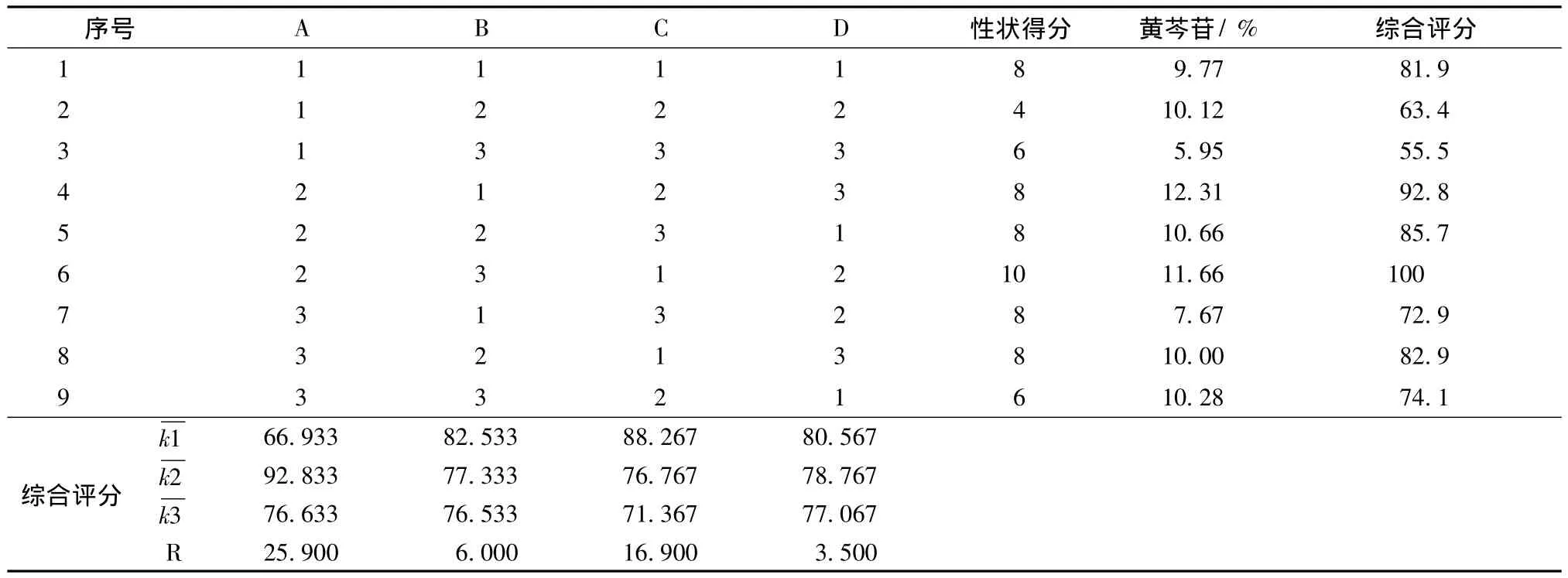
表4 L9(34)正交试验结果和直观分析Tab.4 Results of L9(34)orthogonal test and visual analysis
4.2.2 内在质量评价指标 以黄芩中主要有效成分黄芩苷量作为内在质量评价标准。照“2.3”项下方法进行测定。结果见表4。
4.2.3 综合评分标准 以综合加权评分的方法对各炮制品进行评价,传统质量和内在质量评价指标加权系数均定为0.5,各评价指标加权处理如下:外观性状评分=性状得分/9个样品中最高分×50;黄芩苷量评分=黄芩苷量/9个样品最高含有量×50;综合评分为二者之和;以综合评分为指标进行分析。
4.3 正交试验结果与分析 取净黄芩药材9份,每份100 g,置已“圆气”蒸锅中,照正交设计试验方进行试验。各制备样品进行传统质量和内在质量评分性状评分,结果见表4。
直观分析:由极差 (R)可知,对综合评分影响大小依次为A>C>B>D;对A因素>>,对B因素>>,对C因素>>,对D因素>>,可得黄芩最佳切制工艺为 A2B1C1D1。
由表5方差分析可见A因素 (蒸制时间)和C因素 (烘制时间)对试验结果显著性影响。
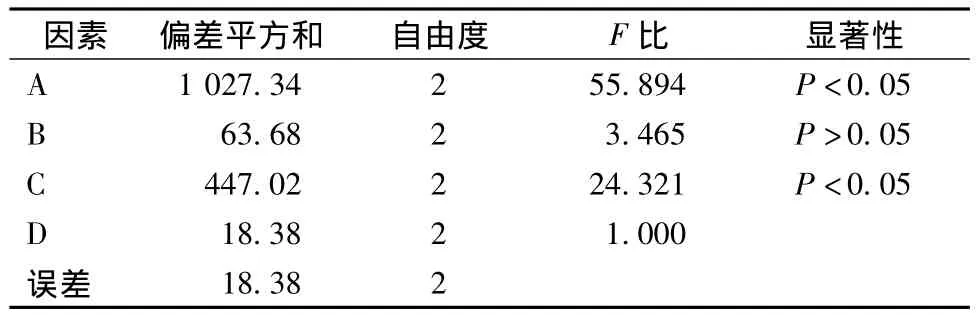
表5 方差分析Tab.5 Variance analysis
综合直观分析和方差分析结果及实际情况,黄芩最佳切制工艺为A2B1C1D2,即取黄芩药材,蒸制30 min,取出切1~2 mm薄片,40℃烘60 min,即得。
5 工艺验证
取3份黄芩药材,每份500 g,按最佳切制工艺制备3批黄芩饮片,分别进行性状评分以及黄芩苷的定量测定,结果见表6。

表6 工艺验证试验结果Tab.6 Results of confirmatory experiment
结果,制备的3批黄芩饮片外观性状均符合药典标准,黄芩苷含有量平均为11.95%,RSD为2.1%,表明确定的黄芩切制工艺稳定可行。
6 小结与讨论
本实验通过预试验对煮法和蒸法进行了比较,结果,煮法制得的黄芩饮片颜色晦暗,片型不齐整,黄芩苷含有量较蒸法低,推测是由于黄芩粗细质地不同,煮法渗透力不够,受热不均,致杀酶效果不一[15]。同时通过比较发现, “圆气”蒸的方法优于不“圆气”蒸,因此最终确定以“圆气”蒸法作为黄芩的软化切制方法。
根据预试验结果,采用正交试验法对黄芩的切制具体工艺参数进行了优选,以传统外观质量要求和内在质量为指标,采用综合评分法,把黄芩饮片的传统质量与内在质量两方面结合在一起,可较客观反映各因素水平对黄芩饮片质量的影响,优选的最佳切制工艺为:取黄芩药材,蒸制30 min,切1~2 mm薄片,40℃烘60 min,即得。采用优选的炮制工艺制备了3批黄芩饮片,验证试验结果表明,优选的切制工艺稳定可行。
通过正交设计,优选出黄芩切制最佳炮制工艺,对于规范黄芩的炮制工艺,指导企业饮片生产,保证黄芩饮片的质量具有一定的意义。
[1]国家药典委员会.中华人名共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:282.
[2]高学敏.全国高等中医药院校规划教材——中药学[M].2版.北京:中国中医药出版社,2007:96-97.
[3]章家铨.黄芩、金银花的药理与临床应用[J].新医学,1975,6(3):155-157.
[4]瞿佐发.黄芩的药理作用及临床应用[J].时珍国医国药,2002,13(5):316-317.
[5]童静玲.黄芩炮制方法及其临床应用[J].实用中医内科杂志,2008,22(8):62.
[6]凌庆罗,吕秉森.应用薄层层析法控制黄芩的炮制时间[J].中成药研究,1980(2):30-31.
[7]于留荣,王孝涛,刘美蓝.黄芩炮制的研究——炮制对粘毛黄芩主要成分的影响[J].中成药研究,1982(6):16-19.
[8]唐恢天.两种加工方法对黄芩质量影响[J].中国中药杂志,1991,16(1):29.
[9]冯 鑫,汪长中,汪天明,等.黄芩苷体外对白念球菌凋亡的影响[J].中成药,2012,34(8):1443-1446.
[10]云 云,汪长中,桂 丽,等.黄芩苷经由TLR4信号转导通路抗呼吸道合胞病毒作用的研究[J].中成药,2013,35(6):1116-1121.
[11]雷 芳.黄芩苷药理作用研究进展[J].中国药业,2010,19(15):87-90.
[12]黄芩苷对人肺腺癌A549细胞的抑制作用及相关机制[J].中成药,2012,34(11):2214-2216.
[13]Zhang D Y,Wu J,Ye F,et al.Inhibition of cancer cell proliferation and prostaglandin E2 synthesis by Scutellaria baicalensis[J].Cancer Res,2003,63(14):4037-4043.
[14]叶定江,张世臣,吴 皓.中医药学高级丛书——中药炮制学[M].2版.北京:人民卫生出版社,2011:386-390.
[15]袁俊贤,邵依囡,仵培坚.黄芩切制工艺的研究[J].中成药,1993,15(11):20-21.

