优化“分离以尿素为氮源的微生物”的实验
刘怡+吴彬
“分离以尿素为氮源的微生物”的实验属于高中生物学选修1《生物技术实践》(浙科版)中的内容。该模块是为了满足学生多样化发展的需要而设计的实验课,但在实际教学中,由于受到高考要求和实验条件的限制,真正以实验形式开展教学的学校很少,对于该实验的理解也停留在了理论的层面上,缺乏实际的操作实践。本文在实验研究的基础上,结合教学实践的尝试,针对该实验中存在的一些问题进行了反思,提出了一些改进的策略。
一、实验材料的选择和处理
该实验的目的是使用含有尿素的培养基分离有脲酶的细菌和利用指示剂颜色的变化检知脲酶所催化的反应;实验的内容是从土壤中分离出能利用尿素的细菌,观察菌落数,了解它在生态平衡中的作用,并以LB全营养培养基为对照,观察全营养生长细菌的菌落数。为了获得实验的成功,首先必须正确地选择和处理实验材料。[1]
(一)土样的获取
为了分离到能分解尿素的细菌,需要获取合适的土样。教材中只提到从有哺乳动物排泄物的地方获取,具体的方法并未说明,操作过程中由于实验材料获取不当很容易导致实验的失败。土壤中的微生物数量繁多、种类复杂,在富含有机质的土壤表层,有更多微生物生长。细菌适宜在中性环境的潮湿土壤中生长,且绝大多数分布在距地表约3~8cm的土壤层。因此在土壤取样时,可以从施用人畜粪便的农田等环境中选择肥沃、湿润的土壤,先铲去表层土3cm左右再取样,将样品装入事先准备好的信封中备用。
(二)制备土壤稀释液
教材中只说明了制备土壤稀释液的过程要在无菌条件下进行,实际上土样的称取也应该无菌操作,在超净台上酒精灯火焰旁进行。
在无菌条件下,称取1g土样,加到99mL无菌水的三角瓶中,振荡,即成10-2稀释液,从该稀释液中取0.5mL悬液加到4.5mL无菌水的试管中,经振荡制成10-3 稀释液,再依次制备10-4、10-5土壤稀释液。实验要求每次稀释后都要振荡10min,在实际教学中很难有那么长的时间给学生操作,可以适当缩短振荡时间,混匀即可。
二、尿素固体培养基的配制
该实验中分离以尿素为氮源的微生物所依据的原理是在氮源只有尿素时,这些微生物能利用尿素获得氮源而存活,其他微生物则因为缺乏氮源而死亡,因此尿素固体培养基的配制是本实验的关键。
(一)用琼脂糖代替琼脂
其他版本的教材中配制尿素固体培养基时添加的是琼脂,浙科版教材改为琼脂糖。琼脂在制作固体培养基时可作为凝固剂,但它是一种未被纯化的混合物,里面有一定量的含氮化合物。
琼脂糖是琼脂进一步纯化,去除了含氮化合物后的产物。利用琼脂糖作凝固剂,能防止含氮化合物对实验的干扰,有利于以尿素为氮源的细菌的筛选。
(二)适当降低尿素的浓度
教材中配制尿素培养基时,25mL培养基溶液中是加入了10mL含有2g尿素的尿素溶液,质量分数达到了8%,实验研究发现,经这种培养基培养长出的细菌含量很少,10-2的稀释度下也只是偶尔能看到1个菌落,高的稀释度下更难有结果出现。文献资料表明,尿素可在脲酶的作用下水解成碳酸铵进而生成氨,尿素浓度过高,产生的氨太多会导致培养基pH增大,不利于细菌生长。[2]若尿素浓度过低,产生的氨太少,酚红的显色现象则不明显。
为了确定尿素溶液的最佳比例,笔者配制了不同浓度梯度的尿素溶液进行实验,在25mL培养基溶液中分别加入10mL含有0.25g、0.5g、1g、1.5g、2g尿素的尿素溶液,结果表明,添加0.5g尿素的培养基中细菌生长较多,显色现象较明显。由此可见,适当降低配方中的尿素浓度,有利于实验效果的改善。
(三)尿素溶液的灭菌方法
尿素加热后会分解,因此不能使用高压蒸汽灭菌,一般采用的是过滤除菌法,可以使用G6玻璃漏斗或针头式过滤器过滤。教材中采用的是G6玻璃漏斗过滤的方法。玻璃漏斗使用前要先在121℃下用纸包好灭菌,使用后需要用1mol/L的HCl浸泡,并抽滤去酸,再用蒸馏水洗至洗出液呈中性,干燥后保存,操作起来非常烦琐,且过滤耗时很长。目前实验室中广泛采用的过滤处理装置为针头式过滤器。一次性针头式过滤器可与一次性注射器配套使用,过滤尿素时,一般选择孔径为0.22μm的针头式过滤器。这种方法不需要换膜和清洗滤器,省去了复杂、费时的准备工作,使用起来快速方便。
也可以使用化学灭菌法对尿素灭菌。取麝香草酚结晶一块,在烧杯中用蒸馏水反复洗涤三次,然后置于一定量的尿素溶液中,在冰箱内保存24小时后即可使用。由于麝香草酚对霉菌的抑制力较差,故配好后应在冰箱中保存,以免受到霉菌污染而使尿素失效,同时可以长期使用。这种方法非常简便,效果也较好,在医院中经常使用。
三、稀释涂布分离法的操作
分离以尿素为氮源的微生物需要使用稀释涂布分离的方法,教材中只是简要介绍了稀释涂布的内容和程序,对于移液枪的正确使用和涂布法的操作都没有说明,对于首次使用涂布分离法的学生来说困难很大。
(一)移液枪的使用方法
在设定容量时先通过粗调将容量值迅速调整至接近自己的预想值,再将移液枪横置,水平放置在自己的眼前进行细调,慢慢将容量值调至预想值,从而避免视觉误差。需要特别注意的是,从大值调整到小值时,刚好就行;但从小值调整到大值时,需要调超1/3圈后再返回,这是因为计数器里面有一定的空隙需要弥补。在该过程中,不能将按钮旋出量程,否则会卡住内部机械装置而损坏了移液枪。将移液枪垂直插入枪头中,稍微用力左右微微转动即可使其紧密结合。
在吸取液体之前,应该先预吸取、排放三次,让吸头内壁吸附一层液膜,确保移液的精度和准度。吸液时,先将移液枪排放按钮按至第一停点,再将吸头垂直浸入液面2~4mm以下,然后慢慢松开按钮回原点。放液时,先将按钮按至第一停点排出液体,稍停片刻后,继续按按钮至第二停点吹出残余的液体,最后松开按钮,确保吸头内无残留液体。整个过程应保持慢吸慢放,避免速度太快而产生反冲和气泡,导致移液的体积不准确,同时还要注意是否会有漏气现象。endprint
(二)涂布分离的操作
涂布分离时,若平板不干燥,会影响涂布的效果,有时会因涂布不均匀使某些部位的菌落不能分开,或在培养基上出现一层薄膜。因此涂布前可将制备好的平板预先放在培养箱里培养一段时间,待表面水分蒸发后再进行涂布。取0.1mL 10-4、10-5土壤稀释液加入尿素培养基和全营养LB培养基中,右手持玻璃刮刀平放在培养基表面,将菌液沿同心圆方向轻轻地向外扩展,可以先按一条线轻轻地来回推动,使菌液分布均匀,然后再按其垂直方向来回推动,平板边缘可弧线推动。需要注意的是,涂布完成后不宜立即将培养基倒置,而应先在室温下静置5~l0min,使菌液渗透入培养基内,再将培养基倒置培养。
此外,玻璃刮刀在使用前保存在70%酒精中,使用时先将玻璃刮刀在酒精灯火焰上引燃,待酒精燃尽、火焰熄灭后,先在培养皿盖内侧稍作冷却后再进行涂布。切忌将刚刚灼烧过的玻璃刮刀立即放入酒精中,以免高温引起酒精燃烧,造成危险。更换稀释度时,需要将玻璃刮刀灼烧灭菌并更换玻璃刮刀,若由低浓度向高浓度更换,也可以不更换。因此,建议先进行10-5土壤稀释液的涂布,再进行10-4土壤稀释液的涂布,这样在使用移液枪滴加液体时可以不用换枪头,玻璃刮刀也可以不用更换,省去了许多麻烦。
四、培养时间的调整
该实验中利用酚红作为指示剂检测脲酶所催化的反应,细菌培养时间为24~48h。
酚红是一种酸碱指示剂,显色范围为pH6.4~8.2,酸性条件下显黄色,碱性条件下显红色。细菌培养后,产生的脲酶将尿素分解成氨,从而使酚红由黄变红,从而可以检测出细菌是否已将尿素分解。随着培养时间的延长,红色区域的面积越来越大,据此也可以判断细菌分解尿素能力的强弱。
实验研究发现,在含有酚红的培养基中细菌生长会较缓慢。在没有添加酚红的尿素培养基中,培养24h后即可看到明显的菌落产生;添加了酚红的培养基中,则要到48h后才能看到菌落出现,若要观察到显色反应,时间则更久,至少需要72h,甚至一周左右。因此,建议可以将培养时间相对延长至72h以后,红色也会越来越明显。
五、改进后的实验效果
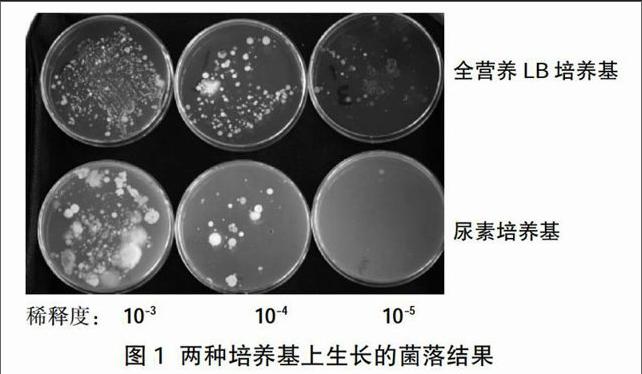
根据预期的实验结果,有脲酶的细菌菌落周围应出现着色环带,但教材中的实验结果图片只能显示出两种培养基上细菌数量的不同,并没有清楚地看见红色环带,学生很难产生直观的认识。经过反思和改进后,取得了较好的实验效果,如图1所示。
实验结果显示,在相同的稀释度下,全营养培养基中有较多菌落,尿素培养基中只有少量菌落;全营养培养基中菌落种类多样,尿素培养基中菌落种类较单一;有脲酶的细菌菌落周围出现红色环带,菌落较多的尿素培养基逐渐变红。值得注意的是,理论上尿素培养基中分离出的只有以尿素为氮源的细菌,但实际上尿素培养基中分离出的细菌不一定全都是以尿素为氮源的,有些细菌会利用其他微生物代谢的产物为氮源,如尿素分解后产生的氨就可为硝化细菌提供氮源,[3]因此还需要通过进一步的检测确定细菌的种类。
六、小结与反思
“分离以尿素为氮源的微生物”的实验教学不仅有助于学生更深入地认识微生物的利用,拓展生物科技视野,增进对生物科技与社会关系的理解,还有助于提高设计实验、动手操作等科学探究的能力。充分的实验准备和良好的实验效果是提高实验教学有效性、达成教学目标的基本途径和重要手段。
经过改良后的实验方案,既提高了实验的效率,又能取得较好的实验效果,学生们基本都能培养分离得到以尿素为氮源的细菌并观察到红色环带的现象。成功的实验结果更能激发学生学习的兴趣和动力,增强实验的自信心和积极性,提升对生物学科的热爱,有助于知识的意义建构,大大提高了实验教学的有效性。
参考文献:
[1] 李其安.高中生物实验教学中存在的问题及解决策略[J].中学生物学,2012(9):13-14.
[2] 窦向梅,王爱丽,郭宁宁.“分离以尿素为氮源的微生物”的实验改进[J].生物学通报,2010(11):51-53.
[3] 毕诗秀.“分离以尿素为氮源的微生物”实验教学目标及组织[J].生物学通报,2013(3):32-36.endprint

