层层组装微胶囊的制备及其缓释性能
张 维,李秋瑾,张健飞
(1.天津工业大学纺织学院,天津 300387;2.天津工业大学先进纺织复合材料教育部重点实验室,天津 300387)
通过层层组装(LbL)技术可以得到聚电解质中空微胶囊,其直径从纳米跨越到微米级别[1]。这类微胶囊的模板可以是固体也可以是液体[2-3],组装材料可以是高分子长链也可以是纳米颗粒[4],通过选用特殊构筑单元修饰囊壁,可使其具有pH响应性、磁响应性、超声响应性[5-7]。在聚电解质微胶囊众多的功能优势之中,缓释作用已成为最受关注的研究热点。将药物包埋到微胶囊中,药物随着时间延长逐渐释放,局部浓度始终保持在一定范围内,可提高对病变部位的作用效果[8]。此外,功能性微胶囊还能够实现不同需要的刺激性释放,如在热的刺激下发生突释,释放量大大增加[9];用葡萄糖调节囊壁的“开”与“合”,在开的状态下,物质可以迅速释放出来,而在合的状态下,物质的释放量微乎其微[10]。这种作用机制可应用到农药、杀虫剂、香精等物质的包埋与释放中。
在前期实验中,以杂化碳酸钙微粒为模板,成功制备了聚烯丙基胺盐酸盐(PAH)/聚苯乙烯磺酸钠(PSS)聚电解质微胶囊,并验证了微胶囊对罗丹明B的自沉积效应。有研究[11]证实,PAH/PSS微胶囊具有pH响应性,但组装选用的聚电解质分子质量不同,对微胶囊的渗透性能会产生很大影响。为后续实验顺利展开,以掺杂0.5 mg/mL PSS的碳酸钙微粒为模板,选用PAH/PSS为组装材料制备聚电解质中空微胶囊,比较不同层数微胶囊的表观形貌及其对罗丹明B的释放性能的影响,并采用2种不同释放方法实现罗丹明B的释放,以筛选出合适的释放方法进行研究。
1 实验部分
1.1 试剂与仪器
聚苯乙烯磺酸钠(PSS,70000)、聚丙烯胺盐酸盐(PAH,分子质量为120000~200000),阿法埃莎(天津)有限公司;四水合硝酸钙(Ca(NO3)2·4H2O)、碳酸钠(Na2CO3)、乙二胺四乙酸(EDTA),均为分析纯,天津市科密欧化学试剂有限公司;氯化钠、磷酸氢二钠、柠檬酸,均为分析纯,天津市风船化学试剂科技有限公司;罗丹明B,天津市天新精细化工开发中心。恒温水浴振荡器(哈尔滨市东联电子技术开发有限公司);台式高速离心机(长沙湘仪离心机仪器有限公司);冷冻干燥机(北京德天佑科技发展有限公司);数显集热式磁力搅拌器(巩义市英峪仪器厂)。
1.2 实验方法
1.2.1 含PSS碳酸钙微粒的制备
溶液配制:将Na2CO3和Ca(NO3)2分别配成浓度为0.05 mol/L的溶液。在Ca(NO3)2溶液中加入一定量PSS,使PSS在混合溶液中质量浓度为0.5 mg/mL,超声分散,使其完全溶解,室温静置20 min。
实验步骤:磁力搅拌条件下,向掺杂 PSS的Ca(NO3)2·4H2O溶液中迅速加入等体积的Na2CO3溶液,持续搅拌15 s,室温静置30 min,即可得到掺杂PSS的碳酸钙(CaCO3(PSS))微粒。将所得微粒洗涤3次,烘干贮存备用。
1.2.2PAH/PSS在CaCO3(PSS)微粒上的组装
溶液配制:将带有相反电荷的聚电解质PSS和PAH分别溶解在0.5 mol/L NaCl溶液中,配成质量浓度为2 mg/mL的组装溶液。
实验步骤:取适量 CaCO3(PSS)微粒分散在PAH溶液中,室温条件下恒温水浴振荡20 min,转速为95~110 r/min,离心去除上清液,洗涤/离心循环3次,如此第1层组装完成;然后将组装一层PAH的粒子分散在PSS溶液中,相同条件下振荡20 min,洗涤/离心循环3次。重复以上操作,组装需要的层数后,得到白色胶体粒子即为未去核的聚电解质微胶囊。
1.2.3 模板微粒的去除和中空微胶囊的制备
溶液配制:用NaOH调节浓度为0.1 mol/L的EDTA溶液,使pH值在7.0~7.5范围内,作为去除模板的专用溶液。
实验步骤:将微胶囊粒子分散到EDTA溶液中,水浴振荡30 min使其充分反应,取出离心,去除上清液,用水洗涤2次。以上过程重复4次以彻底除去CaCO3(PSS)微粒。将所得微胶囊分散在水溶液中并置于冰箱内冷藏。
1.2.4 微胶囊对染料的包埋
取适量微胶囊悬浮液与罗丹明B(80 μg/mL)溶液共混,室温静置12 h。离心分离,收集上清液。用水洗涤包埋后的微胶囊2次,去除溶液浮色。利用紫外-可见分光光度计确定罗丹明B的浓度-吸光度标准曲线,通过标准吸收曲线计算罗丹明B的释放量。
1.2.5 微胶囊对染料的释放
用磷酸氢二钠和柠檬酸配制不同pH值的缓冲溶液作为释放系统,利用标准曲线计算罗丹明B的释放浓度。设计了2种常用释放方法来追踪释放过程。
方法1:将包埋罗丹明B的微胶囊分散在pH值为5、7、9的缓冲溶液中,成为释放系统。在一定时间取样测定吸光度,取样同时补充相同量的缓冲溶液到系统中。每个pH值下,做3组平行数据。
方法2:将包埋罗丹明B的微胶囊分散在pH值为5、7、9的缓冲溶液中,成为释放系统。在规定的释放时间点,用同一个试样测量3组平行数据。
1.3 测试与表征
采用TM1000台式扫描电镜、S-4800场发射扫描电子显微镜(SEM)观察CaCO3(PSS)微粒、中空微胶囊的表观形貌及尺寸范围;通过JEM-2100F电子透射显微镜(TEM)分析聚电解质微胶囊的中空结构;用紫外-可见分光光度计测定罗丹明B的吸光度。
2 结果与分析
2.1 CaCO3(PSS)微粒的形貌表征
图1示出CaCO3(PSS)粒子在扫描电镜下的表观形貌照片。由图可知,采用1.2.1的实验方法制得的模板粒子球形结构较好,且有一定的单分散性,粒径大都分布在6~10 μm范围内。

图1 含PSS的碳酸钙微球Fig.1 SEM images of PSS-doped CaCO3particles.(a)Whole morphology;(b)Surface morphology
在制备碳酸钙粒子过程中掺入0.5 mg/mL的PSS,使其与Ca(NO3)2发生络合,导致 Ca(NO3)2和Na2CO3反应速度下降,从而得到了球形良好的CaCO3(PSS)粒子。在反应过程中,部分PSS被掺杂到CaCO3粒子内部或吸附在粒子表面,这也是CaCO3(PSS)微粒中含有少量PSS的原因。图1(b)示出CaCO3(PSS)微粒在500 nm尺度下的表面形貌,可以看到粒子表面有许多粒状的纳米颗粒,说明CaCO3(PSS)微粒是纳米粒子的聚集体。
2.2 聚电解质微胶囊的表征
2.2.1 聚电解质微胶囊的形貌
图2示出组装了不同层数微胶囊的扫描电镜照片。可以看到,组装3个双层的微胶囊表面仅有微小的起伏,随着组装层数的增加,微胶囊表面的颗粒明显增大,而且起伏程度也增大。EDTA溶液在不破坏囊壁的情况下,可以安全有效地去除CaCO3(PSS)模板,得到的微胶囊在冷冻干燥的情况下完全坍塌,形成了典型的褶皱形态。

图2 组装不同层数的微胶囊扫描照片Fig.2 SEM images of microcapsules with different layers
2.2.2 聚电解质微胶囊的透射电镜照片
(PSS/PAH)3PSS微胶囊水溶液的透射电镜照片如图3所示。微胶囊在溶液中仍然保持球体形貌,可以明显观察到其中空结构,囊内空间完好且饱满,这说明CaCO3(PSS)模板去除较为彻底,溶解过程中囊壁两侧产生的渗透压没有造成微胶囊破裂。

图3 聚电解质微胶囊的透射电镜照片(×3000)Fig.3 TEM image of polyelectrolyte microcapsules(×3000)
2.3 微胶囊对罗丹明B包埋与释放的表征
2.3.1 罗丹明B的浓度-吸光度标准曲线
由紫外-可见分光光度计测量可知,罗丹明B在553 nm处有特征吸收峰。配制不同浓度罗丹明B溶液,分别测量相应的吸光度,绘制罗丹明B浓度与吸光度的标准曲线,如图4所示。对曲线进行线性拟合可得到方程y=196.95x(R2=0.9995)。根据标准曲线方程可计算得到溶液中罗丹明B的浓度。
2.3.2 不同释放方法及pH值下染料释放行为

图4 罗丹明B质量浓度与吸光度标准曲线Fig.4 Calibration curve of RhB concentration vs.absorbancy
图5示出采用不同释放方法时,聚电解质微胶囊对罗丹明B的释放情况。采用方法1,碱性条件比酸性条件下释放速度快,释放量多,而方法2的结果正好相反。分析可知,方法1中影响释放的因素不仅有pH值,还有囊壁内外的渗透压,而方法2中仅有pH值对其释放行为有影响,相比而言,方法2较为科学合理,因此本文的释放实验均采用方法2来衡量。为进一步观察微胶囊在初始时间内的释放行为,选取前8 h的释放行为,结果如图6所示。

图5 不同释放方法下罗丹明B的释放行为Fig.5 Release behaviors of RhB using different methods.(a)Method one;(b)Method two

图6 罗丹明B在前8 h的释放行为Fig.6 Release behaviors of RhB within first 8 h
从图6可以看出,微胶囊在第1小时的释放量最为明显、释放速率较快,是突释区;第2小时是释放诱导区,微胶囊的释放量逐渐上升,但上升速度开始减慢;3~8 h为缓慢释放区,释放量在这个区域变化不大。由于微胶囊可以看成是半透膜,当囊内外存在较大浓度差异时,会形成一个浓度梯度,所以初始阶段释放速度较快,随着时间延长,释放速度逐渐降低。总体来说,聚电解质微胶囊呈现出多区域释放。
2.3.3 不同层数微胶囊对染料的释放行为
图7示出在pH=7的室温条件下,不同层数微胶囊对罗丹明B的释放结果。组装层数为7时,微胶囊对罗丹明B的释放量和释放速度出现最大值。继续增加层数,二者反而减小。这是因为组装层数越多,囊壁越厚,微胶囊的渗透性也随之改变,从而释放结果有所不同。通过层数来控制微胶囊的渗透性和释放量,成为层层组装微胶囊的一大优势。
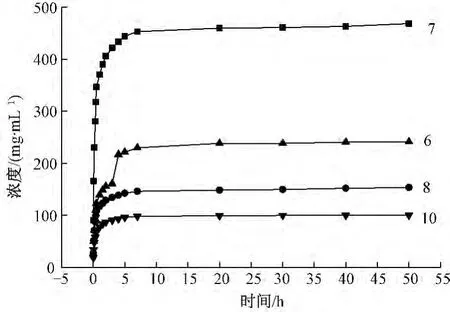
图7 不同层数微胶囊的释放Fig.7 Release behaviors of RhB from microcapsules with different layers
2.3.4 盐浓度对染料的释放行为
离子浓度是微胶囊囊壁结构和渗透性最大的影响因素之一。图8示出微胶囊在不同盐浓度下罗丹明B的释放行为。在0.05 mol/L的低盐浓度下,盐溶液的加入可提高释放量和释放速率,这是因为盐溶液有利于减小沉积在微胶囊内的罗丹明B分子间的排斥[12],增加罗丹明B负载后的稳定性,因此当囊外浓度较低时,罗丹明B可快速地释放。PSS为强聚电解质,微胶囊囊壁呈现负电性,在高盐浓度下其相互排斥作用受到较大屏蔽,部分渗入到囊壁中屏蔽了静电作用力,盐的加入起到了增塑剂的作用,致使囊壁形成无规和紧缩的结构[13],导致释放量降低。

图8 罗丹明B在不同盐浓度下的释放行为Fig.8 Release behaviors of RhB from microcapsules at different salt concentrations.
3 结论
1)以掺杂PSS质量浓度为0.5 mg/mL的碳酸钙微粒为模板、以PAH和PSS为壁材,采用EDTA溶液去除碳酸钙微粒模板,得到微米尺寸的中空微胶囊。层数越多,微胶囊的囊壁越厚,表面粗糙程度也越明显。
2)包埋罗丹明B的微胶囊在不同pH值条件下都能实现释放,且释放趋势相同,但释放速度及释放量有所不同,pH=5时可获得最大释放量。组装层数越多,囊壁越厚,渗透性随之下降,当层数为7时,可获得最优渗透性能。
3)在小于0.05 mol/L的低盐浓度下,盐溶液的加入可以提高罗丹明B的释放速率和释放量,但继续增大盐浓度,释放量反而降低。
[1] SHEPELINA O,LISUNOVA M O,DRACHUK I,et al.Morphology and properties of microcapsules with different core releases[J].Chemistry of Materials,2012,24(7):1245 -1254.
[2] PENG Caiyu,ZHAO Qinghe,GAO Changyou.Sustained delivery of doxorubicin by porous CaCO3and chitosan/alginate multilayers-coated CaCO3microparticles[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2010,353(2 -3):132 -139.
[3] SZCZEPANOWICZ K,DRONKA Gora D,PARA G,et al.Encapsulation of liquid cores by layer-by-layer adsorption of polyelectrolytes [J]. Journal of Microencapsulation,2010,27(3):198 -204.
[4] YUAN Weiyong, LU Zhisong, LI Changming.Controllably layer-by-layer self-assembled polyelectrolytes/nanoparticle blend hollow capsules and their unique properties[J]. Journal of Materials Chemistry,2011,21(13):5148 -5155.
[5] TOKUDA Y,MIYAGISHIMA T,TOMIDA K,et al.Dual pH-sensitive layer-by-layer films containing amphoteric poly(diallylamine-co-maleic acid)[J].Journal of Colloid and Interface Science,2013(399):26 -32.
[6] LIU Jiwei,ZHANG Yu,WANG Chunyu,etal.Magnetically sensitive alginate-templated polyelectrolyte multilayer microcapsules for controlled release of doxorubicin[J].Journal of Physical Chemistry C,2010,114(17):7673-7679.
[7] KOLESNIKOVA T A,GORIN D A,FEMANDES P,et al.Nanocomposite microcontainers with high ultrasound sensitivity[J].Advanced Functional Materials,2010,20(7):1189-1195.
[8] YAN Shifeng,ZHU Jie,WANG Zhichun,et al.Layerby-layer assembly of poly(L-glutamic acid)/chitosan microcapsules for high loading and sustained release of 5-fluorouracil[J].European Journal of Pharmaceutics and Biopharmaceutics,2011,78(3):336 -345.
[9] DING Chunrui,XU Shimei,WANG Jide,etal.Controlled loading and release of methylene blue from LbL polyurethane/poly(acrylic acid)film[J].Polymers for Advanced Technologies,2012,23(9):1283 -1286.
[10] CHEN Xingyu,LUO Jun,WU Wei,et al.The influence of arrangementsequence on the glucose-responsive controlled release profiles of insulin-incorporated LbL films[J].Acta Biomaterialia,2012,8(12):4380 -4388.
[11] ANANDHAKUMAR S,DEBAPRIYA M,NAGARAGA V,et al.Polyelectrolyte microcapsules for sustained delivery of water-soluble drugs[J].Materials Science &Engineering C-Materials for Biological Applications,2011,31(2):342 -349.
[12] GEORGIEVA R,MOYA S,HIN M,et al.Permeation of macromolecules into polyelectrolyte microcapsules[J].Biomacromolecules,2002,3(3):517 – 524.
[13] 仝维鋆,王丰,朱旸,等.原位凝聚法制备聚电解质微胶囊-模板中掺杂聚电解质量对微胶囊结构与性能的影响[J].高分子学报,2009(5):437-443.TONG Weijun,WANG Feng,ZHU Yang,etal.Polyelectrolyte microcapsules fabricated via in situ coacervation:the influence ofdoped polyelectrolyte amount in the templates on the instructures and properties[J].Acta Polymerica Sinica,2009(5):437 -443.

