反式(α)-细辛脑的制备技术与应用
张 宁邓志坚王琳琳何 群陈小鹏谢清若
(1.广西科技大学,广西 柳州 545006;2.广西亿康药业股份有限公司,广西 柳州 545006;3.广西大学,广西 南宁 530004)
反式(α)-细辛脑的制备技术与应用
张 宁1邓志坚2王琳琳3何 群2陈小鹏3谢清若1
(1.广西科技大学,广西 柳州 545006;2.广西亿康药业股份有限公司,广西 柳州 545006;3.广西大学,广西 南宁 530004)
反式(α)-细辛脑具有平喘、止咳、祛痰、镇静、解痉、抗惊厥及抗癌的药理活性,医学临床应用广泛。反式(α)-细辛脑在天然植物中含量低导致提取纯品困难,化学合成法是有效的制备途径。主要的合成路线有:以1,2,4-三甲氧基苯为原料经酰化、还原及脱水反应得到;以细辛醛为原料经还原和脱水反应制备;以氢醌为原料经氧化、三乙酰化、甲基化、甲酰化和脱水反应后即可得到反式(α)-细辛脑;以 erythro-2-甲基-3羟基-3苯丙酸为原料经立体选择合成直接得到目的产物。反式(α)-细辛脑的分离纯化主要有柱层层析的物理方法和催化异构的化学方法。
反式(α)-细辛脑;化学合成;分离;纯化
反式(α)-细辛脑又名 α-细辛脑、α-细辛醚,英文名α-asarone、asarin、asarum camphor,化学名为反式-2,4,5-三甲氧基-1-丙烯苯,分子式 C12H16O3,分子量 208.25,是一种白色或类白色结晶或结晶性粉末,能溶于乙醇、乙醚、冰乙酸、四氯化碳等,几乎不溶于水。其顺式异构体为 β-细辛脑,两者的结构式如图1所示。
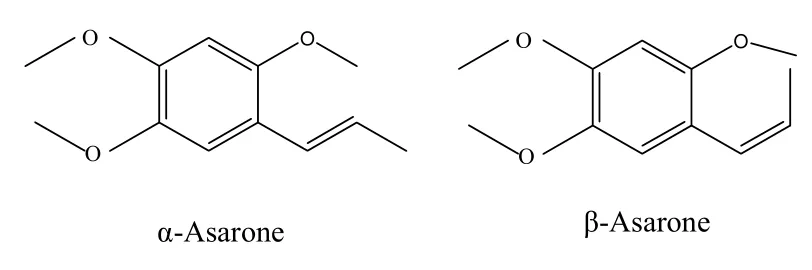
图1 α-细辛脑与β-细辛脑的结构式
反式(α)-细辛脑有抗心肌缺血、止咳去痰、抗惊厥、抗溃疡、抗癌、抗血小板、抗癫痫等多种药理活性,并具有祛风散寒,通窍止痛,温肺化饮的功效还可以抗菌、抗病毒;临床上已经广泛用于治疗上呼吸道感染、支气管炎、支气管哮喘、急性及慢性胆囊炎、胆石症、癫痫大发作等病症,尤其是对于肺炎、支气管哮喘和慢性阻塞性肺病的急性发作的治疗具有显著效果;同时其也是常用的医药中间体,而反式(α)-细辛脑的异构体β-细辛脑则已被证实具有致畸毒性。反式-细辛脑虽然可以从石菖蒲、水菖蒲、马兜铃科等植物的挥发油及胡椒种的叶中提取,但中药资源有限且其在天然植物挥发油和叶中的含量很低、成份复杂导致提取纯品困难,同时极易混入黄梓醚等致癌物[1],因此采用人工合成方法制备反式(α)-细辛脑才能满足医药用途的大量需求。
1 反式(α)-细辛脑合成技术
1.11,2,4-三甲氧基苯氧化-还原合成法
以1,2,4-三甲氧基苯为原料,采用不同溶剂和催化剂制备反式(α)-细辛脑,主要四种合成路线如下。
(1)以1,2,4-三甲氧基苯为原料溶解于其6倍体积的二氯甲烷中,加入催化剂无水三氯化铝、无水氯化锌或碘为催化剂升温至回流反应4 h,经甲醇重结晶得到1,2,4-三甲氧基苯甲醛,或者以二甲基甲酰胺为溶剂与三氯氧磷反应6 h得到1,2,4-三甲氧基苯甲醛,再与格氏试剂乙基溴化镁或乙基溴化碘反应,最后反应产物溶解到苯或无水甲苯中脱水制备反式(α)-细辛脑[2-4],具体的合成路线如图2-2a和2b所示。
(2)以1,2,4-三甲氧基苯为原料直接经Vilsmeier反应,反应产物与丙酸酐混合,搅拌溶解加热升温至回流3h左右减压蒸馏,蒸馏产物重结晶后可制备产物反式(α)-细辛脑[5], 具体的合成路线如图2-2c所示。
(3)以 1,2,4-三甲氧基苯为原料在无水氯化铝的催化作用下与丙酰氯反应生成1,2,4-三甲氧基苯丙酮,将其溶解于甲醇中加入催化剂硼氢化钠或氢化铝锂升温至 40℃,反应 2 h后洗涤干燥得到1,2,4-三甲氧基-1-苯丙醇,再经丙酸酐脱水制得目的产物反式(α)-细辛脑,具体的合成路线如图2-2d所示。
(4)以 1,2,4-三甲氧基苯为原料与二甲基甲酰胺甲酰化制备1,2,4-三甲氧基-1-苯甲醛,产物在丙酸酐作用下得到丁烯酸,再经脱羧制备反式(α)-细辛脑或1,2,4-三甲氧基-1-苯甲醛在格氏试剂作用下还原为1,2,4-三甲氧基-1-苯甲醇,经硫酸铜脱水制备反式(α)-细辛脑。具体的合成路线如图2-2e所示。

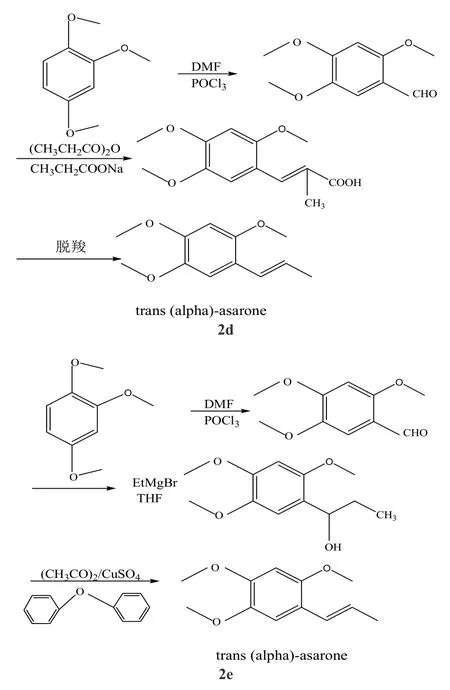
图2 1,2,4-三甲氧基苯为原料制备反式(α)-细辛脑的反应
其中图2-2a中产物的收率高且不需要分离直接可得目标产物,但是在第一步反应中使用了有毒害的溶剂丙酰氯;图2-2b的合成线路第一步生成三甲氧基苯甲醛的过程中副反应较多而且还使用苯和甲苯等有毒有害溶剂,第二步还原过程中格氏试剂的使用导致整个生产过程中不能有水存在,加大了操作难度且脱水步骤控制不当会生成顺反异构体两种产物,为除去有毒的顺式细辛脑必须增加分离顺反异构体的工序,这不仅影响了顺式细辛脑的产品质量还增加其生产成本;图2-2c中反应简单但不宜放大生产,操作过程中需要高温蒸馏且产率不高;图2d反应步骤简单,产物纯度高,成本昂贵,产物分离困难,收率有待进一步提高;图2-2e反应时间短,副反应少,产品的纯度及收率高,但成本较高,但反应温度高,且脱水过程中所用的溶剂二苯醚价格昂贵,整个制备过程成本较高。
1.2细辛醛脱水-异构合成法
细辛醛,又名2,4,5-三甲氧基苯甲醛,以细辛醛为起点制备反式(α)-细辛脑,第一步原料与格氏试剂乙基溴化碘或乙基溴化镁反应,反应产物经无水硫酸铜催化脱水后得到顺式与反式细辛脑两种同分异构体;或者原料直接经Witting反应制备顺式与反式细辛脑的混合物[6-8],最后两种同分异构体的混合物经分离纯化可得到反式(α)-细辛脑,具体合成路线如图3所示。
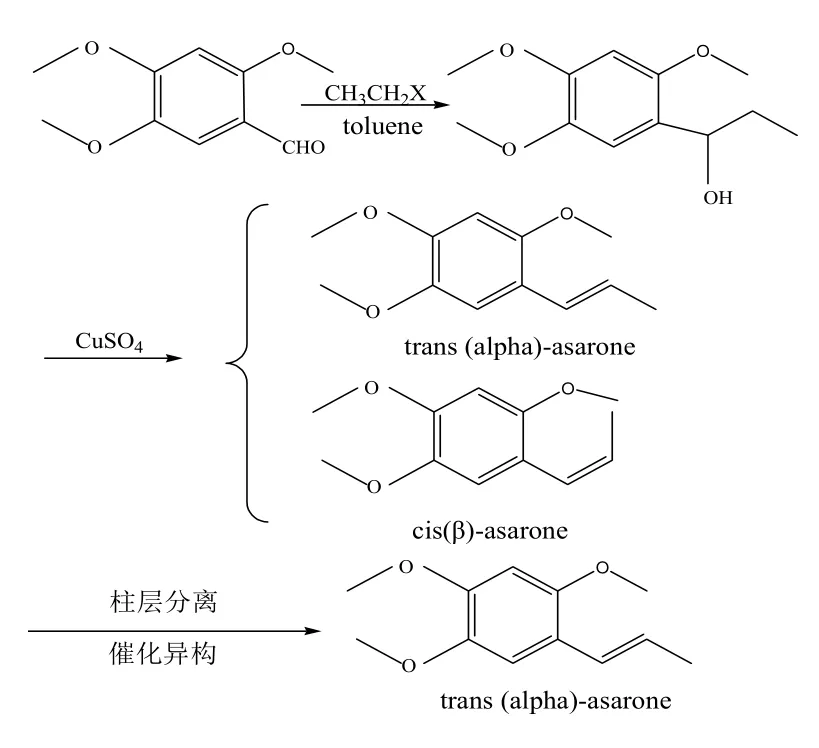
图3 细辛醛为原料制备反式(α)-细辛脑的反应
图3合成路线较简单,可方便地制得顺式与反式-细辛脑,反应经2.5 h后收率达到80.2%,但制备过程中使用了高毒性的有机溶剂甲苯,且最终产物为顺式与反式两种同分异构体,故仍需对其进行分离纯化才能获得反式(α)-细辛脑,同时格氏试剂的使用同样要求无水存在,不便于工业化。
1.3氢醌氧化-酰化-脱水合成法
氢醌,又名对苯二酚,以氢醌为原料经氯酸钠氧化、乙酸酐三乙酰化、硫酸二甲酯甲基化、Vilsmeier甲酰化和丙酸钠脱水反应可制备得到反式(α)-细辛脑[9-11],具体合成路线如图4所示。
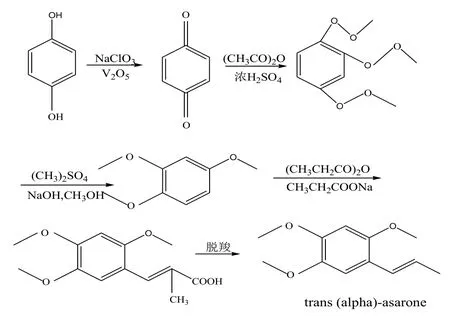
图4 氢醌为原料制备反式(α)-细辛脑的反应
图 4的合成路线中各反应条件相对温和容易控制,收率高,副反应少,立体选择高,反应过程没有使用有毒有害溶剂,成本相对便宜,但其工艺流程太长,工序繁琐。
1.4erythro-2-甲基-3羟基-3苯丙酸合成法
以erythro-2-甲基-3羟基-3苯丙酸为原料经立体选择合成直接得到目的产物或经脱水和脱羧反应得到反式(α)-细辛脑[12-13],具体合成路线如图5所示。
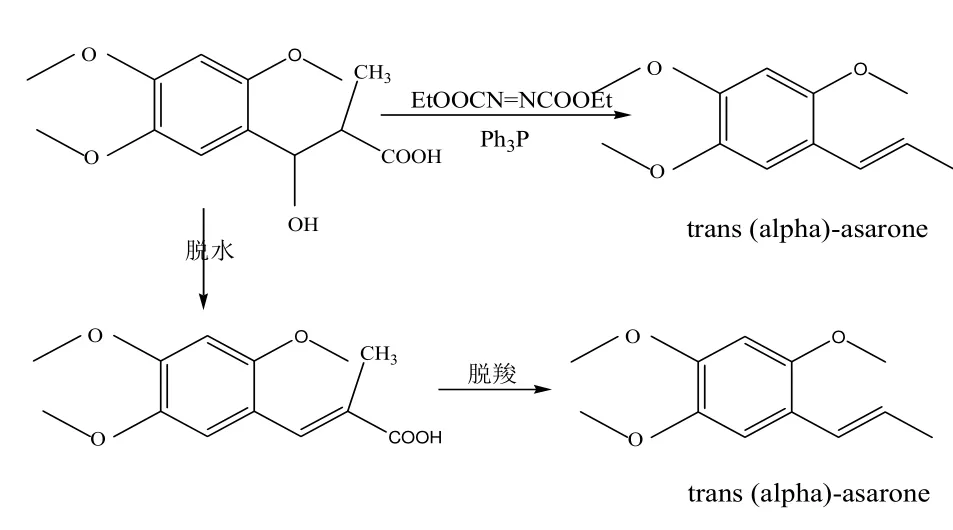
图5 erythro-2-甲基-3羟基-3苯丙酸为原料制备反式(α)-细辛脑的反应
图 5的合成路线较其他路线简单,但所需的原料价格昂贵,中间体的制备不仅困难、不稳定还存在一定的爆炸性,操作过程不易控制且由脱水脱羧步骤制备的产物中混有顺式异构体,然后须经过柱层层析分离得到反式(α)-细辛脑,柱层层析方法不适合工业化生产,影响反式(α)-细辛脑的收率,无形中增加了生产成本。
2 反式(α)-细辛脑的分离纯化
上述的合成路线中得到的很多产物都是顺式和反式细辛脑的同分异构体混合物,需要经过分离纯化过程才能制备得到反式结构无毒的反式(α)-细辛脑,因此反式(α)-细辛脑分离纯化对工业制备过程有重要的意义。目前,有关反式(α)-细辛脑的分离纯化方法主要有物理法和化学法两类。
2.1物理方法
由于顺式-细辛脑与反式(α)-细辛脑的化学结构很相似,导致它们具有相近的分子间力及物性,从而采用常规的物理方法难以分离出纯粹的大量的反式(α)-细辛脑。目前一般采用柱层层析方法可纯化得到少量的反式(α)-细辛脑,其操作过程为:将两种同分异构体的混合物20 g经硅胶色谱层析(100~200目),粗硅胶的量为待分离原料量的2倍,再用石油醚-乙酸乙酯混合液(50:50)梯度洗脱,洗脱下来的各流份再经硅胶柱(200~300目)反复层析及反复Sephadex LH-20色谱纯化可得目标产物反式(α)-细辛脑。采用柱层色谱分离操作步骤繁琐,处理量有限,不适合工业化生产,而且分离得到的顺式细辛脑被丢弃[14],造成资源的浪费。
2.2化学方法
化学方法是将两种同分异构体中的顺式细辛脑通过催化异构化使其转化为反式(α)-细辛脑,具体操作步骤为将α/β-细辛脑混合物溶于溶剂中,其次加入一定量的催化剂,加热回流状态下反应3~4h便可将顺式细辛脑转化为反式(α)-细辛脑。常用的溶剂有苯、二氯甲苯或乙酸乙酯,主要用到的催化剂有 Pd化合物催化剂如 PdCl2(CH3CO)2、PdCl2(CH3CN)2、PdCl2(PhCN)2和 PdCl2(PPh3)4、K(OH)催化剂及碘催化剂。
化学法分离所用的溶剂为苯和二氯甲苯是高毒性的有机溶剂,其中苯还是一种致癌物质,溶剂乙酸乙酯也具有一定的毒性。操作过程中溶剂不可避免地会残留于产品中,影响了作为药品使用的反式(α)-细辛脑的安全,同时对环境也带来一定的危害。催化异构化中Pd催化剂的价格昂贵成本高,且产物中残留的重金属 Pd离子去除困难影响用药的安全性。K(OH)催化剂的使用消耗量大,不仅浪费试剂,污染环境而且需要高温下操作,产物中脱甲基副产物的生成造成二次分离困难[14]。碘催化剂用量小,操作简单,分离彻底且没有副产物的生成,但是碘催化剂易挥发、升华不易回收,因此研发合适的催化剂和无毒的绿色溶剂是化学分离的关键。
3 反式(α)-细辛脑的应用
反式(α)-细辛脑最初发现来源于菖蒲等中药植物资源,具有很好的药理和生物活性,已被开发应用于医学临床。在药理活性方面,1993年Chamorro等[15]研究了反式(α)-细辛脑的药理学和毒理学,结果表明其可以用来治疗高胆固醇血症;1997年Gardufio 等[16]用小鼠研究了细辛脑的降血脂活性,取得了不错的效果;2005年Cassani-Galindo 等[17]对反式(α)-细辛脑的体外毒性进行了研究,发现其具有降血脂的功效。2010年Pages等[18]用动物模型研究了反式(α)-细辛脑的抗氧化及抗癫痫活性。
在医学临床应用方面,1986年杨玉[19]研究了反式(α)-细辛脑片治疗慢性阻塞性肺部疾病,结果证明对咳嗽、喘息、哮鸣都有很好的效果,且对心、肝及肾脏也没有危害。1993年杨正鸿等[20]首次报道了合成反式 α-细辛脑的人体各项药物动力学参数,为人体用药研究打下了坚实基础。2003年梁爱武等[21]研究了反式(α)-细辛脑注射液配合西药用于治疗肺源性心脏病呼吸衰竭,发现有较好的疗效。2005年李国庆等[22]观察了细辛脑辅助治疗新生儿肺炎的疗效,得到的结果很令人满意,且未见明显毒副作用,值得推广使用。2005年刘向东[23]探讨了反式细辛脑吸入治疗小儿哮喘的疗效及安全性,结果表明很安全。2006年郝冬荣等[24]在治疗婴儿毛细管支气管炎的过程中添加了部分细辛脑,结果表明加入后的治疗效果更好。2009年韩琳等[25]的研究中将细辛脑用于癫痫病的治疗,发现其具有较强的抗惊厥、 抗癫痫作用; 2013年Chen等[26]将其用于治疗癫痫病,发现其在抗癫痫方面显示出了很好的活性。2013年Ma等[27]探究了反式(α)-细辛脑注射剂-脂肪乳剂在临床中的应用,结果表明其有很大的应用潜力。2014年Lu等[28]比较了反式(α)-细辛脑通过口服、静脉注射和鼻腔三种不同的给药方式注入小鼠体内后的分布情况。2014年甘海强[29]将其用于治疗小儿呼吸道感染,结果表明治疗过程中细辛脑的加入能迅速缓解症状,提高疗效。
4 结语
由于天然植物中反式(α)-细辛脑的含量较低,因此通过化学合成方法是获得高纯度反式(α)-细辛脑的主要途径。已有的合成路线中还存在一些弊端,比如原料价格昂贵、合成线路长、产物分离困难及有毒有害有机溶剂的使用等,这些都给反式(α)-细辛脑的工业化制备和实际应用带来了一定的困难,因此对其制备的化学合成路线进行改进,用绿色溶剂替代有毒有害溶剂,缩短反应过程,寻找新的分离方法等解决反式(α)-细辛脑由于天然植物提取量少及过度开发使用的问题。同时深入研究其合成过程化学反应的热力学及动力学可为其工业化生产提供理论依据;在临床应用方面尝试不同的剂型提高其生物利用度,为其进一步的开发应用开辟新的路径。
[1] 周伊. 1. α-细辛脑的合成 2. 去氢骆驼蓬碱衍生物的合成及活性研究[D].长沙:湖南师范大学,2000.
[2] Díaz F,Muňoz H,Labarrios F,et al.Synthesis and hypolipidemic activity of some α-asarone analogs[J].Med Chem Res, 1993, 3(2):101-109.
[3] 王植材,蒋腊生,许杏祥. Z-和 E-细辛醚的合成[J].有机化学,1990, (10): 350-352.
[4] 张玲,刘素云.α-细辛脑的制备[J].中国医药工业杂志, 2007,38(7):477-478.
[5] 刘博纯.α-细辛脑原料生产工艺:中国,CN1511817A[P]. 2004-07-14.
[6] 喻爱和,冯勋波,陈超越,等.合成α-细辛脑的脱水剂选择[J].合成化学,2006,14(5):500-502.
[7] Cao R, Chen H, Peng W, et al. Design, synthesis and invitro and in Vivo antltumor activities of novel and carboline derivatives. Eur. J. Med.Chem,2005,40(10):991-1001.
[8] 陈毅平. 合成α-细辛脑的新方法:中国,CN101195562A[P].2007-12-11.
[9] 陈毅平,曾健. 1,2,4-三甲氧基苯的合成[J].广西中医学院学报, 1999, (2): 39-40.
[10] 陈双英.合成 α-细辛脑的工艺研究[D].南宁:广西中医学院,2009.
[11] 兰烨荣,刘素香,张铁军,等.细辛醚的研究进展[J].现代药物与临床, 2013, 28(2):252-257.
[12] Mulzer J, Lamrner O, olefins from β-hydroxycarboxylic acids-synthesis of isomerically pure α- and β-asarone. Angew. Chem. Int. Ed.1983,(22):628-629.
[13] 蒋勇军,徐广宇,周伊,等.一种 α-细辛脑的制备方法:中国,CN 101012159A[P].2006-03-15.
[14] 张为.一种合成 α-细辛脑的方法:中国,CN101215226A[P]. 2008-07-09.
[15] Chamorro G, Salazar M, Salazar S, et al. Pharmacology and toxicology of Guatteria gaumeri and alpha-asarone[J]. Revista de investigation clinica. 1993,45(6):597-604.
[16] Gardufio L, Salazar M, Salazar S, et al. Hypolipidaemic activity of α-asarone in mice [J].Journal of Ethnopharmacology, 1997,(55):161-163.
[17] Cassani-Galindo M, Madrigal-Bujaidar E, Chamorro G, et al. In vitro genotoxic evaluation of three a-asarone analogues [J].Toxicology in Vitro,2005,(19):547-552.
[18] Pages L,Maurois B, Delplanque B,et al.Activities of αasarone in various animal seizure models and in biochemical assays might be essentially accounted for by antioxidant properties[J].Neuroscience Research,2010,68(4): 337-344.
[19] 杨玉.α-细辛脑片治疗18例慢性阻塞性肺部疾病[J].新药与临床,1986,5(4):210-212.
[20] 杨正鸿,吴闯,宋次娇.α-细辛脑在人体中的药物动力学[J].中国医院药学杂志,1993,13(1):7-8.
[21] 梁爱武,黄春萍,范悦.α-细辛脑合灯盏细辛注射液治疗肺源性心脏病呼吸衰竭疗效观察[J].中国中西医结合急救杂志. 2003,10(2):111-113.
[22] 李国庆,魏洪伟,薛慧敏.α-细辛脑注射液雾化吸入铺助治疗新生儿肺炎 45例临床观察[J].中国医药指南,2005,(3): 1-2.
[23] 刘向东.α-细辛脑吸入治疗小儿哮喘效果观察[J].齐鲁医学杂志,2005,20(2):148-149.
[24] 郝冬荣,武国霞.α-细辛脑治疗婴儿毛细支气管炎 43例疗效观察[J].中国综合临床,2006, 22(8):758-759.
[25] 韩琳,汤道权.α-细辛脑的抗惊厥抗癫痫作用研究[J].井冈山医专学报,2009,16(6):9-10,15.
[26] Chen H C, Li W G, Zhang X B, et al, Alpha-asarone from Acorus gramineus alleviates epilepsy by modulating AType GABA receptors[J].Neuropharmacology,2013,(65):1-11.
[27] Ma W C,Zhang Q,Li H,et al. Development of intravenous lipid emulsion of α-sarone with significantly improved safety and enhanced efficacy[J].International Journal of Pharmaceutics.,2013,(450):21-30.
[28] Lu J, Fu T M, Qian Y Y, et al. Distribution of α-asarone in brain following three different routes of administration in rats[J].European Journal of Pharmaceutical Sciences, 2014, (63):63-70.
[29] 甘海强.α-细辛脑佐治小儿下呼吸道感染的疗效观察[J].白求恩医学杂志,2014,12(5):84-485.
The preparation and application of trans-asarone
Trans (alpha)-asarone has the pharmacological activity of cough, removing phlegm and preventing asthma, sedative, anticonvulsant and anti-cancer, and the clinical application of which is extensively. There are many difficulties in the extraction of α-asarone due to the low content in the natural plant, thus, the method of chemical synthesis is an effective way of preparing α-asarone. The main synthesis methods are: the α-asarone is obtained by acylation, reduction and dehydration reaction with 1,2,4- trimethoxy benzene as the raw material; the α-asarone is obtained by reduction and dehydration reaction, taking asarum aldehyde as raw material; the α-asarone is obtained by oxidation, three acetylation methyl, formylation and dehydration reaction, using hydroquinone as raw materials; the α-asarone is obtained with erythro-2- methyl -3 hydroxy -3 phenyl propionic acid as raw materials by stereoselective synthesis. The seperation of α-asarone includes physical separation method of layer chromatography column and the chemical separation method of catalytic isomerization.
α-asarone; chemical synthesis; separation; application
R625.1
A
1008-1151(2015)07-0033-04
2015-06-10
广西科学研究与技术开发计划项目(桂科能1298025-19)。
张宁(1989-),女,广西科技大学生物与化学工程学院硕士研究生,从事化学反应工程研究。
谢清若,男,广西平南人,广西科技大学生物与化学工程学院硕士研究生导师。

