高效液相色谱法测定保泰松片的有关物质
李玲 姜燕 陈乃江
[摘要] 目的 建立测定保泰松片有关物质的高效液相色谱法。 方法 采用Phenomenex Luna C18(250mm×4.6mm,5μm)色谱柱,流动相为乙腈-水(磷酸调pH至3.0)(50∶50),检测波长为239nm,流速1.0mL/min,柱温为30℃,进样体积为10μL。 结果 在选定的色谱条件下,主成分能与杂质峰之间分离度良好;方法的检测限为0.2μg/mL;供试品溶液在8h内稳定性良好。 结论 本方法简单,准确,重现性好,可用于保泰松片的有关物质检查。
[关键词] 高效液相色谱法;保泰松片;有关物质;强制降解试验
[中图分类号] R927.2 [文献标识码] A [文章编号] 2095-0616(2015)19-72-03
[Abstract] Objective To establish a HPLC method for the determination of related substances of phenylbutazone tablets. Methods A Phenomenex LunaC18 column(250mm×4.6mm,5μm) was used, and the mobile phase was acetonitrile–water[adjusting pH to 3.0 with phosphoric acid] (50:50).The flow rate was 1.0 mL/min and the detection wavelength was set at 239nm.The column temperature was set at 30℃ and the injection volume was 10 μL. Results Related substances were completely separated from the main constituent.The limit of detection was 0.2μg/mL.The sample solution was stable within 8h.Conclusion The method wsa simple,accurate with good reproducibility,and can be used in the determination of related substances of phenylbutazone tablets.
[Key words] HPLC;Phenylbutazone tablets;Related substances;Stressing test
保泰松片为非甾体类抗炎镇痛药,用于治疗类风湿性关节炎、风湿性关节炎及痛风。保泰松片的质量标准收载于卫生部药品标准二部第5册[1],但现有质量标准中未收载其有关物质检查项,本研究查阅相关文献[2-6],发现目前国内还没有文献报道保泰松片的有关物质。保泰松片在生产过程中可能会引入工艺杂质,也可能会产生降解产物[7],而且本品不良反应发生率较高[8-11],为了更好地控制本品的质量,我们采用高效液相色谱法对保泰松片中的工艺杂质及可能降解杂质进行了测定和方法学考察,并对收集到的2个厂家的4批样品进行了检验,结果表明该方法专属性强,操作简便,结果准确可靠。
1 仪器与试药
Waters 2695 高效液相色谱仪、Waters 2996 DAD检测器,Empower色谱工作站,Sartorius BP-211D电子天平,PHS-3C型酸度计,BRANSON B5500S-MT型超声仪。
对照品保泰松(批号100481-200601,含量99.9%)购自中国食品药品检验研究院;保泰松片(A厂家,国药准字H41024168,批号13082702,14043001,15012101;B厂家,国药准字H41025373,批号20141001),规格均为0.1g;乙腈、甲醇为色谱纯,磷酸为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件与系统适用性
采用Phenomenex Luna C18(250mm×4.6mm,5μm)色谱柱;流动相为乙腈-水(磷酸调pH至3.0)(50∶50);流速为1.0mL/min;检测波长为239nm;柱温为30℃;进样量为10μL。理论板数按保泰松峰计算不低于4000,保泰松与相邻杂质峰的分离度应符合要求。
2.2 溶液的制备
取本品20片,除去包衣后,精密称定,研细,精密称取适量(约相当于保泰松50mg),置25mL量瓶中,加甲醇约20mL,超声处理30min,放冷,加甲醇稀释至刻度,摇匀滤过,取续滤液作为供试品溶液;精密量取供试品溶液适量,用甲醇定量稀释制成每1mL约含保泰松20μg的溶液,作为对照溶液。
精密称取保泰松对照品10.0mg,置100mL量瓶中,加甲醇超声使溶解并稀释至刻度,摇匀,作为对照品溶液。
3 方法
3.1 强制降解试验
取A企业样品(批号:13082702)进行高温、水浴、光照、酸、碱和氧化破坏的强制降解试验[12-15]。
3.1.1 高温破坏 取本品细粉适量,105℃放置2h,精密称取适量(约相当于保泰松50 mg),置25mL量瓶中,照“2.3”项下配制供试品溶液。
3.1.2 水浴破坏 精密称取本品细粉适量(约相当于保泰松50mg),置25mL量瓶中,加甲醇约20mL,超声处理30min,水浴温度加热3h,放冷,用甲醇稀释定容,摇匀滤过,取续滤液。
3.1.3 光照破坏 取本品供试品溶液置4500 lx日光灯下,照射24h。endprint
3.1.4 酸破坏 精密称取本品细粉适量(约相当于保泰松50mg),置25mL量瓶中,加甲醇约10mL,超声处理30min,再加1mol/L盐酸溶液2mL,放置6h,加1mol/L氢氧化钠溶液2 mL中和,用甲醇稀释定容,摇匀滤过,取续滤液。
3.1.5 碱破坏 精密称取本品细粉适量(约相当于保泰松50mg),置25mL量瓶中,加甲醇约10mL,超声处理30min,再加1mol/L氢氧化钠溶液2mL,放置7h,加1mol/L盐酸溶液2mL中和,用甲醇稀释定容,摇匀滤过,取续滤液。
3.1.6 氧化破坏 精密称取本品细粉适量(约相当于保泰松50mg),置25mL量瓶中,加甲醇约10mL,超声处理30min,再加30%过氧化氢溶液2mL,放置5h,用甲醇稀释定容,摇匀滤过,取续滤液。
3.1.7 辅料干扰试验 取不含保泰松的空白辅料适量,制成空白辅料溶液。
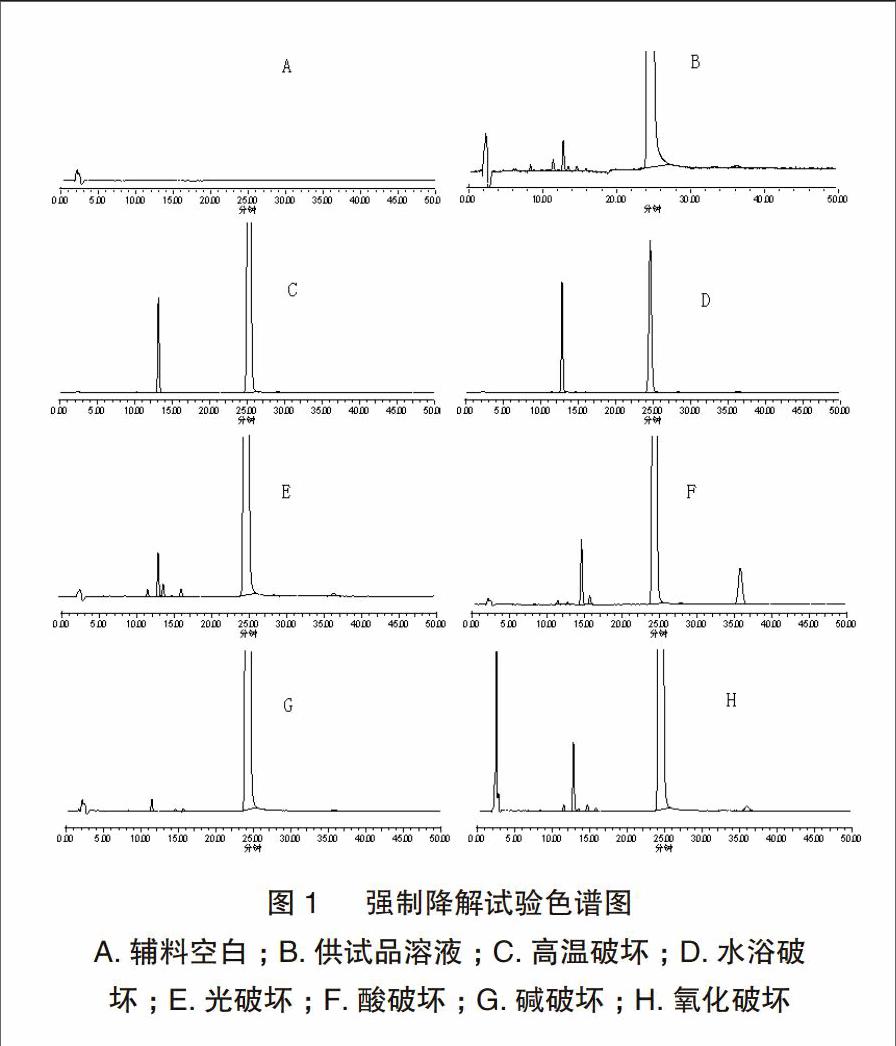
3.1.8 强制降解试验结果 按“2.1”项下色谱条件测定上述溶液,记录色谱图,见图1,试验结果表明:各降解产物峰与保泰松主峰完全分离,辅料无干扰。说明本法专属性强,适用于保泰松片有关物质的测定。
3.2 检测限和定量限
精密吸取保泰松对照品溶液适量,加甲醇逐步稀释至色谱图中保泰松峰高分别为噪音的3倍和10倍,测得保泰松的检测限和定量限分别为0.2μg/mL和0.5μg/mL。
3.3 精密度试验
取样品测定项下的对照溶液,照“2.1”项下的色谱条件,连续进样测定6次,保泰松峰面积的RSD为0.7%。结果表明仪器精密度符合要求。
3.4 稳定性试验
取样品测定项下的供试品溶液在0、2、4、8h分别测定保泰松与各杂质的峰面积。结果单个最大未知杂质均为0.09%,杂质总量均为0.22%,说明溶液在8h内稳定。
3.5 样品有关物质检测
根据供试品溶液中的有关物质含量和强制降解试验条件下的杂质降解情况,制定保泰松片的有关物质限度。供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.5倍(0.5%),各杂质峰面积的和不得大于对照溶液主峰面积(1.0%)。结果批号分别为13082702、14043001、15012101、20141001的样品中单个最大未知单杂分别为0.09%、0.09%、0.05%、0.07%,杂质总量分别为0.22%、0.19%、0.18%、0.15%。
4 讨论
4.1 流动相的选择
考察缓冲液-乙腈、水-甲醇系统在不同pH条件下对峰型的影响,对杂质与主峰的分离及杂质之间的分离情况的影响。发现在pH3.0条件下,杂质均能完全分离;杂质在乙腈系统下,杂质的分离情况优于甲醇系统;在水系统与缓冲液系统下,杂质分离情况基本相当。考虑流动相操作简便,且对色谱柱损害最小原则,选择乙腈-水(pH 3.0)作为流动相。
4.2 检测波长的确定
本研究通过DAD检测器进行光谱扫描,结果显示保泰松的最大吸收波长为239nm,按规定贮存的样品杂质和强制降解试验条件下的降解杂质的最大吸收波长均在236~239nm之间;可见各种杂质的最大吸收波长均非常接近保泰松的最大吸收波长,所以试验选择在保泰松的最大吸收波长239nm下测定有关物质。
4.3 杂质谱分析
不同条件下的降解试验表明,保泰松片在碱性条件下较稳定,在光照、氧化条件下略有降解,在酸、高温、水浴条件下降解严重;各个降解试验条件下的降解杂质为光照(RRT=0.52)、氧化(RRT=0.52、1.47)、酸(RRT=0.60、1.47)、高温(RRT=0.52)、水浴(RRT=0.52);供试品溶液放置48h,有轻微降解,降解杂质为RRT=0.52、1.47,而在两个厂家4批供试品溶液中单个最大未知杂质均为RRT=0.52,该杂质在光照、氧化、高温、水浴条件下均有降解,要进一步确认主要降解产物的结构,应用LC-TOF-MS,LC-MS-MS联用技术分析。
本研究采用的高效液相色谱法能够较准确地测定保泰松片中的有关物质,各杂质峰均能有效分离,方法专属性强,灵敏度高,操作简便,方法可靠。
[参考文献]
[1] 中华人民共和国卫生部药典委员会.卫生部药品标准(二部)[S].第五册.1996:65.
[2] 孙旌文,马洪涛.高效液相色谱法测定保泰松片的含量[J].西北药学杂志,2010,25(5):332-333.
[3] 穆同娜,王浩,刘艳琴,等.高效液相色谱法测定化妆品中的保泰松[J].日用化学工业,2011,41(6):459-461.
[4] 车洪勇,杨元玉,冯爱萍.HPLC法测定关节镇痛片中保泰松和马来酸氯苯那敏的含量[J].中国药事,2003,17(3):167-168.
[5] 杜兴.HPLC法测定风湿松片中保泰松及氨基比林的含量[J].西北药学杂志,1999,14(2):53.
[6] 姜泽慧,吴勇.市售保泰松片溶出度方法的考察[J].中国药师,2014,17(6):962-964.
[7] 刘文英.药物分析[M].北京:人民卫生出版社,2003:27-29.
[8] 朱学义,董乐,李泽纯.保泰松合用地塞米松致药物剥脱性皮炎并药物性肝炎1例[J].中国药业,2013,22(13):77.
[9] 但蓓蓓.保泰松急性中毒患儿1例救治报道[J].儿科药学杂志,2012,18(3):1.
[10] 肖曙芳,李亚玲,陈祝,等.保泰松中毒致多器官功能障碍1例[J].儿科药学杂志,2006,12(6):62.
[11] 王蕊婷,卢亚弟,尉亚娥.保泰松引起频发多源性室性期前收缩一例[J].山西医药杂志,2002,4(2):156.
[12] 中国药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2010:附录204-206.
[13] 刘文英.药物分析[M].北京:人民卫生出版社,2004:380-381.
[14] 施捷,车宝泉,郑焱,等.HPLC法测定不同来源米非司酮胶囊的有关物质[J].药物分析杂志,2014,34(3):480-484.
[15] 石云峰,林丽琴.HPLC法测定孟鲁司特钠片含量与有关物质[J].药物分析杂志,2013,33(2):308-311.
(收稿日期:2015-06-18)endprint

