MgO/SiO2纳米复合材料同步吸附亚甲基蓝和Cu2+
陈显坤,龚继来,曾光明
(湖南大学 环境科学与工程学院环境生物与控制教育部重点实验室,湖南 长沙 410082)
MgO/SiO2纳米复合材料同步吸附亚甲基蓝和Cu2+
陈显坤,龚继来,曾光明
(湖南大学 环境科学与工程学院环境生物与控制教育部重点实验室,湖南 长沙 410082)
采用化学沉积法合成了MgO/SiO2纳米复合材料,通过扫描电子显微镜和X射线能谱分析(SEM-EDX)、X射线衍射(XRD)、Zeta电位仪、FTIR等方法对其进行了表征。研究了MgO/SiO2对亚甲基蓝(MB)和Cu2+的吸附行为及同步吸附效果。表征结果表明:MgO/SiO2为褶皱、凸起的球形形貌;MgO成功负载在SiO2表面。实验结果表明:MgO/SiO2对MB和Cu2+的吸附符合准二级动力学模型和Langmuir等温吸附模型,MB和Cu2+的饱和吸附量分别为83.72 mg/g和208.70 mg/g;MB和Cu2+的同步吸附在MgO/SiO2表面存在竞争关系;在溶液体积为30 mL、MgO/SiO2加入量为10 mg、MB 质量浓度为10 mg/L或Cu2+质量浓度为100 mg/L、吸附温度为25 ℃、吸附时间为24 h、初始溶液pH为4.00、解吸时间为4 h的条件下,MgO/SiO2第1次吸附MB和Cu2+的去除率分别为92.8%和90.1%,第5次吸附的去除率分别为59.6%和 57.4%。
氧化镁/二氧化硅;亚甲基蓝;二价铜离子;同时吸附
印染废水COD高、色度高、难生物降解[1-3]。亚甲基蓝(MB)是使用最广泛的染料之一,广泛使用在印刷、印染等领域。除此之外,在印刷和印染过程中,铜盐常用作媒染剂[4-5]。因此,印染废水中MB和Cu2+可能共存。MB的致癌性、致突变性及毒性已经在水生生物中得到证明[6],而过量的铜对水生生物的内脏、代谢功能等也有很大的威胁,因此印染废水在排放前必须得到妥善的处理。
吸附法具有易操作、效率高、适应性强等特点,常用来处理印染废水。吸附效果的优劣取决于所选用的吸附剂。SiO2由于其独特的结构以及纳米尺寸,比表面积巨大且具有离子交换和吸附能力,常用作吸附剂处理有机物及重金属废水。然而纯SiO2由于其中性结构,缺发足够的活性位点限制了吸附剂的使用[7],因此需要对SiO2进行改性,增加活性位点和比表面积[8-10]。MgO是一种典型的价格低、环境友好的金属氧化物,易于合成形状和尺寸可变的晶体[11]。有报道称MgO众多的边角以及结构缺陷,赋予其很高的比表面积和反应活性[12],因此,将MgO负载在SiO2表面进行改性增加吸附位点有一定可能。
本工作通过化学沉积法合成MgO/SiO2纳米复合材料,采用SEM-EDX、XRD、RTIR、Zeta电位、BET比表面积测定等方法对其进行了表征。以MB和Cu2+作为目标污染物,考察了MgO/SiO2对MB和Cu2+的同步吸附效果,研究了MgO/SiO2对MB和Cu2+的吸附动力学、等温吸附过程以及MB和Cu2+同步吸附的相互影响。
1 实验部分
1.1 试剂和仪器
MgCl2·6H2O、十六烷基三甲基溴化铵 、三乙醇胺、亚甲基蓝、三水硝酸铜、氨水、正硅酸乙酯、乙醇:分析纯。
AA700型原子吸收分光光度计:PerkinElmer公司;UV-2550型紫外-可见光光度计:日本岛津公司;SHY-2A型数显恒温水浴振荡器 、JHS型恒速搅拌器:杭州仪表电机厂;ZEN3690型zeta电位仪:Malvern公司;JMS-5600L型扫描电子显微镜:日本JEO集团;IRAff nity-1型傅里叶红外光谱仪:Shimadzu公司;KUBO-1108型全自动比表面积分析仪:北京彼奥德电子技术有限公司。
1.2 MgO/SiO2的制备
SiO2微球的制备:在碱性条件下,通过正硅酸乙酯水解制备SiO2微球[13]。将15 mL超纯水和4 mL氨水加入到100 mL乙醇中,在磁力搅拌下分散30 min。将3 mL正硅酸乙酯迅速加入上述混合液中,缓慢搅拌1 h,用5 mol/ L HCl中和,离心,于70 ℃下烘干24 h。
MgO/SiO2的制备:将0.4 mol MgCl2·6H2O加入100 mL超纯水中,加入适量十六烷基三甲基溴化铵,超声分散30 min,制备溶液A。将2 g SiO2微球加入100 mL超纯水中,加入适量的三乙醇胺,超声分散30 min,制备溶液B。将溶液A加入溶液B中,在45 ℃下不断连续搅拌直到分散均匀,同时逐滴加入5 mL氨水,继续缓慢搅拌反应2 h。反应产物经水洗、醇洗 ,于 80 ℃下烘干, 600 ℃下煅烧3 h,得MgO/SiO2纳米复合材料。
1.3 MB和Cu2+的吸附
单独吸附:将10 mg MgO/SiO2加入30 mL含一定质量浓度的MB或Cu2+的溶液中,用0.1~1.0 mol/L HCl/NaOH溶液调整初始溶液pH(pHi)为2.00~9.00。在25 ℃下,以120 r/min的振荡速率反应一定时间,离心分离,取上清液,测定MB或Cu2+的质量浓度 。
同步吸附:1)混合溶液中MB质量浓度为10 mg/L,Cu2+质量浓度分别为0,10,20,40,80 mg/L,pHi为4.00,在相同的其他吸附条件下,进行同步吸附实验。2)混合溶液中Cu2+质量浓度为100 mg/L,MB质量浓度分别0,5,10,15,20 mg/L,pHi为4.00,在相同的其他吸附条件下,进行同步吸附实验。
预负载吸附:1)溶液中MB质量浓度为10 mg/ L,pHi为4.00,在相同的其他吸附条件下,进行MB预负载;再加入Cu2+溶液,使混合液中Cu2+质量浓度分别为10,20,40,80 mg/L,进行吸附实验。2)溶液中Cu2+质量浓度为100 mg/L,pHi为4.00,在相同的其他吸附条件下,进行Cu2+预负载;再加入MB溶液,使混合液中MB质量浓度分别为5,10,15,20 mg/L,在相同的其他吸附条件下,进行吸附实验。
1.4 MgO/SiO2的解吸与再生
在相同吸附条件下,在30 mL MB 质量浓度为10 mg/L或Cu2+质量浓度为100 mg/L的水溶液中分别加入10 mg MgO/SiO2,吸附饱和后离心分离,弃掉上清液,用超纯水清洗吸附剂,然后用30 mL浓度为0.1 mol/ L的 HCl溶液解吸4 h,再将解吸后的MgO/SiO2加入同上溶液中进行吸附。吸附-解吸步骤重复进行4次。
1.5 分析方法
采用紫外-可见光分光光度计在波长664 nm处测定溶液吸光度,计算MB质量浓度。采用原子吸收分光光度计测定Cu2+的质量浓度。采用扫描电子显微镜和X射线能谱分析法(SEM-EDX)表征吸附剂的表面形貌和元素分析。采用X射线衍射法(XRD)对吸附剂进行物相分析。采用傅里叶红外光谱法(FTIR)表征吸附剂表面官能团。采用Zeta电位仪分析吸附剂的等电点。采用比表面积分析仪测定吸附剂的比表面积。
2 结果与讨论
2.1 SEM和EDX表征结果
MgO/SiO2的SEM照片(a)和EDX能谱谱图(b)见图1。由图1(a)可见,材料形貌呈球形,表面有褶皱、凸起,能增大比表面积,有利于表面吸附。由图1(b)可见,MgO/SiO2中含有O、Mg、Si等元素,含量分别为50.80%、23.89%、25.32%。
2.2 XRD表征结果
MgO/SiO2的XRD谱图见图2。由图2可见:在2θ=22.3°处出现SiO2的衍射峰;在42.9°,62.3°,78.6°处出现MgO的衍射峰,与MgO的标准图谱一致,说明MgO成功负载在SiO2上。

图1 MgO/SiO2的SEM照片(a)和EDX能谱谱图(b)

图2 MgO/SiO2的XRD谱图
2.3 FTIR表征结果
MgO/SiO2的FTIR谱图见图3。
由图3可见: 1 625 cm-1处的弱峰归属于MgO/ SiO2表面水分子上—OH的伸缩振动;1 100 cm-1处的强峰归属于Si—O—Si伸缩振动[14];690 cm-1处的宽峰归属于Mg—O—Mg或Mg—O的伸缩振动[15];而475 cm-1处的强峰归属于Mg—OH的伸缩振动[16]。
2.4 等电点及BET测定结果
MgO/SiO2在不同溶液pH下的Zeta电位见图4。由图4可见,在溶液pH为1.00~9.00范围内,随着溶液pH的增加,MgO/SiO2表面电势由正变负,等电点为2.64。当溶液pH小于2.64时MgO/SiO2表面带正电荷,当溶液pH大于2.64时MgO/SiO2表面带负电荷。BET比表面积测定结果为121 m2/g。

图3 MgO/SiO2的FTIR谱图

图4 MgO/SiO2在不同溶液pH下的Zeta电位
2.5 pHi对MB和Cu2+吸附效果的影响
在溶液体积为30 mL、MgO/SiO2加入量为10 mg、初始MB质量浓度为10 mg/L、吸附温度为25 ℃、吸附时间为24 h的条件下, pHi对MB平衡吸附量的影响见图5。由图5可见:pHi为2.00~4.00时,随着pHi的增加, MB平衡吸附量不断加大;pHi为4.00~8.00时, MB平衡吸附量基本不变。图5还表明了吸附过程中pH的变化,在吸附过程中,当pHi小于4.00时,由于吸附剂表面质子化和酸中和反应的影响,溶液最终的pH(pHf)高于pHi,当pHi为4.00~8.00时,pHf维持在8.50~9.40之间。从图4可知,MgO/SiO2的等电点为2.64,pH小于2.64时MgO/SiO2表面带更多正电荷,H+与MB竞争吸附位点,而MB带正电荷,产生排斥力;当pH大于2.64时MgO/SiO2表面带更多负电荷,而MB带正电荷,H+竞争吸附位点能力变弱,静电引力起主要作用。

图5 pHi对 MB平衡吸附量的影响
在溶液体积为30 mL、MgO/SiO2加入量为10 mg、初始Cu2+质量浓度为100 mg/L、吸附温度为25℃、吸附时间为24 h的条件下,pHi对 Cu2+平衡吸附量的影响见图6。由图6可见:pHi为2.00~6.00时,Cu2+的平衡吸附量有轻微的增加;pHi大于6.00时,平衡吸附量迅速增加。MgO/SiO2的等电点为2.64,pH大于2.64时MgO/SiO2表面的负电荷不断增多,静电引力以及材料表面上的羟基络合作用促使Cu2+吸附在MgO/SiO2表面。pHi为6.00~8.00时平衡吸附量的剧增可能是由于吸附和沉淀共同作用的结果,而沉淀起主要作用。由图6还可知:反应过程中pH发生变化,pHf高于pHi;当pHi大于6.00时,pHf大于9.00,此时溶液中已产生化学沉淀。
综上所述,选择pHi=4.00作为适宜吸附条件。
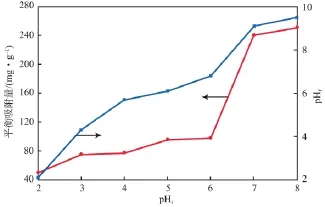
图6 pHi对 Cu2+平衡吸附量的影响
2.6 吸附动力学
在溶液体积为30 mL、MgO/SiO2加入量为10 mg、初始MB质量浓度为10 mg/L、初始Cu2+质量浓度为100 mg/L、吸附温度为25 ℃、吸附时间为24 h的条件下, MgO/SiO2对MB(a)和Cu2+(b)的吸附效果见图7。由图7a可见,在10 min之内MB的吸附速率极快,MB的平衡吸附量达到23.0 mg/g,之后吸附速率比较缓慢,在3 h左右就达到吸附饱和。这是由于MgO/SiO2比较大的比表面积以及对MB较强的亲和力。而由图7b可见,在100 min之内,MgO/SiO2对Cu2+的吸附过程达到平衡,此后Cu2+的吸附量不再随着吸附时间的增加而增加。

图7 MgO/SiO2对MB(a)和Cu2+(b)的吸附效果
为了研究MgO/SiO2对MB和Cu2+的吸附动力学特征,用准一级、准二级动力学方程(见式(1)~式(2)) 拟合数据。

式中:t为吸附时间,min;qt为吸附量,mg/g;qe为平衡吸附量,mg/g;k1,k2分别为动力学方程系数,min-1。
吸附动力学方程拟合参数见表1。由表1可见,MB和Cu2+的吸附过程更接近准二级动力学,R2都在0.99以上,表明该吸附伴随着化学吸附过程。

表1 吸附动力学方程拟合参数
2.7 等温吸附研究
MgO/SiO2对MB(a)和Cu2+(b)的吸附等温线见图8。为了研究吸附效率,采用Langmuir和Freundlich等温吸附模型拟合数据。Langmuir模型假定吸附平衡后形成单分子层,而Freundlich模型假定为多分子层吸附。两种模型的方程式见式(3)~式(4)。

式中:qm为吸附剂表面形成完整的单分子层的平衡吸附量,mg/g;ρe是吸附平衡时吸附质的质量浓度,mg/L;KL为Langmuir吸附常数,L/mg;KF和n为Freundlich模型常数。
等温吸附方程拟合参数见表2。由图8及表2可见: Langmuir模型能更好地描述MgO/SiO2对MB和Cu2+的等温吸附,计算得出25 ℃下MB和Cu2+的饱和吸附量分别为83.72 mg/g和208.70 mg/g;Freundlich吸附参数0<1/n<1,表明MB和Cu2+易于吸附在MgO/SiO2表面。

图8 MgO/SiO2对MB(a)和Cu2+(b)的吸附等温线

表2 等温吸附方程拟合参数
2.8 同步吸附
MB和Cu2+的同步吸附效果见图9。由图9可见,Cu2+/MB质量浓度越高,MB/Cu2+的平衡吸附量均越少,说明Cu2+与MB存在竞争吸附关系。
MB和Cu2+的预负载吸附效果见图10。由图10可见:在MB预负载之后,随着Cu2+质量浓度的增大,吸附剂表面的MB解吸增多;当Cu2+预负载之后,加入的MB的质量浓度越高,Cu2+的平衡吸附量越少。这一现象的原因一是因为MB与Cu2+竞争材料表面的吸附位点,二是因为吸附在材料表面的MB/Cu2+分子层掩盖了MgO/SiO2表面的羟基官能团,造成吸附剂表面Cu2+/MB有一定程度的解吸。

图9 MB和Cu2+的同步吸附效果

图10 MB和Cu2+的预负载吸附效果
为方便数据分析,引入吸附容量比(Rq,i)的概念,见式(5)。

式中:qb,i为污染物i在二元体系中的吸附量,mg/ g;qo,i为污染物i在相同初始浓度的单组份体系中的吸附量,mg/g。
当Rq,i>1时,共存污染物加强污染物i的吸附。
当Rq,i=1时,共存污染物对污染物i的吸附没有影响。
当Rq,i<1时,共存污染物抑制污染物i的吸附。
由图9 及图10可见:在Cu2+-MB二元体系中,与单组分体系相比,MgO/SiO2对MB的吸附量减少,且随Cu2+质量浓度的增加而减少;当MB初始质量浓度为10 mg/L 时,单组份体系MB的吸附量为 23.65 mg/g,在Cu2+初始质量浓度为80 mg/L的Cu2+-MB二元体系中MB的吸附量为19.79 mg/g,为单组分体系中的83.67%。计算得出,Cu2+-MB二元体系中MB的Rq,i均小于1,且Cu2+质量浓度越大MB的Rq,i值越小,Cu2+对MgO/SiO2吸附MB有抑制作用;当Cu2+的初始质量浓度为80 mg/L时,单组分体系Cu2+的吸附量为127.41 mg/g,在MB初始质量浓度为20 mg/L的Cu2+-MB二元体系中Cu2+的吸附量为91.56 mg/g,为单组分体系中的72.09%,说明MB对MgO/SiO2吸附Cu2+也有抑制作用。
因此,上述现象可以很好地解释,MgO/SiO2对Cu2+和MB的吸附存在一定的竞争关系。
2.9 解吸与再生
MgO/SiO2对MB和Cu2+的重复吸附效果见图11。由图11可见,第1次吸附后MB和Cu2+的去除率分别为92.8%和90.1%,吸附-解吸4次后第5次吸附的去除率分别为59.6%和 57.4%,表明MgO/SiO2具有一定再生能力,在印染废水处理过程中能够作为高效的、可重复使用的吸附剂。

图11 MgO/SiO2对MB和Cu2+的重复吸附效果
2.10 与其他吸附剂的比较
在pHi为4.00、MB质量浓度为10 mg/L或Cu2+质量浓度为100 mg/L、吸附温度为25 ℃、吸附时间为24 h的条件下,MgO/SiO2与其他吸附剂的比较见表3。由表3可见, MgO/SiO2具有更好的吸附效果,平衡吸附量远超其他几种吸附剂。

表3 MgO/SiO2与其他吸附剂的比较
3 结论
a)采用化学沉积法成功合成了MgO/SiO2纳米复合材料。表征结果表明:MgO/SiO2为褶皱、凸起的球形形貌;MgO成功负载在SiO2表面;等电点为2.64;BET比表面积为121.23 m2/g。pHi=4.00为适宜的吸附条件。
b)MB和Cu2+能快速被吸附在MgO/SiO2表面,采用准二级动力学方程能很好地拟合吸附过程。Langmuir模型更适合描述MB和Cu2+的等温吸附,MB和Cu2+的饱和吸附量分别为83.72 mg/g和208.70 mg/g。
c)MB和Cu2+的同步吸附在MgO/SiO2表面存在竞争关系。
d)在溶液体积为30 mL、MgO/SiO2加入量为10 mg、MB 质量浓度为10 mg/L或Cu2+质量浓度为100 mg/L、吸附温度为25 ℃、吸附时间为24 h、pHi为4.00、解吸时间为4 h的条件下,MgO/SiO2第1次吸附后MB和Cu2+的去除率分别为92.8%和90.1%,吸附-解吸4次后第5次吸附的去除率分别为59.6%和57.4%,是一种较好的吸附材料。
[1]Wang Shaobin,Boyjoo Y,Choueib A,et al. Removal of dyes from aqueous solution using f y ash and red mud[J]. Water Res,2005,39(1):129-138.
[2]吴威,龚继来,曾光明. 氧化石墨烯负载纳米零价铁的制备及其对亚甲基蓝的吸附[J]. 化工环保,2015,35(4):426-431.
[3]陈东,曾玉彬,李源,等. 磁性纳米 γ-Fe2O3/SiO2去除水中亚甲基蓝[J]. 化工环保,2015,35(5):481 -486.
[4]Haddar W,Ticha M B,Guesmi A,et al. A novel approach for a natural dyeing process of cotton fabric with hibiscus mutabilis(gulzuba):Process development and optimization using statistical analysis[J]. J Clean Prod,2014,68:114-120.
[5]Das J,Velusamy P. Catalytic reduction of methylene blue using biogenic gold nanoparticles from sesbania grandif ora L[J]. J Taiwan Inst Chem Eng,2014,45(5):2280-2285.
[6]Yu Ying,Zhuang Yuanyi,Wang Zhonghua,et al. Adsorption of water-soluble dyes onto modif ed resin[J]. Chemosphere,2004,54(3):425-430.
[7]Xu Junqiang,Chu Wei,Luo Shizhong. Synthesis and characterization of mesoporous V-MCM-41 molecular sieves with good hydrothermal and thermal stability[J]. J Mol Catal A:Chem,2006,256(1):48-56.
[8]Jazi M B,Arshadi M,Amiri M J,et al. Kinetic and thermodynamic investigations of Pb(Ⅱ)and Cd(Ⅱ)adsorption on nanoscale organo-functionalized SiO2/Al2O3[J]. J Colloid Interface Sci,2014,422:16-24.
[9]Miao Guang,Ye Feiyan,Wu Luoming,et al. Selective adsorption of thiophenic compounds from fuel over TiO2/SiO2under UV-irradiation[J]. J Hazard Mater,2015,300:426-432.
[10]Tomer V K,Duhan S,Sharma A K,et al. One pot synthesis of mesoporous ZnO-SiO2nanocomposite as high performance humidity sensor[J]. Colloid Surf,A,2015,483:121-128.
[11]Gong Jilai,Wang Bin,Zeng Guangming,et al. Removal of cationic dyes from aqueous solution using magnetic multi-wall carbon nanotube nanocomposite as adsorbent[J]. J Hazard Mater,2009,164(2):1517-1522.
[12]Tang Wangwang,Zeng Guangming,Gong Jilai,et al. Simultaneous adsorption of atrazine and Cu(Ⅱ)from wastewater by magnetic multi-walled carbon nanotube[J]. Chem Eng J,2012,211:470-478.
[13]Stöber W,Fink A,Bohn E. Controlled growth of monodisperse silica spheres in the micron size range[J]. J Colloid Interface Sci,1968,26(1):62-69.
[14]Kou Liang,Gao Chao. Making silica nanoparticlecovered graphene oxide nanohybrids as general building blocks for large-area superhydrophilic coatings[J]. Nanoscale,2011,3(2):519-528.
[15]Feng Jing,Zou Linyi,Wang Yuting,et al. Synthesis of high surface area,mesoporous MgO nanosheets with excellent adsorption capability for Ni(Ⅱ)via a distillation treating[J]. J Colloid Interface Sci,2015,438:259-267.
[16]Hao Liying,Song Hongjie,Zhang Lichun,et al. SiO2/graphene composite for highly selective adsorption of Pb(Ⅱ)ion[J]. J Colloid Interface Sci,2012,369(1):381-387.
[17]Cottet L,Almeida C A P,Naidek N,et al. Adsorption characteristics of montmorillonite clay modified with iron oxide with respect to methylene blue in aqueous media[J]. Appl Clay Sci,2014,95:25-31.
[18]Dotto G L,Dos Santos J M N,Rosa R,et al. Fixedbed adsorption of methylene blue by ultrasonic surface modif ed chitin supported on sand[J]. Chem Eng Res Design,2015,100:302-310.
[19]Banerjee S,Sharma G C,Chattopadhyaya M C,et al. Kinetic and equilibrium modeling for the adsorptive removal of methylene blue from aqueous solutions on of activated fly ash(AFSH)[J]. J Environ Chem Eng,2014,2(3):1870-1880.
[20]Wu Yongjun,Zhang Lijun,Gao Congli,et al. Adsorption of copper ions and methylene blue in a single and binary system on wheat straw[J]. J Chem Eng Data,2009,54(12):3229-3234.
[21]Cretescu I,Soreanu G,Harja M. A low-cost sorbent for removal of copper ions from wastewaters based on sawdust/fly ash mixture[J]. Int J Environ Sci Technol,2015,12(6):1799-1810.
[22]张琪,罗琳,张嘉超,等. 磁性水滑石快速吸附水体中 Cu(Ⅱ)离子[J]. 环境工程学报,2015,9(9):4339-4344.
(编辑 叶晶菁)
Simultaneous adsorption of methylene blue and Cu2+using MgO / SiO2nanocomposite
Chen Xiankun,Gong Jilai,Zeng Guangming
(Key Laboratory of Environmental Biology and Pollution Control,Ministry of Education,College of Environmental Science and Engineering,Hunan University,Changsha Hunan 410082,China)
MgO /SiO2nancomposite was synthesized by chemical deposition method and characterized by SEMEDX,XRD,Zeta potentiometer,and FTIR. The adsorption of methylene blue(MB)and Cu2+on MgO /SiO2and their simultaneous adsorption effect were investigated. The characterization results show that:MgO /SiO2has spherical morphology with wrinkles and embossment;MgO is successfully loaded onto the surface of SiO2. The experimental results show that:The adsorption process fits the pseudo-second-order kinetic model and Langmuir isothermal adsorption model,and the saturated adsorption capacity of MB and Cu2+is 83.72 mg/g and 208.70 mg/g respectively;When MB and Cu2+are simultaneously adsorped,a competitive relationship between MB and Cu2+is appeared on the surface of MgO /SiO2;Under the conditions of solution volume 30 mL,MgO /SiO2dosage 10 mg,MB mass concentration 10 mg/L or Cu2+mass concentration 100 mg/L,adsorption 25 ℃,adsorption time 24 h,initial pH 4.00 and desorption time 4 h,the removal rates of MB and Cu2+are 92.8% and 90.1% for the f rst adsorption,and 59.6% and 57.4% for the f fth adsorption,respectively.
MgO/SiO2;methylene blue;Cu2+;simultaneous adsorption
X703
A
1006-1878(2016)06-0617-08
10.3969/j.issn.1006-1878.2016.06.006
2016-02-22;
2016-07-19。
陈显坤(1989—),男,河南省信阳市人,硕士,电话 15274911625,电邮 1126670930@qq.com。联系人:龚继来,电话 13787219458,电邮 jilaigong@hnu.edu.cn。
国家自然科学基金资助项目(51579095)。

